多羧酸稀土配合物(La,Ce,Nd)的合成及其表征
刘 艳,贾 尧,姜 敏
(陕西省催化基础与应用重点实验室,陕西理工大学化学与环境科学学院,陕西 汉中 723000)
稀土元素特殊的电子结构,决定了其化合物具有独特的光、电、磁学等性质。随着配位化学的发展,近年来大量结构新颖、性能优良的稀土配合物,被应用于催化反应、发光材料、荧光传感及仿生合成等领域[1-3]。稀土金属离子具有较高的正电荷,因此形成的配合物通常具有较高的配位数和多样的配位结构,在金属有机化学或者配位化学中显示出特殊的性能[2-3]。
羧酸类化合物作为配体时,其羧基去质子化后形成的羧酸根有多个配位点,对大多数金属离子都有较强的配位能力,展示了多样的配位模式,可以形成单齿、多齿配合物乃至配位聚合物[4]。很多稀土金属配合物的结构中,都含有一些中性分子如水、乙醇等,它们可以与稀土金属离子配位成键,也可以不发生配位,而是通过其它作用结合于晶体结构中[5]。
本研究选取苯氧醚类多羧酸配体3,5-二(2-羧基苯氧基)苯甲酸(3,5-bis(2-carboxyphen-oxy)benzoicacid,H3L)为主配体,与稀土金属离子进行配位,合成了3种新型的稀土金属配合物。采用红外光谱、XRD粉末衍射等方法,对得到的稀土配合物进行了初步表征,并对其可能的热分解机理进行了探讨。
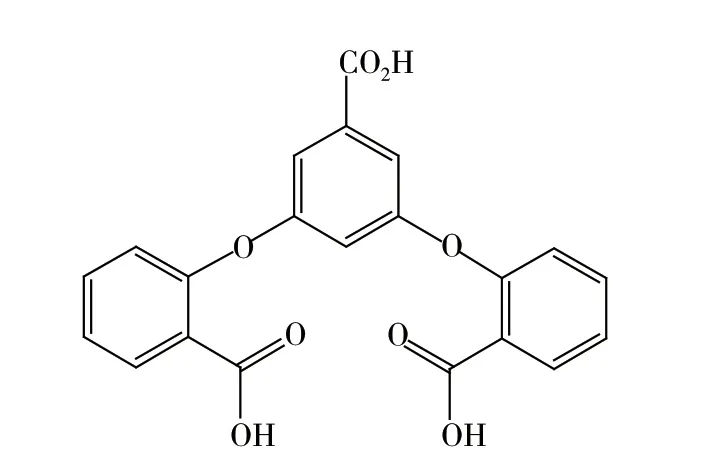
图1 3,5-二(2-羧基苯氧基)苯甲酸的结构式Fig. 1 The skeleton of3,5-bis(2-carboxyphenoxy)benzoic acid
1 实验部分
1.1 试剂与仪器
La(NO3)3·4H2O(AR)、Ce(NO3)3·2H2O(AR)、Nd(NO3)3·2H2O(AR)、3,5-二(2-羧基苯氧基)苯甲酸、N,N-二甲基甲酰胺(AR)。所有试剂均未经纯化。
VERTEX70型红外分光光度计,STA449F3型热重分析仪,APEX-11 CCD型XRD粉末衍射仪,PE-2400型元素分析仪EA,760CRT型紫外可见分光光度计。
1.2 系列稀土金属配合物的合成
镧配合物的合成:称取0.1mmol的La(NO3)3于闪烁瓶中,依次加入0.1mmol的3,5-二(2-羧基苯氧基)苯甲酸、10 mL混合溶剂(N,N-二甲基甲酰胺和H2O,体积比为1∶1),随后将闪烁瓶放入超声仪中超声震荡30min。超声完毕转入恒温箱,以5℃·min-1的升温速率程序升温至100℃,恒温3d,然后再以0.5℃·min-1的降温速率程序降温至室温。过滤,洗涤沉淀,干燥后得白色小颗粒状粉晶,记作配合物1,产率67%(以La计)。
铈配合物的合成:金属盐为0.1mmol的Ce(NO3)3,其他实验条件与镧配合物的合成相同,干燥后得白色小团状粉晶,记作配合物2,产率48%(以Ce计)。
钕配合物的合成:金属盐为0.1mmol的Nd(NO3)3,其他实验条件与镧配合物的合成相同,干燥后得紫色小团簇状粉晶,记作配合物3,产率为55%(以Nd计)。
2 结果与分析
2.1 系列稀土金属配合物的XRD数据分析
在X射线衍射仪上对所得产物进行结构测试。XRD测试以石墨单色器单色化的Cu-Kα射线为衍射光源,入射波长λ=0.154nm,管电流为40mA,管电压为40kV,扫描范围2θ为 3°~ 100°,扫描速度为10°·min-1,得到该系列配合物的衍射图谱(图2)。
从图2可见,在16.8°、34°及45°处,3种稀土金属配合物的峰形大致相同,推测其配位方式基本相同,可能为同晶结构。同时也可以看到,配合物1即镧配合物的峰形相对较低,可能是该配合物在这些晶面层的生长比另外2个配合物慢而导致的。
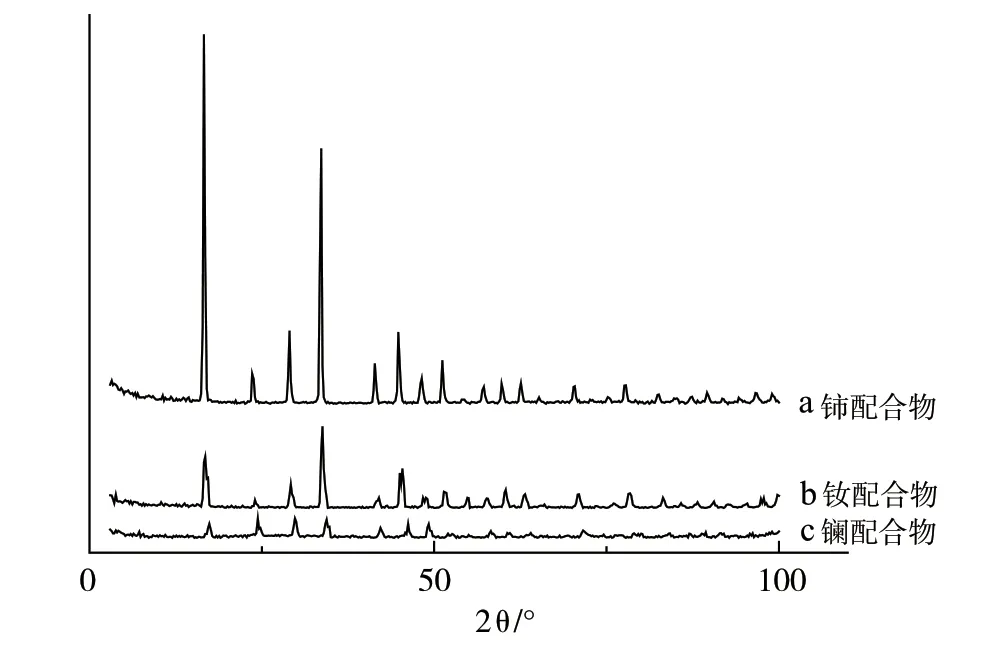
图2 稀土金属配合物的XRD衍射分析图Fig.2 The XRD pattern of rare earth complexes
2.2 稀土金属配合物的红外光谱分析
采用KBr压片法,对得到的金属配合物进行红外光谱测试, 3种配合物的红外吸收光谱图见图3(a)、图3(b)和图3(c)。3种配合物的红外吸收图谱非常类似,羧基特征吸收峰νC=O都出现在1500~1384cm-1左右,推测是配体的羧基与金属离子发生配位效应后,羧基特征吸收峰发生红移所致。3种配合物在900~650cm-1左右均有芳环的δ=CH(面外)特征吸收峰,在1230~1000 cm-1左右出现了2个强的特征吸收峰,指派为配体中所含C-O-C键的伸缩振动νC-O-C。3种配合物在713 cm-1附近,均出现了特征吸收峰,推测是稀土金属离子和DMF进行了配位。
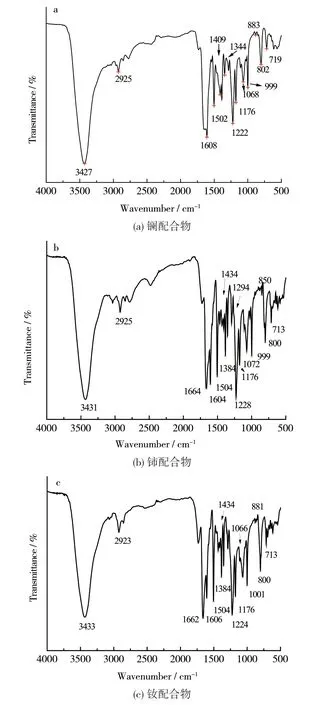
图3 配合物的红外光谱图(a) La complex;(b) Ce complex;(c) Nd complexFig.3 IR spectrums of complexes
2.3 元素分析
对所得目标配合物进行元素分析,其元素分析数据见表1。结合系列配合物的XRD衍射图谱及红外图谱分析,推测该系列配合物可能的组成为:M∶C21H11O8∶DMF=1∶1∶2,M=La、Ce、Nd,可能的化学式为:M(C21H11O8)(C3H7NO)2,其理论值和实测值基本相符。
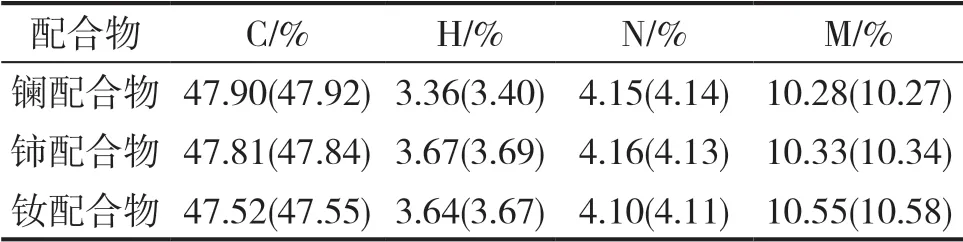
表1 稀土金属配合物的元素分析(括号内为理论值)Table 1 Elemental analysis of rare earth metal complexes(The theoretical value in parentheses)
2.4 系列金属配合物的紫外-可见光谱分析
镧、铈及钕稀土配合物的紫外-可见光谱见图4(a)、图4(b)和图4(c)。3个谱图中,263nm及300nm附近均有类似的吸收峰,可指派为苯环的π→π*跃迁及n→π*跃迁光谱,说明多羧酸配体和中心金属离子发生了有效的配位,这与此系列配合物相应的红外谱图有着较好的对应关系。
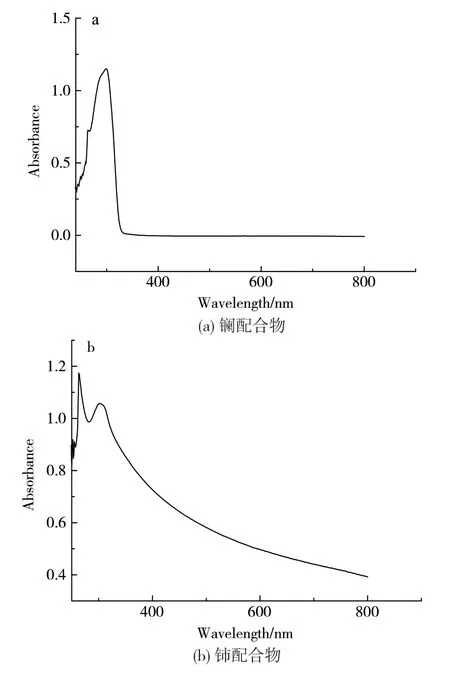
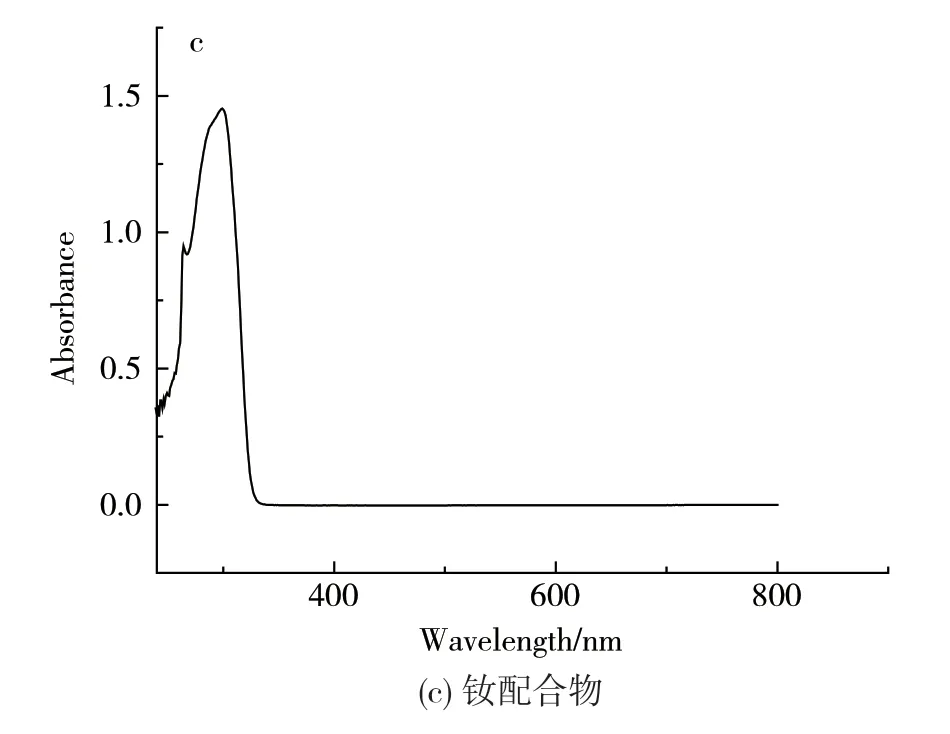
图4 配合物的紫外-可见光谱图 (a) La complex;(b) Ce complex;(c) Nd complexFig.4 UV-Vis spectrums ofcomplexes
2.5 稀土金属配合物的热重-差热分析
在氮气气氛中,以10 ℃·min-1的升温速率,测定了3种配合物由室温至1400 ℃的热分解行为,所得的热重曲线见图5。由配合物1的TG曲线可知,此配合物的热分解过程可分为2个阶段:第一阶段从300℃到420℃,失重率为40%,推测此处失去的可能是配位的N,N-二甲基甲酰胺(DMF)分子,归因于溶剂分子与中心金属原子的配位作用较弱,故而先期裂解;第二阶段是从420℃到900℃,失重率为36%,该阶段失去的可能是3,5-二(2-羧基苯氧基)苯甲酸分子碎片。最终残余物约为24%,推测可能为稀土金属的氧化物La2O3。该热分解过程可表述为:
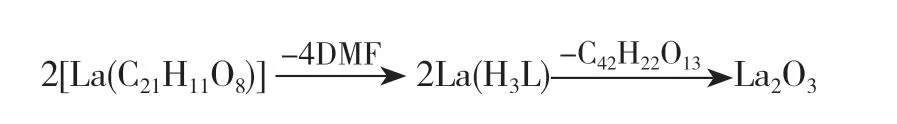
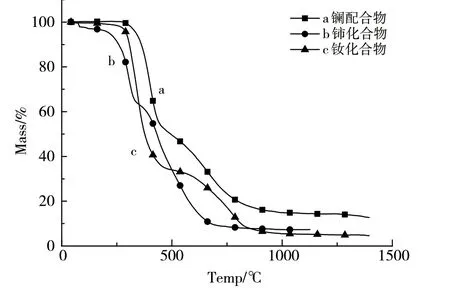
图5 稀土金属配合物的热重曲线图 (a) La complex; (b) Ce complex; (c) Nd complexFig.5 Thermogravimetric diagram of rare earth complexes
配合物2的TG曲线表现出与配合物1类似的热分解行为。配合物2于350℃左右开始分解,800℃左右分解完全。热分解过程同样也分为2个阶段,第一阶段从350℃到460℃,失重率为38%,推测此处失去的依然可能是N,N-二甲基甲酰胺(DMF)分子;第二阶段从460℃到800℃,失重率为50%(理论值为54%),该阶段失去的是剩余的三羧酸分子碎片。最终残余物约为12%,推测可能是该稀土金属的氧化物Ce2O3。该热分解过程可表述为:
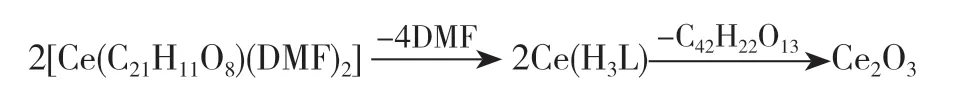
配合物3的TG曲线提示,在热分解过程中,该配合物的分子骨架塌陷始于300℃,850℃左右基本分解完全。在该配合物热分解的2个阶段中,第一阶段从300℃到400℃,失重率为40%,推测失去的依然是N,N-二甲基甲酰胺(DMF)分子,第二阶段从400℃到850℃,失重率为36%,失去的可能是3,5-二(2-羧基苯氧基)苯甲酸分子碎片,最终残余物约为24%,推测可能同样是该稀土金属的氧化物Nd2O3。该热分解过程可表述为:
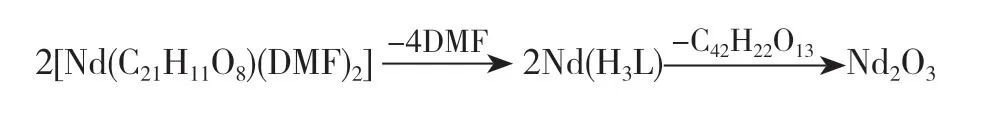
综合考察该系列配合物的热分解过程后可以看出,DMF溶剂分子与中心金属离子的配位作用较弱,在加热过程中会先期裂解后失去,随之失去的则是残余的3,5-二(2-羧基苯氧基)苯甲酸分子碎片。该系列配合物有相近的热分解规律性,同样也证明了该系列配合物同晶结构的特点。
3 结论
本文以3,5-二(2-羧基苯氧基)苯甲酸为配体,采用溶剂热法合成了稀土镧、铈、钕配合物。元素分析、红外、紫外、热重、XRD粉末衍射等性能测试结果表明,3种稀土金属配合物的组成相近,配位方式大致相同,使得其热分解过程也呈现了类似的规律性。

