对羟基苯甲醛制备新工艺的研究
吴德旺
(厦门欧米克生物科技有限公司,福建 厦门 361000)
对羟基苯甲醛是重要的精细化工产品,是许多药物、香料和农药的关键中间体。在香料化学方面,对羟基苯甲醛可以合成大茴香醛、香兰素、洋茉莉醛、丁香醛和覆盆子酮等香料。近年来,市场对这些药物、香料和农药的需求量越来越大,对羟基苯甲醛的合成引起了人们的极大关注。目前,对羟基苯甲醛的合成方法主要有以下4种:1)苯酚法。苯酚法又分为Reimer-Tiemann反应[1]、Gattermann反应[2]、苯酚-三氯乙醛路线[3]、苯酚-乙醛酸路线[4]、苯酚-甲醛路线[5]等多种合成工艺,其工艺特点是原料易得,制造工艺较简单,但收率偏低,成本较高。2)对硝基甲苯法。对硝基甲苯法生产对羟基苯甲醛的工艺过程包括氧化还原、重氮化、水解等3个步骤[6],优点是原料价格便宜,缺点是工艺路线长,设备庞大,且中间产物对氨基苯甲醛有毒,重氮化反应温度低,冷冻条件高。目前国内有山西祁县精细化工厂采用此工艺生产对羟基苯甲醛。3)微生物法。以对甲酚为原料,在一定的温度和pH下,用菌种在甘露糖酵母和盐等介质中发酵得到对羟基苯甲醛[7]。该法是一条绿色无污染、操作简单的工艺,但生产周期太长。4)对甲酚催化氧化法。该工艺是在催化剂的作用下,用空气或氧气直接氧化对甲酚为对羟基苯甲醛[8]。目前该法所使用的催化剂的活性和选择性尚未达到理想的效果,存在副产物多、分离困难、催化剂重复使用的效率低、生产周期长、生产成本高等问题。
鉴于对羟基苯甲醛具有极大的商业价值,我们开发了一条简便、廉价、具有工业应用前景的合成工艺。以廉价的对伞花烃为原料,氧气为氧化剂,在催化剂和引发剂的作用下,氧化得到对甲酚中间体,再在强碱性条件下继续用氧气催化氧化得到对羟基苯甲醛,是一条制备对羟基苯甲醛的新工艺。该法的原料价格便宜,操作简便,绿色无污染,是一条具有工业应用价值的合成方法。
1 实验部分
1.1 仪器及试剂
仪 器:Agilent7890B 气 相 色 谱 仪,GCMSQP2010 Ultra 气-质联用仪,IKA RV8数显型旋转蒸发仪,DF-2000 集热式恒温加热磁力搅拌器。
试剂:对伞花烃(98%,AR)、七水硫酸钴(AR)、六水硝酸钴(AR)、六水氯化钴(AR)、四水醋酸钴(AR)、N-羟基邻苯二甲酰亚胺(NHPI,AR)、偶氮二异丁腈(AIBN,AR)、乙腈(CR)、乙酸乙酯(CR)、甲醇(CR)、酒精(CR)、碳酸氢钠(CR)、浓硫酸(CR)、无水硫酸钠(CR)、氢氧化钠(CR)、氯化钠(CR)、O2(纯度≥99.99%)。
1.2 合成路线
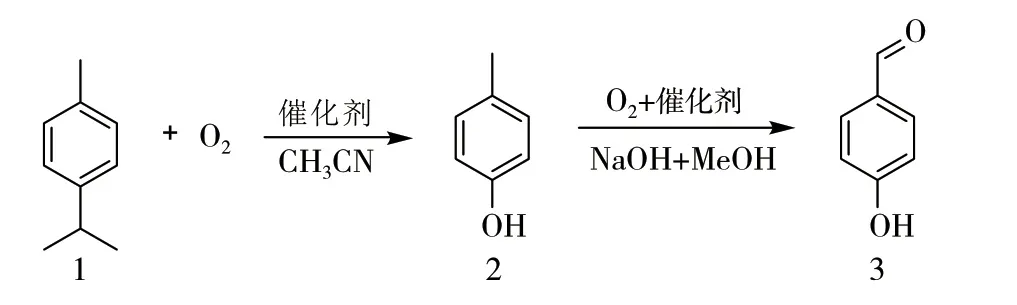
1.3 实验方法
1.3.1 对甲酚的合成
将134g(1.0mol)对 伞 花 烃、16g(0.1mol)N-羟基邻苯二甲酰亚胺、1.6g(0.01mol)偶氮二异丁腈和900g的乙腈依次加入2L的反应釜中。反应釜抽真空后置换成氧气,缓慢升温至90℃,待温度稳定后加压至1.0MPa,反应16h。冷却至室温,倒出反应液,冰水浴冷却,缓慢滴加10%硫酸200g,使中间体对甲异丙苯氢过氧化物缓慢分解,冷却至室温后再搅拌1h。
向淬灭后的反应液中加入10%的NaHCO3溶液400g,中和至pH=7.0~8.0,浓缩回收乙腈后,再加入乙酸乙酯500mL萃取,静置分层。有机相用饱和食盐水200g洗涤,无水硫酸钠干燥,浓缩得对甲酚粗品90g(73.64%)。蒸馏对甲酚粗品,收集沸点为80~84℃/1.1kPa的产品55g,色谱检测得到对甲酚含量为98%,产率51%。产品用气-质联用仪检测,分子碎片峰如下:MS(m/z):109(M+1),108(M, 95%),107(100%),77(25%),51(10%),39(10%),与对甲酚标准品的质谱结果一致。
1.3.2 对羟基苯甲醛的合成
将108g(1.0mol)对甲酚、240g(6.0mol)氢氧化钠、1000g甲醇依次加入装有电磁搅拌器、回流冷凝器和气体导管的玻璃反应器中,开启搅拌至固体完全溶解后,加入2.5g(0.01mol)四水醋酸钴。水浴中加热,缓慢升温至75℃,待温度稳定后,以60mL·min-1的气速缓慢通入氧气,维持反应体系压力为0.1MPa,反应温度控制在75~80℃之间,加热10h,停止加热。
冰水浴冷却,缓慢滴加30%硫酸900g,调节至pH=4~5。抽滤以除去固体,固体用乙酸乙酯洗涤,滤液浓缩除去大部分甲醇后,用乙酸乙酯萃取3次(250g×3)。合并有机相,用饱和食盐水300g洗涤,有机相浓缩得粗品110g(90.17%)。粗品用30%酒精水溶液重结晶,真空干燥后得对羟基苯甲醛92g。色谱检测对羟基苯甲醛含量为98%,收率75%。产品用气-质联用仪检测,分子碎片峰如下:MS(m/z):123(M+1),122(M, 95%),121(100%),93(44%),65(25%),39(10%),与对羟基苯甲醛标准品的质谱一致。
1.3.3 检测方法
色谱分析条件:采用30m×320μm×0.25μm 的HP-5毛细管柱和30m×250μm×0.25μm 的DBWAX毛细管柱,进样口温度250℃,程序升温:起始温度70℃,保持3min,以5℃·min-1升温至230℃。高纯氮作载气(纯度≥99.99%),流量1mL·min-1。进样量0.2μL,分流比50∶1。采用面积归一法定量。
质谱检测条件:接口温度250℃,离子源(EI)电压350V,温度200℃,发射电流150mA。扫描时间0.3s·次-1,扫描范围15~500 amu,扫描速度1666。检测器增益0.9kV,溶剂延迟时间0.2min。
2 结果与讨论
2.1 对伞花烃制备对甲酚的影响因素
2.1.1 反应温度的影响
对伞花烃的氧化反应属于自由基反应历程[9],提高反应温度有利于反应的进行。但氧化反应进行的同时伴随着分解副反应的发生,当氧化到一定程度时,这种分解反应会加速并抑制反应的进行。一般认为最适合的氧化条件下,氧化反应的温度控制在80~130℃为宜,本实验的反应温度控制在90℃。
2.1.2 反应压力的影响
增加反应压力可加速氧化反应的进行。日本的堤繁[10]以NaHCO3为pH调节剂, 硬脂酸钠为乳化剂,过氧化苯甲酰为引发剂,对4-异丙基甲苯进行了加压氧化实验。结果证明,在同样的温度下,氧气吸收量随压力的增加而增加。在60℃、3.0MPa下反应9h,对甲异丙苯氢过氧化物的积累浓度达最大值43.2%。因此增加压力可以加快氧化速度,但压力的增加也促进了对甲异丙苯氢过氧化物的分解,因此反应压力不宜太高。最适宜的反应压力为1.0~3.0MPa,本实验的反应体系氧气压力控制在1.0MPa。
2.1.3 催化剂的影响
对伞花烃的氧化反应属于自由基反应,反应前存在一个诱导期。为了缩短甚至消除诱导期,加速氧化反应,可以添加适当的催化剂和引发剂。本实验采用N-羟基邻苯二甲酰亚胺作为催化剂,用量为0.1当量。氧化反应适用的引发剂有叔丁基过氧化氢、过氧化苯甲酸叔丁酯、苯酰过氧化物、偶氮二异丁腈和异丙苯过氧化氢等。实验中发现,偶氮二异丁腈作为引发剂时的氧化反应效果最好,偶氮二异丁腈的用量为0.01当量时,对甲酚的收率最高。
2.2 由对甲酚制备对羟基苯甲醛的影响因素
2.2.1 氢氧化钠和甲醇用量的影响
在其他实验条件相同的情况下,改变氢氧化钠与对甲酚的摩尔比分别为3∶1、4∶1、5∶1、6∶1、7∶1、8∶1,考察氢氧化钠用量对反应收率的影响,结果见图1。可以看出,随着氢氧化钠的用量增加,反应收率随之增加,当氢氧化钠与对甲酚的摩尔比超过6∶1后,反应体系变得黏稠,反应体系中各种底物的扩散受到限制,导致原料与催化剂表面接触的效率降低,最终反应的转化率和收率下降。实验结果表明,氢氧化钠与对甲酚的摩尔比为6∶1时的反应收率最高。
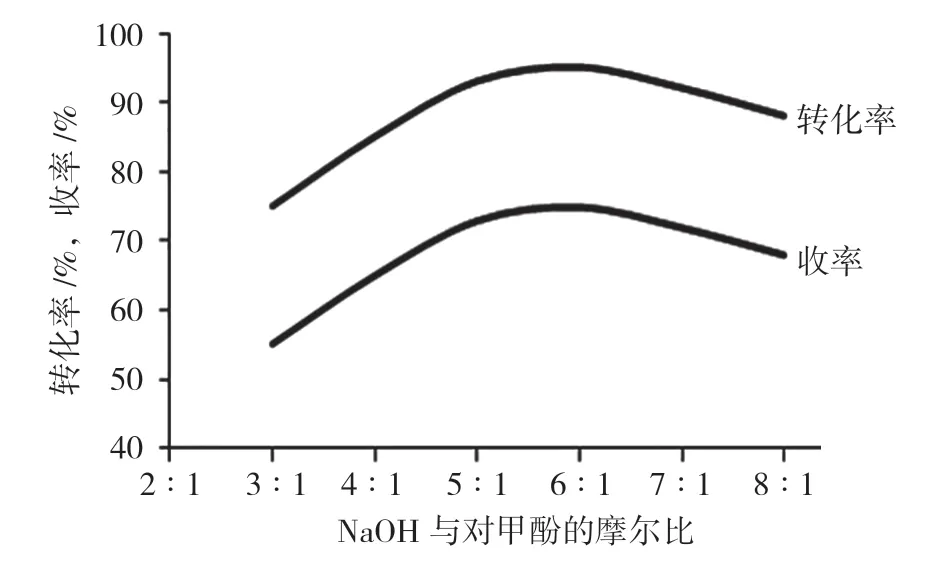
图1 NaOH用量的影响
同时考察了溶剂甲醇用量对反应的影响,发现甲醇用量为对甲酚质量的7~10倍为宜。如果甲醇用量过大,各反应物浓度偏低,会导致反应速度缓慢,转化率和反应收率也随之降低,生产成本随之增加。但甲醇用量过低时,反应物浓度偏大,黏度也增大,会使得气液间的传质阻力增大,影响反应速度,导致对羟基苯甲醛的收率明显降低。
2.2.2 催化剂种类的影响
在相同的实验条件下,用4种钴盐作为催化剂进行氧化对甲酚的反应,实验结果见表1。从反应的转化率和收率可以看出,不同的钴盐对该氧化反应的催化性能有很大的区别。Co(OAc)2·4H2O的催 化 效果最 好,CoSO4·7H2O、Co(NO3)2·6H2O和CoCl2·6H2O的转化率和收率都比较低,因此选择Co(OAc)2·4H2O作为反应催化剂进行后续的实验。
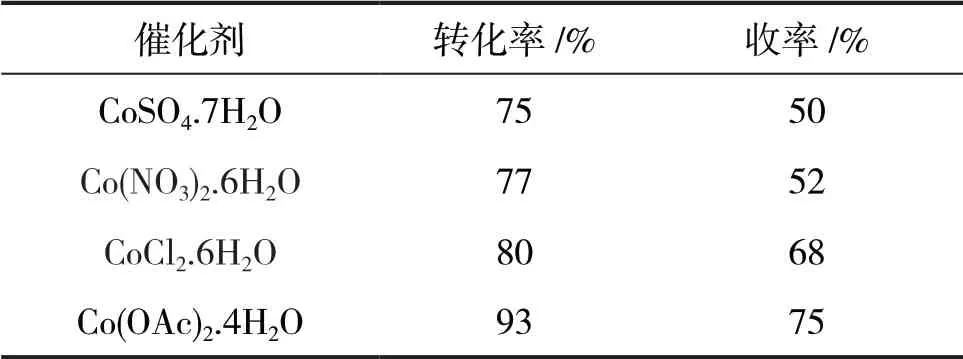
表 1 催化剂的选择
2.2.3 催化剂用量对反应的影响
催化剂用量对反应的影响见图2,可以看出,催化剂用量少,溶液中催化剂的浓度低,因此转化率低,收率低;催化剂用量多,反应剧烈,目标产物可能继续氧化,同时聚合物也增多,催化剂出现暂时性中毒现象,转化率和收率也没有明显提高,反而增加了生产成本。实验结果表明,若要加快反应速度又要控制生产成本,催化剂与对甲酚的摩尔比为0.01∶1时为最佳,收率达到75%。
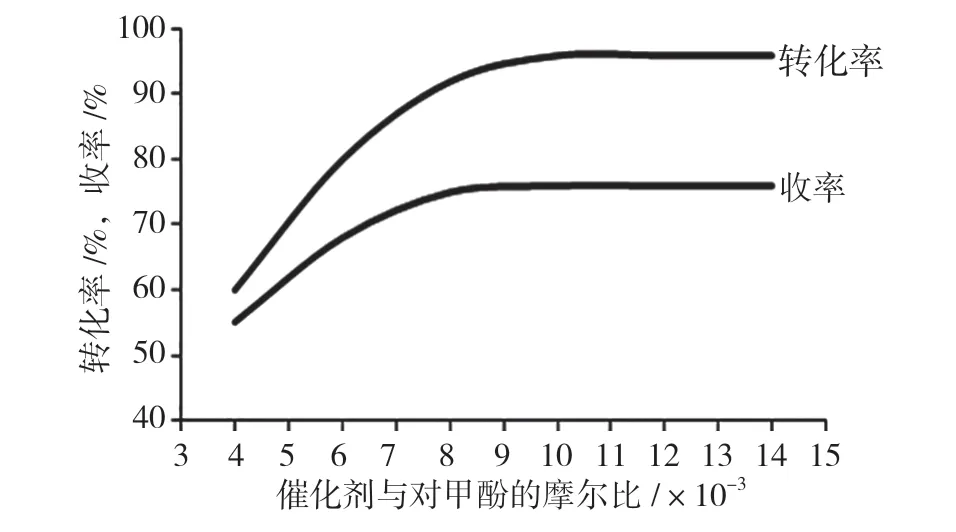
图2 催化剂用量的影响
2.2.4 反应时间和反应温度的影响
反应时间的影响见图3,可以看出,随着反应时间延长,反应转化率和收率随之增加,反应时间为10h时,转化率达97%,收率为76%,再继续延长反应时间,转化率和收率均未有明显的增加,甚至出现微微下降。这是因为反应为气液反应,延长反应时间有利于提高对甲酚的转化率,但时间过长又会导致焦油等副产物增多,且增加了产物的分离和提纯难度,影响反应收率。综合分析,氧化反应时间以10h为宜。
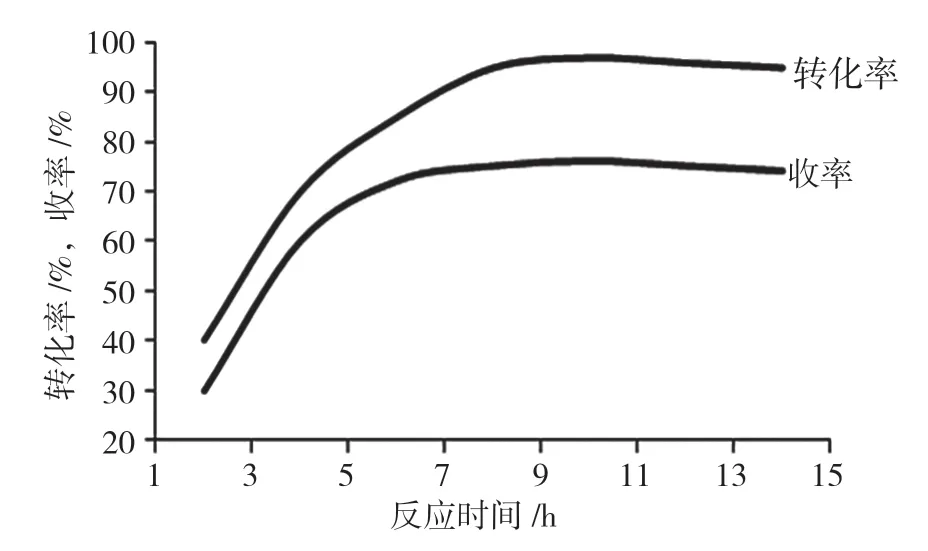
图3 反应时间的影响
同时考察了反应温度对反应的转化率和收率的影响(图4)。反应温度过低,反应很慢,反应不完全;温度过高,目标产物对羟基苯甲醛容易继续被氧化,导致焦油大量生成,使得催化剂部分失活,催化活性降低,造成反应转化率和收率下降。从图4可以看出,最佳的反应温度为75~80℃。
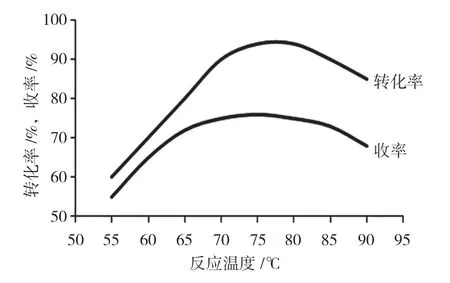
图4 反应温度的影响
3 结论
我们探索了一条制备对羟基苯甲醛的新工艺。以廉价的对伞花烃为原料,以氧气为氧化剂,先催化氧化得到中间体对甲酚,再用氧气催化氧化对甲酚制备对羟基苯甲醛。该工艺的原料便宜,操作简单,绿色无污染,是一条适合工业化生产的新工艺。考察了反应时间、反应压力、反应温度、溶剂、催化剂种类及用量对反应转化率和收率的影响。实验结果表明,以对伞花烃为原料,当催化剂N-羟基邻苯二甲酰亚胺的用量为0.1当量,引发剂偶氮二异丁腈的用量为0.01当量,反应温度为90℃,氧气压力为1.0MPa时,中间体对甲酚的收率最高为51%。继续用氧气氧化中间体对甲酚,实验结果表明,当催化剂Co(OAc)2·4H2O用量为0.01当量,NaOH用量为6当量,甲醇用量为对甲酚的7~10倍量,反应温度为75~80℃,反应10h时,对羟基苯甲醛的收率达到75%以上。

