贝伐珠单抗对EGFR突变型非小细胞肺癌患者肿瘤标志物水平的影响与安全性分析
梁海凤
(玉林市红十字会医院呼吸内科,广西 玉林 537006)
肺癌按组织病理学特征可分为小细胞肺癌和非小细胞肺癌,其中非小细胞肺癌的发病率较高,而表皮生长因子受体(EGFR)突变又在非小细胞肺癌患者中较为常见,瘤细胞的转移和侵润等均由EGFR突变引发,进而形成肿瘤,对患者生命健康造成严重威胁[1]。临床主要采用以铂类药物为基础的化疗和分子靶向治疗,其中分子靶向治疗具有选择性、低毒性、高效性等特点,吉非替尼是一种表皮生长因子受体酪氨酸激酶抑制剂,其可阻碍肿瘤的生长、转移及血管生成,缓解患者病情,但单一用药效果不佳,且易产生耐药性[2]。作为血管内皮生长因子(VEGF)的单克隆抗体,贝伐珠单抗可抑制新生血管形成,并阻止肿瘤生长,进而改善患者生活质量[3]。本研究旨在探讨贝伐珠单抗对EGFR突变型非小细胞肺癌患者肿瘤标志物水平的影响与安全性,现作如下报道。
1 资料与方法
1.1 一般资料 依据随机数字表法将2019年9月至2020年8月玉林市红十字会医院收治的60例EGFR突变型非小细胞肺癌患者分为对照组和观察组,每组30例。对照组中男、女患者分别为22例、8例;肿瘤直径1.8~5.6 cm,平均(3.32±0.77) cm;年龄 45~70岁,平均(55.73±5.71)岁。观察组中男、女患者分别为23例、7例;肿瘤直径1.5~5.8 cm,平均(3.54±0.92) cm;年龄45~70岁,平均(54.94±5.41)岁。对比两组患者一般资料,差异无统计学意义(P>0.05),组间具有可比性。院内医学伦理委员会批准本研究,且患者或家属对本研究知情同意。纳入标准:患者均符合《中华医学会肺癌临床诊疗指南(2018版)》[4]中的相关诊断标准;可耐受靶向药物治疗者;经细胞学和组织学检查确诊为EGFR突变型者等。排除标准:患者伴有精神障碍;妊娠期或哺乳期女性;患者伴有肝、肾重要脏器衰竭等。
1.2 方法 给予对照组患者靶向药物吉非替尼片[齐鲁制药(海南)有限公司,国药准字H20163465,规格:0.25 g/片]口服治疗,0.25 mg/次,1次/d。在对照组的基础上给予观察组患者贝伐珠单抗注射液(Roche Diagnostics GmbH,注册证号S20170035,规格:100 mg/瓶)治疗,按照15 mg/kg的剂量静脉滴注,1次/d。 21 d为1个周期,两组患者均治疗3个周期。
1.3 观察指标 ①对比两组患者治疗后临床疗效,完全缓解(CR)即肿瘤消退 > 90%;部分缓解(PR)即肿瘤消退50%~90%;病情稳定(SD)即肿瘤消退50%以下;疾病进展(PD)即肿瘤增生或出现新病灶。总有效率=(CR+PR)例数/总例数×100%[4]。②对比两组患者治疗前后生活质量评分,采用癌症患者生命质量核心量表(EORTCQLQ-C30)[5]评价,包括社会、认知、角色、情绪、躯体5个方面,其中每项分值为0~100分,并将5项结果相加后计算总分平均值,得分越高表示生存质量越高。③对比两组患者治疗前后肿瘤标志物水平,采集两组患者空腹静脉血4 mL,3 000 r/min离心10 min,取上清液,血清癌胚抗原(CEA)、糖类抗原125(CA125)、血管内皮生长因子(VEGF)水平采用西门子自动电化学发光免疫系统检测。④对比两组患者治疗期间恶心呕吐、乏力、口腔溃疡、毒性(血液、神经)等不良反应发生情况。
1.4 统计学方法 运用SPSS 20.0统计软件处理数据,临床疗效、不良反应等计数资料以[ 例(%)]表示,行χ2检验;生活质量评分、肿瘤标志物水平以()表示,行t检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 临床疗效 相较于对照组,治疗后观察组患者的临床总有效率明显提升,差异有统计学意义(P<0.05),见表1。

表1 两组患者临床疗效比较[ 例(%)]
2.2 生活质量评分 与治疗前比,治疗后两组患者社会、认知、角色、情绪、躯体方面的生活质量评分及总分平均值均升高,且观察组升高幅度大于对照组,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者生活质量评分比较( ,分)

表2 两组患者生活质量评分比较( ,分)
注:与治疗前比,*P<0.05。
组别 例数 社会 认知 角色治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 30 58.55±6.68 75.61±8.72* 48.93±5.72 76.86±5.37* 62.15±7.38 68.38±4.66*观察组 30 57.35±6.72 87.57±6.39* 47.25±5.28 88.64±4.62* 61.72±7.52 73.42±4.35*t值 0.694 6.060 1.182 9.108 0.224 4.330 P值 > 0.05 < 0.05 > 0.05 < 0.05 > 0.05 < 0.05组别 例数 情绪 躯体 总分平均值治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 30 54.34±6.21 73.73±8.24* 46.64±6.67 77.68±5.75* 63.09±5.29 77.65±8.43*观察组 30 54.72±6.73 81.43±6.11* 45.35±6.57 88.73±2.86* 61.13±5.34 86.37±6.14*t值 0.227 4.111 0.755 9.424 1.240 4.580 P值 > 0.05 < 0.05 > 0.05 < 0.05 > 0.05 < 0.05
2.3 肿瘤标志物 相较于治疗前,治疗后两组患者血清CEA、CA125、VEGF水平均下降,且观察组下降幅度大于对照组,差异均有统计学意义(均P<0.05),见表3。
表3 两组患者肿瘤标志物比较()

表3 两组患者肿瘤标志物比较()
注:与治疗前比,*P<0.05。CEA:癌胚抗原;CA125:糖类抗原125;VEGF:血管内皮生长因子。
组别 例数 CEA(μg/L) CA125(U/mL) VEGF(pg/mL)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 30 87.03±9.05 39.17±5.21* 465.76±43.60 342.77±41.52* 517.15±91.15 336.49±43.87*观察组 30 89.14±9.03 31.16±7.03* 476.52±43.53 195.33±37.87* 518.94±89.68 228.17±39.76*t值 0.904 5.014 0.957 14.370 0.077 10.021 P值 > 0.05 < 0.05 > 0.05 < 0.05 > 0.05 < 0.05
2.4 不良反应 相较于对照组,治疗期间观察组患者的不良反应总发生率明显降低,差异有统计学意义(P<0.05),见表 4。
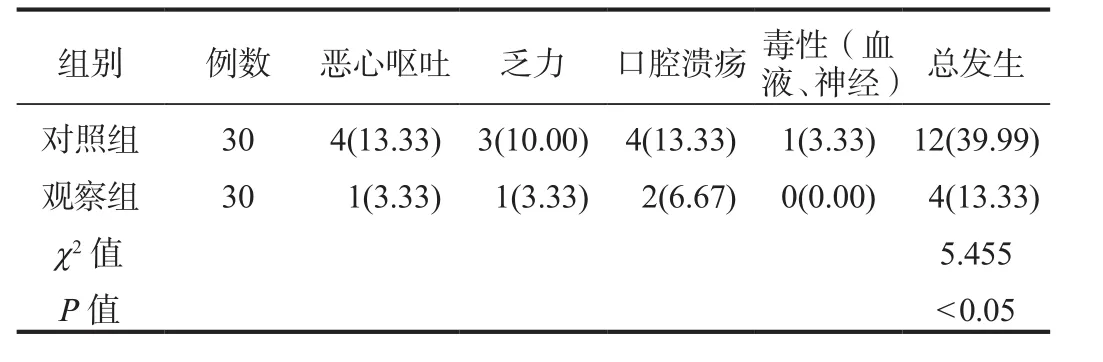
表4 两组患者不良反应发生率比较[ 例(%)]
3 讨论
随着环境污染的加剧、吸烟人数的增加,肺癌的发病率和病死率不断增长,严重影响患者的生活质量,威胁患者的生命安全。非小细胞肺癌具有肿瘤细胞生长速度快、侵袭力强的特点,其由多种因素共同导致。大多数非小细胞肺癌患者在确诊时已发展至晚期,EGFR突变是非小细胞肺癌常见的驱动基因,其与肺癌的增殖、生长、运动、黏附、侵袭、转移、凋亡密切相关,导致临床治疗难度增大[6]。近年来,分子靶向治疗逐渐成为治疗非小细胞肺癌患者的一项重要手段,吉非替尼可抑制EGFR酪氨酸激酶活性,还可将信号通路传导阻断,对瘤细胞的增生、转移及侵袭起到抑制作用,但患者长期服用可出现耐药性,因此需要通过联合其他药物来提高整体疗效。贝伐珠单抗是VEGF阻滞剂,属于一种重组人免疫球蛋白G1(IgG1)克隆抗体,通过与游离VEGF结合,可抑制肿瘤组织血管增生和形成,进而改变肿瘤组织微环境,抑制其增殖和转移[7]。在本研究中,观察组患者临床总有效率高于对照组,表明贝伐珠单抗可延缓EGFR突变型非小细胞肺癌患者病情进展,提高治疗效果。
若过度激活机体内的EGFR则可引发肿瘤细胞的侵袭、黏附等,使正常细胞周期出现紊乱,肿瘤细胞的凋亡也相应减少,导致肿瘤进展。CEA是一种非特异性肿瘤标志物,在多种肿瘤中含量均较高;CA125是一种多聚糖蛋白,主要用于卵巢癌的诊断和监测,但在肺癌患者的血清和胸腔积液中也显著升高;VEGF可由多种肿瘤细胞释放,具有促进血管内皮细胞增殖的作用,可使肿瘤不断新生血管,导致病情加重,肿瘤转移风险增加。贝伐珠单抗可直接作用于促血管生长相关因子,从而控制肿瘤转移,其还可与内源性VEGF产生竞争性结合,且不受肿瘤组织学特性的影响[8]。在本研究中,相较于对照组,治疗后观察组患者血清CEA、CA125、VEGF水平明显下降,表明贝伐珠单抗可降低EGFR突变型非小细胞肺癌患者体内肿瘤标志物水平,抑制肿瘤进展。此外,贝伐珠单抗联合分子靶向药物可增强抗肿瘤治疗效果,促进患者生活质量改善,延长其生存期限,且患者耐受性较好,安全性较高[9]。在本研究中,相较于对照组,观察组患者社会、认知、角色、情绪、躯体等生活质量评分及总分平均值明显升高,不良反应总发生率较低,表明贝伐珠单抗可提升EGFR突变型非小细胞肺癌患者的生活质量,降低不良反应发生风险,具有良好的临床应用安全性。
综上,贝伐珠单抗可延缓EGFR突变型非小细胞肺癌患者病情发展,提高治疗效果,同时降低体内肿瘤标志物水平,抑制肿瘤进程,并提升生活质量,降低不良反应发生风险,具有良好的临床应用安全性。

