彩色多普勒超声对卵巢恶性生殖细胞肿瘤的诊断分析
徐 莲,岳媛媛,罗 瑜,黄丽琼,程印蓉,马晓娟(成都市第一人民医院超声科 四川 成都 610041)
卵巢生殖细胞肿瘤起源于胚胎原始性腺生殖细胞,发病率仅次于卵巢上皮来源性肿瘤,约占卵巢肿瘤的三分之一[1]。大部分卵巢生殖细胞肿瘤发生于儿童和青春期[2],其中成熟性畸胎瘤为良性,其余均为恶性,而且恶性程度极高。准确的影像学诊断能够帮助临床制定更合适的治疗方案。故本文旨在分析卵巢恶性生殖细胞肿瘤的临床特点、肿瘤标志物水平和超声特征,提高彩色多普勒超声对卵巢恶性生殖细胞肿瘤的诊断正确率,为临床提供可靠的依据。
1 资料与方法
1.1 资料与方法
一共选取收集2015 年1 月—2020 年10 月在我院经手术病理证实为卵巢恶性生殖细胞肿瘤的35 例病例,均有完整的临床资料、超声检查和病理结果,记录患者的年龄、临床症状、肿瘤标志物(AFP、hCG 和CA125)和病理结果。
1.2 仪器与方法
所有病例均在术前行经腹部或经阴道彩色多普勒超声检查,使用超声诊断仪Philips IU Elite、GE LOGIQ S8,腹部探头频率3.5 ~5 MHz 和腔内探头频率3 ~10 MHz,常规检查子宫附件,记录肿块的大小、回声、边界、形态、肿块内部及周边的血流信号,测量血流频谱参数包括收缩期最高流速(PSV)及阻力指数(RI),以及有无盆腔、腹腔、胸腔积液。
1.3 统计学分析
应用SPSS 13.0 统计软件进行分析,服从正态分布的定量资料以均数±标准差(±s)表示。
2 结果
2.1 临床特点
术后病理确诊为卵巢恶性生殖细胞肿瘤35 例,包括无性细胞瘤13 例、卵黄囊瘤12 例、未成熟畸胎瘤6 例、混合型生殖细胞肿瘤4 例(其中3 例为未成熟畸胎瘤合并肝样型卵黄囊瘤,1 例为未成熟畸胎瘤合并无性细胞瘤)。患者年龄12 ~57 岁,平均(22.5±10.3)岁,仅1 例57 岁,其余均≤28 岁。11 例因体检发现腹部包块就诊,8 例因腹胀就诊,16 例因腹痛就诊,8 例伴发热,9 例伴恶心、呕吐,5 例伴体重减少,8 例伴纳差、精神不振,5 例伴阴道不规则流血、6 例伴尿频排便困难。病程最短0.5 d,最长6 个月,平均病程(27.2±47.5)d。
2.2 肿瘤标志物
卵巢恶性生殖细胞肿瘤不同病理类型的肿瘤标志物水平。所有的卵黄囊瘤AFP 明显升高,4 例未成熟畸胎瘤AFP 升高,4 例混合型生殖细胞肿瘤AFP 也有一定程度的升高。CA125 在各个类型均有一定程度的升高。5 例无性细胞瘤hCG 升高,1 例混合型hCG 升高,见表1。
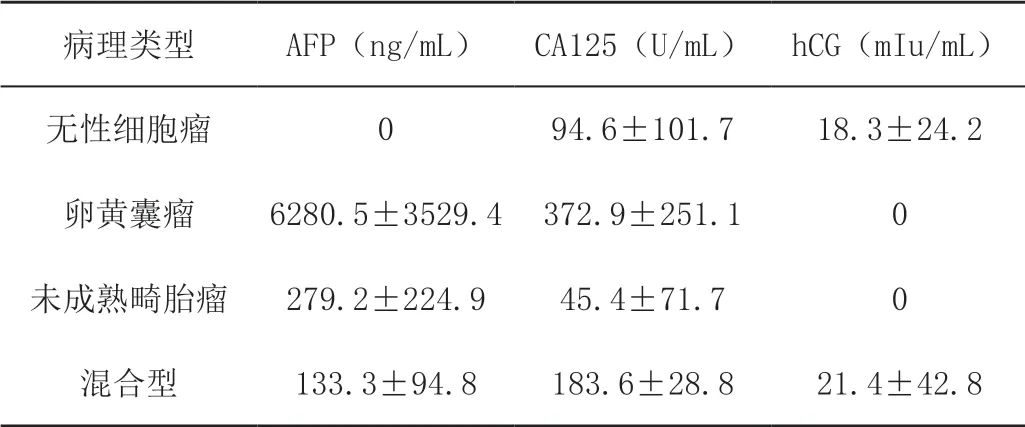
表1 卵巢恶性生殖细胞肿瘤不同病理类型的肿瘤标志物水平(均数±标准差)
2.3 声像图表现
肿块形态不规则,最大直径为8.5 ~25.7 cm,平均(13.8±4.3)cm。声像图上可分为囊性肿块4 例(2 例卵黄囊瘤、2 例未成熟畸胎瘤),实性低回声肿块12 例(均为无性细胞瘤),囊实混合回声肿块19 例(10 例卵黄囊瘤、4 例未成熟畸胎瘤、4 例混合型生殖细胞肿瘤、1例无性细胞瘤)。无性细胞瘤主要表现为实质性低回声团,部分可伴小片状液性暗区(见图1A 和B)。卵黄囊瘤声像图主要表现为囊实混合回声团,内呈蜂窝状改变(见图2A 和B)。未成熟畸胎瘤和混合型生殖细胞肿瘤主要表现为不规则的囊实混合回声团,内可见蜂窝状及多房样分隔回声,部分内见细小点状强回声(见图3A 和B)。彩色多普勒显示所有肿块血流信号丰富,频谱峰值流速8.5 ~25.7 cm/s(13.8±4.3 cm/s),RI 0.27 ~0.62(0.44±0.11)。8 例卵黄囊瘤伴有大量盆腹腔积液(见图2C 和D),4 例卵黄囊瘤伴有胸腔积液,2 例混合型及4 例无性细胞瘤伴有中量盆腹腔积液(见图3C 和D)。
3 讨论
卵巢肿瘤按照细胞起源分为上皮性肿瘤、性索间质肿瘤、生殖细胞肿瘤及其他类型。除了成熟性畸胎瘤是良性的生殖细胞肿瘤,其余均为恶性,病理类型以无性细胞瘤多见,其次为内胚窦瘤(又称卵黄囊瘤)、未成熟畸胎瘤、混合型生殖细胞肿瘤,而非妊娠期绒毛膜癌、胚胎性癌及恶性卵巢甲状腺肿非常罕见[3]。恶性生殖细胞肿瘤主要好发于少女及青春期,恶性程度高,肿块较大,可伴有腹盆腔积液[4]。大部分病人因腹胀或腹痛、腹盆部包块就诊,少部分有阴道的不规则流血。由于卵巢位于盆腔内,多数患者可无明显的临床症状,直至就诊发现的时候通常肿块较大,因此早期发现以及术前准确的影像学诊断能够帮助临床制定更合适的治疗方案。文献报道彩色多普勒超声对卵巢恶性肿瘤的诊断敏感性可达87%,结合肿瘤标志物、CT、MRI 等检查,术前可初步判断卵巢肿瘤的良恶性[5-7],因此彩色多普勒超声对恶性卵巢生殖细胞肿瘤的诊断非常重要。
肿瘤标志物升高的原因与肿瘤细胞成分有关。恶性卵巢肿瘤常伴有AFP、CA125、hCG 的异常升高。AFP 是由胚胎期卵黄囊及不成熟肝细胞产生的一种特异性糖蛋白,出生后AFP 的合成很快受到抑制,当组织细胞发生恶性病变时有关基因重新被激活,原来丧失合成AFP 能力的细胞又重新开始表达,以致血清AFP 含量成倍增加,故为卵黄囊瘤的特异性标志物,它对卵黄囊瘤的术前诊断、疗效观察及术后随访非常重要[8]。同时文献报道未成熟畸胎瘤AFP 阳性率为66.7%[9]。本文显示所有的卵黄囊瘤AFP 明显升高,最大值可达10000 ng/mL。4 例未成熟畸胎瘤和4 例混合型AFP 也有一定程度的升高。CAl25在胚胎时期的体腔上皮及羊膜有阳性表达,在出生后消失。在临床上CA125 升高的主要意义是提示卵巢癌的可能,同时CA125 的升高程度与卵巢癌的恶性程度有关[10]。本文显示CA125 在各个类型均有一定程度的升高,平均191.7 U/mL。绒毛膜癌、胚胎性癌常伴有绒毛膜促性腺激素(hCG)的升高。成分单一的无性细胞瘤不分泌激素,但是约5%的无性细胞瘤含合体滋养层,可分泌hCG。所以无性细胞瘤和混合型生殖细胞肿瘤hCG 水平可升高,本文5 例无性细胞瘤和1 例混合型hCG 值升高,平均53.9 mIu/mL。
恶性卵巢生殖细胞肿瘤的患者都较年轻,本文患者年龄最小12 岁,最大57 岁,平均年龄(22.5±10.3)岁,仅一例57 岁(病理为无性细胞瘤)。肿瘤体积较大,最大25.7 cm,平均(13.8±4.3)cm。超声表现为囊性、实性低回声或囊实混合性包块,囊壁厚薄不均。文献报道,RI 小于0.4 对卵巢恶性肿瘤的诊断有较高的敏感性和特异性[11-12]。本文彩色多普勒显示所有肿块血流信号丰富,频谱峰值流速8.5 ~25.7 cm/s(13.8±4.3 cm/s),RI 0.27 ~0.62(0.44±0.11),与文献一致[13]。8 例卵黄囊瘤伴有大量盆腹腔积液,2 例混合型及4 例无性细胞瘤伴有中量腹腔积液,4 例卵黄囊瘤伴有胸腔积液。卵黄囊瘤为卵巢高度恶性生殖细胞肿瘤,占卵巢恶性肿瘤的1%,生长极快,转移的发生率也高,预后较差,90%于术后一年复发,大部分患者两年内死亡,因此对于儿童及年轻女性患者保留其生育功能显得非常重要[14]。未成熟畸胎瘤较少见,占恶性生殖细胞肿瘤的第三位,声像图以囊实混合性肿块为主,如肿块内有特征性的强回声(如毛发或骨骼)有助于诊断,但若肿块以神经组织为主、不含有特征性的强回声时,则难以和卵巢其他恶性肿瘤鉴别。本文4 例未成熟畸胎瘤术前超声表现为囊实混合回声的包块,肿块内部回声杂乱强弱不等,术后病理为未成熟畸胎瘤,可见未成熟神经外胚层组织及未成熟的间叶组织(伴灶性幼稚软骨、脂肪及骨样组织);2 例超声表现为单纯的囊性肿块,壁增厚不均匀,囊内透声差,血流信号丰富,频谱呈低阻,术前超声未正确诊断未成熟畸胎瘤。虽然未成熟性畸胎瘤复发率较高,但复发性瘤具有自未成熟向成熟转化的特点,随着时间的推移,恶性程度逐渐减低,复发瘤的病理分级减低。故应积极治疗复发瘤,并且采取有效的联合化疗,有望保留患者的生育功能[15]。
青春期的卵巢恶性肿瘤以生殖细胞肿瘤最常见,其次为性索间质肿瘤。笔者翻阅既往一例超声病例,声像图上见盆腔内10×5×9 cm 的囊实混合回声肿块,血流信号丰富,RI=0.43,术前超声诊断为卵黄囊瘤,术后病理诊断是卵巢幼年型颗粒细胞瘤。卵巢颗粒细胞瘤是性索间质肿瘤中发病率最高的一类,它具有内分泌功能,颗粒细胞可分泌雌激素,临床上常出现阴道不规则流血、性早熟、闭经、子宫增大合并内膜增生,因此结合临床表现及激素检查可在一定程度上与卵黄囊瘤鉴别。
卵巢恶性生殖细胞肿瘤容易误诊为卵巢浆液性或黏液性癌,声像图上都可呈囊实混合回声团,但生殖细胞肿瘤常见于幼女及年轻女性,而且可伴有AFP 或hCG 的升高;而浆液性或黏液性癌更多见于中老年女性,并且伴有CA125 的显著升高。近年来超声造影技术在妇科领域的应用日趋成熟,文献报道超声造影与磁共振检查对卵巢肿瘤的诊断效能相当,诊断结果高度一致[16-17]。良性的卵巢病变增强模式多呈较缓慢的均匀的低增强,血管分布以囊壁为主,;而恶性的卵巢病变则多为快速的不均匀的高增强,内部血管丰富且分支杂乱[18]。本文中8 例患者术前进行了超声造影检查(3 例为无性细胞瘤,5 例为卵黄囊瘤),超声造影表现为肿块整体呈快速的不均匀的高增强,并可见多条粗大的滋养动脉血管进入肿块内部,平均13 秒开始增强18 秒达峰,与文献报道一致。此外,经阴道超声弹性成像在附件肿块的良恶性鉴别方面也有一定的价值,一般良性肿瘤质地软因此弹性评分低;恶性肿瘤质地硬因此弹性评分高,弹性成像鉴别卵巢肿块良恶性的敏感性、特异性和准确率可高达90%[19]。特别是对于鉴别附件区炎性病变与恶性肿瘤、附件区黏稠囊性病变与实性病变,超声造影和弹性成像就很有价值。
综上所述,卵巢恶性生殖细胞肿瘤组织成分复杂,并且伴有肿瘤标记物水平的异常升高,声像图表现多样,但仍具有一定特征性,彩色多普勒超声结合临床特点及肿瘤标记物水平诊断卵巢恶性生殖细胞肿瘤具有较高的准确率。

