小梁切除术与Ahmed植入术治疗穿透性角膜移植术后继发青光眼的疗效比较△
李海军 任静 董良 杨潇远 祝磊
穿透性角膜移植(penetrating keratoplasty,PK)是治疗严重角膜病变,尤其是感染性角膜溃疡、圆锥角膜、角膜变性等,恢复眼球结构与视功能康复的主要术式。然而,文献报道[1],PK术后继发性青光眼(post-penetrating keratoplasty glaucoma,PKG)发病率18%~35%,其病因复杂,处理困难,眼压失控是导致角膜植片枯竭或移植失败的主要原因之一。探寻适宜治疗手段,提高手术成功率值得探讨。本研究回顾性分析常规小梁切除(TRA)术与Ahmed阀(AGV)植入术对PKG眼压的有效控制及角膜植片的影响。
1 资料与方法
1.1 一般资料收集我院2015年4月至2018年4月PKG患者资料47例47眼,按手术方式分为TRA组22例、AGV组25例,随访(24.3±5.2)个月。纳入标准:(1)PKG最大剂量降眼压药物使用后,眼压>21 mmHg(1 kPa=7.5 mmHg);(2)随访>6个月以上;(3)年龄>18岁。排除标准:(1) 角膜移植术后眼压增高,药物控制眼压<21 mmHg;(2)既往有青光眼病史;(3)板层或角膜内皮移植患眼;(4) 失访或随访统计资料不全者。本研究遵守赫尔辛基宣言,遵循河南省人民医院伦理委员会基本准则。
1.2 方法常规裂隙灯、眼底、眼压及前节光学相干断层扫描(AS-OCT)检查,并记录检查结果、手术治疗方式及药物使用情况及各项疗效指标。
1.2.1 穿透性角膜移植术主要步骤如下:5 g·L-1聚维酮碘结膜囊浸泡冲洗,眼球固定后用黏弹剂维持前房,植床制备,以角膜光学顶点为中心环形切除病灶,供体植片直径大于植床0.25~0.50 mm(植片>9.0 mm为大病灶角膜移植),10-0缝线间断密闭对称缝合植片,BBS置换前房黏弹剂,术毕给予常规抗炎及抗排斥处理[2]。
1.2.2 TRA术上方象限以穹隆部为基底制作结膜瓣,对应区域做4 mm×3 mm的巩膜瓣,0.2 g·L-1MMC棉片瓣下及筋膜下放置3 min,约100 mL生理盐水充分冲洗,瓣下灰线移行区域穿透性切除1 mm×2 mm小梁组织,对应位置虹膜根切,10-0尼龙线缝合巩膜,前房成形,8-0尼龙线缝合结膜组织,1.0 mL地塞米松针结膜下注射,术毕给予常规抗炎及抗排斥处理。
1.2.3 AGV植入术颞上方象限以穹隆部为基底,大于3点钟位范围放射状结膜切口,经外直肌与上直肌间钝性分离筋膜组织,暴露至巩膜赤道部,角巩膜缘后常规制作4 mm×3 mm巩膜瓣,1 mL空针插入阀管口,推注生理盐水初始化阀门,11~12 mm处预置5-0不可吸收丝线,固定阀盘,斜形修剪阀管,保留约1.5 mm适宜长度经瓣下植入前房,以不接触角膜及虹膜面为宜,10-0尼龙线缝合巩膜瓣及8-0尼龙线缝合结膜组织,术毕给予常规抗炎及抗排斥处理。
术后滤过泡瘢痕化,行针拨及结膜下注射5-氟尿嘧啶(5-Fu)抗瘢痕处理,眼压>21 mmHg者给予降眼压治疗,若超过三联用药,角膜植片水肿等改变,行经巩膜睫状体光凝(transscleral cyclophotocoagulation,TCP)治疗,手术均由角膜与青光眼专家完成,术后常规给予左氧氟沙星眼液、10 g·L-1环孢素A眼液抗炎及抗排斥处理,感染性角膜溃疡根据药敏试验给予抗炎药物治疗,糖皮质激素类药物酌情使用。
1.3 观察指标与疗效评价记录患者一般资料,如年龄、性别、视力、角膜原发病因,以及手术治疗方式及并发症,术前、术后眼压及角膜植片透明度作为主要疗效判定指标。眼压判断标准:(1)绝对治愈:无降眼压药物使用,且眼压≤21 mmHg;(2)条件治愈:使用≤2种降眼压药物,且眼压≤21 mmHg;(3)无效:最大剂量药物使用,眼压>21 mmHg[3]。角膜移植片混浊判断标准:(1)显效:单一抗青光眼术后角膜植片透明;(2)有效:联合降眼压药物和(或)TCP处理后角膜植片透明;(3)枯竭:即在强效类固醇药物治疗下,植片水肿持续≥1个月,新生血管形成导致不可逆性混浊或瘢痕形成[4]。
1.4 统计学分析所有数据均采用 SPSS 24.0 统计学软件分析。计量资料以均数±标准差表示,采用独立样本t检验或Mann-Whitney U非参数秩和检验,多个时间点两组整体比较采用重复测量数据方差分析,组内不同时间点比较采用LSD-q检验;手术成功率及并发症计数资料以“率(%)”表示,分别采用Mann-WhitneyU检验、Pearsonχ2检验,连续性校正或Fisher精确检验,导致眼压失控及角膜植片枯竭的危险因素采用多因素Cox比例风险回归分析。检验水准:α=0.05。
2 结果
2.1 一般资料TRA组与AGV组感染性角膜炎病变病例最多,烧伤次之,两组间不同病因所占百分比差异均无统计学意义(均为P>0.05)(见表1)。两组术前基线眼压差异无统计学意义(P=0.231)。两组间以自身晶状体为主,不同晶状体所占百分比比较,差异无统计学意义(P=0.659)。两组间性别、年龄、视力及用药种类、视力等基线资料差异均无统计学意义(均为P<0.05)。
2.2 眼压情况TRA组与AGV组术后1个月、3个月、6个月、1 a、2 a眼压均较术前下降,重复测量数据方差分析提示组内术后与术前比较,组间及各时间点交互比较,差异均有统计学意义(F组间=5.863,P=0.02;F时间=210.510,P<0.001;F组间×时间=14.880,P=0.005);进一步采取LSD-q检测,TRA组与AGV组内术后不同时间点眼压均较术前降低,术后3个月、1 a、2 a眼压,AGV组眼压均较TRA组更低,差异均有统计学意义(均为P<0.05),术后1个月、6个月,两组间眼压比较差异均无统计学意义(均为P>0.05)(见表2)。TRA组与AGV组绝对治愈分别为8例(36.36%)、16例(64.00%);条件治愈分别6例(27.27%)、6例(24.00%);无效分别为8例(36.36%)、3例(12.00%),总有效率分别为63.64%、88.00%,差异均具有统计学意义(均为P<0.05),AGV组有效率更高(Z=-2.13,P=0.033)。

表1 各组患者一般情况

表2 各组手术前后不同时间点眼压比较
2.3 术后并发症及处理TRA组与AGV组早期并发症以浅前房为主,TRA组共9例发生:8例I-II度浅前房,其中4例仅伴有脉络膜脱离,3例仅滤过过强,1例两者兼具,给予阿托品及激素药物治疗,1周左右维持前房稳定,结膜滤过过强者,加固巩膜瓣缝合后改善;1例恶性青光眼伴III度浅前房,行玻璃体切割联合晶状体摘除处理。AGV组3例发生浅前房,1例伴脉络膜脱离,未见III度浅前房发生,两组浅前房发生率差异有统计学意义(P=0.023)。其余前房积血、炎性渗出均有发生,但两组差异均无统计学意义(均为P>0.05)。后期以滤过泡包裹为主,行针拨包裹滤过泡+5-Fu注射处理,眼压失控后,改行TCP治疗,共8例行TCP治疗,其中2例单次TCP治疗,6例需重复TCP治疗眼压控制;AGV组4例发生包裹,其中3例行阀体包裹筋膜囊切除+5-Fu注射处理,辅助术后按摩,1例眼压相对控制,3例重复行TCP治疗眼压控制,但两组差异无统计学意义(χ2=3.628,P=0.057)。除AGV组1例发生特有阀管角膜接触外,两组间均无视网膜脱离、脉络膜下爆发性出血,两组术后总并发症发病率分别为45.45%、20.00%,差异无统计学意义(χ2=3.166,P=0.075)(见表3)。
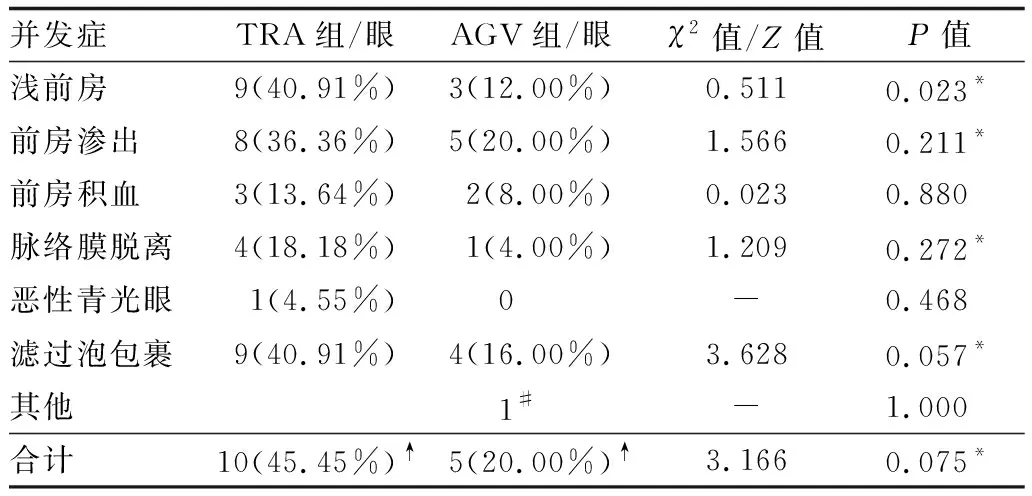
表3 各组术后并发症发生率比较
2.4 PKG术后角膜植片预后及危险因素单一抗青光眼术后TRA组与AGV组角膜植片显效改善分别为 11例(50.00%)、18例(72.00%);联合药物或TCP处理后有效改善TRA组9例(40.90%),其中6例(66.67%)联合TCP治疗,AGV组6例(24.00%),其中3例(50.00%)联合TCP治疗。TRA组角膜植片枯竭患眼共2例,1例TCP后眼球萎缩致使角膜枯竭,1例因烧伤植片新生血管化所致;AGV组1例角膜植片枯竭,原因不详,两组间植片总存活率分别为90.90%、96.00%,差异无统计学意义(Z=-1.544,P=0.123)。
对术后角膜植片发生混浊与否进行多因素Cox比例风险回归分析,提示角膜感染性病变、眼压反复升高是风险因素(均为P<0.05),其他手术方式与人工晶状体状态并无显著影响(见表4)。

表4 术后角膜植片发生混浊多因素Cox比例风险回归分析
3 讨论
角膜移植术后继发眼压增高,增加导致角膜植片排斥风险,严重影响术后视觉康复。PKG的发病病因复杂,治疗困难,PKG患眼最大剂量使用降眼压药物仍然失控者,及时采取有效的手术治疗是减少角膜植片排风险及促进视功能康复的必要选择[5-7]。然而,如何选择适宜的手术方式,国内较少探讨,本研究回顾性分析我院PKG患眼TRA术与AGV植入术临床效果,旨在合理施治,进一步提高手术成功率。
TRA术或AGV植入术,眼压的有效控制依赖于功能性滤过泡形成,PKG患眼往往合并活动性炎症或非健康状态结膜,滤过泡更易瘢痕化,即使联合MMC或5-Fu抗代谢药物处理,仍有10%~30%的滤过泡瘢痕形成或包裹,属于难治性青光眼之列[5,8]。本研究病例中,PKG发病以感染性角膜炎病例居多、眼烧伤次之,术后2 a多次随访中,术后眼压均较术前下降,且AGV组降眼压幅度更大(均为P<0.05),就有效率而言,TRA组与AGV组术后绝对治愈率分别为36.36%、64.00%,联合降眼压药物总体有效率提高至63.40%、88.00%,但仍有36.38%、12.00%无效率(Z=-2.13,P=0.033),国外Akdemir等[9]报道1 a随访TRA与AGV治疗PKG研究,AGV植入术降眼压幅度为64.2%,TRA为46.9%。Ajmousa等[10]5 a随访研究中报道也有证实AGV植入术后较TRA后利于控制眼压。尹文惠等[11]报道在PKG的TRA术后1 a随访中,其有效率为71.4%。本研究结果中,与国内研究报道具有一致性,两组均能有效降眼压,但AGV组降眼压幅度更大且有效率高,这应归因于PKG患眼TRA术后功能性滤过泡难以有效形成或AGV植入术后对功能性滤过泡的依赖更小。
本研究中早期常见并发症以浅前房为主,TRA组共发生9例(40.90%),I-II度浅前房8例,其中4例仅伴有脉络膜脱离,3例仅滤过过强,1例两者兼具,给予阿托品及激素药物治疗,1周左右维持前房稳定,结膜滤过过强者,加固巩膜瓣缝合后改善,1例恶性青光眼伴III度浅前房,行玻璃体切割联合晶状体摘除处理。AGV组3例(12.00%)发生浅前房,伴脉络膜脱离1例,未见III度浅前房发生,两组差异有统计学意义(P=0.023)。可见,TRA术后更易发生浅前房,往往因合并滤过过强或(和)脉络膜脱离所致,除外III度浅前房影响角膜植片需要前房形成处理外,I-II度浅前房辅助阿托品药物治疗,观察变化趋势予以处理,AGV植入术较TRA术发生率相对较低,应为阀门单相压力梯度控制或无巩膜穿透性切开致使持续低眼压而相对保持眼压稳定的原因,但也增加阀管植入机械性接触风险,良好的术中操作可减少相关风险。王正艳等[12]在PKG眼行TRA术的临床观察报道,浅前房是影响角膜植片的危险因素,围手术期的正确处理可降低其发生率与减少术后并发症。术后远期并发症以滤过泡包裹致使眼压失控为主,感染性角膜病变因其活动性炎症与手术创伤因素,易于促进滤过泡瘢痕,且化学烧伤患眼本身结膜等眼表的损伤,均不易形成滤过[13]。本研究病例中,TRA组2例针拨分离联合5-Fu结膜下注射,8例反复TCP治疗后有效,1例发生眼球萎缩;AGV组3例行Ahmed阀体包裹筋膜囊切除联合5-Fu注射,辅助术后按摩,眼压相对控制,3例反复行TCP治疗,术后无并发症。如李霞等[14]在经巩膜TCP术治疗PKG的研究中报道,TCP可重复运用于其他抗青光眼手术治疗眼压失控的患眼,利于眼压控制,减少严重并发症发生,且能保持角膜植片透明。因此,我们选择TRA治疗,应遵循感染性角膜病例控制稳定下,且无眼表损伤患眼为宜,若无AGV植入术禁忌证,应作为PKG患眼首选治疗方式,以减少滤过泡影响,TCP治疗是多运用于抗青光眼手术治疗失败后较好备选,但存在结果不可预料性风险因素,严重可导致眼球萎缩,临床治疗过程中,应分次、少量给予激光治疗为宜。
PKG患眼治疗成功,除眼压控制外,角膜植片的透明也是重要的衡量指标。本研究中,单一或联合处理后,TRA组与AGV组角膜总体存活率分别为90.90%、96.00%,差异无统计学意义(Z=-1.544,P=0.123)。致使角膜植片混浊的原因复杂,我们进一步采取多因素Cox比例风险回归分析,结果提示角膜感染性病因及眼压反复升高是风险因素。角膜植片混浊影响因素是多方面,正如Elhofi等[8]及关卫卫等[15]在PK术后移植片的转归研究中报道,早期角膜移植片混浊的主要原因为供眼角膜内皮细胞损伤及继发性青光眼;中晚期混浊的主要原因为排斥反应和病灶复发。Patel等[16]观察TRA术角膜植片情况,认为眼压的有效控制能降低植片混浊;Yakin等[17]比较AGV植入术与TRA术后对PKG角膜植片转归的研究中,AGV植入术更加适用于疑难青光眼类型,眼压失控不利于角膜植片存活。尽管本研究中手术方式与角膜植片混浊无显著关联,但术后浅前房与远期眼压反复升高是植片混浊的风险因素,AGV植入术较TRA术更能降低浅前房发生率,且单一的治疗其眼压控制的绝对有效率也更高,这有利于降低角膜植片混浊的术源性因素影响,同时加强围手术期抗炎,降低排异风险,也是降低角膜植片混浊的重要防控手段。
本研究尚存在许多不足,样本量小、随访时间短,为更全面了解术后继发性青光眼的影响因素、治疗方式的差异,尚需要对此类病例资料进行多中心大样本的随访研究。
总之,PKG属于难治性青光眼之一,眼压失控严重影响视功能康复,甚至导致角膜移植失败,TRA术与AGV植入术是有效治疗手段,但AGV植入术更适用于复杂青光眼,同时,加强围手术期抗炎,防治术后浅前房并发症,功能性滤过泡失效后辅助TCP治疗,更利于眼压控制及降低眼压反复升高对角膜植片混浊的影响。

