两种糖化血红蛋白临床检验方法的一致性评价
张小静 潘晓芳 邢立森 张润锋 李杨玲 吴静标
糖化血红蛋白(Glycated Hemoglobin,HbA1c)作为糖尿病早期诊断和病后血糖监测的重要指标,是评估糖尿病病人长期糖化控制的主要度量[1]。2011年世界卫生组织(World Health Organi⁃zation,WHO)推荐采用HbA1c 作为糖尿病的诊断金标准生物标志物[2]。《中国2 型糖尿病防治指南》建议用HbA1c 评估患者的血糖控制情况[3]。实验室检测中,有新的检验方法或检验仪器时,为保证测量结果的一致性,需要评价新的检验方法或检验仪器的结果的一致性,以保证新检测系统的测量结果与旧检测系统的结果一致。本文使用对照和考核系统的糖化血红蛋白检测试剂进行检测,除常规的统计方法外,还使用了Bland⁃Altman 分析法,以期全面比对两个检测系统的检测方法一致性。
1 材料和方法
1.1 材料
1.1.1 检测样本
2019年3月至6月收集本院检验科的99 名受试者静脉全血样本,保存在-80℃的冰箱中,收集完毕后试验前一次性解冻后进行测试。
1.1.2 仪器和试剂
①对照系统仪器:全自动糖化血红蛋白分析仪(型号:HA⁃8180,厂家:ARKRAY Factory,Inc.)。②考核系统仪器:全自动糖化血红蛋白分析仪(型号:HA⁃120,厂家:广东优尼德生物科技有限公司(以下简称优尼德))。③对照系统试剂:洗脱缓冲液ELUENT 80A 和80B(高效液相色谱法(HPLC法))(批号分别为:8H1321 和8H1331)、HbA1c 溶血剂(批号:8H1361)、HbA1c 校准品(批号:8H1327)、HbA1c 质控品(批号:8H1326),以上厂家均为ARKRAY Factory,Inc.。④考核系统试剂:糖化血红蛋白A1c 洗脱缓冲液A 试剂盒和B 试剂盒(高效液相色谱法)(批号分别为:2820190101 和2920190101)、HbA1c 溶血剂(批号:3020190101)、HbA1c 校准品(批号:HJ20190101)、HbA1c 质控品(批号:HZ20190101),以上厂家均为优尼德。
1.2 检测方法
分别用考核系统和对照系统单次检测99 例全血样本。
1.3 统计学处理
采用SPSS 19.0 进行基础数据、分布频数、线性相关分析和回归分析、对数据进行正态性D'Agostino 检验和t 检验,对试验的系统误差进行分析。并用Medcalc V19.0.4 进行Bland⁃Altam 分析。参照《体外诊断试剂临床试验技术指导原则》、《体外诊断试剂临床试验技术指导原则》、EP9⁃A、《医学统计学》等法规性文件和书籍,对表检测结果行统计学分析[4⁃7]。
2 结果
2.1 检测结果
99 例全血样本分别在对照系统和考核系统的糖化血红蛋白检测试剂中分别进行测试,每个样本均是单次测定。对照系统和考核系统检测结果及两者配对差值。见表1。
2.2 一致性分析
2.2.1 基础计算
对照系统、考核系统及两个系统的各个统计量计算结果。见表2。
2.2.2 数据分布频数图
结果表明对照系统、考核系统的测量结果主要集中在5.42 和6.42 之间。见图1。

表1 对照系统和考核系统检测结果和配对差值Graph 1 Results of control system,assessment system,and paired difference results
2.2.2.1 线性相关分析 以对照系统为自变量X,考核系统为因变量Y,作散点图,R2=0.9779,两个检测系统之间的结果具有良好的线性关系。见图2。
2.2.2.2 线性回归分析 回归模型F 检验和回归系数b 的t 检验:H0:b=0,H1:b≠0,α=0.05,作数据分析与统计检验,两种检测系统的测量结果间存在着显著的直线关系,差异有统计学意义(P<0.05)。见表3。

表2 基础计算结果Table 2 Basic calculation results
2.2.3 Bland⁃Altam 分析
Bland⁃Altam 分析,仅有4/99(4.04%)界外点数,对照系统、考核系统的测量结果一致。见图3。
2.2.4 分析系统误差
2.2.4.1 D'Agostino 检验 采用D(D'Agostino)检验进行正态性检验,建立假设:H0:数据总体服从正态分布,H1:数据总体服不从正态分布,α=0.05,作数据分析与统计检验,对照系统、考核系统的测量结果服从正态分布。见表4。
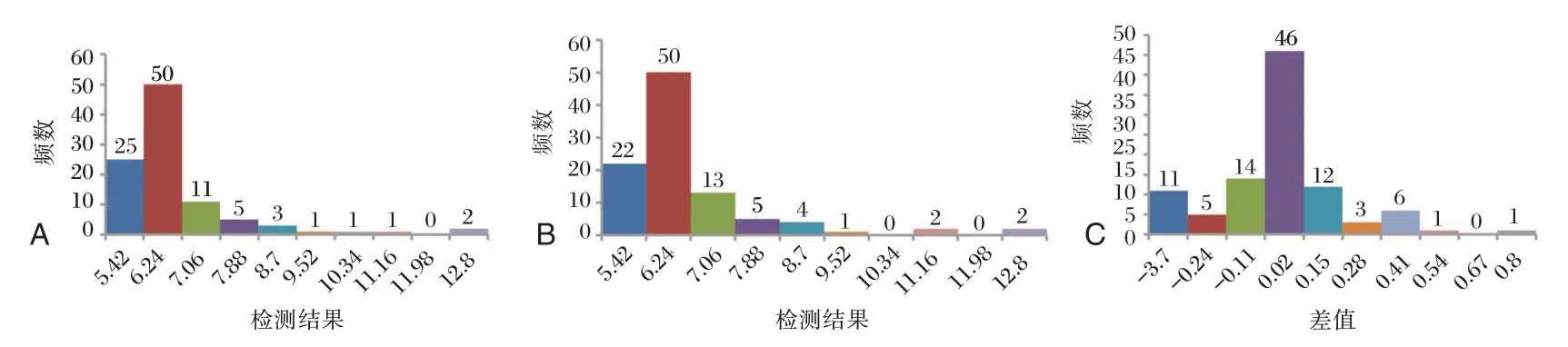
图1 对照系统、考核系统及配对差值分布频数图Figure 1 Distribution frequency graph of control system,assessment system results and paired difference results

图2 对照系统与考核系统测量结果散点图Figure 2 Scatter plot of control system and assessment system results
2.2.4.2 t 检验数据分析 Spearman 进行分析,95%CI:0.901 0~0.954 3。两种检测系统直线相关关系成立(r=0.932 5,t=25.436,P=0.000)。
3 讨论
糖尿病是临床上发病率最高的慢性病之一,长期处于高血糖的患者,会引发糖尿病并发症,并引起糖尿病患者残疾或死亡,因此做到早发现、早预防、早治疗是降低糖尿病发病率和死亡率的关键[8]。HbA1c 可以规避服用药物和胰岛素、短时间血糖波动、饮食和运动情况等影响,使糖尿病的诊断更稳定,结果更可靠,是评价长期血糖控制的金标准[9⁃10]。

表3 数据直线回归分析结果Table 3 Linear regression analysis results
Bland⁃Altman 法作为新的图形分析法,可以从集中趋势、离散趋势、同步变化程度多角度评价新旧检验方法或检验系统的一致性,弥补了t检验、相关分析和回归分析的不足,是评价两种检验方法一致性的标准方法之一[11]。

图3 对照系统和考核系统检测结果的Bland⁃Altam 图Figure 3 Bland⁃Altam diagram of control system and assessment system
临床上检测血清糖化血红蛋白的方法主要有离子交换高效液相色谱分析法、微柱法、电泳法、亲和层析法、免疫法5 种[12⁃13]。美国临床化学协会(American Association for Clinical Chemistry,AACC)糖化血红蛋白标准化分会和国际临床化学和实验医学联合会(International Federation of Clinical Chemistry and Laboratory Medicine,IFCC)HbA1C 标准化工作组建议,以糖尿病控制与并发症研 究(Diabetes Control and Complications Trial,DCCT)中所“指定的方法”—高效液相色谱法(High Performance Liquid Chromatography,HPLC)作为检测糖化血红蛋白的金标准,希望以此使大多数的实验方法能够参照“指定的方法”实现标准化[14]。2002年美国糖尿病协会(American Dia⁃betes Association,ADA)将HPLC 法作为监测糖尿病控制的金标准,并规定所有糖尿病患者均应测定HbA1c[15]。

表4 数据差值正态性检验结果Table 4 Normality of difference between control system and assessment system
ARKRAY Factory,Inc.公司的高效液相色谱系统被中国三甲等大型医院广泛应用,在中国市场占有率高,检测糖化血红蛋白口碑好[16⁃18]。美国HbA1c 标准化计划使用离子交换HPLC 为“参考方法”,是目前为HbA1c 测定的指定比对方法[19]。本文选用优尼德的糖化血红蛋白A1c 洗脱缓冲液A 试剂盒(高效液相色谱法),原理实际上就是HPLC 法,该方法具有检测结果变异系数小、可以通量检测的优势。利用Bland⁃Altman 法作为图形分析法,可以从集中趋势、离散趋势、同步变化程度多角度评价两种检验方法的一致性,弥补t检验、相关分析和回归分析的不足。结果表明优尼德和ARKRAY Factory,Inc。公司两种检测系统对糖化血红蛋白测量结果一致性良好,优尼德的检测系统适用于糖化血红蛋白检测。Bland⁃Al⁃tam 分析显示界外点数/总分析样本数为4/99,只有4.04%不在[⁃1.96Sd,+1.96Sd]内,对照系统与考核系统测量结果测量结果一致性良好。D'Agostino 检验结果表明99 例样本不服从正态分布,t检验、线性相关分析和回归分析都表明考核系统与对照系统测量结果之间具有良好线性关系。
但是此次实验尚有不足,首先是分析样本数量不大;其次是未引入国际标准品或者国家标准品。未来将通过比对或参加原卫生部林建中心室间质评等方式进一步进行试剂考核来确证该体系的临床符合率,并对试剂的稳定性、可重复性、批间差等相关性能验证进一步开展。

