打造有生活味的化学课堂
陈玲
摘要:基于“从生活中来,到生活中去”的教学设计思想,分析了以生活情境、核心问题、学生活动、评价任务和学科知识为主线的教学设计结构。以“几种常见的盐”为例,分享了打造有生活味的课堂实录与设计意图。从生活化情境引入新课、生活化内容展开探究、生活化应用小结知识、生活化素材布置作业四个方面进行了反思,促进对有生活味课堂的深入研究。
关键词:生活味;几种常见的盐;教学设计;核心素养
文章编号:1008-0546(2021)11-0053-05中图分类号:G632.41文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.11.013
杜威提出“教育即生活”“学校即社会”的教育思想,强调要从学习者的经验和活动中学,要把知识的获得过程与学习者的生活活动紧密联系起来[1]。《义务教育化学课程标准(2011版)》也指出,化学教学要密切联系学生生活实际,要从学生已有经验出发,让他们在熟悉的生活情景和社会实践中感受化学的重要性,了解化学与日常生活密切关系,逐步学会分析和解决与化学相关的一些简单的实际问题[2]。而纵观现在的化学课堂,部分教师的教学脱离了学生生活,更多地注重化学学科知识的解析,使得学习单调而乏味,无法使学生感受学科知识的有用性。笔者以“几种常见的盐”为例,展示如何充分挖掘生活化的素材,让化学课堂具有生活味,让学生在具体的生活情境中习得知识、增长能力、丰富情感。
一、打造有生活味的课堂教学设计结构分析
打造有生活味的课堂教学设计基于“从生活中来,到生活中去”的理念进行整体设计。每一环节注重以生活情境(实物或图片)为起点,引发出生活中的真实问题,通过探究、阅读分析、交流讨论等多样化的活动产生新的认知,最后又走进生活,分析生活现象,解决实际问题。
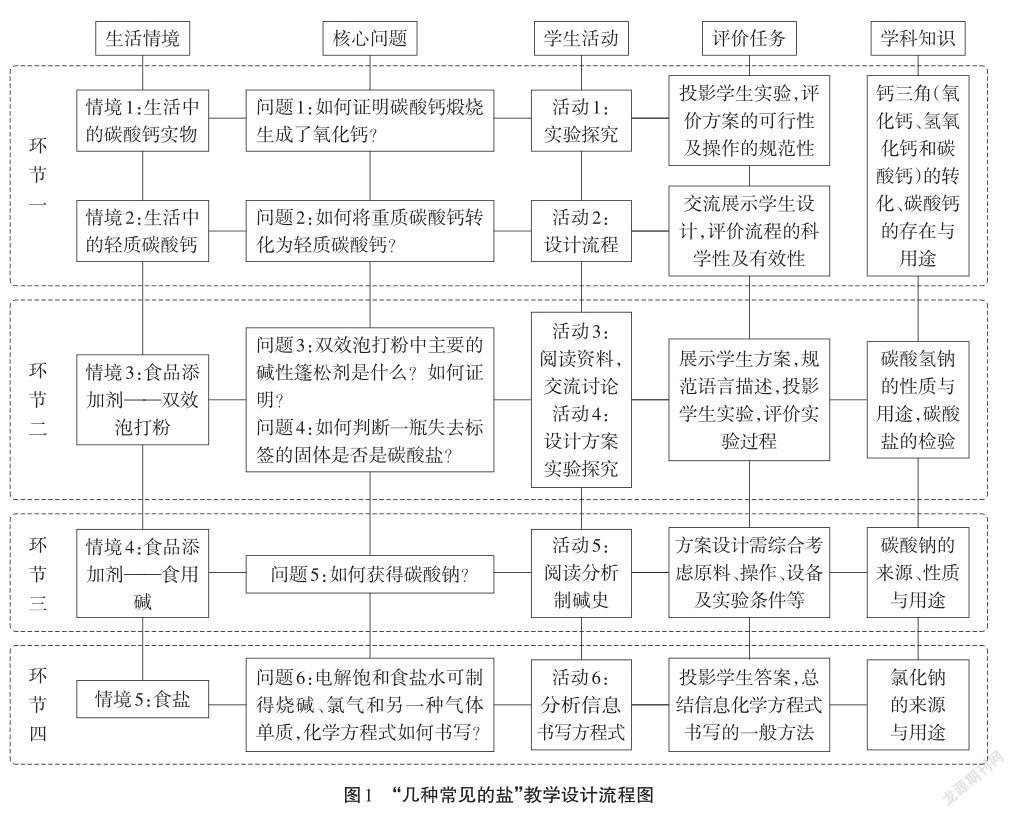
“几种常见的盐”课标要求是“了解食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途”。生活中,学生对氯化钠和碳酸钙有一定的了解,对纯碱和小苏打相对比较陌生,笔者基于学生已有的生活经验,充分挖掘生活素材,以“碳酸钙的性质与用途→碳酸氢钠性质与用途→碳酸盐的检验→碳酸钠的性质与用途→氯化钠性质与用途”为主要内容线索进行教学活动设计,具体教学设计结构见图1。
二、打造有生活味的课堂实录与设计意图
【教师】(实物展示)一只无色透明的玻璃瓶(内装生活中常见的含碳酸钙的物质,如石灰石、鸡蛋壳等);(图片展示)汉白玉、溶洞、水垢。提问:这些物品形状各异,但它们都含有同一种物质。大家知道是什么吗?
【学生】碳酸钙
设计意图:生活中含碳酸钙的物品随处可见,在之前的教学中,学生对碳酸钙也有了一定的了解。学习是一个主动的过程,以学生熟悉的实物进入课堂,坚持以生为本,有助于激发学生兴趣,帮助学生快速进入课堂,提高学习效率。
环节一:生活中的碳酸钙
【教师】对于碳酸钙,大家已经知道了些什么?
【学生】(代表回答,同伴补充)碳酸钙难溶于水,会与稀盐酸反应,可用于实验室制取二氧化碳。
【教师】作为建筑材料的石灰石,它是“怕”酸的。那它还怕什么吗?(展示图片)圆明园焚烧前后对比图。
实验1:先敲打石灰石、再煅烧、最后再敲打煅烧后的物质。
【教师】探究石灰石煅烧后的固体是什么?如何证明?
【学生】设计并完成实验(教师巡视、捕捉学生操作及现象,拍照上传。)
【教师】(图片展示烧烤扇贝的场景)为什么扇贝壳未变得疏松易碎?
【学生】(各抒己见,教师布置生活作业)烧烤时,分别将扇贝贝壳直接置于碳上灼烧、将扇贝壳放在距离碳有一定距离的金属架上灼烧,对比贝壳的变化,可拍照或拍成视频与未烧烤的同学分享。
【教师】碳酸钙有哪些实际应用?
【学生】烧制生石灰、制玻璃、炼铁等。
【教师】有的组在刚才的探究过程中,制得了轻质碳酸钙。
资料卡1:轻质碳酸钙又称沉淀碳酸钙,轻质碳酸钙是用化学加工方法制得的。重质碳酸钙,简称重钙,是由天然碳酸盐矿物如方解石、大理石、石灰石磨碎而成。
【教师】请设计出石灰石为原料生产轻质碳酸钙的主要流程(形式不限,可图示,亦可用化学方程式表示)
【学生】独立完成后,展示不同方案,分析评价。
【教师】轻质碳酸钙有哪些实际应用?
【学生】可做牙膏里面的摩擦剂、补钙剂、石头纸等。
设计意图:建构主义教学观指出,教学不能无视学习者的已有知識经验,而是应当把学习者原有的知识经验作为新知识的生长点,生长出新的知识经验。学生生活中认识到的大理石、石灰石等是坚硬的,是不怕风吹雨淋、不怕火烧的,然而圆明园的3D复原图与现在的图片同时呈现,强烈的视觉反差一方面激发学生的爱国热忱,另一方面让学生认识到碳酸钙是“怕”火烧的。接着经历探究的一般过程,通过探究对碳酸钙的性质有了更深的认识。再抓住学生实验过程中的生成资源——制得了轻质碳酸钙,引导学生设计生产流程图,巩固了钙三角的转化,渗透转化观,体现了变化与守恒的学科观念,发展了学生分析、综合、创造的高阶思维,帮助学生形成实验探究与创新意识的核心素养,同时也拓展了碳酸钙的用途,还起到了很好的承上启下的作用,为碳酸氢钠的学习做了铺垫。
环节二:生活中的碳酸氢钠
【教师】实物展示“双效泡打粉”,阅读说明(见图2)。

资料卡2:双效泡打粉一般由酸性蓬松剂(焦磷酸二氢二钠、磷酸二氢钙等)和碱性蓬松剂(____和轻质碳酸钙等)以及淀粉等复配而成。双效泡打粉在接触水过程中,碱性蓬松剂与酸性蓬松剂反应产生二氧化碳。
【教师】“双效泡打粉”中起发泡作用的碱性蓬松剂是什么?(碳酸钙的含量只有≤3%)
【学生】(继续看说明,结合产品说明中各成分的含量,提出猜想)碳酸氢钠能与酸溶液反应生成二氧化碳。
实验2:碳酸氢钠与稀盐酸反应并检验产生的气体
【学生】(书写化学方程式并解释)双效泡打粉中,“碱性蓬松剂与酸性蓬松剂反应产生二氧化碳”是第一次产气,而第二次产气是在烘焙加热过程中释放出。
【教师】(布置家庭实验)利用生活中的物质(如小苏打或双效泡打粉、白醋、生石灰干燥剂等)和设备,探究双效泡打粉的第二次产气原理。
【教师】碳酸氢钠在生活中有哪些实际应用?
【学生】泡沫灭火器(化学泡沫灭火器内有两个容器,内筒内盛放酸性溶液Al2(SO4)3,外筒内为NaH? CO3,灭火器倒立,两种溶液混合在一起,就会产生大量的CO2);碳酸氢钠片(治疗胃酸过多)。
【教师】为什么碳酸钙和碳酸氢钠都能与稀酸溶液反应生成二氧化碳?
【学生】(交流讨论,教师点评小结)碳酸盐的检验方法。
设计意图:通过对生活中双效泡打粉发泡原理的探究,突破本节课的重难点知识——碳酸盐的性质及检验方法。学生第一次看双效泡打粉的成分说明书,对发泡的原理有了初步猜想:碳酸钙与酸性蓬松剂反应产生气体;再看泡打粉说明书中碳酸钙的含量只有≤3%,对碳酸钙起发泡作用产生疑虑;学生结合资料信息,三看泡打粉成分说明书,对碳酸氢钠起发泡作用做出大胆猜想。通过同伴互助,设计方案,完成实验,同学们证明了自己的猜想,收获了成功的喜悦,提升了科学探究与实践的核心素养。同时,在分析双效泡打粉的成分说明书的过程中,从定性走向了定量,凸显了证据推理,发展了阅读、分析、提取信息的能力。对于双效泡打粉的第二次发泡原理的探究,让学生回家完成,体现了科学的真实与严谨。由碳酸氢钠与酸反应到碳酸氢钠的实际用途,体现了性质决定用途的学科观念;由碳酸氢钠和碳酸钙都能与酸反应这一共性,反思它们的结构,体现了化学学科的性构观,凸显了宏观辨识与微观探析素养。
环节三:生活中的碳酸钠
【教师】刮刮乐游戏:判断实验盒内一瓶未贴标签的白色固体是否含碳酸盐,得出结论后刮开覆盖层。
实验3:(学生分组实验,教师指点操作规范)巩固碳酸盐的检验方法。
【学生】根据微观示意图,说出反应的微观本质。
【教师】对于碳酸钠,你还有哪些认识?
【学生】学习溶液酸碱性时,知道碳酸钠的俗称叫纯碱,水溶液呈碱性;学习碱时知道纯碱可用于制备烧碱;学习盐第一课时知道,还可以与氯化钙溶液反应。
【教师】(实物展示食用碱,拓展纯碱的实际应用)日用化学工业、造纸、印染、制玻璃等。
【教师】碳酸钠的用途很广,需求量也很大,碳酸钠从何而来?
【学生】盐碱湖里。
【教师】(图片展示盐碱湖)自然界中的纯碱纯度低,产地分散,远远不能满足社会对它的需求,所以需要通过化学方法生产。
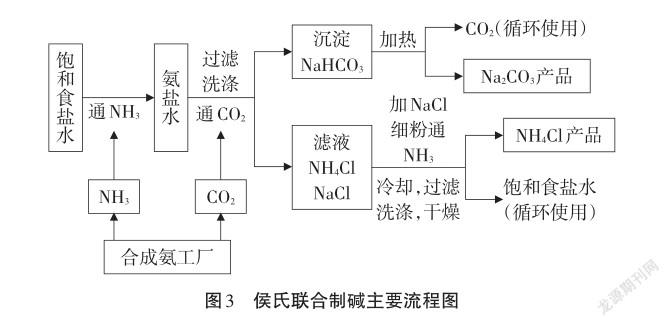
资料卡3:1788年第一个工业制碱法——吕布兰制碱法→1861年,索尔维制碱法→察安法制碱→1943年侯德邦创立侯氏联合制碱法。1918年11月,范旭东等人正式创办亚洲第一座纯碱厂——永利制碱公司,经过不断地改进,1926年6月,永利碱厂生产出洁白、合格的“红三角”牌纯碱,打破了洋碱在中国的垄断地位。侯德榜撰写了《纯碱制造》一书,将制碱工艺与世人分享,显示出中华民族兼善天下的传统美德。1938年,侯德榜下决心自主研究新法制碱。经过近一年的反复、扎实试验,取得了突破,一个新的制碱方法悄然出现。侯氏联合制碱主要流程如图3。
【教师】制取原理是什么?请写出流程中的涉及的两个核心反应。
【学生】先独立完成,有困难时交流讨论(教师小结信息方程式书写方法)。
设计意图:刮刮乐游戏增强了实验的趣味性,巩固了碳酸盐的检验这一重点知识,顺理成章地引出碳酸钠的学习。通过宏微结合,了解碳酸盐与酸反应的微观本质。好的教学不仅要注重学生已学知识,更要走在发展前面。关于碳酸钠的学习,笔者设计了三个问题:对于碳酸钠,你还有哪些认识?→碳酸钠从何而来?→制取原理是什么?问题的设置有梯度,符合学生认知规律,通过三个问题,学生建构了关于碳酸钠的较完备的知识网络,让零散的知识更系统;世界制碱史的介绍,一方面激发了学生的民族自信心和自豪感,另一方面制碱工艺的改进史渗透了绿色化学观念,也让学生感受到科学家们永不言弃,不断追求完美的精神,帮助学生形成科学精神与社会责任的核心素养。侯氏制碱法主要流程的分析,渗透了守恒观、变化观,也为下一环节中氯化钠的教学做了铺垫。
环节四:生活中的氯化钠
【教师】流程中我们看到,饱和食盐水是制备纯碱的重要原料之一。工业上电解饱和食盐水还可制得烧碱、氯气和另一种非金属单质。请同学们尝试著书写出化学方程式。
【学生】化学方程式书写
【教师】关于氯化钠,大家还知道些什么?
【学生】可以蒸发结晶获得。氯化钠生活中可用于调味,腌制食品,菠萝浸泡过食盐水后口感更好,积雪上撒盐可以融化冰雪;医疗上可用于制生理盐水;农业上还可以用于选种。
【教师】(补充氯化钠的用途)氯化钠可增大硬盘存储空间。
【教师】氯化钠,家家户户都有的一种盐,在生活、医疗、农业、工业乃至科技方面都有着重要用途。
设计意图:拓展氯碱工业,一方面丰富了氯化钠的工业用途,另一方面及时巩固了化学方程式的书写。氯化钠的知识在沪教版第五章、第六章都有涉及,通过回忆已学知识,让氯化钠的性质及用途更加全面。将氯化钠安排在最后环节,一方面是因为四个环节中涉及的四种物质是环环相扣的,更重要的是因为,作为学生每天都接触的一种盐,它在生产、生活,在工业、农业、生命科学、科技领域等方面都有着广泛的用途,将它安排在课的最后,无需任何豪言壮语,就能让学生真切感受到盐的广泛用途,感受到化学的价值。
三、打造有生活味的课堂教学思考
1.生活化情境引入新课,激发学生学习兴趣
兴趣是一种心理倾向,是以认识和探索外界事物的需要为基础。本节课从学生已有的经验出发,引入了大量的生活素材。课堂伊始,展示有关碳酸钙实物及图片直接吸引了学生的眼球,抓住了学生的注意力,高效地展开了教学;通过双效泡打粉实物展示,承接上一环节碳酸钙的教学,也开启了下一环节碳酸氢钠的探究,将课堂气氛推向高潮;再有关于食用碱的实物展示,让学生对碳酸钠有了系统的认识;最后,氯化钠的展示让学生惊叹看似平凡的氯化钠居然有那么广泛的用途,让人惊叹让人着迷。生活情境适时适当地引入课堂,不断地激发并维持着学生的学习兴趣,让学生的学习更有主动性,切实转变了学生的学习方式。
2.生活化内容展开探究,发展学生核心素养
从生活化的内容出发,产生实际问题,通过多个探究实验促进学生素养发展。本节课,环节一中探究了石灰石煅烧后的固体产物,同学们经历了猜想假设→设计方案→合作实验→得出结论→交流反思的过程,培养了学生科学探究及创新意识的素养,实验中钙三角的转化培养了学生变化观念和守恒思想。环节二中通过定性与定量相结合的方式对比分析了双效泡打粉的成分,对泡打粉的发泡原理做了探究;由性构观推理出碳酸钙、与碳酸氢钠有共性的原因;紧接着环节三中碳酸盐的检验证明了猜想,通过宏微结合,得出碳酸盐与酸反应的微观本质。环节三中从环保、原料利用率等角度分析了制碱工业的发展史,有助于学生形成科学精神与社会责任的素养。
3.生活化應用小结知识,体验化学学科之美
学习化学的最终目的是为生产生活服务。本节课,在研究物质后及时联系生活应用进行小结,体现了物质性质与用途的辩证关系,展示了化学物质的价值美。环节一通过设计制备轻质碳酸钙的流程,体现了化学变化的神奇美;环节二碳酸盐的应用中,将“宏观—微观—符号”表征相结合,体现了化学思维的独特美;环节三中,化学家们对绿色化学的孜孜追求,使得制碱工艺不断完善,体现了化学追求的真善美;环节三、四中氯化钠的用途,学生利用质量守恒定律认识反应原理,体现了化学的思辨美。
4.生活化素材布置作业,形成科学物质观念
义务教育阶段化学课程的基础性与课堂时间的有限性往往使得生活中的化学问题未能在一节课得到很好地解决,此时切不可将生活问题理想化、虚假化,而是需要学生本着严谨求实的科学态度课后继续探究。本节课,一个是带着疑问继续探究碳酸钙是否真的“怕”火?让学生对碳酸钙的分解条件有更科学的认识;另一项作业是继续探究双效泡打粉的第二次发泡原理,学生根据研究,充分利用生活中的物品完成探究,锻炼了学生的能力,保证了知识的科学性。
参考文献
[1]张芳芳.高中化学生活化教学的应用探索与案例设计研究[D].开封:河南大学,2016
[2]中华人民共和国教育部.义务教育化学课程标准(2011版)[S].北京:北京师范大学出版社,2012

