基于核心素养的“教学设计”
——以钠与溶液反应复习课为例
胡世丰 张 雨
(1.广东省珠海市广东实验中学金湾学校 519090;2.广东省开平市第一中学 529367)
一、问题的提出
《2017年版普通高中课程标准》从化学观和思维模式对学科思维进行阐述,确定证据推理与模型认知是化学核心素养的思维核心,如何利用化学学科特点来孕育学生的核心素养和培养其理性思维是教学的重点?高三一轮复习教师培养学生的化学素养,教师得基于对整个高中化学教材的理解和把握,结合学情以及自己的理解创造性的使用高中教材.
发展心理学家皮亚杰的图式理论认为:思维间接性是以原有化学知识为媒介(模型)来认识(类比)客观事物,借助已有的知识和经验理解或把握那些没有感知过的事,预见和推知化学反应现象和原理;思维的概括性就是把同一类化学知识的共同特征和本质特征抽取出来加以概括,形成化学反应原理模型.认知规律受维果斯基的最近发展区理论影响.因此高三复习重点在于创设情境,创设情境有利于学生理解和掌握化学的基本原理和模型;通过引导学生观察实验现象,提高学生的实证意识和逻辑思维;培养学生运用科学的思维方式认识事物、解决问题、指导行为等素养.
二、课前设想
在化学教学情景的创设中,劳顿认为要根据对学生已有知识的了解作为基础,设计出有针对性、有效性的教学设计.创设情境能帮助学生有效地整合、同化所学内容,形成知识体系.让学生运用已有知识在阅读、比较、分析、讨论的基础上解决化学问题,在此基础上培养学生的化学学科素养,提升高三学生解决实际问题的能力.其次,泰勒的目标模式认为在高三的教学中,教师要深入研究高考试题及命题趋势,通过师生双边活动,将学生的问题分解成小问题、小专题,化解知识难点逐个突破.以上理论也为本节课提供了三条线索:一是知识线,二是能力线,三是认知能力.可以构建出以下的教学设计思路如图1.

图1
三、课堂教学过程与设计意图
课堂活动1.引入:联系旧知,创设情境.西汉时期记载的“曾青得铁,则化为铜”,描述的化学反应是什么?该反应能发生是因为铁比铜的什么性质强?那么我们在高一学习过一种金属性很强的物质,把它丢到水里可以剧烈反应,该物质是什么?它与水反应的现象如何描述?这些现象分别对应了它的哪些性质?能否写出相应的化学方程式?

图2
[学生活动]回顾必修1教材,根据图2回忆实验现象并完成学案.
[师生活动]请各学习小组代表对钠与水反应实验现象进行汇总,对学生的表现进行鼓励和评价,请学生代表根据表1在黑板上写出简要的现象跟本质.
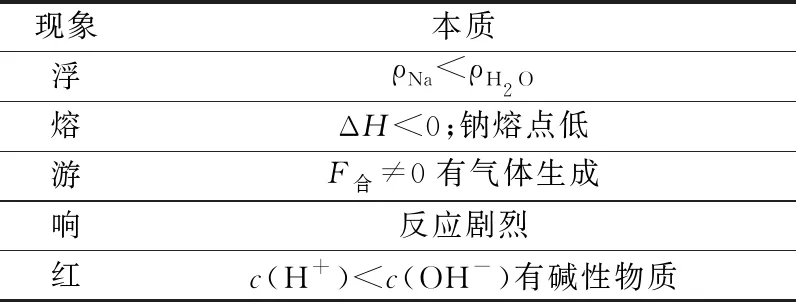
表1 钠与水反应的现象及其对应的本质原因
[师生活动]大家宏观上的现象描述的很好,化学方程式也写的很好.那是否能够利用实验现象、质量守恒和氧化还原分析产物是如何确定的?

设计意图:通过传统文化,由熟悉的铁衍生到钠性质的复习,从宏观辨识迁移到微观探析.依据学生对钠与水反应的了解及化学反应原理的理解程度,讲学评一体化提升学生思考分析的能力,并捕捉学生思维中的不足,引导学生发散思维将化学反应原理与元素化合物的知识相结合,让学生充分认识到元素化合物反应现象实际上就是化学原理的应用.
课堂活动2.根据金属的活泼性顺序表,铁可以将硫酸铜溶液中的铜离子置换出来生成铜.那么将钠投入硫酸铜溶液是得到单质铜了吗?为什么没有得到单质铜呢?在微观上反应如何进行?哪些实验现象可以证明你的结论呢?
[教师活动]启发学生从得失电子守恒、质量守恒的角度分析产物.强调观察实验重点现象,猜测原因,讨论实验设计方案.实验探究前思考:要从哪些方面进行描述,才能全面准确描述现象?可以借鉴哪个实验?
[学生活动]引导各小组讨论,综合得出描述实验现象从“视觉、听觉、嗅觉、味觉、肤觉”等角度进行观察.利用钠与水反应的现象:浮、熔、游、响、红作为模板进行有序的描述实验现象.汇集整理得出将钠投入硫酸铜溶液中的现象:浮、熔、游、爆、蓝:爆鸣声,有蓝色沉淀生成.
[学生活动]钠的密度比水小,所以Na漂浮在水上,先和水接触,置换出氢气,溶液中氢氧根离子浓度增大,与Cu2+结合生成蓝色絮状沉淀氢氧化铜,并使得氢氧化铜的沉淀溶解平衡一直向沉淀方向移动.
设计意图:钠与硫酸铜溶液反应的现象明显知识内涵丰富.通过对实验现象的观察、描述和分析,培养学生的证据推理能力,能基于证据对物质变化提出可能的假设,通过分析推理加以证实或证伪,能基于实验设计与结果分析,对实验进行评价,培养学生的学科素养.利用集中思维引导学生将化学反应原理与元素化合物的知识相结合,让学生充分认识到元素化合物反应现象实际上就是化学原理的应用.
课堂活动3.钠与醇反应回顾必修2教材,请学生代表根据图2描述钠与乙醇反应实验现象并用化学方程式表示.
[师生活动]模仿钠与水反应现象答题模板回忆总结出:
钠沉到试管底部,缓慢冒泡.并完成反应方程式:
CH3CH2OH + Na→;通式:ROH + Na→.
[教师活动]总结现象:沉到乙醇底部、冒泡.
追问:与钠反应,醇和钠哪个反应更剧烈?说明理由.
[学生活动]回忆实验现象得出钠与乙醇反应速率慢,类比钠与硫酸铜溶液反应分析思路,可知是乙醇中的氢离子浓度比水的少,浓度小使反应速率变慢.
[师生活动]乙醇能电离出氢离子吗?提示乙醇是属于非电解质,但是绝对不电离的物质是不存在的,说明乙醇电离能力比说小.利用反应原理中电离度知识可知,电离度越大电离氢离子的越容易,即对应酸的酸性越强,而等浓度溶液中,氢离子浓度越大与钠反应越剧烈:醋酸>碳酸>水>乙醇.
[学生活动]完成化学方程式:H2O+CH3CH2ONa→.另一小组代表用盐类的水解进行分析,越弱越水解:酸性越弱,对应酸根离子结合溶液中的氢离子能力越强,即“抢亲(H+)”能力越强.也就是我们常说的强酸制弱酸.
课堂活动4.有没有比乙醇还难电离出氢离子的物质?哪些物质不与钠反应,可以跟钠共存?如何保存钠?
[师生活动]将钠用煤油油封,煤油来源于石油,主要成分是烷烃,说明烷烃的氢与钠不反应,由此可知烷烃的氢比乙醇更难电离.
设计意图:创设问题情景,将知识线索回归到生活化学情境中,激发学生的求知欲.培养发散思维和集中思维相结合的思维方式,呈现创造性思维活动的全过程,过程发散结果集中抽象概括,提升学生的判断能力.
课堂活动5.根据本节课的分析方法,利用逻辑推导完成下列实验习题.
(1)设计实验证明:丙三醇分子中有三个羟基.
(2)现象和化学反应方程式:钠与饱和石灰水,钠与饱和氯化铵溶液.
设计意图:讲学评一体化检测学生,引导小组描述、比较、分类、发散思维、集中思维得出结论.培养学生由典例到一般的归纳与迁移能力,练习定性定量分析物质的科学方法.

