选择性入肝血流阻断在肝叶切除术中的临床应用价值
周新红,魏征,易杰明,曾长江,胡明道
(1.长江大学附属仙桃市第一人民医院 肝胆胰外科,湖北 仙桃 433000;2.昆明医科大学第二附属医院肝胆胰外科,云南 昆明 655000)
肝叶切除术是目前治疗肝脏占位性疾病的首选方式,由于肝脏的血供解剖学特点,如何控制肝叶切除过程中的出血及术后肝功能的恢复一直是外科中的难题。第一肝门阻断(Pringle法)是控制肝脏术中出血较为普遍的方式,但术后也带来了缺血再灌注损伤和肝功能损害等问题[1]。选择性入肝血流阻断是通过在术中阻断患侧肝血供,保留健侧肝血供,术者术中不用担心阻断肝门对肝脏的缺血再灌注损伤,能从容不迫、游刃有余地行肝切除术[2]。本研究主要是通过对上述两种肝血流阻断术式的术前、术中、术后资料进行对比,探讨选择性入肝血流阻断在肝叶切除术中的临床运用价值,为肝叶切除术中最佳的血流阻断方式提供理论依据。现报道如下。
1 资料和方法
1.1 一般资料
收集长江大学附属仙桃市第一人民医院2012年1月至2019年9月间行肝叶切除的136例病例进行回顾性研究,其中包括原发性肝癌(肝细胞癌和肝内胆管癌)、肝血管瘤、肝局灶性结节增生、肝腺瘤、肝内胆管结石等。纳入排除标准:(1)所有患者均行开腹手术,腹腔镜手术除外;(2)肝功能为Child-Pugh A或B级,C级经护肝治疗转化为A或B级,肝功能Child-Pugh C级除外;(3)患者行肝叶切除至少为肝叶或肝段的切除,肝局部(肿瘤直径<3 cm)剜除除外;(4)肝切除过程中采用Pringle法或选择性入肝血流阻断法,联合使用的除外。患者按术中血流阻断方式分为两组,对照组施行第一肝门阻断(Pringle法,66例,研究组施行选择性入肝血流阻断(70例)。两组患者术前的资料包括年龄、性别、BMI、肝功能分级、肝硬化、AFP、HbsAg等差异无统计学意义(P>0.05),具有可比性。详见表1。
1.2 术中血流阻断方式
所有患者均行开腹手术,行右侧肋缘下斜切口或者反L型切口。
对照组:采用Pringle法。游离肝十二指肠韧带,用8号红色导尿管行第一肝门悬吊,术中切肝出血时,缩紧导尿管,行第一肝门阻断,一般采用15 min+5 min模式,一次阻断不超过15 min,松开阻断带5 min,直至手术完成。
研究组:采用入肝血流阻断法。游离肝十二指肠韧带,用电刀及超声刀逐渐打开Glisson鞘,降低肝门板(术前通过腹部CTA明确肝动脉及门静脉的走形及变异),分离血管鞘时最好用精细剪刀解剖,防止电刀的热损伤,逐渐分离出肝固有动脉左、中、右支,门静脉左、右支(门静脉三支型时要注意),行左右半肝切除时,阻断患侧血流即可。若行肝段切除,继续向肝门板分离,切除肝门板部分肝组织,充分显露血管走向,右肝门静脉一般可分为右后叶支及右前叶支,左肝门静脉一般在矢状部高位,可分为肝左内叶支和左外叶支,行肝左叶肝段切除时常规阻断门静脉左支主干。阻断相应的肝段血流,见缺血线出现后,和术中B超一起拟定肝段的切除线,血流阻断直至切肝结束。具体见图1。
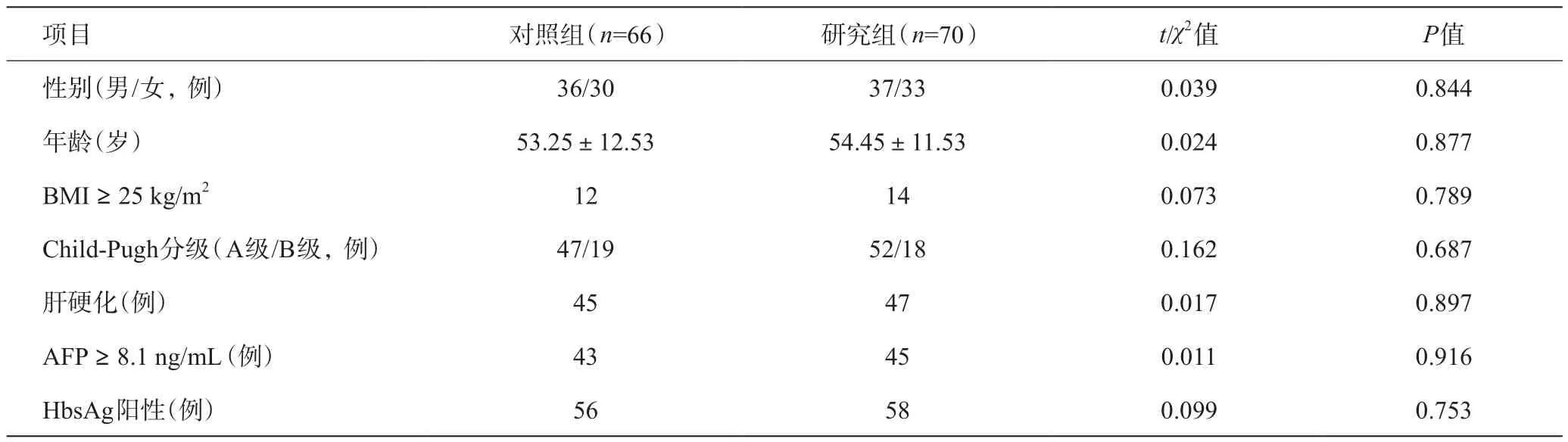
表1 两组患者术前一般情况

图1 入肝血流阻断法术中操作
1.3 观察指标
观察两组患者的手术时间、血流总阻断时间、术中出血量、术中输血量、输血率;术前和术后生化指标(术后第1、3、5天血清ALT、AST、TBIL、ALB)及PT时间等。
1.4 统计学分析
所有数据均应用SPSS 23.0统计软件进行分析,计量资料描述以(±s)表示,两组比较采用t检验,计数资料以例(%)表示,组间比较采用χ2检验,当理论频数<5时,采用χ2检验校正公式或Fisher确切概率法,以P<0.05为差异有统计学意义。
2 结果
2.1 术中情况
两组的手术时间、血流阻断时间、术中出血量、术中输血量及输血率比较无统计学差异(P>0.05),详见表2。
2.2 术前和术后生化指标及凝血时间对比
术后第1、3、5天血清丙氨酸氨基转移酶(ALT)、天门冬酸氨基转移酶(AST)、总胆红素(TBIL)、白蛋白(ALB)对照组高于研究组(均P<0.05);术后凝血时间(PT)两组无统计学差异(均P>0.05),详见表3。
2.3 术后并发症
术后并发症包括胆漏、腹腔出血、腹腔积液、切口感染、肝性脑病、胸腔积液、腹腔感染、肺部感染、肝功能衰竭等。两组患者无一例发生肝功能衰竭。研究组与对照组术后总并发症发生率对比无统计学差异[71.42%(50/70)vs65.15%(43/66),t=3.188,P>0.05],见表4。
并发症的处理如腹腔出血,两组患者各有1例因24 h内出血量超过500 mL,监测到血红蛋白呈进行性下降,于介入室行肝动脉的超选栓塞,术后出血好转,治疗效果佳。其余并发症均对症处理后出院,无一例再开腹手术。
2.4 术后病理类型
具体见表5。
3 讨论
肝脏是人体重要的储血器官,供血系统也是由肝动脉及门静脉两重管道供血,同时肝细胞对缺血、缺氧敏感,长时间肝血流阻断会造成肝细胞缺血缺氧损伤,而复流又会造成缺血再灌注损伤,进一步损害肝功能[3]。合适的血流控制技术是肝脏疾病行肝切除的核心问题。第一肝门阻断法由Pringle于1908年首次提出,通过阻断肝十二指肠韧带达到阻断门静脉及肝动脉血流的目的[4]。此法无需解剖肝门,操作简便、省时、易行,通过收紧第一肝门达到控制肝断面出血,效果明显,应用范围广,几乎适用于各种类型的肝切除术,也是手术医师最常选用的肝血流阻断方式[5]。但长时间阻断使余肝组织发生缺血再灌注损伤,同时门静脉血流阻断致肠道淤血、黏膜屏障功能破坏,易发生肠道细菌及毒素的移位,引起继发感染,加重肝脏的损伤[6-7]。我国的慢性肝病患者持续性入肝血流阻断的安全时限一般认为是30 min,无肝硬化患者不超过15~20 min,合并肝硬化者不超过10 min[8];如仍需阻断,应在间隔5 min后再次实施,中间如果肝断面出血,用纱布轻轻压迫即可。Sakamoto等[9]认为累计阻断时限可达322 min。Procopio等[10]报道一例68岁的老年患者累计阻断时间为348 min。我们认为,Pringle法中肝门间断累计时间为60 min是安全的,一般肝脏肿瘤在60 min内可以切除。本研究中采用Pringle法病例血流总阻断时间为(32.33±13.24)min,术后无肝衰竭发生。
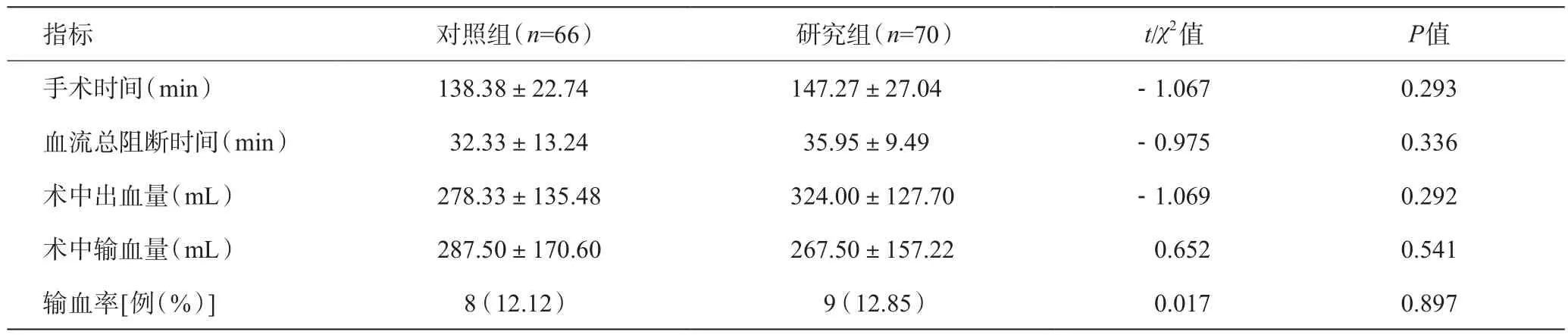
表2 两组患者术中情况
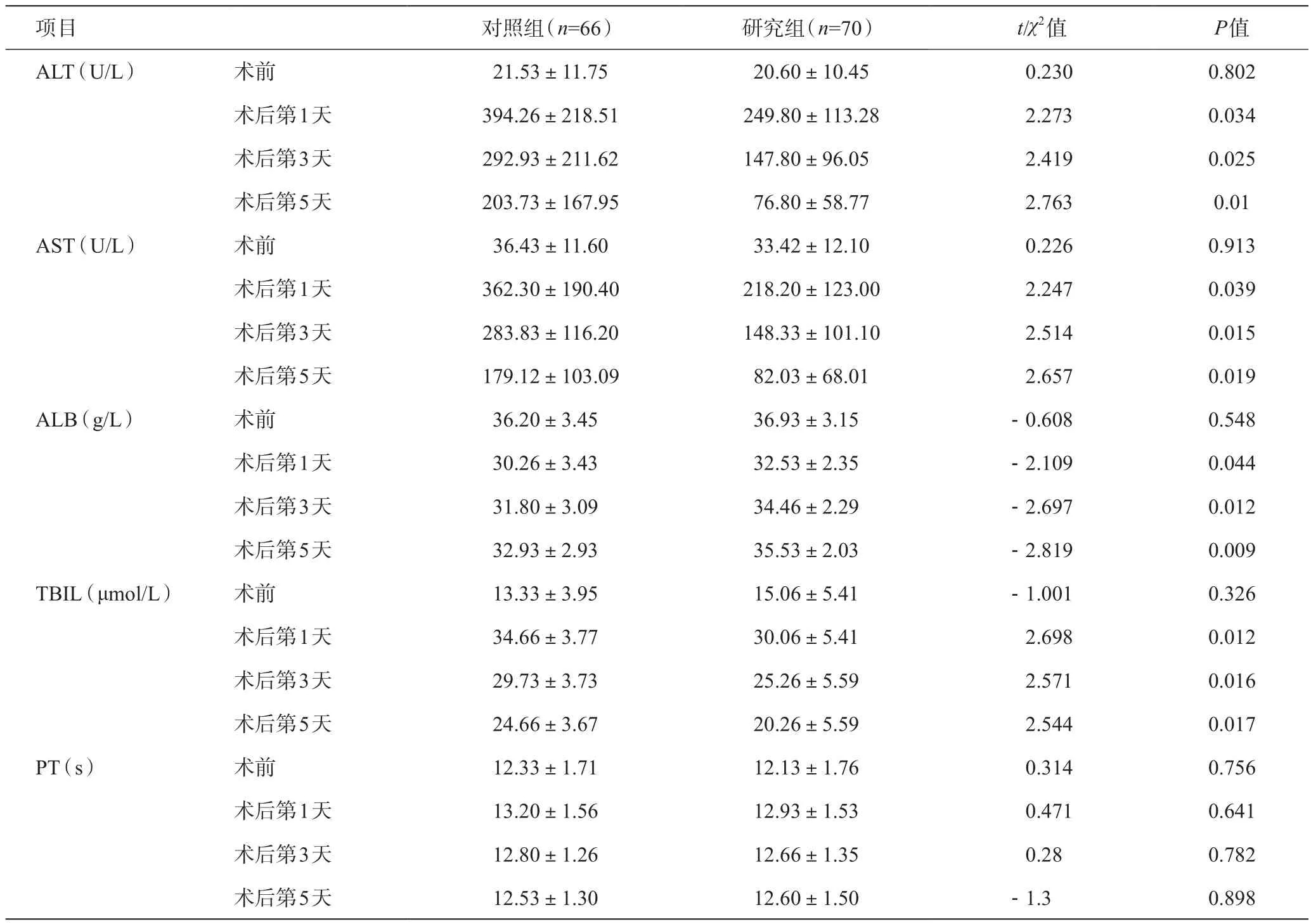
表3 两组患者术前、术后各时间段生化指标对比
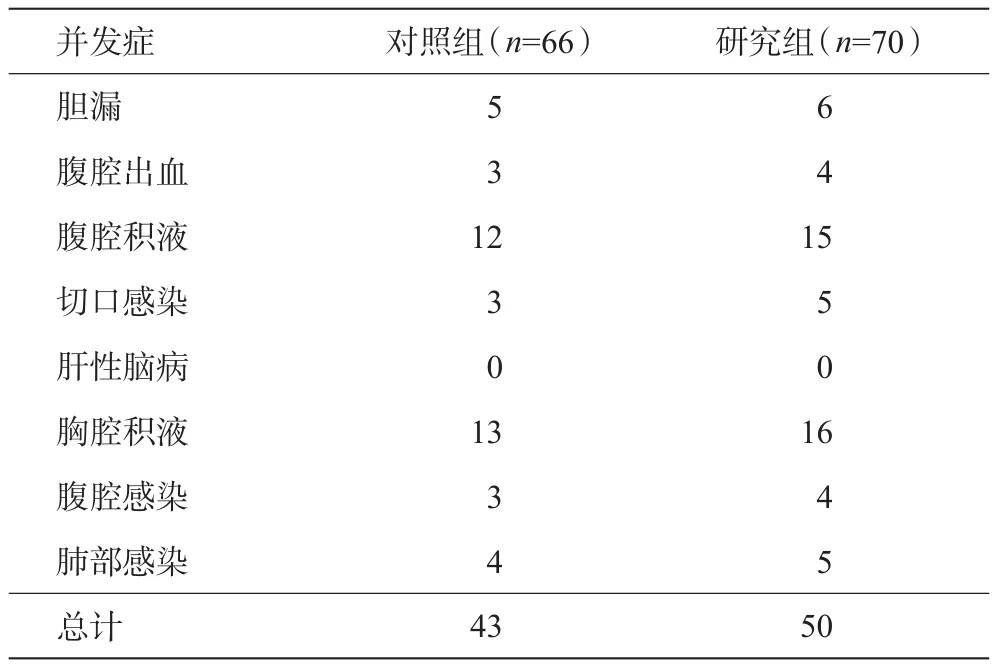
表4 两组患者术后并发症情况(例)
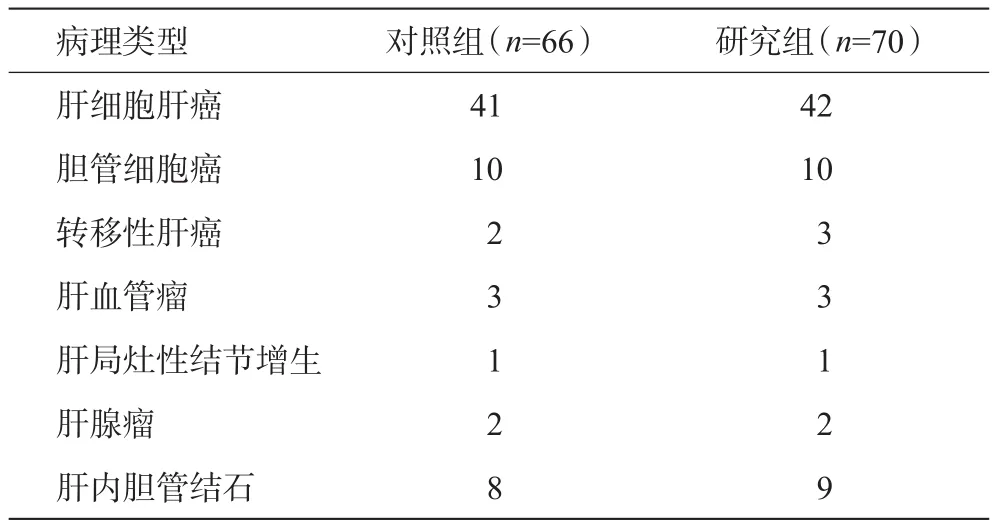
表5 两组患者术后病理类型(例)
入肝血流阻断术首先由日本Makuuchi等[11]在1987年报道,方法为在第一肝门选择性的阻断左右半肝入肝血流,在残肝保持正常血流的情况下切除病变肝脏,从而达到减轻残肝缺血再灌注损伤的目的[12],同时也可以阻断患侧肝脏的静脉(肝右静脉或肝左、中静脉共干),术中可以减少肝静脉的反流出血,文献报道此种方法对减少肝癌患者的复发、转移具有潜在的肿瘤学优势[13]。此种方法与Pringle法比较难度在于要解剖第一肝门,我们术前将增强CT及MRI数据融入计算机系统合成的高清3D模型图,术前对手术患者肝脏各种管道系统及变异情况充分了解与掌握,做到精准解剖和精准切除。解剖第一肝门可分为鞘内法和鞘外法,我们一般选用鞘内法,打开肝十二指肠韧带,下降肝门板,若肿瘤为肝右叶,一般常规切除胆囊便于肝门的显露,于肝门部做精细解剖一般可以将肝S5、S8、S6、S7肝蒂分离出,结合术中B超了解肝静脉的走形,必要时行肝段门静脉的美兰染色,定好肝段切除线后再行肝切除。若是行左右半肝切除时,在下降肝门板后,我们部分采用了鞘外阻断法(1998年日本Takasaki教授报道的“肝蒂横断式肝切除术”[14]),一般胆管的左右分叉比门静脉和肝动脉分叉更贴近肝门,在胆管分叉处用血管钳向肝十二指肠韧带后方,尾状叶及肝下下腔静脉前方穿出,用血管带行半肝血流阻断。 解剖肝门时,术者通过3D影像必须对肝门解剖了如指掌,遇到出血,要保持冷静,缩紧第一肝门,用吸引器吸血,明确出血部位后用血管缝线仔细缝合,避免严重的血管及胆管损伤。研究组70例无论鞘内还是鞘外均在肝门区解剖成功,只要分离时仔细解剖,保持耐心,均可成功分离。但解剖变异或二次手术粘连严重,无法分离时不必强求,可行Pringle法阻断肝门,按照对照组方法行肝叶切除术,另外资料显示如果癌栓位于肝门部,此种手术方式可能不适合,患侧肝蒂的阻断可能会造成癌栓脱落、断裂,进入健侧肝内引起肝内转移[15]。
入肝血流阻断的肝切除术是精准肝切除的基本,据文献报道选择性入肝血流阻断后观察组患者的氧化/抗氧化系统平衡并未受到过度破坏,反观行Pringle法全肝血流阻断者,恢复血流后氧自由基大量产生且机体抗氧化能力减弱,过度的脂质过氧化是造成对照组患者肝功能下降的重要原因[16-17],本研究中研究组术后第1、3、5天血清胆红素、转氨酶水平升高幅度及白蛋白下降幅度较小,肝功能损害较轻(P<0.05)。手术中两组的手术总时间、肝门阻断总时间、术中出血量、术中输血率比较没有明显差异,但在切肝过程中,入肝血流阻断能让术者从容不迫的切肝,增加术者手术信心。同时有研究报道阻断预切除肝区、段、叶,根据缺血范围在肝脏表面标记缺血线,当标记线不明显时标记线可以通过门静脉穿刺美兰实施,Ahn等[18]根据肿瘤和门静脉的空间位置关系提供四种门静脉穿刺染色策略:肿瘤由单支或两支门静脉供血情况,穿刺一支或两支门静脉;当荷瘤肝段部分染色或染色不明显时,常需采取穿刺健侧门静脉反染色法确定荷瘤肝段切除边界,但对于初学者来说门静脉的穿刺染色仍然非常困难,经常出现点状染色或部分染色的情况,需要不断学习和经验积累才能精准实施[19]。进入肝实质后,通过肝静脉及术中B超作为肝内解剖标志来引导肝实质的离断,以获得最精准的切肝平面和最大的无瘤切缘[20]。在术后并发症上,两者无明显统计学差异,术中都注重肝功能的保护及肝缺血再灌注损伤的预防,PT时间无统计学差异(P>0.05),并发症都及时迅速处理,均治愈出院,但研究组术后肝功能恢复快,有利于患者的早日康复,与Ozsoy等[21]报道的选择性入肝血流阻断可减轻术中肝脏缺陷再灌注反应,促进患者术后肝功能提升,内环境稳态恢复结果一致。
综上所述,选择性入肝血流阻断技术应用于肝切除术可以减轻残肝缺血再灌注损伤,有利于术后患者肝功能恢复,增加术者信心,使术者能清楚辨别术中解剖变异情况,保证病灶的最佳切缘和肿瘤的R0切除,同时也为行其他较为复杂肝切除术奠定一定的技术基础,有利于在临床上开展和推广,是一种可行的肝血流阻断方式。但同时病例的选择、数量和术者的技术水平对结果会产生一些偏倚,需要多中心、大样本的随机对照研究加以验证。

