5’- 核苷酸酶不同检测系统测量结果一致性探讨
钱志平,陈蕾,徐俊驰,杨玉婷,王凤平,惠李
(1. 苏州市广济医院,江苏 苏州215008;2.苏州市第五人民医院检验中心,江苏 苏州215007)
临床检验量值溯源受到国际广泛重视,检验结果的准确在疾病诊断、危险因素分析、治疗效果评价以及健康状况监测重要依据。 目前临床医学实验室量值溯源主要从两个环节体现,一是用于正确性评价定值参考物(即标准物质或产品校准物),二是临床实验室检验结果一致性(实验室间比对)[1]。现临床实验室使用有注册证商品试剂盒或分析系统对标准物或产品校准物的溯源由为重要,是评价临床检验结果正确性和一致性的依据。 5’-核苷酸酶(5’-Nucleotidase,5’-NT)分布于心、肝、脑、肾等组织,在肝内分布胆小管和肝窦间隙[2]。 众多文献表明血清5’-NT 主要用于肝胆系统疾病和某些恶性肿瘤的诊断和鉴别诊断, 与其它生化指标如r-GT、AST、ALP、LAP 等在相关疾病诊断与病情预后判断存在量值关系[3]。 5’-NT 项目卫生部或省临检中心并未开展室间质量评价(EQA)对实验室间检测能力一致性验证,按照ISO15189 文件和GP29-A 文件采用替代方案实验室间比对[4,5]。本实验室利用几家国产5’-NT 试剂初步评估发现, 尽管各家试剂说明书提供参考范围基本一致,但是实际检测同一样本时差异较大,对临床实验室选择合适产品带来很大困扰。
1 材料与方法
1.1 检验系统的组成 选择《苏州市医疗卫生机构医用耗材及试剂中标目录》5’-NT 商品试剂共6家,方法学均为过氧化物酶法。 厂家试剂、配套校准品、 质控与日立全自动生化分析仪7600-110E(日立7600-P)组成6 个检测系统。 实验中使用仪器及设备定期进行校准,各项指标均符合实验仪器性能及计量学要求。 考虑到本实验结果仅对不同检验系统临床样本检测结果一致性评价,不能对结果准确性验证,实验结果评价可能对选择试剂厂家产生影响,故厂家用A、B、C、D、E、F 代替。 各厂家商品试剂主要成份及溯源情况见表1。
1.2 实验样本的选择 通过医院检验LIS 系统从每日常规检测血清样本中筛选比对实验样本, 要求5’-NT 检测值高、中、低浓度,覆盖线性范围内不同浓度临床患者样本,样本无溶血、脂血,分装于血清专用样本管,于-20℃保存待用。生物参考区间验证样本,随机选择来院健康体检个体20 名,年龄分布18~55 岁,男女比例1:1。健康个体选择原则,健康人群评价指标及体格检查达到标准或评价指标阴性,排除非健康个体,实验室免疫学、生化学及尿检均正常。
1.3 5’-NT 纯品酶校准品 Sigma 纯品酶,CAS 号9027-73,货号N8661,用生理盐水配制成101U/L,厂家加入少量稳定剂及激活剂(A 厂家提供)。
1.4 不同检验系统5’-NT 比对实验 实验按照ISO15189 文件和GP29-A 文件替代评估方案要求,各厂家试剂及配套校准品、质控与日立7600-P组成6 个不同检测系统。 各试剂厂家均按照试剂说明书要求进行参数设定,校准及质控结果确认。本次以A 厂家试剂与日立7600-P 为对照检测系统,用于5’-NT 在不同检测系统比对一致性评价。
1.5 各试剂校准品、 质控5’-NT 检测结果一致性利用Sigma 5’-NT 纯品酶校准品与各厂家试剂及日立7600-P 组成检测系统, 观察各试剂校准品、质控5’-NT 检测结果一致性。
1.6 新鲜混合血清进行赋值 利用A 厂家5’-NT试剂并采用理论K 值与日立7600-P 组成检测系统,对新鲜混合血清进行赋值,并进行赋值确认,即利用赋值混合血清作为校准品与A 厂家试剂配套,测定Sigma 5’-NT 纯品酶校准品<±10%为偏差较小,可接受。
1.7 评价在不同检测系统5’-NT 结果比对一致性及各试剂厂家生物参考区间验证 利用赋值混合血清为校准品与各厂家试剂及日立7600-P 组成检测系统, 评价在不同检测系统5’-NT 结果比对一致性及各试剂厂家生物参考区间验证。
1.8 统计分析 使用单因素方差(One-way analysis)分析组间样本差异,Dunnett's test 作两两比较分析,P<0.05 为差异具有统计学意义。 统计分析使用数据统计分析绘图软件GraphPad Prism 5.0。
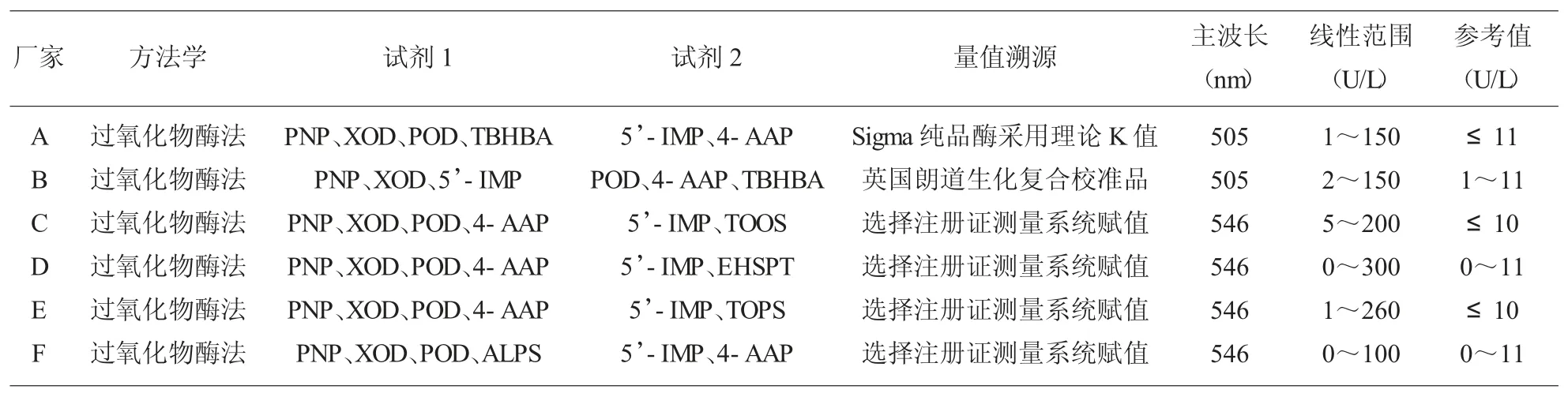
表1 各厂家商品试剂主要内容及溯源情况
2 结果
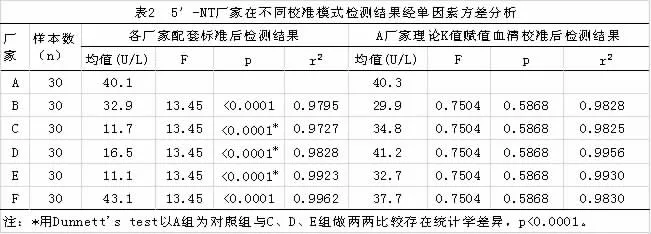
各厂家5’-NT 试剂及校准品与日立7600-P组成不同检测系统检测30 份低、中、高筛选实验比对样本结果,组间样本均数分别40.1U/L、32.9U/L、11.7U/L、16.5U/L、11.1U/L、43.1U/L,经单因素方差分析(One-way analysis)发现各厂家标准校准后检测结果组间存在差异,用Dunnett's test 以A 组为对照与C、D、E 组做两两比较差异有统计学意义,P<0.0001。 见表2 。
赋值后混合血清为校准品与各厂家试剂及日立7600-P 组成检测系统, 组间样本均数分别40.3U/L、29.9U/L、34.8U/L、41.2U/L、32.7U/L、37.7U/L。 经单因素方差分析(One-way analysis)发现以理论K 值赋值血清校准后组间差异无统计学意义,P>0.05。 见表2。
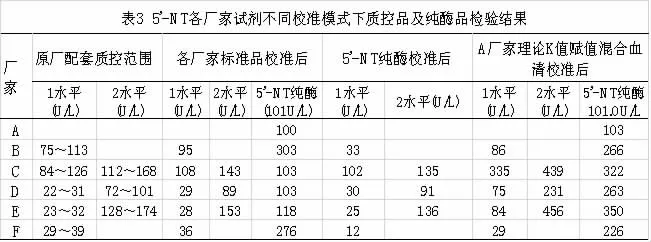
5’-NT 在不同检测系统不同校准模式下各试剂配套质控及纯酶品检测结果,利用各厂家配套校准品组成检测系统配套质控测值均在可接受范围,其中C、D 厂家与A 厂家5 ‘-NT 纯酶测值较一致(5‘-NT 纯酶理论值101U/L),而B、F 厂家5‘-NT纯酶品测量较A 厂家高约三倍。 而5‘-NT 纯酶校准后各厂家质控检测,C、D、E 配套质控可接受,B、F 厂家配套质控测值约为目标值1/3。 A 厂家检测系统赋值混合血清校准后质控结果,B、F 厂家质控可接受, 而C、D、E 三家测值约为目标值三倍,5‘-NT 纯酶测值除A 厂家外,均达二倍以上。 见表3。
5’-NT 在厂家配套校准及赋值血清校准模式下组成测量系统对30 份低、中、高实验样本检测结果,各厂家配套校准模式样本均数离散较明显,而理论K 值赋值血清校准后各组样本均数趋于一致,以A 组为对照经相关性分析发现各组均有较好的相关性,见图1、图2。
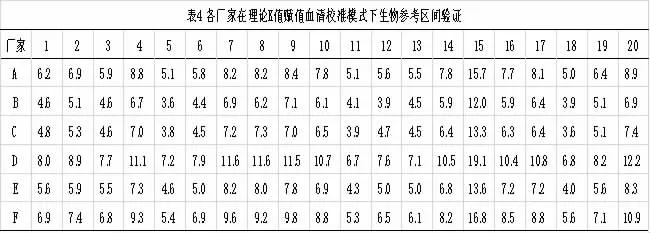
生物参考区间验证程序, 按健康人群评价指标排除非健康个体20 例样本检测结果,除D 厂家30%样本测值超过厂家建议参考值,不符合验证程序(<10%),其余5 家1 例样本结果超过参考值区间,符合验证程序。
3 讨论
5’-NT 是一种磷酸水解酶,血清酶活性升高主要用于肝胆系统疾病以及与其它疾病鉴别诊断,5’-NT 上升程度及其它相关生化指标如ALP、r-GT 等呈量值关系[6]。 从选择的几家国产试剂发现检测同一样本存在较大差异,对终端用户选择产品带来很大困扰。 本研究选择6 家国产商品试剂采取厂家配套校准、 理论K 值赋值血清两种校准模式探讨临床样本检测一致性评价。
从表2 可见, 选择6 家5’-NT 商品试剂采用厂家配套校准方式与日立7600-P 组成检测系统30 份实验样本结果显示, 组间样本均数离散较明显,同一份样本不同检测系统差值近达四倍,经单因素方差分析组间存在差异,用Dunnett's test 分析并以A 组为对照与其它五组做两两较,C、D、E 组差异有统计学意义,P<0.0001。 本实验选用5’-NT试剂均为以5’-次黄嘌呤核苷酸为底物,生成的过氧化氢与苯胺盐和4-AAP 在过氧化物酶作用形成醌亚胺类化合物,通过吸光度速率变化计算5’-NT活性。 5’-NT 项目卫生部、省临床检验中心未开展室间质量评价, 属无能力验证制造商选定测量程序,厂家量值溯源区别在于制造商对工作校准品赋值方式[7,8]。 A 厂家理论K 值确定以次黄嘌呤为标准,采用双波长Trinder‘s 反应监测5’-NT 反应速率,并利用5’-NT 定量浓度Sigma 纯品酶对原厂试剂采用理论K 值组成检测系统进行量值传递验证,使测量结果的可溯源性及不确定度<±10%,故本次实验以A 厂家试剂为对照组。 表3 显示,厂家配套校准模式下配套校准品及质控检测均可接受,5’-NT 纯酶测值C、D、E 与A 厂家较一致, 且5’-NT纯酶校准后,C、D、E 三家配套质控在控, 但是表2显示临床比对样本检测组间存在显著性差异。 分析原因酶校准品生产及长期保存原因,制造过程需加入稳定剂、激活剂等,或校准品非人源物质,产生不同程度基质效应[9]。 厂家配制纯酶品只适合自身测量系统评价,对于其它测量系统采用比对厂家纯酶为校准物质可能出现临床样本测值差异。
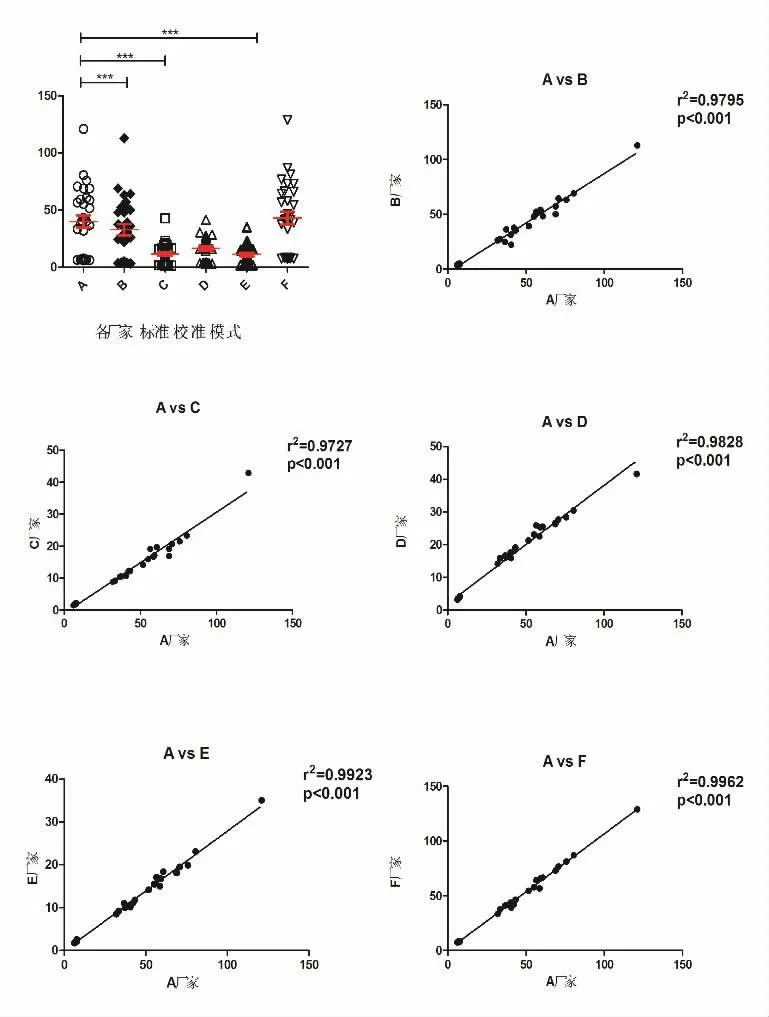
图1 5’-NT 各厂家配套校准模式
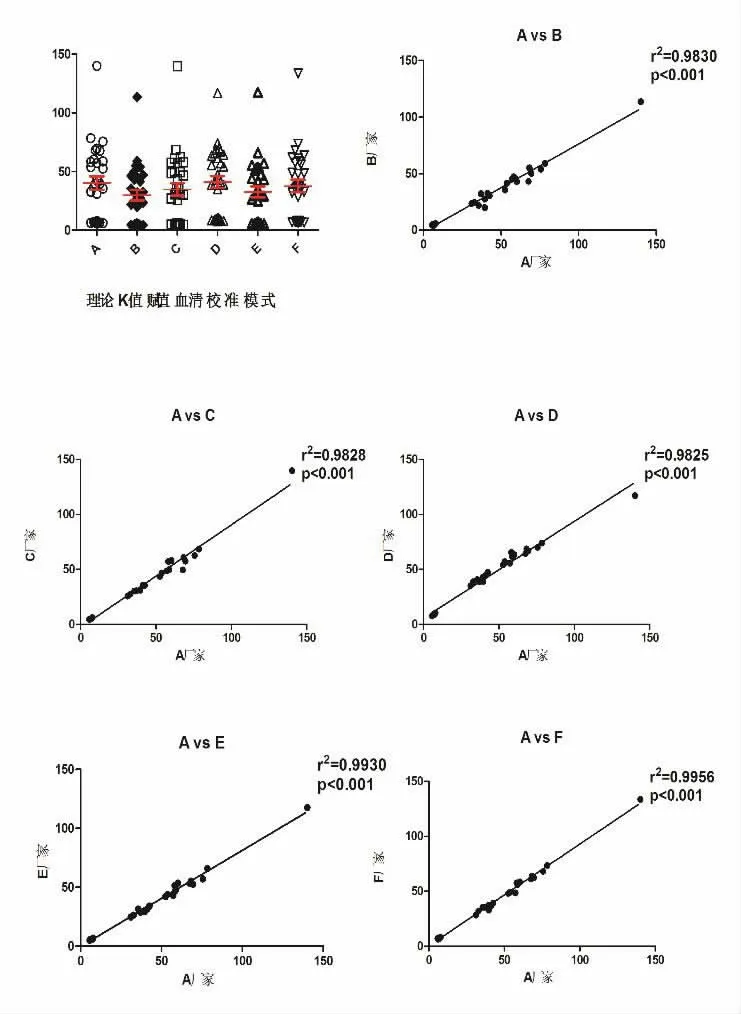
图2 5’-NT 理论K 值赋值血清校准模式
5’-NT 无国际、国家标准参考物及参考方法属制造商选定测量程序,对于部分厂家采用纯品酶制备产品校准物在其自身系统内可很好将测量结果在选定测量程度和常规测定方法进行量值传递,但对于其它厂家可能存在不通用性[10]。而利用赋值新鲜混合血清为校准品可使不同检测系统酶测量结果有互通性, 组间差异缩小并且比对结果达到一致性[11,12]。表2 可见A 厂家5’-NT 试剂采用理论K 值与日立生化7600-P 组成对新鲜混合血清赋值,其余厂家以赋值血清为校准物与日立生化组成测量系统,检测30 份实验比对样本。从表2 显示组间样本均数趋于一致, 经One-way analysis 分析组间差异无统计学意义,P>0.05。 另厂家配套校准和赋值血清校准模式下30 份比对实验样本,以A 厂家为对照组经相关性分析组间存在显著性相关(r2>0.95,P<0.001),见图1、图2。 分析厂家配套校准模式下出现实验比对样本均数离散且方差分析组间有显著性差异,进一步佐证说明现用部分5’-NT 试剂厂家工作校准品的量值溯源及常规校准品的量值传递不严谨。 表4 显示在理论K 值赋值混合血清校准模式下,排除非健康个体生物参考区间验证20 例样本检测结果,5 家均只有1 例结果超过参考值范围,符合验证程序,D 厂家有30%样本结果超参考区间,不符合生物参考区间验证程序要求(<10%)[13]。 分析考虑5’-NT 在选定测量程序和常规测量程序以及量值传递过程存在不确定度的增加, 如不确定度按<±10%, 则D 厂家仅2 例超范围符合生物参考区间验证。
通过5’-NT 在不同检测系统实现实验室结果一致性研究,医学临床实验室对无能力验证项目在选择商品试剂时应充分考虑产品制造量值溯源及区域实验室比对方法, 从5’-NT 三种量值溯源方式, 作为终端用户应选择采用理论k 值或赋值混合血清为校准品实验室间比对,才能保持临床样本结果一致性。

