鼻咽癌调强放射治疗后发生椎动脉狭窄的危险因素
江舟 黄海欣 陈达桂 杨慧 吴思蓓 许卓华 陆颖作者单位:545005 柳州 广西柳州市工人医院肿瘤科
鼻咽癌(nasopharyngeal carcinoma,NPC)是我国南方地区常见的头颈部恶性肿瘤[1]。放疗是主要的治疗手段,随着放疗及多学科综合治疗的不断进步,大部分患者可获得长期生存[2-4]。因此,放疗引起的远期并发症日益受到关注。其中椎动脉狭窄是鼻咽癌患者放疗后一种常见的并发症之一,易造成动脉缺血,从而引起小脑缺血等一系列较严重的并发症[5-6],影响患者生活质量甚至可导致严重不良预后。目前也有少数研究分析了放疗后颈部动脉狭窄的发生[7-10],但其具体的发生机制尚未完全清楚。本研究回顾性分析2013年8月—2017年8月柳州市工人医院148例鼻咽癌患者的临床资料,探讨导致鼻咽癌调强放射治疗(intensity-modulated radiation therapy,IMRT)后椎动脉狭窄的因素,以期为临床诊疗提供参考。
1 资料和方法
1.1 研究对象
收集2013年8月—2017年8月在广西柳州市工人医院就诊的鼻咽癌患者纳入研究。纳入标准:⑴年龄18~70岁;⑵鼻咽部活检病理确诊为非角化性癌;⑶ECOG(Eastern Cooperative Oncology Group)评分为0~1分。排除标准:⑴有其他恶性肿瘤病史;⑵有头颈部手术、放射治疗、化疗病史;⑶重要脏器功能衰竭;⑷合并控制不良的心脑血管等内科疾病。本研究获广西柳州市工人医院伦理委员会批准。
1.2 治疗方案
所有患者均接受调强放射治疗,参照《2010鼻咽癌调强放疗靶区及剂量设计指引专家共识》[11]勾画靶区,采用直线加速器6 MV-X线常规分割照射,要求95%等剂量线覆盖PTV,处方剂量:鼻咽部DT 69.96 Gy,2.12 Gy/f/d,5 f/w;颈部预防照射区 DT 55.8 Gy,1.8 Gy/f/d,5 f/w。Ⅰ期患者采用单纯放疗。Ⅱ~Ⅲ期患者接受同步放化疗(顺铂80 mg/m2d1,21 d为1周期,共2个周期)±新辅助化疗(顺铂 75 mg/m2d1,紫杉醇175 m2/d1,21 d为1周期,共2个周期),或者接受放疗+同步靶向治疗(尼妥珠单抗200 mg,d1,7 d为1个周期,共7个周期);其中只行同步放化疗11例,同步放化疗+新辅助化疗30例,放疗+同步靶向治疗18例。ⅣA期患者接受同步放化疗及新辅助化疗,用药方法同上。
1.3 资料收集与随访
收集入组患者的临床资料,包括年龄、性别、治疗方案、糖尿病史(既往诊断糖尿病或空腹血糖>7.0 mmol/L、或随机血糖>11.1mmol/L)、高血压史[既往诊断高血压或随访中不同一天3次收缩压≥140 mmHg和(或)舒张压≥90 mmHg]、吸烟史[连续或累积吸烟6个月或以上)、临床分期(参照中国鼻咽癌2008年分期)、高脂血症(总胆固醇>5.72 mmol/L和(或)甘油三酯>1.70 mmol/L]、椎动脉平均受照射剂量(通过剂量体积直方图读取)。
采用门诊复查形式进行随访,随访截至2019年9月30日。放疗后第1~2年每3个月随访1次,此后每6个月随访1次。随访主要内容包括患者椎动脉超声检测、肿瘤转移、复发及生存状况。放疗后平均随访时间为5.1年,随访期间死亡13例。
1.4 椎动脉检查方法及狭窄的判断标准
治疗前及随访时行彩色多普勒超声(CDFI)检测双侧椎动脉情况。脉冲多普勒(PW)检测各节段血流频谱,狭窄段测量狭窄处管腔内径及收缩期峰值流速(PSV)、舒张末期血流速度(EDV)。椎动脉内径缩小>50%即判断为狭窄,即PSV≥140 cm/s,EDV≥35 cm/s,PSVOR/PSVIV≥2.1(PSVOR:起始段,V1 段;PSVIV:椎间隙段,V2 段)[12]。
1.5 统计学方法
采用SPSS 16.0软件进行数据分析。计量数据以均数±标准差(±s)表示,分类资料采用 n(%)表示。放疗前后椎动脉狭窄率的比较采用配对χ2检验,其余分类资料比较采用四格表χ2检验。采用非条件Logistic回归分析影响椎动脉狭窄的因素,计算风险比(OR)及其对应的95%可信区间(CI)。以双侧P<0.05为差异有统计学意义。
2 结果
2.1 患者的基线资料
共148例患者纳入分析,其中男性110例,女性38例;平均年龄(53.8±11.2)岁;放疗后椎动脉狭窄发生率为47.3%,高于放疗前的8.1%(χ2=12.376,P<0.001)。有无椎动脉狭窄两组患者的高血压、吸烟、临床分期、高脂血症和椎动脉平均受照射剂量比较差异有统计学意义(P<0.05);而年龄、性别、糖尿病及是否联合化疗差异无统计学意义(P>0.05)。见表1。
2.2 影响椎动脉狭窄的单因素Logistic回归分析
单因素Logistic回归分析显示,高血压(OR=2.400,95% CI:1.214~4.743,P=0.012)、吸烟(OR=1.044,95% CI:1.012~1.077,P=0.006)、高脂血症(OR=2.326,95% CI:1.113~4.859,P=0.025)和椎动脉平均受照射剂量>60 Gy(OR=3.998,95% CI:1.909~8.374,P<0.001)与椎动脉狭窄有关。见表2。
2.3 影响椎动脉狭窄的多因素Logistic回归分析
将单因素分析中可能影响椎动脉狭窄的因素以及临床分期纳入多因素分析,结果显示除临床分期(OR=1.454,95% CI:0.621~2.967,P=0.217)以外,椎动脉平均受照射剂量>60 Gy(OR=3.130,95% CI:1.417~6.914,P=0.005)、高脂血症(OR=2.549,95% CI:1.118~5.812,P=0.026)、高血压(OR=2.407,95% CI:1.130~5.127,P=0.023)、吸烟(OR=1.041,95% CI:1.006~1.077,P=0.022)均是放疗后椎动脉狭窄的独立危险因素。见表3。
3 讨论
椎动脉狭窄是头颈部肿瘤外照射的常见并发症,但是放疗引起动脉狭窄的机制仍不清楚[13-15]。研究认为放射线诱导的血管损伤与动脉狭窄密切相关,而放射线损伤血管可能与血管缺血性坏死导致的纤维化,血管外膜纤维化导致血管的阻塞,动脉粥样硬化加速等有关[16-17]。另有研究报道血管所受的放疗照射剂量若超过60 Gy,动脉硬化及血管狭窄的发生率将明显增加[18-19],本研究将60 Gy设定为放疗照射剂量临界值,分析其与椎动脉狭窄的关系,结果发现椎动脉放疗剂量超过60 Gy的患者狭窄发生率更高,多因素分析亦显示椎动脉平均受照射剂量>60 Gy是影响椎动脉狭窄的独立危险因素,与上述放射线损伤血管的机制相契合,进一步验证了放疗与血管狭窄的密切关系,且随着放疗剂量的增加,血管狭窄发生风险升高。
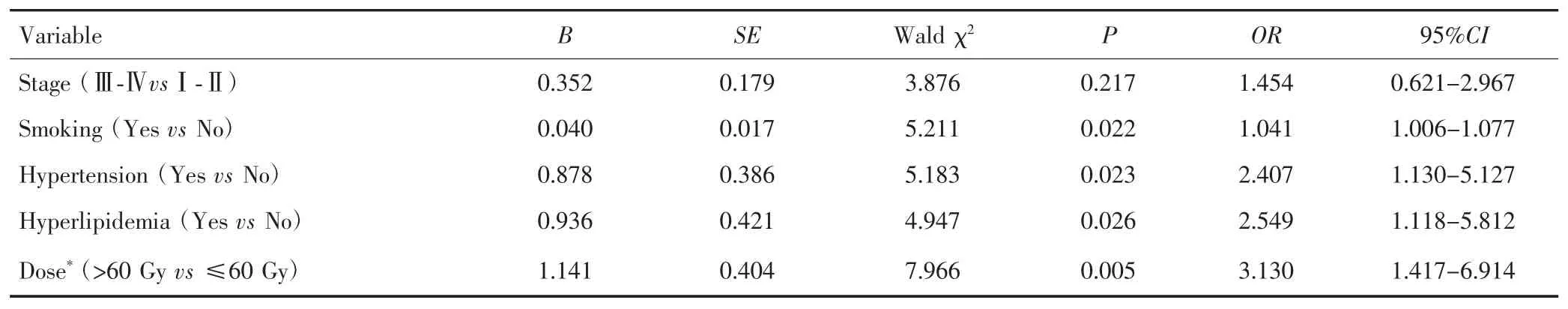
表3 影响椎动脉狭窄的多因素Logistic回归分析Tab.3 Multivariable logistic regression analysis of vertebral artery stenosis
本研究的Logistic回归分析还显示,高脂血症、高血压、吸烟是放疗后椎动脉狭窄的独立危险因素。MILGROM等[20]研究也报道伴心血管危险因素的患者放疗后发生动脉钙化的可能性更高。LAM等[21]分析放疗后头颈部血管狭窄的影响因素,结果也发现其影响因素包括高血压(HR=2.941,95% CI:1.216~3.737,P=0.012)、高脂血症(HR=4.041,95% CI:2.096~7.274,P=0.032)、吸烟(HR=5.442,95% CI:2.106~9.881,P=0.008)等。说明以上临床特征可能与放射线相互作用,促进放疗后椎动脉狭窄的发生,致使患者放疗后发生椎动脉狭窄风险更高。MARTIN等[22]在分析50例头颈部放疗患者,其中年龄≥60岁的患者颈动脉狭窄发生率为60.2%,远高于<60岁患者的11.3%。另有研究报道头颈部恶性肿瘤放疗后,临床分期较晚的患者颈动脉狭窄发生率明显高于早期患者(23% vs 6%,P=0.029)[23]。然而本研究中未发现年龄、临床分期为椎动脉狭窄发生的影响因素,可能与样本量较少及患者入组年龄相对较小而临床分期较晚有关,有关结论仍需进一步验证。
综上所述,本研究结果显示,椎动脉平均受照射剂量>60 Gy、高脂血症、高血压、吸烟是鼻咽癌患者调强放射治疗后椎动脉狭窄发生的独立危险因素,临床上应重点预防具有以上临床特征患者放疗后椎动脉狭窄的发生。但本研究为回顾性分析且样本量较少,因此有关结论仍需开展大样本多中心的前瞻性研究进一步证实。

