高精密度标测指导镜面右位心并发的阵发性心房颤动射频消融一例∗
王志琴 张大勇 李德才 邸云峰 李双菲 徐敏

图1 前后位胸平片

图2 超声下心脏镜面改变
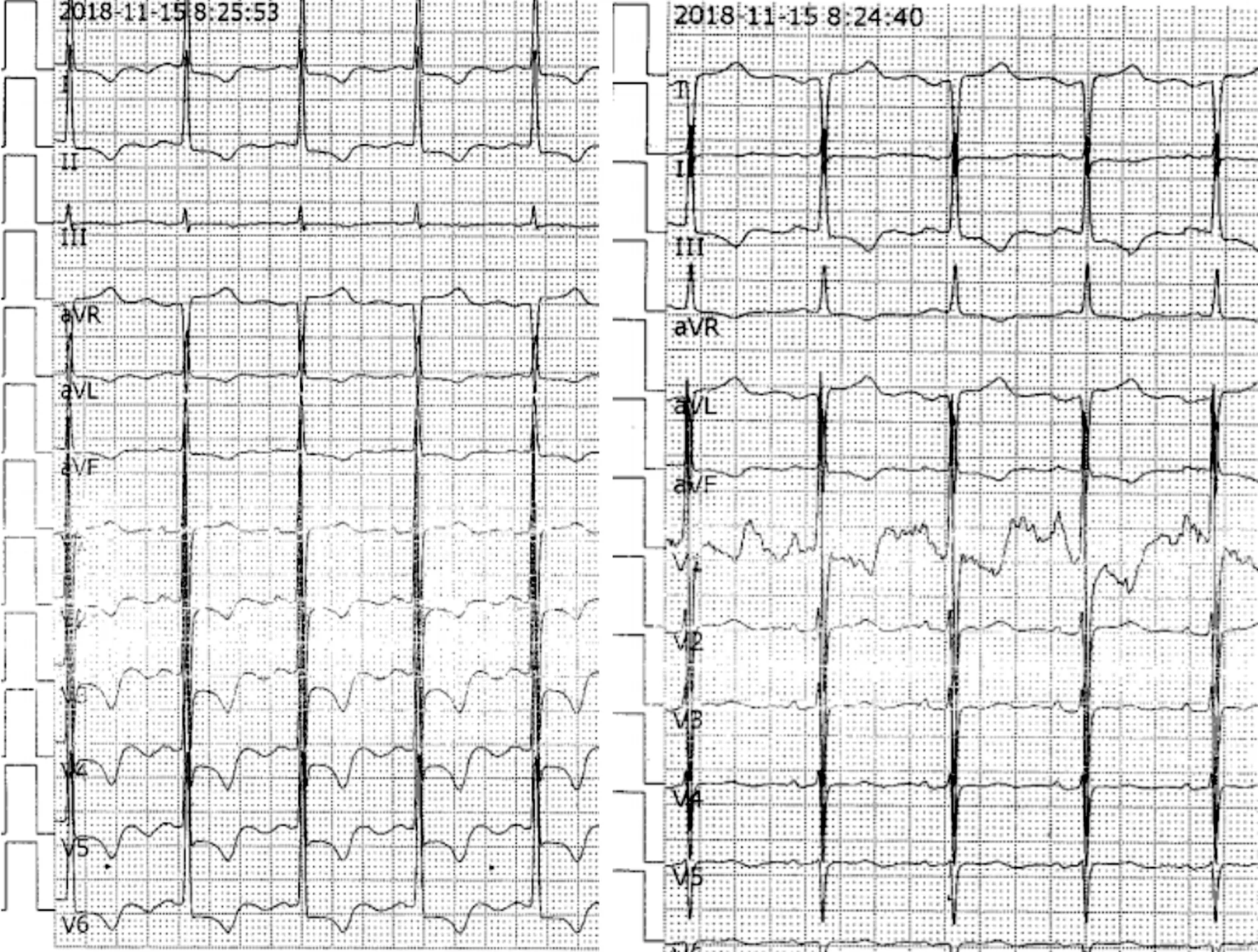
图3 患者体表12导联心电图
患者女性,67岁,主因“反复心悸7年余,加重1月余”入院。入院前7余年,患者开始无明显诱因出现心悸,阵发性发作,每次持续半天至一天后自行缓解,伴全身乏力,小便增多、头昏,无胸闷、胸痛,无头痛,无视物旋转,无大小便失禁。心电图诊断心房颤动(简称房颤),胸片提示右位心。入院时体格检查:心尖搏动右第五肋间锁骨中线内0.5 cm,无震颤,叩诊心脏浊音界正常,心律不齐,心音强弱不等,各瓣膜区未闻及病理性杂音,其余无特殊。辅助检查:心脏X 线平片(图1):右位心,左房增大,右肺少许感染,所示腹腔脏器反位。心脏彩超(图2):镜面右位心,左房增大,室间隔增厚,二尖瓣轻度返流,房颤频谱。心电图如图3、4。消化系统彩超:腹部内脏反位,脾脏多发稍强回声小结节,胆囊切除术后,残余胆系未见异常声像,肝、胰未见异常声像。经食道右位心,左室壁明显增厚,心律不齐,二尖瓣轻度返流,双心耳及双心房未见血栓声像。CHA2DS2-VASc评分5 分,治疗上予以充分抗凝后,选择Pentaray+Confidense高精密度+压力导管射频消融治疗,手术过程:采用Seldinger法穿刺右股静脉成功,造影右股静脉不能通过导丝,造影提示右髂静脉畸形(图5),穿刺左股静脉,分别置入8F 及6F 鞘管。送入10极电极至冠状窦,6 极电极至右室。行心内电生理检查,CS7-8 S1S1230 ms诱发房颤。送入房间隔穿刺鞘及穿刺针,调C臂使图像呈镜面翻转,可视心脏“正常位”(图6),房间隔穿刺针及穿刺鞘指示7点钟方向,回退导管至卵圆窝,再右前斜位(RAO)30°穿过卵圆窝,送导引钢丝至肺静脉,再送穿刺鞘至左房后,行心房及左右肺静脉造影,发现左肺静脉共干(与心脏CT 三维重建时发现左肺静脉共干相吻合)(图6、7);术中为窦性心律,送入Patenray至左房,建立窦性心律下左房三维电解剖模型及基质标测,明确左房基质未见异常,可见右肺静脉前壁大片前庭电位(图8),采用冷盐水压力导管压力监测下行环肺静脉隔离+右肺静脉前壁前庭电位区均质化消融。用Patenray电极检查消融后无肺静脉电位,肺静脉内双向阻滞,前庭电位消失,术后患者心悸症状消失,复查心电图恢复窦性心律,术后继续服用胺碘酮和达比加群酯治疗。
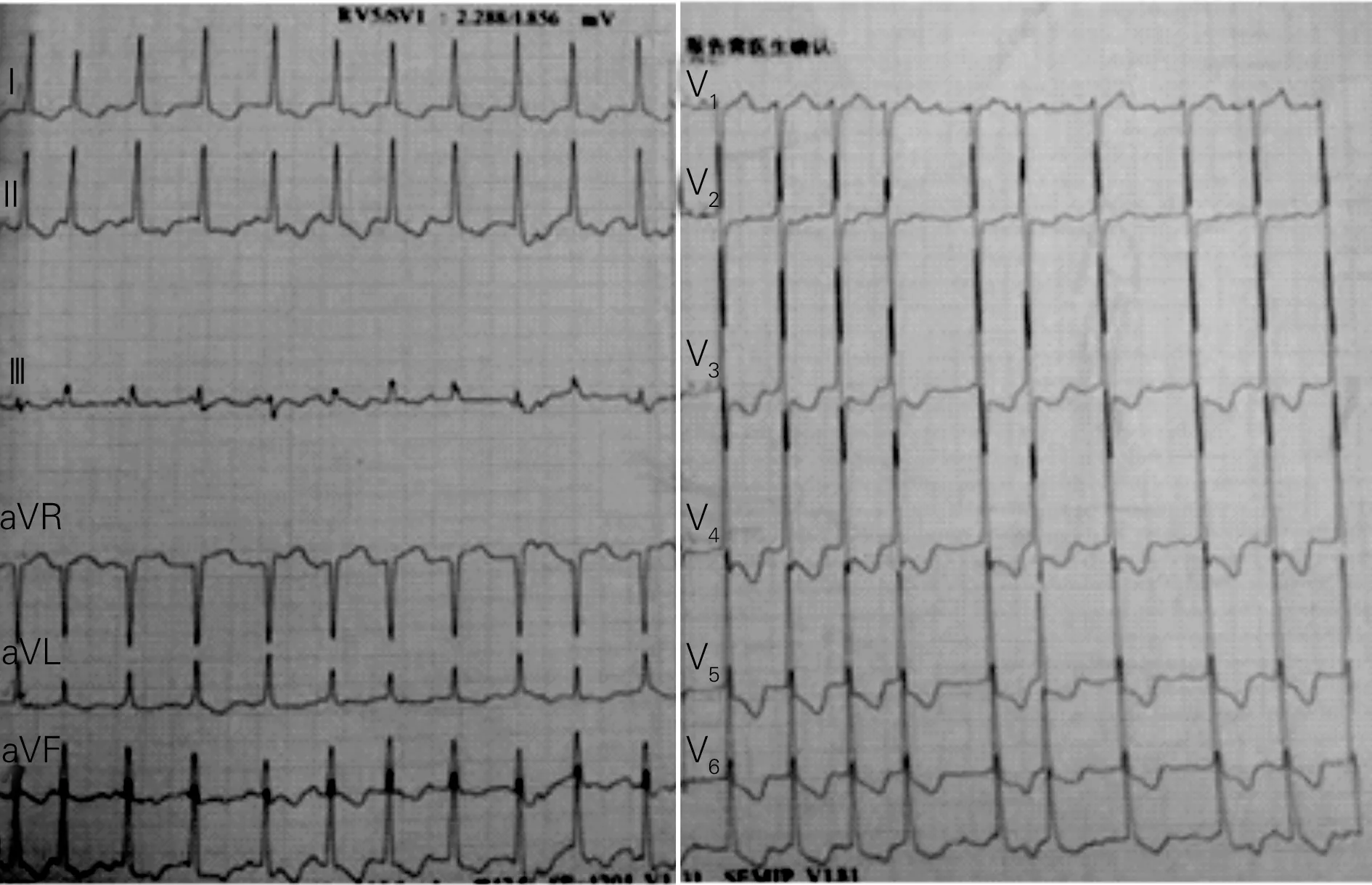
图4 心悸发作时左右反接后的心电图

图5 右髂静脉畸形

图6 X 线胸部影像

图7 心脏CT 三维重建(后前位)图

图8 左房高精密度标测可见右肺静脉前壁前庭电位带(白色标记点)
讨论右位心是心脏在胸腔的位置移至右侧的总称,分为真正右位心(镜面右位心)、右旋心和心脏右移,镜像右位心发病率大约为0.01% 先天性心脏病[1]。右位心的发生是由于常染色体突变引起[2],是一种结构异常,镜面右位心合并房颤少见。
目前高精密度标测+压力导管指导下的环肺静脉消融电学隔离肺静脉,肺静脉狭窄率低,已成为房颤导管消融治疗最主要的方法,治疗房颤相对简单,操作时间缩短,并发症少,单次手术后一年至两年阵发性房颤成功率达60% ~80%,持续性房颤成功率达60%左右[3-4]。但本例患者为镜像右位心,内脏转位,造成解剖位置反位,使房间隔穿刺以及消融过程中穿孔风险极高,容易造成心包压塞;建立左房电解剖模型时有很大难度,进行射频消融时,与术者一般手术习惯流程顺序相反,因此需要更精准的心房模型指引,精确的消融部位避免肺静脉术后狭窄;明确的压力指导导管的贴靠情况,避免贴靠不良导致的消融不透壁,或者贴靠压力过高导致穿孔;其次该患者合并有右髂静脉畸形以及左肺静脉共干两种异常,手术难度明显加大,术中术者需要时刻提醒忘记平时形成的手术习惯才能确保治疗安全进行。
镜面右位心合并房颤导管消融的患病率极低,国内外相关报道很少,可借鉴的经验较少,总结如下:术前通过经胸心脏彩超,食道心脏超声,心脏CT 及三维重建,胸片及内脏器官彩超等检查,做到尽可能充分了解心脏解剖结构及和功能状态;患者心脏结构相对反位,房间隔穿刺难度大,需术前利用C臂功能使图片翻转,即在显示屏上显示似正常人心脏结构,便于引导房间隔穿刺,如仍然存在困难,可借助术中经食道超声指导房间隔穿刺;穿刺后行心房及肺静脉造影,可进一步了解心房及肺静脉解剖结构情况;运用高精密度标测能最真实呈现心房+肺静脉结构情况,并可和心脏CT 三维重建模型进行图像融合,建立更准确心脏三维模型指导消融,同时高精密度标测可明确心房基质有无异常,标测前庭电位,建立个体化消融策略;术中压力导管实时监测贴靠情况,减少并发症;消融后测试消融线完整,肺静脉电位消失,肺静脉内双向阻滞,电生理检查或药物诱发除外异位触发灶,尽可能以房颤不能诱发作为手术终点;术后继续药物治疗可进一步减少房颤的再发,长期门诊监控房颤再发。

