婴儿完全性肺静脉异位引流的个性化方案治疗
荣书函,廖健毅,冉旭东,沈维嘉,袁洪樑,黄红娟,沈啸威,李 炘
(苏州大学附属儿童医院心胸外科,江苏 苏州 215025)
完全性肺静脉异位引流(total anomalous pulmonary venous connection, TAPVC)是较常见的婴儿和新生儿期危重型先天性心脏病,占先天性心脏病的1%~3%,如不及时进行手术矫治,多数患儿在出生后1 年内死亡,尤其是伴有肺静脉梗阻者,生后早期死亡风险极高[1]。过去的几十年里,TAPVC手术方式不断改进,预后逐渐改善,但由于吻合位置在心脏后方且肺静脉解剖变异多,对手术技术要求较高,术后易并发肺静脉梗阻,影响预后[2]。我们近年来主要采用左侧入路以及个性化手术方案进行TAPVC矫治,取得了满意的近、中期疗效,现总结和报告如下。
1 资料与方法
1.1 临床资料 2017年1月—2020年12月连续收治并进行手术的TAPVC患儿共34 例,男23 例,女11例。年龄1 d~13 个月(中位值15 d),其中新生儿21 例。体重2.4~7.0 kg(中位值3.6 kg)。分型:心上型10 例(9 例经左侧垂直静脉回流、1 例直接回流至右侧上腔静脉);心内型13 例(其中特殊心内型3 例:回流入右心房顶近上腔静脉处2 例、四支肺静脉分别回流入右心房后壁1 例);心下型6 例(均回流入肝门静脉总干或分支);混合型5 例(均为心内型和心上型混合)。所有患儿均合并卵圆孔未闭或房间隔缺损,此外合并动脉导管未闭18 例,合并主动脉缩窄1 例,合并甲型血友病1 例,合并三尖瓣反流2 例。术前肺静脉梗阻12 例(41%),包括:心上型6 例(梗阻部位在垂直静脉入口处5 例,垂直静脉中段处1 例);特殊心内型2 例(梗阻部位在肺静脉共同开口于右心房顶近上腔静脉开口处);心下型 1 例(梗阻部位在垂直静脉入门静脉开口处);混合型3 例(其中梗阻部位在三支肺静脉汇合与冠脉静脉窦开口处2 例,左侧垂直静脉中上段1 例)。共同肺静脉的形态:心上型10 例中9 例为水平位,1 例为垂直位(图1);特殊心内型3 例均为向右上斜行;心下型6 例变化较大且形态各异,共同肺静脉位于心包正后方3 例,共同肺静脉短小略斜位2 例,在心包后方偏右侧1 例。行急诊或亚急诊手术12 例,其中病情危重、血流动力学不稳定、需要呼吸机辅助和血管活性药物维持者5 例行急诊手术。
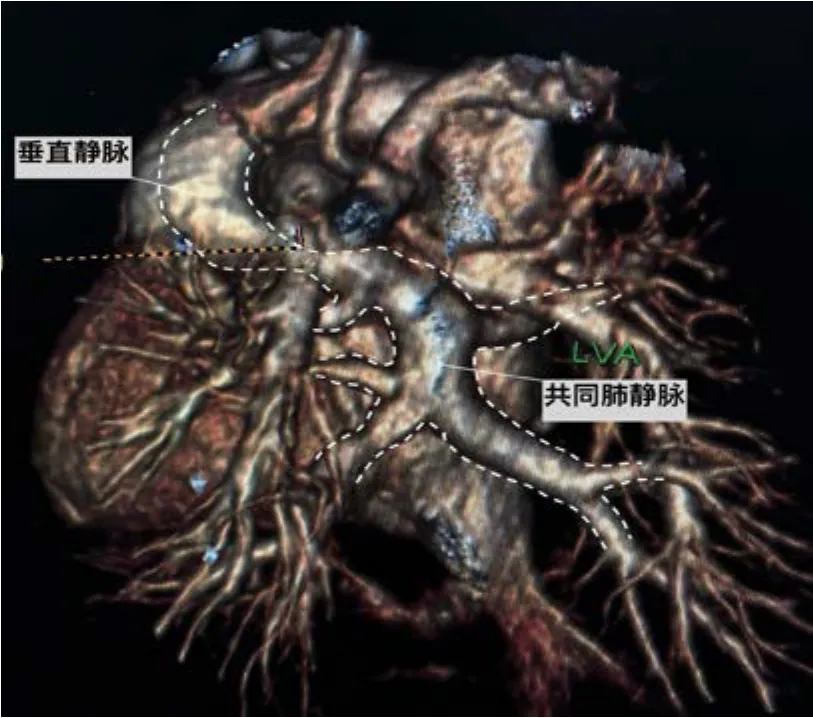
图1 1 例心上型TAPVC的CT心血管造影,显示共同肺静脉呈垂直位。
1.2 手术方法 针对不同分型采用个性化手术及入路。左侧入路手术方法(图2):用于所有心下型和大部分心上型TAPVC。全部采用深低温停循环,打开右侧胸膜腔,拔除右心房插管后将心脏提起并向右侧胸腔内翻转,肺静脉可获得良好显露。切开心脏后方的心包并沿长轴切开共同肺静脉,于共同肺静脉相应位置切开左心房后壁。用7/0单股可吸收缝线(PDS)连续法吻合。吻合过程中,逐渐将心脏返回原位。经右心房切口以自体心包补片重建房间隔,或直接修补房间隔缺损/卵圆孔未闭。缝合右心房后重新插入静脉插管,恢复体外循环并复温,36 ℃时撤离体外循环。
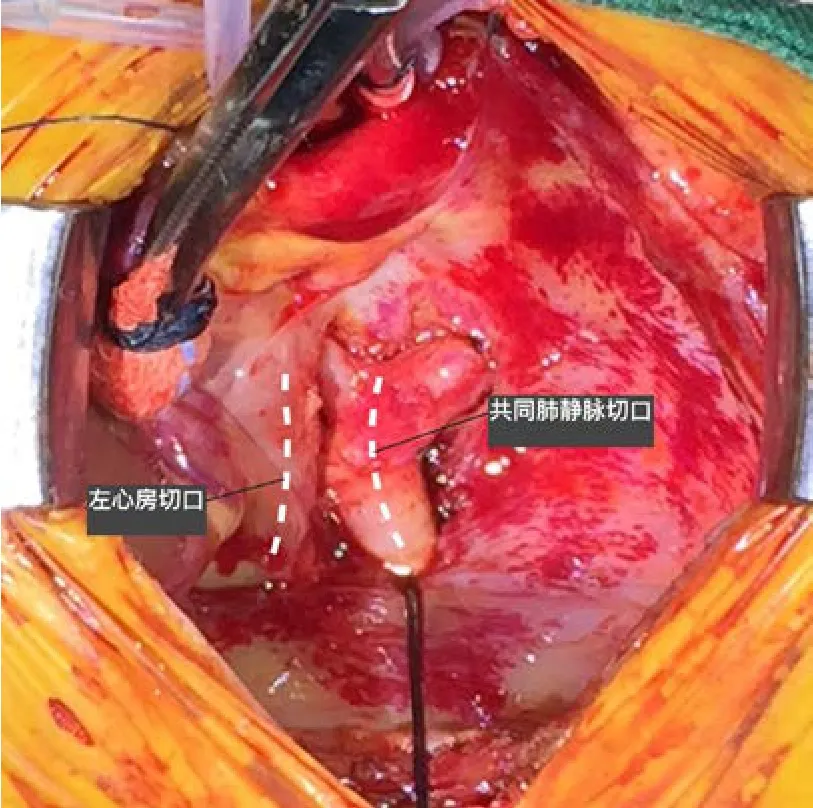
图2 左侧入路矫治1 例心下型TAPVC的术中照片,深低温停循环后拔除静脉插管,心脏已翻转入右侧胸腔,心包后方的共同肺静脉和左心房后壁显露十分满意(右侧虚线为肺静脉切口,左侧虚线为左心房切口)。
心上途径手术方法:用于共同肺静脉横向走行的大部分心上型TAPVC。采用中度低温体外循环,心脏停跳后向两侧牵开升主动脉和上腔静脉,充分显露共同肺静脉和左心房顶,延长轴切开共同肺静脉并向左侧延长至垂直静脉,于对应部位切开左心房顶并向左侧延长至左心耳,二者作吻合。
房间隔入路手术方法:用于大部分心内型TAPVC,共同肺静脉回流入冠状静脉窦者。先切除菲薄的原发房间隔,再将冠状静脉窦顶部与左心房之间的房壁组织彻底切除,避免损伤二尖瓣,再用自体心包补片连续缝合重建房间隔;各支肺静脉分别回流至右房者,尽量切除肺静脉开口与卵圆窝之间的间隔组织,用较大的自体心包补片重建房间隔,将各支肺静脉开口隔入左侧。
心内路径/心后吻合手术方法:用于共同肺静脉回流入右心房顶部近上腔静脉处的特殊心内型TAPVC。于右房顶部的肺静脉开口处探查共同肺静脉走行,并沿长轴切开,同时切开右房后壁,跨越房间隔向左心房后壁延伸,将共同肺静脉与心房后壁吻合。
无内膜接触(Sutureless)吻合:多用于心下型TAPVC中共同肺静脉短小或解剖不理想、因肺静脉梗阻再次手术或吻合困难的患儿(图3C)。术中将共同肺静脉切口延长至肺静脉分支,将左心房切口边缘吻合至肺静脉切口外侧的心包缘上,吻合口缝线不接触各肺静脉内膜。
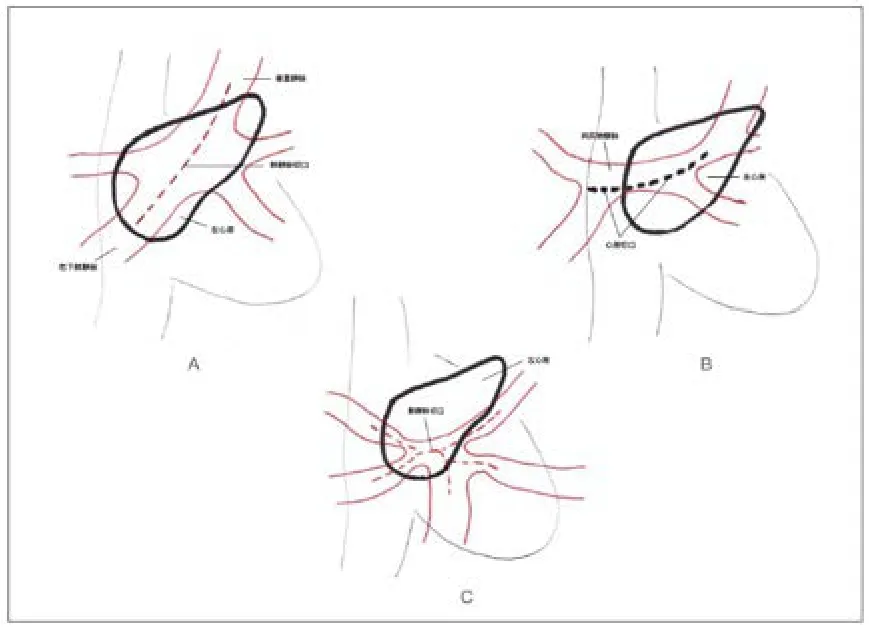
图3 不同肺静脉解剖特点的吻合口设计。A:共同肺静脉较短,但右下肺静脉和垂直静脉较粗大且位于左心房后方,肺静脉切口向右下肺静脉和垂直静脉延长。B:共同肺静脉偏向右侧,心房切口可向右侧延长并跨越房间隔达右心房后壁。C:共同肺静脉短小且存在肺静脉分支开口狭窄,可采用Sutureless缝合,即将共同肺静脉切口延长至肺静脉分支,将左心房切口边缘吻合至肺静脉切口外侧的心包缘上,吻合口缝线不接触各肺静脉内膜。
垂直静脉的处理:心上型患者于体外循环降温期间在心包外进行游离,于汇入无名静脉水平预制丝线,手术完成撤离体外循环后常规试阻断后结扎;心下型患者在停循环心脏翻转后,在膈肌水平套入丝线并结扎。
2 结果
本组无手术或住院死亡,深低温停循环下左侧入路共15 例,包括全部心下型(6 例)和大部分心上型患儿(9 例),1 例1月龄心上型患儿采用心上途径入路,共同肺静脉显露良好,避免了使用深低温停循环。混合型5 例均为心上型和心内型的混合,根据解剖特点采取心上与心内型手术方式的组合。单独回流至无名静脉的左肺静脉或分支,将其离断纵行切开并与左心耳做端-侧吻合(表1)。
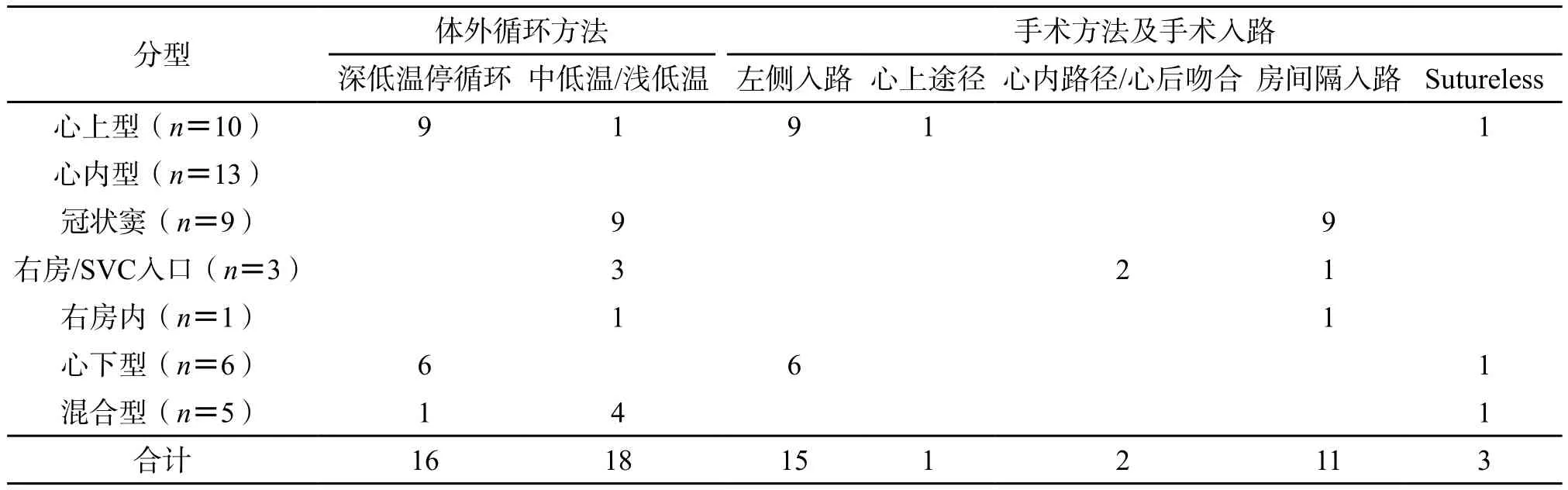
表1 本组TAPVC手术方法及体外循环方法
本组体外循环时间58~245 min(中位值119 min),主动脉阻断时间29~116 min(中位值 53 min)。深低温停循环时间3~50 min(中位值38 min)。术后常规应用米力农和肾上腺素等正性肌力药物。呼吸机辅助时间5~252 h(中位值80 h),监护室滞留时间2~45 d(中位值8 d),住院时间12~54 d(中位值18 d)。
接受深低温停循环的患者术后出现神经系统症状3 例,临床表现为一过性肢体抖动,肌力肌张力增高,出院时症状均减轻或消失,随访1 年后头颅核磁共振检查结果均正常。术后延迟关胸2 例;心包填塞需引流1 例;右侧少量气胸1 例,自行吸收;腹膜透析2 例,出院时肾功能均恢复正常;一过性快速心律失常5 例,4 例经药物和1 例经电复律治疗后均恢复;Ⅲ度房室传导阻滞植入永久起搏器1 例。本组心上型TAPVC合并甲型血友病患儿围术期给予Ⅷ因子补充,无出血并发症。
所有患儿均得到随访,随访期1~41 个月(中位数25 个月)。1 例心下型患儿术后1 个月因肺静脉梗阻再次手术,采用Sutureless吻合,术后恢复良好。其余患儿心超均提示肺静脉吻合口血流速度小于1.2 m/s。除1 例安装永久起搏器患儿外其余患儿心电图均为窦性心律,心功能NYHA Ⅰ级,生长发育良好。
3 讨论
TAPVC是新生儿期和婴儿期最常见的危重型先天性心脏病之一。随着影像学和手术技术的进步,TAPVC明确诊断的时间越来越早,TAPVC的手术成功率和生存率逐年提高[3-6](表2)。
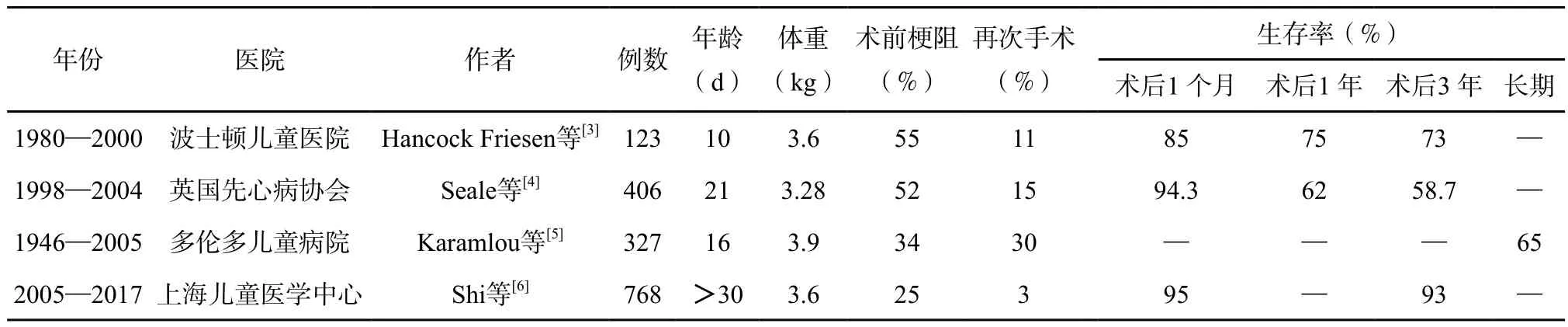
表2 各大中心报道TAPVC手术的近远期疗效
据统计,TAPVC诊断后1 年内若不接受治疗,死亡率高达78%[7],伴有肺静脉梗阻者死亡风险更高,因此手术时机的把握至关重要。当TAPVC出现肺静脉梗阻时,药物治疗无效,急诊手术是唯一选择。对非梗阻型TAPVC,生后1~2 周内尽早进行手术是必要的,因为随着生后肺阻力下降,左向右分流量逐渐增加,肺静脉梗阻风险增高,病情易恶化。心内型TAPVC若心房间交通充分,症状出现可能较晚,但新生婴儿仍处于相对低氧状态,一旦呛奶或并发呼吸道感染等,病情易迅速进展,因此也建议在生后1 个月内手术。早产低体重儿如未出现肺静脉梗阻,可在密切监护下等待体重增长到2~2.5 kg再手术,以降低体外循环带来的风险[8]。本组12 例梗阻型TAPVC患儿均接受急诊手术和亚急诊手术;非梗阻型患儿除部分心内型外均在生后1~2 周接受手术。
术后肺静脉梗阻是死亡的高危因素[9],术后18个月内患儿死亡风险最高[10],术后梗阻患者1 年和3年生存率分别为62.0%和58.7%[11]。肺静脉梗阻分为吻合口狭窄、肺静脉开口狭窄、肺静脉管状狭窄和弥漫性狭窄[3]。研究表明经术中食道超声监测吻合口平均压差≥2 mmHg与术后肺静脉梗阻需再手术显著相关。术中残留的轻度狭窄,可进行性发展为重度狭窄[12]。吻合口对位不齐、肺静脉牵拉张力、扭曲变形都会造成肺静脉梗阻[13],所以吻合口设计及吻合质量至关重要。
完善的术前影像学检查有助于吻合口的设计。目前二维经胸超声心电图能较准确地鉴别大多数TAPVC类型,对于单纯心内型以外的各种类型,CT心血管造影还可以进一步明确共同肺静脉及肺静脉各分支的形态、走行和发育状况,及其与左心房的位置关系,本组2 例心上型TAPVC术前通过CT心血管造影发现共同肺静脉呈垂直位,为个性化的吻合口设计提供指导。
术中良好的显露至关重要,左侧入路将心脏翻至右侧胸腔可获得满意的共同肺静脉显露,深低温停循环又保证了无血的手术视野。个性化的吻合口设计保证吻合质量,首先需要尽量延长共同肺静脉切口和心房切口以保证足够大的吻合口;其次若共同肺静脉短小或解剖位置不佳时共同肺静脉切口可向垂直静脉或较粗大的肺静脉分支适当延长(图3A),如共同肺静脉位置偏右,左心房切口可向右侧的右心房或下腔静脉后壁延长(图3B);最后对吻合困难、肺静脉分支开口有狭窄或因肺静脉梗阻再次手术者采用Sutureless吻合技术有一定优势(图3C)。Wu等[14]通过Meta分析总结Sutureless技术的优点,一方面吻合口不受肺静脉解剖位置形态影响,避免了彻底游离肺静脉和减少深低温停循环的使用,另一方面缝合线与血管内膜无直接接触,减少了相关炎症反应,可降低术后肺静脉梗阻的发生率。也有研究[8]指出Sutureless技术对于手术复杂程度高的病人的确具有一定好处,如术前有肺静脉梗阻、肺静脉发育不良的心下型、混合型TAPVC患者。但日本长野医院[15]报道了1 例首次手术应用Sutureless技术后4 年吻合口直径由9.5 mm缩小至7.6 mm,压差增至10 mmHg,再次手术时看到左房和共同肺静脉吻合口处有一增生组织,病理活检是肺静脉血管壁增生。Sutureless技术目前仍缺少长期的循证医学研究,远期疗效尚不明确。本组除3 例初次手术肺静脉解剖位置不理想的患儿和1 例再梗阻后二次手术的患儿采用了Sutureless技术外均采用传统吻合方式,效果均满意。
术后肺动脉压力的控制也需重视。近年来,新的治疗策略是通过联合使用内皮素拮抗剂、磷酸二酯酶-5抑制剂、前列环素类似物等靶向药物来降低肺血管阻力[16]。本组对术前有肺静脉梗阻及术后早期有重度肺动脉高压的5 例患儿,体外循环撤离前开始静脉用曲前列尼尔或吸入一氧化氮,术后采用二联或三联使用肺动脉高压靶向药物,包括曲前列尼尔,西地那非,波生坦等。住院及长期随访显示
患儿肺动脉压力控制良好,所有患儿随访心功能恢 复至NYHA Ⅰ级。

