三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物的合成及其对HL60细胞增殖的抑制作用
齐志文, 周 昊, 薛兴颖, 颜洋洋, 王成章
(中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业和 草原局林产化学工程重点实验室;江苏省生物质能源与材料重点实验室; 江苏省林业资源高效加工利用协同创新中心,江苏 南京 210042)
没食子酸广泛存在于掌叶大黄、大叶桉、山茱萸等植物中,是一种来源丰富的次生代谢产物[1],具有抗炎、抗肿瘤、抗致突变和抗氧化[2-4],诱导表皮生长因子受体(EGFR)突变型非小细胞肺癌(NSCLC)细胞凋亡[3],增加MCF-7细胞Bax/Bcl-2在细胞凋亡中表达[5]等作用。此外,没食子酸能够诱导急性髓系白血病细胞系(AML)、原代单核细胞(MNC)和CD34干细胞/祖细胞的凋亡[6]。有研究表明,许多药物结构中存在甲氧基基团[7-8],甲氧基能够增强药物分子脂溶性,从而增加人体对药物的吸收[9]。同时,没食子酸甲氧基和杂环诱导癌症凋亡的分子机制[10-11],特别是抗白血病机制仍不清楚。此外,对正常造血细胞无明显毒性的4-苯甲基-2-甲基-1,2,4-硫双偶氮定-3,5-二酮(TDZD-8)是非ATP竞争性GSK-3H抑制剂,IC50值约为2 μmol/L,对酪蛋白激酶II、蛋白激酶A(PKA)和蛋白激酶C(PKC)有抑制作用[12-15]。TDZD-8可诱导细胞膜完整性丧失,使细胞迅速凋亡[14]。基于药物协同理论[16-19],不同活性基团的药物之间具有协同增效作用。因此,本研究以没食子酸为原料,合成了含氮、硫的新型三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮杂环衍生物,并测试了目标化合物单独存在及其与TDZD-8协同存在时对人急性白血病细胞株HL60细胞增殖的抑制作用,以期为抗急性白血病药物的开发提供理论依据。
1 实 验
1.1 原料、试剂与仪器
没食子酸,阿拉丁公司;其他试剂均为分析纯,使用前按常规程序纯化溶剂。人急性髓系白血病HL60细胞,江苏凯基有限公司;四甲基偶氮唑蓝(MTT),美国Sigma公司;伯克改良伊格尔培养基(DMEM培养基)、胎牛血清,美国Gibco公司;配置1 g/L的TDZD-8水溶液,存放在4 ℃的黑暗环境中,备用;HSGF254薄层硅胶板及0.065 mm左右的分离硅胶,青岛黄海化工厂;制备液相色谱prep-HPLC(色谱柱Phenomenex Luna C18,75 mm×30 mm,3μm);分析用色谱柱Diamonsil C18柱(250 mm×20 mm,5 μm),流动相为石油醚(PE)与乙酸乙酯(EA)体积比1 ∶1。Bruker核磁共振仪,样品溶于CDCl3,TMS为内标,其中1H NMR为400 MHz;13C NMR为100 MHz。
1.2 三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物的合成
1.2.1合成过程 以没食子酸为原料,参考文献[12]所述方法制备目标化合物。首先,经过两步反应合成甲氧基异硫氰酸酯,具体步骤为:没食子酸(1)在磺酸羟胺(HOSA)等试剂的存在下,进行两步亲核反应,生成3,4,5-三甲氧基苯甲胺(2)和3,4,5-三甲氧基苯胺;未经分离,直接在丙二酸二乙酯、哌啶作用下进行下一步反应,生成主要产物3,4,5-三甲氧基苯甲基异硫氰酸酯(3),同时检测到少量的3,4,5-三甲氧基苯基异硫氰酸酯。苄基异硫氰酸酯(—NCS)和异氰酸酯(—NCO)在N-氯代丁二酰亚胺和SOCl2条件下,发生环合反应生成三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物(4)[12,20]。合成过程如图1所示。
1.2.2化合物2的制备 在含磺酸羟胺(HOSA,1 mmol,113 mg)的4 mL二氯甲烷溶剂中,加入没食子酸(170 mg,1 mmol),继续滴加1 mol/L HCl溶液1 mL;回流5 h后,用大量乙酸乙酯(50 mL)稀释该溶液,大量水(50 mL)洗涤,硫酸钠干燥,过滤,减压蒸发。得到的浓缩物经硅胶柱层析纯化(PE与EA体积比3 ∶1)及制备液相色谱,得到白色固体粉末。

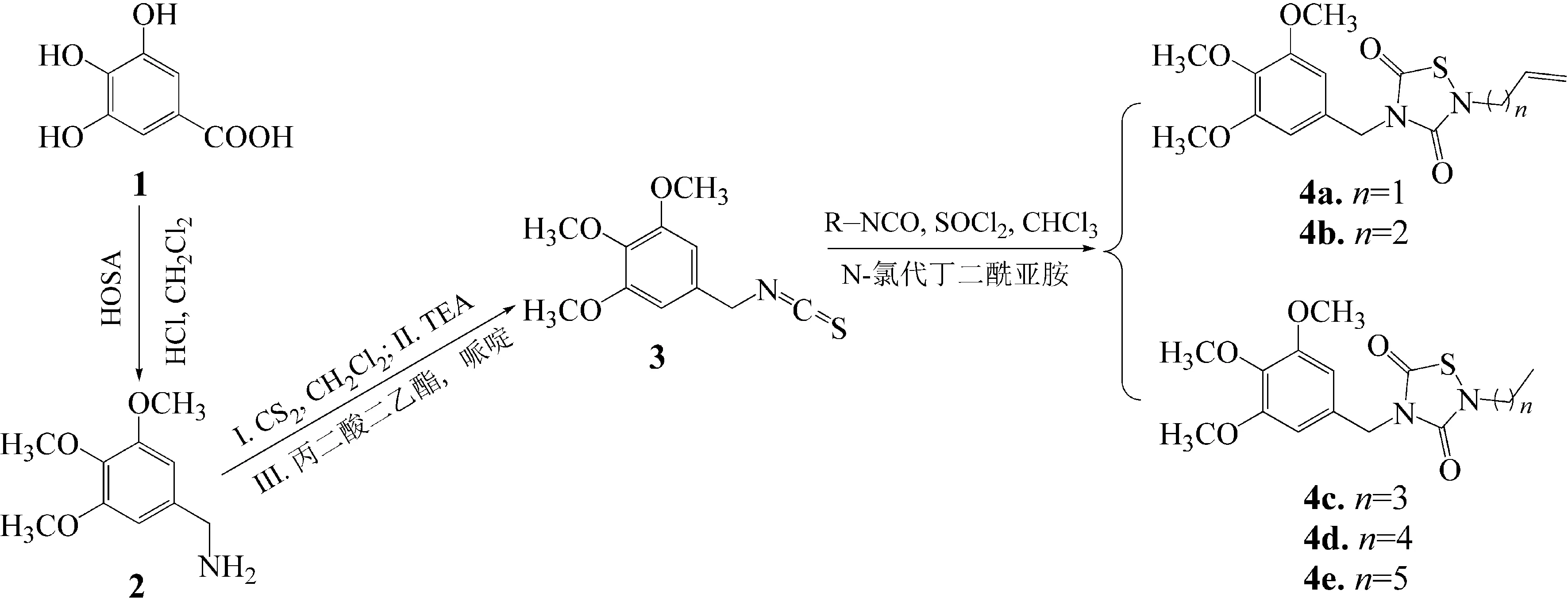
图1 三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物的合成Fig.1 Strategies for the preparation of 1,2,4-thiadiazolidine-3,5-dione derivatives of trimethoxy gallic acid
1.2.4化合物4a~4e的制备 向2 mL氯仿和1 mL二氯亚砜中加入N-氯代丁二酰亚胺(0.1 mmol),继续缓慢加入化合物3(0.1 mmol),滴加异氰酸酯(R—NCO)对应化合物(0.1 mmol)。回流反应10 h,大量水(100 mL)稀释,分液,减压旋干。浓缩物经柱分离纯化(二氯甲烷与正己烷体积比3 ∶1),得到白色固体粉末。
1.3 化合物2、3和4a~4e抑制HL60细胞增殖实验
采用MTT法测试化合物对HL60细胞增殖的抑制作用。将对数生长期的细胞以3.5×103个/孔接种于0.2 mL/孔的96孔培养板中,用不同浓度的7个化合物样品孵育72 h。然后,每孔加入10 μL MTT溶液(5 g/L),继续培养4 h,小心吸去孔内培养液,加入150 μL/孔二甲基亚砜(DMSO),使结晶充分溶解。用微板阅读器测定空白对照组和实验组在波长490 nm处的吸光度(A)。空白对照组:未经任何药物处理;单药组:用浓度为30.0、15.5、10.0、9.0、8.0、5.0、3.5、2.5、1.2、1.0、0.8和0.5 μmol/L的化合物4b或4c与HL60细胞混合培养72 h;用浓度为1.923、1.641、1.156、0.932、0.809、0.365、0.311、0.258、0.128、0.079和0.041 μmol/L的TDZD-8与HL60细胞混合培养72 h;按下式计算细胞增殖抑制率(η) ∶η=(1-A实验组/A空白对照组)×100%。
1.4 化合物4b、4c协同TDZD-8抑制HL60细胞增殖实验
选择对HL60细胞抑制率较高的化合物4b、4c,按照1.3节实验方法,测试4b、4c协同TDZD-8抑制HL60细胞增殖作用。化合物4b/4c与TDZD-8均设置6个浓度配比[21],TDZD-8+化合物4b或4c:用浓度为0.68、0.34、0.17、0.057、0.029和0.015 μmol/L的TDZD-8与浓度为8.0、5.0、3.5、2.5、1.2和1.0 μmol/L的化合物4b/4c均匀配比混合,再与HL60细胞混合培养72 h。计算细胞增殖抑制率,并采用CACUSYYN软件计算协同指数(CI),CI<1表示协同作用,CI>1表示拮抗作用;Fa为分析两种药物是否具有协同作用的联合指标。
2 结果与分析
2.1 目标产物的合成机理

2.2 目标化合物的结构表征
化合物2: 3,4,5-三甲氧基苯甲胺,白色固体,纯度98.2%,产率81%。1H NMR (400 MHz,CDCl3)δ:6.56 (s,2H,Ar—H),3.87~3.83 (d,J=5.1 Hz,2H,Ar—CH2—)。13C NMR (101 MHz,CDCl3)δ:152.36,146.34,138.04,135.76,102.96,100.91,45.78。[M+Na]+:177.0。
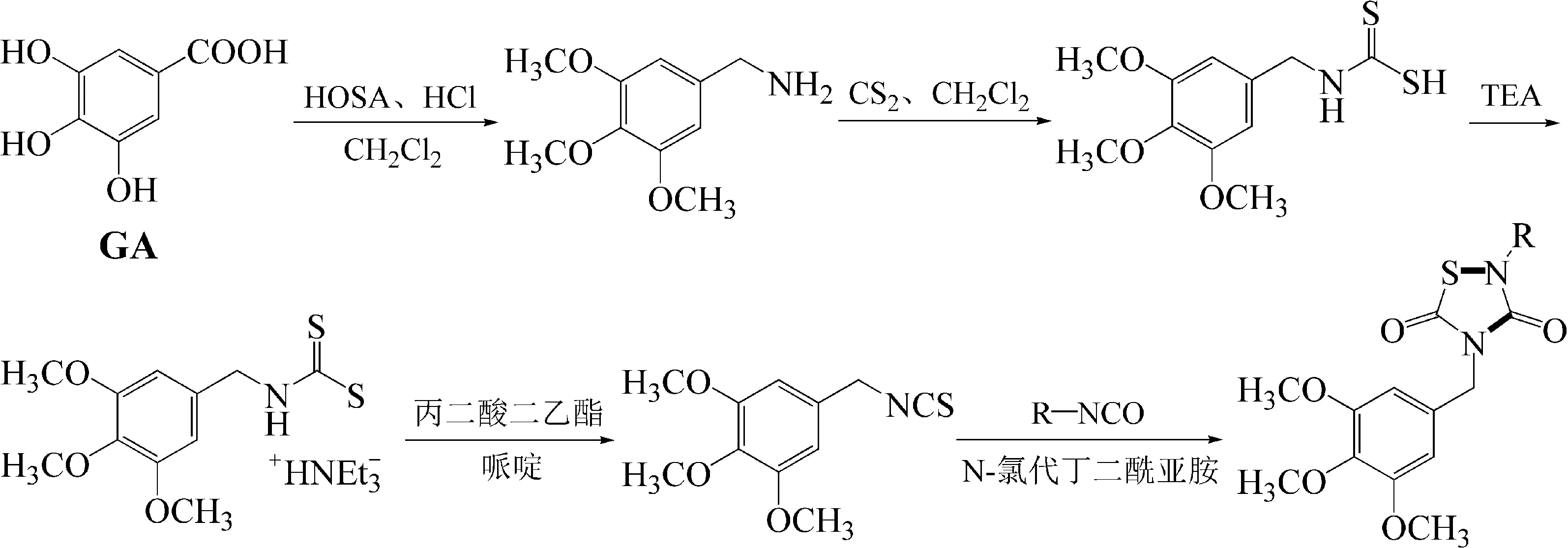
图2 目标产物的合成机理Fig.2 Synthesis mechanism of target compounds
化合物3: 3,4,5-三甲氧基苯甲基异硫氰酸酯,白色固体,纯度95.6%,产率57%。1H NMR (400 MHz,CDCl3)δ:6.44 (s,2H,Ar—H),4.45 (s,2H,Ar—CH2—),3.78~3.73 (d,J=5.2 Hz,9H,CH3O—)。13C NMR (101 MHz,CDCl3)δ:151.45,131.23,131.55,123.23,101.85,88.63,60.01,54.25。[M]:239.0。


化合物4c: 2-丁基- 4-(3,4,5-三甲氧基苄基)-1,2,4-噻二唑-3,5-二酮,白色固体,纯度95.0%,产率65%。1H NMR (400 MHz,CDCl3)δ:7.44~7.42 (d,J=8.0 Hz,2H,Ar—H),4.12 (s,2H, Ar—CH2—),4.04~3.76 (m,9H,CH3O—),3.15 (s,2H,—CH2—N—),1.49 (m,2H,—CH2—,1.30~1.28 (m,2H,—CH2—CH3),0.88 (m,3H,CH3—CH2—)。13C NMR (101 MHz,CDCl3)δ:156.94,149.41,149.33,146.84,141.64,130.23,126.98,125.70,61.34,61.23,61.16,60.83,51.42,26.16,22.51,14.61。[M+Na]+:405.1。
化合物4d: 2-戊基- 4-(3,4,5-三甲氧基苄基)-1,2,4-噻二唑-3,5-二酮,白色固体,纯度95.3%,产率37%。1H NMR (400 MHz,CDCl3)δ:7.41~7.40 (d,J=9.7 Hz,2H,Ar—H),4.10 (s,2H, Ar—CH2—),4.01~3.65 (m,9H,CH3O—),3.10 (s,2H,—CH2—N—),1.47 (m,2H,—CH2—),1.29~1.26 (m,4H,—CH2—CH2—CH3),0.87 (m,3H,CH3—CH2—)。13C NMR (101 MHz,CDCl3)δ:156.75,149.11,149.13,146.24,140.23,129.12,126.11,121.23,61.23,61.42,61.01,60.87,60.13,31.08,25.78,22.89,14.59。[M+Na]+:391.1。
化合物4e: 2-己基- 4-(3,4,5-三甲氧基苄基)-1,2,4-噻二唑-3,5-二酮,白色固体,纯度95.0%,产率36%。1H NMR (400 MHz,CDCl3)δ:7.41~7.40 (d,J=8.1 Hz,2H,Ar—H),4.09 (s,2H, Ar—CH2—),4.01~3.61 (m,9H,CH3O—),3.08 (s,2H,—CH2—N—),1.46 (s,2H,—CH2—),1.28~1.26 (m,6H,—(CH2)3—CH3),0.88 (m,3H,CH3—CH2—)。13C NMR (101 MHz,CDCl3)δ:156.54,149.00,148.87,146.01,140.13,128.89,126.05,121.22,61.21,60.98,60.95,60.57,60.10,31.09,25.57,23.23,22.77,14.54。[M+Na]+:377.1。
2.3 化合物2、 3和4a~4e抑制HL60细胞增殖结果
采用MTT法测定了化合物2、3、4a~4e和阳性对照药TDZD-8对人急性白血病细胞株HL60细胞增殖的抑制作用,结果见表1。其中,阳性对照药TDZD-8对HL60细胞的IC50值为0.30 μmol/L。
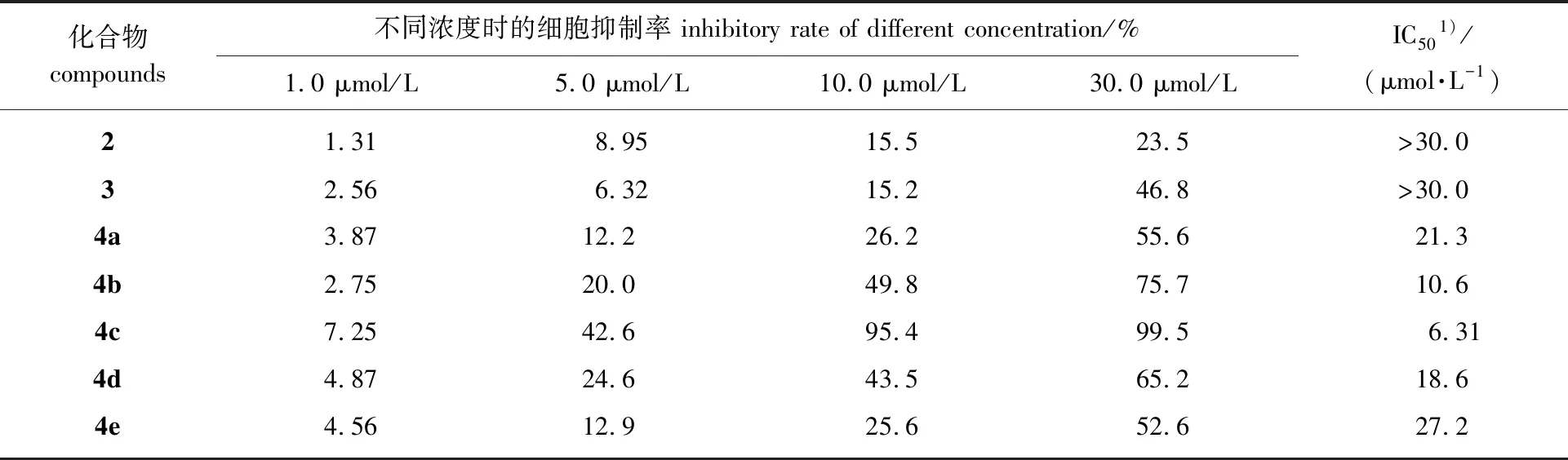
表1 三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物对人HL60细胞的抑制率
1)IC50>30 μmol/L:化合物为低活性 the compound is considered as low activity
由表1可知,化合物4b和4c具有较好的抑制HL60增殖的活性:化合物4b和化合物4c在10 μmol/L浓度下均表现出较好的抑制HL60细胞增殖作用,而在1.0 μmol/L浓度下则抑制率较低,表明2种化合物对HL60的半数抑制浓度(IC50)值应介于1.0~15 μmol/L之间;经计算得到化合物4b和4c的IC50值分别为10.60和6.31 μmol/L。而阳性对照药TDZD-8对HL60细胞的抑制增殖活性较强,IC50值仅为0.30 μmol/L。虽然化合物4b和4c对HL60的抑制活性表现均不如阳性对照药物TDZD-8,但是作为林源活性衍生物,却表现出了开发成为HL60抑制剂的潜力。此外,同文献[12]中与化合物4c结构类似的1,2,4-噻二唑-3,5-二酮衍生物(对急性白血病细胞株IC50值为11.6 μmol/L)对比,本研究中含三甲氧基没食子酸衍生物4c表现出更优异的抑制急性白血病细胞活性(IC50值为6.31 μmol/L)。原因可能是三甲氧基的存在增加了化合物的亲脂性和药物与受体的疏水结合作用,进而增加了药物吸收,使化合物4c表现出更好的抑制活性。HL60细胞形态学观察显示,随着化合物4c浓度增加,HL60细胞增殖速率逐渐受到抑制;随着化合物4c浓度的升高HL60细胞的减少量加快,抑制细胞增殖作用逐渐增强。随着时间的推移,形态学观察显示,HL60细胞的生长逐渐受到抑制,且随着化合物4c浓度的增加,细胞数量显著减少,光学折光度减小;高浓度化合物4c处理细胞后,细胞悬浮脱落,大量细胞不再粘附在壁上。
以上结果表明:三甲氧基的存在能够增加没食子酸1,2,4-噻二唑-3,5-二酮衍生物对HL60细胞的抑制活性。三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物的杂环侧链为端烯结构时,含碳数量越多则活性越高;当杂环侧链为烷烃结构时,则含碳数量越少活性越高。
2.4 化合物4b/4c协同TDZD-8对HL60细胞增殖抑制作用
用不同浓度化合物4b/4c和阳性对照药TDZD-8混合处理HL60细胞72 h,结果表明:随着药物浓度的增加,HL60细胞增殖抑制率显著增加(P<0.05),说明化合物4b/4c和阳性对照药TDZD-8存在一定的协同抑制HL60细胞增殖活性。
基于上述结果,对化合物4b/4c与TDZD-8进行协同抑制HL60细胞增殖研究,结果见表2。HL60肿瘤细胞抑制率显示:当化合物4b与TDZD-8的浓度分别为5.0和0.34 μmol/L时,两者的协同抑制率较高,抑制率为94.45%,CI值最小为0.58;当化合物4c与TDZD-8的浓度分别为5.0和0.34 μmol/L时,两者的协同抑制率较高,抑制率为98.76%,CI值最小为0.31,CI值越小表明两种药物的协同作用越强。可以看出,化合物4c和TDZD-8对HL60细胞的增殖有最好的协同抑制作用(P<0.01)。
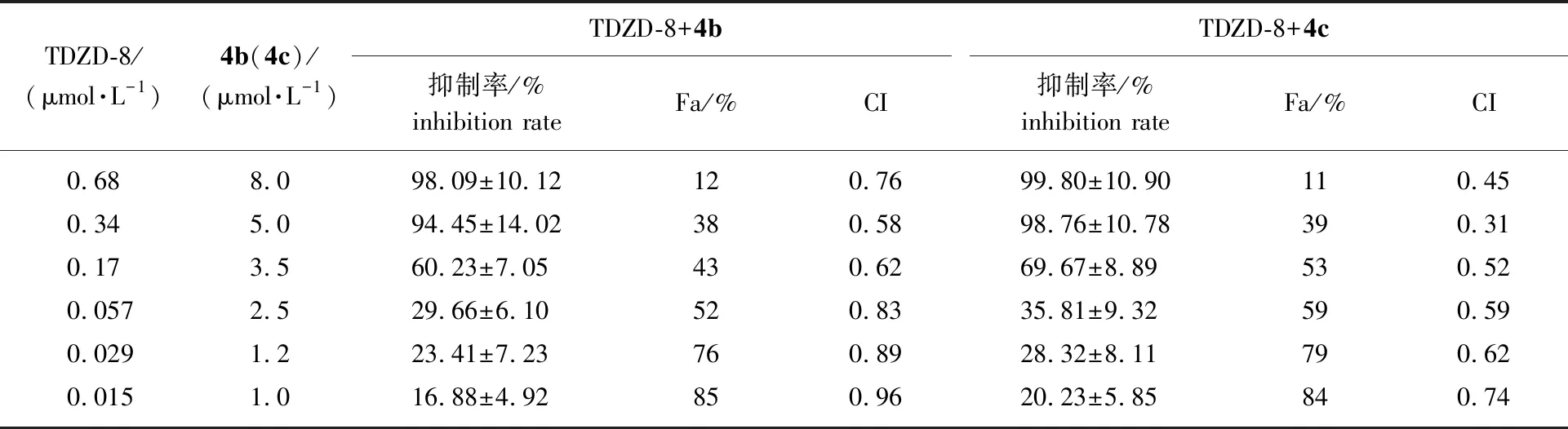
表2 化合物4b和4c协同TDZD-8对HL60细胞的抑制作用(72 h)1)
1)Fa<30%:拮抗作用antagonism;Fa>30%:协同增强synergism
3 结 论
3.1以没食子酸为原料,合成了三甲氧基没食子酸1,2,4-噻二唑-3,5-二酮衍生物(4a~4e),表征了化合物结构,并测定了其对人急性白血病HL60细胞增殖的抑制作用。结果表明:该类化合物对HL60细胞增殖均具有一定的抑制作用,其中化合物4b和4c的抑制效果较好,IC50值分别为10.60和6.31 μmol/L。
3.2化合物4b和4c能够与TDZD-8达到协同抑制HL60细胞增殖的作用,当4c与TDZD-8浓度分别为5.0和0.34 μmol/L时,两者的协同抑制率为98.76%,最小协同指数(CI)值为0.31。可以看出,该类化合物具有作为HL60抑制剂的潜力,也为该类化合物与传统药物TDZD-8的配伍使用提供了实验依据,从而为林源活性物没食子酸开发成为临床抗急性白血病细胞系的医药中间体提供了思路。

