汉族人拉莫三嗪相关过敏反应与HLA-B*1502的相关性
张存玲 朱太卿 张莉峰 郑 蕾
郑州人民医院神经内科,河南 郑州 450003
癫痫是神经内科常见疾病,发病率4‰~7‰[1],治疗方法包括药物治疗、手术治疗等,其中药物治疗仍是主要方法,芳香族化合物包括卡马西平、拉莫三嗪、奥卡西平等是常用的抗癫痫药物,过敏反应也是这些药物常见的严重不良反应。许多研究证据表明卡马西平相关的过敏反应与HLA-B*1502有关,尤其是与亚裔人群具有相关性[2],并在卡马西平的说明书里明确指出亚裔人群在使用前需进行HLA-B*1502的检测,阳性者慎用。拉莫三嗪是妊娠期女性首选的抗癫痫药物,拉莫三嗪与丙戊酸联合为首选的联合用药方案,用于许多难治性癫痫的治疗[3],因此临床应用广泛,但严重的过敏反应让许多医生及患者对其心生畏惧。既然同为芳香族化合物,HLA-B*1502是否也与拉莫三嗪引起的过敏反应有关,目前研究结果不一致[4-5]。本研究探讨HLA-B*1502是否与汉族人拉莫三嗪的相关过敏反应有关。
1 对象及方法
1.1研究对象收集2015-01—2018-12在郑州人民医院门诊及住院癫痫患者中服用拉莫三嗪者,根据服用拉莫三嗪后的反应将其分别纳入实验组和对照组1,同时期服用其他非芳香族抗癫痫药物出现过敏反应者为对照组2。实验组纳入标准:(1)诊断为癫痫(诊断标准依据2014年国际抗癫痫联盟制定的癫痫实用性定义),且服用拉莫三嗪单药治疗;(2)服用拉莫三嗪12周内出现过敏反应,过敏反应类型由皮肤科医师进行诊断;(3)过敏反应排除由其他原因引起;(4)汉族人。对照组1纳入标准:(1)诊断为癫痫(诊断标准依据2014年国际抗癫痫联盟制定的癫痫实用性定义),且服用拉莫三嗪单药治疗;(2)服用拉莫三嗪12周后未出现过敏反应;(3)汉族人。对照组2入组标准:(1)未服用拉莫三嗪及其他芳香族抗癫痫药物;(2)出现过敏反应;(3)汉族人。所有入组人员签署知情同意书。研究方案被郑州人民医院伦理委员会批准。
1.2研究方法采集实验组及对照组1、对照组2人员外周静脉血测定HLA-B*1502基因型,由郑州人民医院院士工作站采用序列特异性引物-聚合酶链式反应技术进行基因测定。

2 结果
共收集服用拉莫三嗪的癫痫患者150例,12周后出现过敏反应者43例入实验组,其中41例(95.35%)表现为轻型斑丘疹,给予停药及抗过敏药物治疗后皮疹消退,2例出现SJS,经治疗后好转;未出现过敏者107例,入对照组1,因服用其他药物出现过敏反应者30例为对照组2,对照组2均表现为轻型斑丘疹。实验组及对照组1、对照组2基本资料见表1。
实验组与对照组1及对照组2在年龄及性别构成上无显著差异,对照组1及对照组2在年龄及性别组成上差异无统计学意义(P>0.05)。
实验组43例拉莫三嗪引起过敏的患者中HLA-B*1502的阳性率为41.86%,对照组1为14.02%,对照组2为13.33%。将实验组与对照组1、对照组2,对照组1与对照组2的HLA-B*1502阳性率分别进行比较,从表2可以看出,实验组阳性率高于对照组1(χ2=13.86,P<0.05)及对照组2(χ2=6.83,P=0.009),对照组1与对照组2差异无统计学意义(χ2=0.009,P=0.924)。另外,41例轻型斑丘疹中HLA-B*1502阳性为16例(39.02%),而2例由拉莫三嗪所致SJS患者中,HLA-B*1502均为阳性(100%)。41例表现为斑丘疹组的HLA-B*1502阳性率与对照组1及对照组2比较,差异均有统计学意义(P<0.05)。
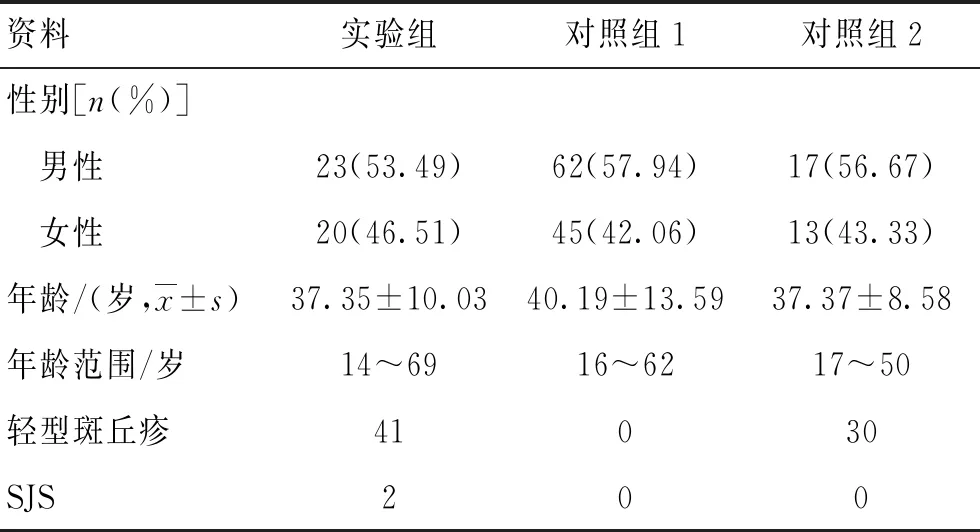
表1 实验组与对照组1、对照组2基本资料

表2 实验组及对照组1、对照组2 HLA-B*1502结果 [n(%)]
注:*为实验组与对照组1比较;^为实验组与对照组2比较结果;#为对照组1与对照组2比较;&为41例轻型斑丘疹组与对照组1比较;$为轻型斑丘疹组与对照组2比较
3 讨论
人类白细胞抗原基因是主要的免疫相关基因,研究发现,HLA基因具有种族特异性,与多种疾病有关[6]。皮肤过敏反应是拉莫三嗪常见的不良反应,包括轻微的斑丘疹、还有严重的SJS综合征和TEN,SJS和TEN的发生率虽然很低,每年(0.4~6)/100万人,但致死率非常高,达到5%~12.5%,甚至有报道称TEN的致死率高达50%[7]。拉莫三嗪作为一个常用的抗癫痫药物,过敏反应是其最常见的不良反应,也是医生及患者在用药时最担心的一点,同时严重的过敏反应也限制了其在临床上的广泛应用,如果可以通过某些方法提前预测这种过敏反应的出现,从而避免严重过敏反应的发生,将会使许多癫痫患者获益。
在大洋洲、东亚、中南亚人群中,HLA-B*1502被普遍检测出[8],有些地方报道的阳性率为1%~10%,甚至高于10%。本组150例病人中HLA-B*1502阳性率为15.33%,与王倩等[9]报道的17.74%接近,说明HLA-B*1502在亚裔人中阳性率很高,如果它确实与拉莫三嗪相关过敏反应相关,那么在用药前对HLA-B*1502进行筛查就尤为必要。
近年来国内外学者对卡马西平诱导的SJS和TEN与HLA-B*1502的相关性研究比较多[10-11],而拉莫三嗪相关过敏反应与基因多态性的相关性研究很少,并且这些研究结果并不一致。SUN等[12]认为HLA-B*1502可能与芳香族抗癫痫药引起的SJS有关。KAZEEM等[13-14]发现拉莫三嗪引起的SJS/TEN可能与HLA-B*1502有关,且不仅仅局限于亚裔人,方登富等[15]也发现HLA-B*1502与拉莫三嗪引起的SJS/TEN有关,ZENG等[16]对HLA-B*1502等位基因与拉莫三嗪诱导的史蒂文斯-约翰逊综合征与中毒性表皮坏死松解症在汉族人中的相关性进行了Meta分析认为汉族人中,携带有HLA-B*1502者服用拉莫三嗪出现皮肤过敏反应的概率是未携带者的4.98倍。本组2例拉莫三嗪相关的SJS均表现为HLA-B*1502阳性,也支持这些研究结果。而高阳等[17]却认为HLA-B*1502与拉莫三嗪所致药疹无关,PARK等[18]发现韩国人拉莫三嗪相关的SJS可能与HLA-B*4403有关,而MOON等[19]一项对于韩国人的研究却发现韩国人拉莫三嗪引起的皮肤过敏反应可能与HLA-A*2402 /Cw*0102有关。SHIRZADI等[20]对挪威人群的研究也发现拉莫三嗪诱导的皮肤反应可能与HLA-A*2402有关。TONEKABONI等[21]对伊朗儿童抗癫痫药物引起的皮肤反应与HLA-B*1502的相关性研究没有发现两者的相关性,SHI等[22]发现拉莫三嗪相关的过敏反应在白种人中与HLA-B*38强相关,与HLA-B*1502无明显相关性,同样关于卡马西平与HLA-B*1502的相关性研究也发现白种人卡马西平相关过敏反应与HLA-B*1502无关,而与HLA-A*3101有关[23],可能与HLA的种族特异性有关。
本研究发现,服用拉莫三嗪的150例患者中,出现皮肤过敏反应43例,发生率28.67%,其中95.35%为轻型斑丘疹,2例(4.65%)为SJS,在拉莫三嗪引起过敏反应组HLA-B*1502的阳性率明显高于服用拉莫三嗪未出现过敏反应组及服用其他药物出现过敏反应组,其中2例表现为SJS的患者中,HLA-B*1502均为阳性,说明拉莫三嗪引起的过敏反应,尤其是SJS与HLA-B*1502具有相关性,与相关研究结论一致。同时发现HLA-B*1502 在轻型皮疹组的阳性率也高于对照组1及对照组2,说明拉莫三嗪相关的轻型斑丘疹与HLA-B*1502相关,但也有研究发现轻型皮疹与HLA-B*1502无明确相关性[24]。DENG等[25]研究拉莫三嗪相关的轻型斑丘疹与HLA-B*1502无关,而与HLA-A*2402有关。
本研究显示,在汉族人中拉莫三嗪引起的过敏反应,包括轻型的皮肤斑丘疹和严重的SJS,可能与HLA-B*1502有关,鉴于过敏反应引起的严重后果,建议类似于卡马西平,对亚裔人,尤其是汉族人,如果要服用拉莫三嗪,服用前进行HLA-B*1502检测,如果为阳性,则慎用拉莫三嗪,可选择其他非芳香族抗癫痫药。
鉴于目前关于拉莫三嗪引起的过敏反应是否与HLA-B*1502相关,国内外研究尚无定论,本次研究纳入的病例数较少,关于拉莫三嗪相关的轻型皮疹及SJS与HLA-B*1502是否具有相关性,还需要更大样本量数据研究以期望得到更准确的结果。

