改性魔芋葡甘聚糖对水中三氯乙酸的吸附影响
许秀真
泉州师范学院资源与环境科学学院(泉州 362000)
氯化消毒是应用最广泛、时间最长久的饮用水消毒方式之一[1]。氯化消毒方法所使用的消毒剂会产生消毒副产物(DBPs)。卤乙酸(HAAs)、三卤甲烷(THMs)二者含量之和可占全部DBPs的80%以上[2]。卤乙酸致癌风险超过DBPs总致癌风险的91.9%[3],HAAs中又以高检出率的(二氯乙酸)DCAA和(三氯乙酸)TCAA的致癌风险为主,DCAA的致癌风险低于TCAA。《生活饮用水卫生标准》规定居民饮用水中TCAA最大允许浓度不能超过100 μg/L[4]。
对三氯乙酸的去除方法有采用相对光/电催化氧化技术、Fe/Cu催化还原去除法、生物强化降解作用与活性炭的吸附作用协同、紫外光降解法等[5-8]。而用光催化法降解过程繁琐复杂,效果也较差,受到的影响因素也较多,不利于实际应用[8];零价铁还原产生大量铁泥等二次污染[9];生物与活性炭/陶粒协调降解要保持生物活性稳定性有一定困难;从安全、方便问题上考虑,紫外光降解法不适用于管网中残留TCAA的控制。
魔芋葡甘聚糖(Konjac glucomannan,KGM)作为一种高分子植物多糖,可以从魔芋块茎获得,其属于水溶性非离子型天然聚多糖,被广泛应用于生物食品、医药、石油、化工、环保以及建筑等众多领域,已成为国内外研究的热点[10]。改性魔芋葡甘聚糖(DKGM)是指通过化学改性,即由魔芋葡甘聚糖的分子链上接入或减少一些基团,可以令魔芋葡甘聚糖分子结构产生变化,研究出具备特定功能的魔芋葡甘聚糖衍生物。KGM分子链上有丰富的乙酰基以及羟基,能够很轻易地对它实现交联、接枝以及脱乙酰基等操作,从而得到多种功能用途的材料[11]。试验结合魔芋葡甘聚糖具有安全、无毒、可再生、可降解、絮凝、抗菌等优点,通过物理和化学作用对其进行改性,使其作为缓释剂吸附饮用水中TCAA。
1 材料与方法
1.1 试验器材
1.1.1 试验材料
基金项目:福建省科技计划项目(2016J01694),福建省中青年教师教育科研项目(JA14267),泉州市科技计划项目(2014Z121)
魔芋精粉(湖北省天源协力食品有限公司)。
氢氧化钠、无水乙醇、三氯乙酸、硫酸、甲醇、碳酸氢钠、无水硫酸钠(均为分析纯,国药集团化学试剂有限公司);无水硫酸铜(AR,上海展云化工有限公司);1-2DBP甲基叔丁基醚(美国进口)。
1.1.2 设备仪器
电热恒温水浴锅(HWS 26型,上海一恒科学仪器有限公司);恒温振荡培养箱(HZC-250,太仓市实验设备厂);气相色谱仪(CN 11191007,福建省计量科学研究院);电子天平(BS 323 S,北京赛多利斯仪器系统有限公司)。
1.2 试验步骤
1.2.1 改性的魔芋葡甘聚糖制备阶段
称取一定量高纯度魔芋精粉(W1)到250 mL锥形瓶内,加入65 mL 40%乙醇,在55 ℃下溶胀1 h,加入已标定好适量的NaOH(W2)及数滴酚酞指示剂,在50 ℃恒温振荡反应到无色。用10%盐酸调节使待测液pH 7.0,真空过滤出样品,用40%乙醇清洗数次,将清洗后的样品放入烘箱中在105 ℃下烘干至恒重,等样品冷却到室温之后进行研磨过筛后密封保存,按式(1)求得DKGM的脱乙酰度,所得脱乙酰度≥95%。
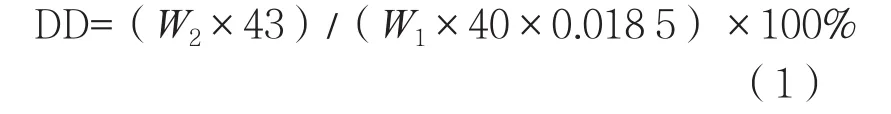
式中:W1表示KGM质量,g;W2表示NaOH质量,g。
1.2.2 标准曲线的制备
试验标准曲线的制备采用GB/T 5750.10—2006《生活饮用水标准检验方法-消毒副产物指标》中三氯乙酸的标准曲线制备法制备[12]。
1.2.3 吸附试验
将100 mL一定浓度的三氯乙酸加入250 mL锥形瓶中,用0.1 mol/L的NaOH溶液和0.1 mol/L的HCl溶液进行调节到适当pH,同时加入一定质量DKGM,用保鲜膜贴住瓶口,封紧。将瓶子放到恒温振荡培养箱上用100 r/min的转速进行振荡。振荡完后过滤样品,利用气相色谱法[11]来测定滤液中吸附后的三氯乙酸浓度。通过式(2)和(3)计算三氯乙酸去除效率以及DKGM吸附量。

式中:B表示三氯乙酸去除效率,%;De表示DKGM吸附量,mg/g;C0表示三氯乙酸初始浓度,mg/L;Ce表示吸附平衡之后溶液中剩余的三氯乙酸浓度,mg/L;V表示溶液体积,mL;w表示DKGM质量,g。
1) 确定吸附材料的初始用量
对照改性魔芋葡甘聚糖吸附水中单宁试验[11],在同一浓度三氯乙酸溶液中分别加入不同量的吸附材料,在同一温度下振荡吸附同一时间,确定吸附材料初始用量。
2) pH的影响
使用初始质量浓度0.150 mg/L的三氯乙酸溶液,用0.1 mol/L的NaOH溶液和0.1 mol/L的HCl溶液调节pH,pH分别为5,6,7,8和9。在25 ℃下把0.35 g吸附材料放入指定pH的三氯乙酸溶液,进行振荡吸附1.5 h。
3) 吸附材料的用量的影响
使用已调好pH 6.74初始质量浓度0.150 mg/L的三氯乙酸溶液。在25 ℃下分别将0,0.15,0.25,0.35,0.45和0.55 g吸附材料加入到三氯乙酸溶液中,振荡吸附1.5 h。
4) 吸附时间的影响
使用已调好pH 6.74初始质量浓度0.150 mg/L的三氯乙酸溶液。在25 ℃下分别将0.35 g吸附材料加入到三氯乙酸溶液中振荡吸附0.5,1.0,1.5,2.0,2.5和3.0 h。
5) 吸附温度的影响
使用已调好pH 6.74初始质量浓度0.150和0.200 mg/L的三氯乙酸溶液。将0.35 g吸附材料加入到15,25,35,45和55 ℃三氯乙酸溶液中振荡吸附2 h。
6) 吸附浓度的影响
在25 ℃温度下,将0.35 g吸附材料加入到初始质量浓度0.100,0.125,0.150,0.175和0.200 mg/L的三氯乙酸溶液中振荡吸附2 h。测得各个不同溶液pH为6~7,考虑到饮用水对pH的要求,试验中只对0.2 mg/L的三氯乙酸溶液pH条件调节到pH>6.5,其他溶液不调节。
2 结果与分析
2.1 pH对吸附的影响
DKGM分子结构上含有大量的羟基基团,主要通过氢键与TCAA作用,对TCAA有较好的吸附性。从图1可看出,当pH<6时,pH变化对DKGM吸附TCAA的效果不大;pH 6~7时,吸附量随pH的升高而增大;pH 7~8时,吸附量随pH的升高而快速减小;pH 8~9时,pH的改变对吸附效果无多大作用。由此可见,三氯乙酸溶液的pH变化对DKGM的吸附能力有很大作用,DKGM对TCAA吸附最佳pH约为7。究其原因,可能是溶液在pH<6时,其中溶液游离的H+优先与DKGM相结合,同TCAA形成竞争关系,DKGM对TCAA吸附能力较小。当pH越接近中性时,溶液中的H+含量下降,即与TCAA的竞争力减小,DKGM与TCAA的分子氢键增强,吸附量上升。TCAA水溶液呈中强酸性,溶液pH 7~8即弱碱性时,TCAA的电离能力增强,TCAA酸表面呈负电荷,其溶液游离出来的H+优先与溶液中调节的NaOH中的OH-生成水,但又没有反应完全。NaOH减弱DKGM与TCAA的分子间氢键作用力,同时又使带负电荷的TCAA与DKGM分子之间相互排斥增强,在这些因素的共同作用下,吸附量急剧下降。而pH>8时,TCAA达到电离平衡,pH的改变对吸附量无多大作用。
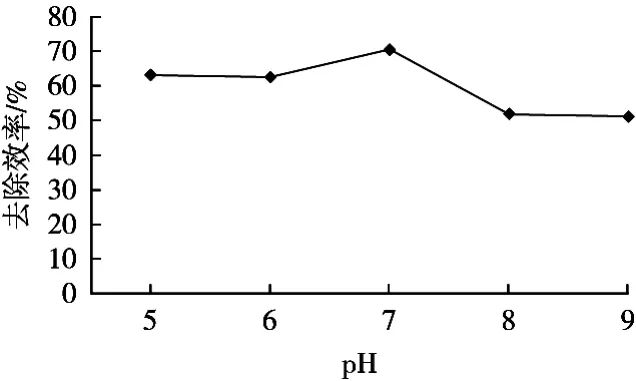
图1 pH对吸附的影响
2.2 吸附材料用量的影响
为考察吸附材料对TCAA去除效率,选择0.15和0.20 mg/L这2种浓度的TCAA溶液。由图2和图3可知,随着吸附材料用量的增大,其对TCAA去除效率呈先增长后下降的趋势,当吸附材料用量小于0.35 g时,脱除效率随着吸附材料用量不断增大而上升;当吸附材料用量大于0.35 g时,不断增大吸附用量,脱除效率反而减小;当吸附材料用量为0.35 g时,脱除效率达到最大,2种浓度的TCAA最大脱除效率约为78%。通常,吸附用量增加时,活性官能团和比表面积也会增大,脱除效率更高。当加入DKGM的量一定时,DKGM对TACC的吸附达到最大,脱除效率最高,进一步增加吸附用量反而使脱除效率降低。这可能是因为DKGM对TCAA的吸附之间存在一个解吸现象,部分已被吸附的TCAA脱离DKGM游离出来,即DKGM对TCAA的吸附不稳定。当增加投加量时,不同DKGM之间出现竞争,使得DKGM对TCAA的吸附不稳定性增加,解吸现象增加,从而使脱除效率下降。从吸附容量的角度分析,随着吸附材料的增加,吸附容量呈下降的趋势。可能是在一定浓度一定体积的TCAA溶液中,TCAA分子数量有限,进一步增大吸附材料的用量,在DKGM对TCAA吸附的解吸以及DKGM对TCAA吸附竞争性的双重影响情况下,吸附材料也未达到饱和。
2.3 吸附时间的影响
从图4可以看出,DKGM对TCAA的吸附效率呈先升高后下降的趋势,在0.5~2.0 h,DKGM对TCAA的吸附去除能力不断提高,去除效率在2.0 h时达到一个最大值,为91.7%;超过2 h,随着时间的增加,吸附去除TCAA能力下降。这可能是因为在前2 h反应时间内,溶液中TCAA游离出来的H+含量较多,能快速与DKGM的羟基基团进行反应,吸附容量达到最大;同时,由于DKGM对TCAA的吸附的不稳定性,随着时间的推移,出现解吸现象,吸附效率下降,吸附容量减小。
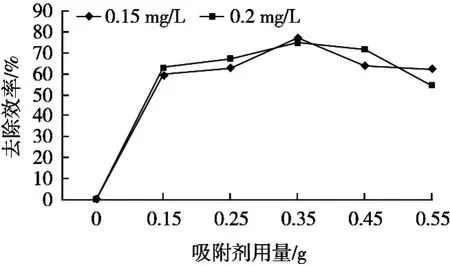
图2 吸附材料用量的影响
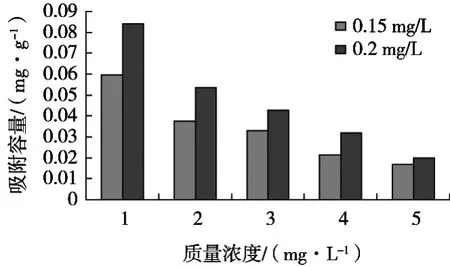
图3 不同吸附用量的吸附容量

图4 吸附时间的影响
2.4 吸附温度的影响
从图5可以看出DKGM对TCAA的吸附效率呈先升后降再上升的趋势。随着温度的增加,吸附容量也呈先升后降再上升的趋势,数据变化见表1。在15~25℃,DKGM对TCAA的吸附去除能力不断提高,去除效率达到最大,吸附容量也达到最大;在25~35 ℃,随着温度的升高,吸附去除TCAA能力下降,这可能是因为在35 ℃之前的吸附偏向于物理吸附,吸附过程快,虽然温度升高,可吸附过程放出热量,两者相互抵消,温度的升高不会加强化学的吸附能力,因此吸附力不强,DKGM对TCAA的吸附的不稳定性,出现解吸现象,吸附效率下降,吸附容量也减小。但随着温度继续升高,其表现更偏向于化学吸附,DKGM对TCAA的吸附去除能力也在提高,解吸出来的TCAA重新被吸附,去除效率提高,吸附容量也在增大,到55℃时,吸附容量与25 ℃时的吸附容量很接近。
试验尝试使用DKGM对TCAA的吸附用热力学函数来说明系统的变化状态,热力学函数采用式(4)[11]。

式中:K表示吸附平衡常数;C0表示初始质量浓度,mg/L;Ce表示平衡后的溶液中剩余的三氯乙酸浓度,mg/L;T表示吸附绝对摄氏温度,℃。
通过对lnK和1/T作图(图6),lnK和1/T之间的线性关系不好,线性相关度为0.116,可见DKGM对TCAA的吸附物理和化学吸附同时并存,其热力学作用较为复杂,解吸与吸附并存,作用机理复杂。
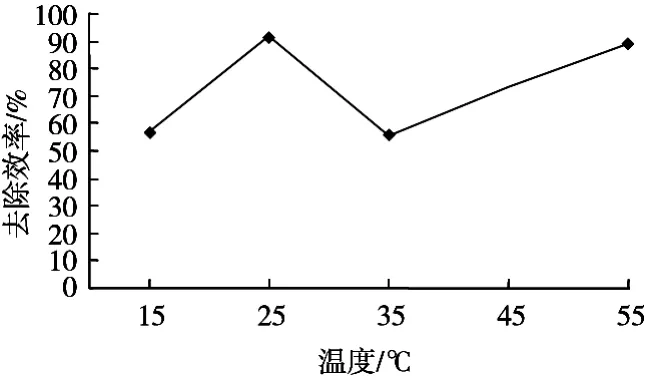
图5 吸附温度的影响
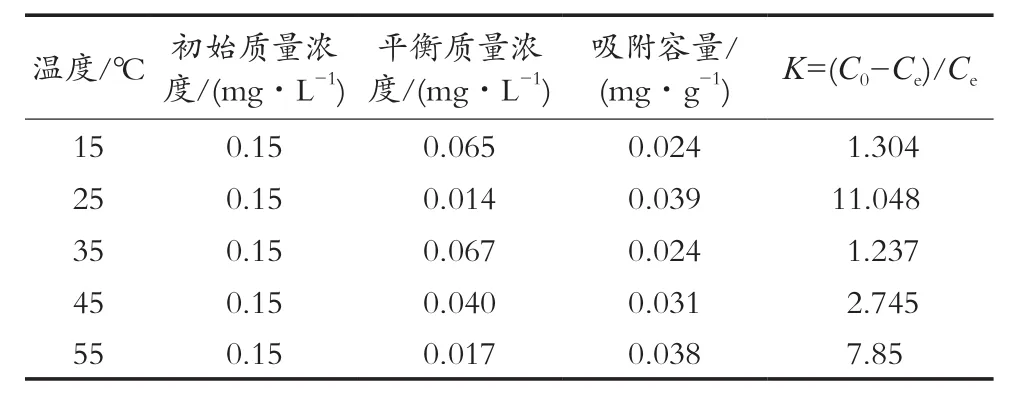
表1 不同温度下的吸附参数

图6 lnK与1/T之间的线性关系
2.5 吸附浓度的影响
从图7可以看出DKGM对TCAA的吸附效率呈先降后上升再降趋势。随着三氯乙酸的质量浓度从0.100 mg/L增加到0.125 mg/L,DKGM对TCAA的去除效率下降,可能是因为刚开始时,DKGM吸附TCAA速度很快,但是不稳定,随着TCAA浓度增加,过量的DKGM羟基基团竞争与TCAA中的H+进行反应,极易发生吸附。当TCAA浓度增加到0.15 mg/L时,DKGM对TCAA的去除效率提高,此时DKGM羟基基团与TCAA中的H+进行的反应不再相互竞争,每个DKGM羟基基团都能够从TCAA中获得对应的H+,分子间氢键作用力得到增强。当TCAA浓度不断增加时,DKGM对TCAA的吸附效率继续下降,TCAA中的H+数量大于DKGM中的羟基基团,H+之间相互竞争以期获得与羟基反应的机会,削弱分子间氢键作用力,解吸趋势明显。

图7 吸附浓度的影响
3 结论
在pH 6~7、DKGM吸附材料用量0.35 g、吸附时间2 h、吸附温度25 ℃、TCAA质量浓度0.15 mg/L的条件下,TCAA的去除效率最佳。
DKGM对TCAA吸附亲和能力随外在条件变化而发生较为明显的变化,吸附稳定性较差。

