基于MEMS技术的压力感应内藏式膀胱造瘘器的设计与安全性检测*
林婷婷 陈烨辉 李晓东 许 宁 孙雄林 魏 勇 薛学义 郑清水
福建医科大学附属第一医院泌尿外科,福建省福州市 350005
膀胱穿刺造瘘术用于永久性尿流改道,是泌尿外科治疗神经源性膀胱的最常用手术之一[1-2]。目前临床常使用蕈状造瘘管或气囊导尿管作为膀胱造瘘管予以引流尿液,但存在不少缺陷,如易堵塞、携带不便、易发生尿路感染、可诱发膀胱痉挛等[3]。因此,拟研制一种基于微电子机械系统(Micro electro-mechanical system,MEMS)技术实时监测膀胱压力的新型内藏式的膀胱造瘘器,能够做到及时报警、有效固定、避免刺激及外表美观,解决传统膀胱造瘘装置的不足。现将研究前期阶段关于膀胱造瘘器设计原理、样式及安全性检测实验结果进行报道。
1 材料与方法
1.1 伦理审批 本研究通过福建医科大学附属第一医院伦理委员会审核后获批进行。
1.2 设计原理 本装置由穿刺套件(包括内芯及外鞘)及造瘘器本体组成。穿刺套件的内芯为一根长条形头端尖锐的金属制品,用于穿刺时帮助外鞘突破组织进入膀胱。外鞘包括装置固定及长度调节两个模块,如图1示:注水后膨胀的环形水囊及旋转螺母共同起到将外鞘牢固固定在腹壁上的作用,并且通过外鞘长度调节装置,可个体化地根据病人的实际情况,找到最合适的固定距离。如图2所示,造瘘器本体安装于外鞘上,并可灵活拆卸。其主要由引流内芯、压力感应、显示及报警三个模块组成:引流内芯模块用于膀胱内的尿液的引流,可通过出口处的阀门控制;半导体硅压阻式压力传感器直接与尿液接触,感受膀胱内压的变化,将信号传至处理器,并显示于液晶屏上,若压力大于预设值,则触发警报,提醒患者打开排尿阀门进行排尿。图3为实际样品设计图。
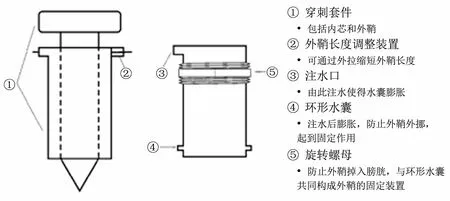
图1 新型膀胱造瘘装置穿刺套件示意图

图2 新型膀胱造瘘装置造瘘器本体示意图
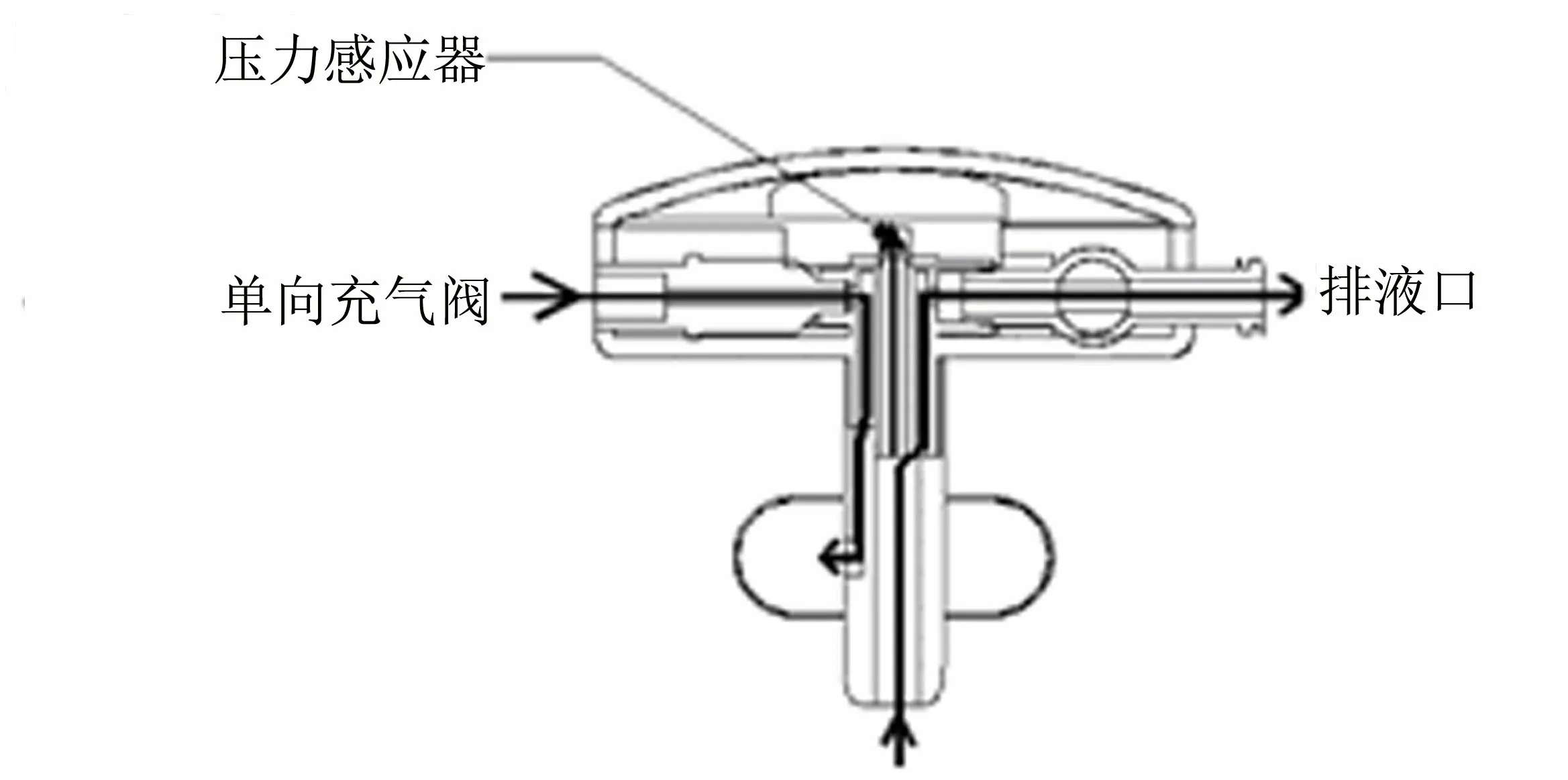
图3 新型膀胱造瘘器样品实际设计图
1.3 安全性检测
1.3.1 细胞毒性实验:(1)细胞株:L929细胞(ATCC)。(2)实验试剂;胎牛血清(GIBCO)、RPMI1640(GIBCO)、胰酶/EDTA(GIBCO)、琼脂(奥博星)、中性红(Amresco)。(3)实验组、对照组:实验组为本产品样品,以20ml生理盐水于37℃浸提24h;阴性对照为高密度聚乙烯(上海赛科),以20ml生理盐水于37℃浸提24h;阳性对照为含有机锡添加剂的聚氯乙烯(SIMS Portex Ltd,Hythe,Kent,CT21 6JL,UK),以20ml生理盐水于37℃浸提24h。(4)实验方法:通过琼脂扩散实验[4]来评估样品对细胞的毒性。①将预处理好的L929细胞悬浊液10ml加入培养皿,水平转动使细胞均匀分散,置入CO2培养箱37℃培养24h,形成近汇合单层细胞;②弃去培养液,将配制好的琼脂培养基10ml加入培养皿内,水平转动使琼脂培养基均匀分布并在室温下凝固。每个培养皿内加入10ml中性红染液,置培养箱37℃避光保持15min后弃去多余染液;③分别吸取0.01ml样品或对照材料浸提液,加入直径为5mm圆形滤纸片中,将滤纸片放置在琼脂表面。将培养皿置CO2培养箱继续培养24h;④置显微镜下观察滤纸片周围及下方的细胞溶解情况,参照表1进行结果判定。

表1 琼脂扩散实验细胞毒性反应分级
1.3.2 皮肤刺激实验:(1)实验动物:健康成年新西兰兔,共6只,雌雄各半,体重(2.0±0.5)kg,购自福建医科大学实验动物中心,饲养于室温23℃,湿度54%的环境中,饲养过程中自由进食与饮水。(2)实验试剂:生理盐水、橄榄油。(3)实验组、对照组:实验组为本产品样品,分别以20ml生理盐水和20ml橄榄油于37℃浸提24h;以20ml生理盐水和20ml橄榄油作为空白对照组。(4)实验方法:①将6只家兔洗净皮肤,在实验前24h褪去背部脊柱两侧绒毛(面积为10cm×15cm),作为实验和观察部位,如图4所示,每只兔子背后分别有2处实验部位及2处对照部位;②将实验组生理盐水浸提液、实验组橄榄油浸提液、空白组生理盐水、空白组橄榄油取0.5ml,分别滴到2.5cm×2.5cm大小的吸收性纱布上,分别贴于家兔背后相应区域,用绷带固定纱布4h后,去除纱布,并将实验部位清洗、擦拭干净;③在去除纱布后的1h、24h、48h和72h于自然光下观察各区域皮肤反应情况,参照表2予计分并计算原发性刺激指数(Primary irritation index,PII),计算公式为:PII=(红斑总计分+水肿总计分)/观察次数,根据表3判断刺激反应类型。
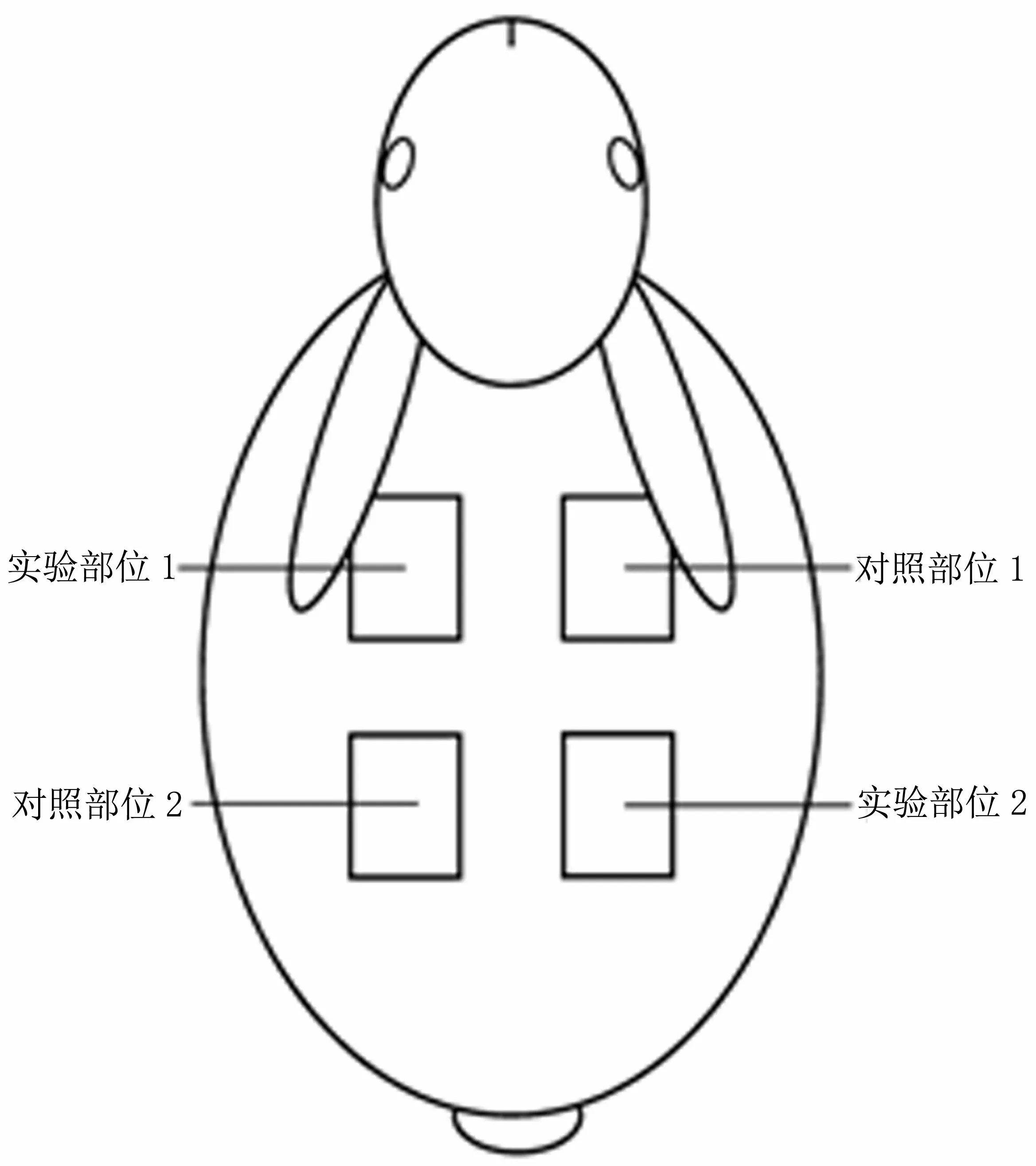
图4 兔子背部实验区域示意图

2 结果
2.1 细胞毒性实验 培养24h后,显微镜下观察实验结果,如表4所示。实验组毒性反应级别均≤1级,细胞溶解率均<10%,与阴性对照组无明显差异;而阳性对照组毒性反应级别均为4级,细胞溶解率均>90%,显著高于实验组及阴性对照组。
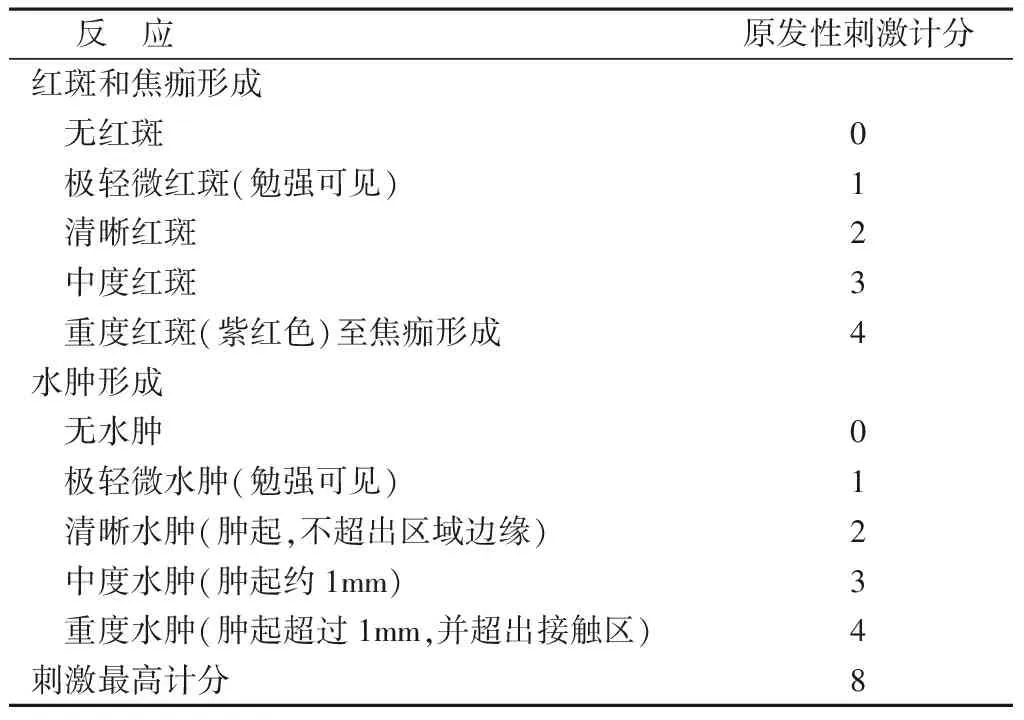
表2 皮肤反应计分系统
注:记录并报告皮肤部位的其他异常情况。

表3 刺激反应类型
2.2 皮肤刺激实验 在去除纱布后的1h、24h、48h和72h后各组计分如表5所示。表6示:PII(实验组生理盐水浸提液)=0.375±0.440;PII(对照组生理盐水)=0.250±0.274;PII(实验组橄榄油浸提液)=0.375±0.209;PII(对照组橄榄油)=0.333±0.258。相比于对应的空白对照组,生理盐水及橄榄油浸提的实验组对皮肤刺激程度无明显差别(P分别为0.568与0.765),刺激反应类型均为极轻微。

表4 琼脂扩散实验的实验结果
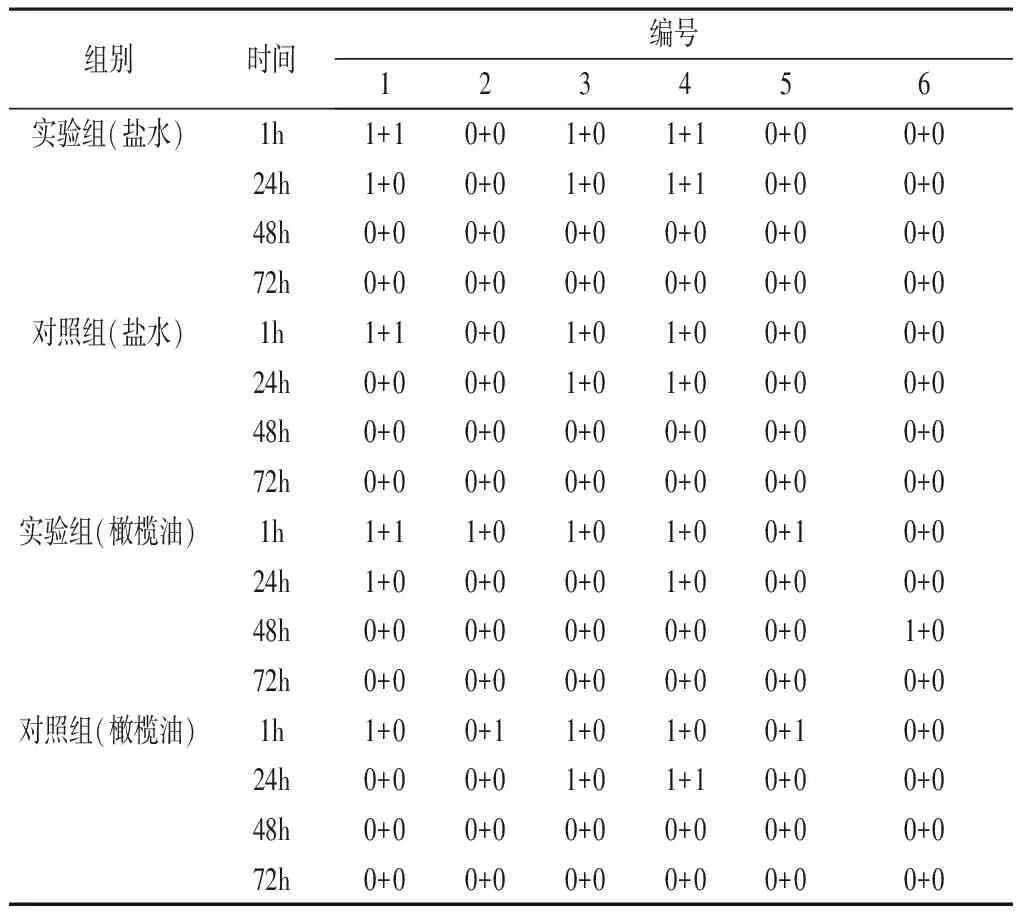
表5 随时间改变各实验样本对兔皮肤刺激反应计分
注:结果表示为:红斑和焦痂得分+水肿得分。

表6 各实验兔的原发性刺激指数计算结果
3 讨论
目前临床常使用蕈状造瘘管或气囊导尿管作为膀胱造瘘管予以引流尿液[1],但存在不少缺陷:由于气囊导尿管尖端为盲端,管侧壁引流口直径较小,易被膀胱黏膜、絮状物、结石等阻塞导致引流不畅;永久性膀胱造瘘患者需要终生携带狭长的导尿管和集尿袋,外观不美观且需定期更换,造成诸多不便,给患者身心健康和正常社交带来不良影响[5];在带管期间易发生感染,部分患者须长期服用抗生素预防[6];导尿管气囊前端管道较长,置入膀胱腔内相对过深,悬浮的导尿管前端因体位、膀胱容量等变化因素,刺激膀胱三角区或膀胱颈部,诱发膀胱痉挛,给患者身心带来巨大痛苦[3]。部分患者造瘘管不能与腹壁组织紧密结合,闭管时易从造瘘管旁大量溢尿。因此,设计一种新型的能克服上述缺陷、改善患者用户体验的膀胱造瘘器势在必行。
MEMS技术是指由微机械加工方法加工的微传感器和微执行器,与微电子信号处理和控制电路有机结合而成的自动化和智能化的微系统[7]。目前基于MEMS 技术的设备在医疗领域中得到了广泛应用[8-10]。本造瘘器充分发扬MEMS技术的优点,通过多处设计上的创新,旨在解决上述缺陷:环形水囊及旋转螺母双重固定,能个性化地适合各种腹壁厚度的患者,牢固地固定造瘘器,避免了漏尿的发生及导管前端摩擦造成的膀胱痉挛;基于MEMS技术的压力感应器与报警装置,能实时监测膀胱内压并做出反馈,从而使患者能模拟生理条件膀胱的周期性扩张与排空,在解决即时排尿问题的同时,促进膀胱功能的恢复,降低尿路感染及上尿路损害的概率;小巧美观的外表及无尿袋化的设计,最大限度减轻了患者生理、心理上的不适感及社交障碍。
本研究依照GB/T16886国家医疗机械生物学评价标准,对新研发的医用材料需进行生物学安全性评价,分为细胞毒性的评价与皮肤刺激性的评价[11-12]。琼脂扩散法[4]是一种常用的半定量评价实验样品对细胞毒性作用的方法,研究显示实验组与阴性对照组对细胞的毒性反应无明显差别;此外,皮肤刺激实验也显示,实验组对小鼠皮肤刺激性与阴性对照组无明显差异。因此,安全性评估得出:本造瘘器在实验条件下无细胞毒性及皮肤刺激性,可进行临床试用,进一步评价其安全性及临床实用性。

