奥拉帕利联合阿比特龙治疗BRCA2突变转移性激素敏感性前列腺癌一例
韦 煜 王弘恺 吴俊龙 叶定伟 朱 耀
1 病例资料患者男,45岁,因尿频、尿急于2017年4月18日入外院,检测血前列腺特异性抗原(PSA)为606.1 ng/mL(正常参考值为1~4 ng/mL)。直肠指检:前列腺Ⅲ度大,双侧叶质硬,与直肠可疑粘连。前列腺穿刺病理学检查确诊为前列腺腺癌,Gleason分级4+5。盆腔MRI检查:前列腺外周带异常信号灶,双侧髂血管旁和盆底淋巴结肿大,腰椎、骨盆和双侧股骨转移可能。骨扫描:全身多发骨转移,见图1。诊断为前列腺癌(TxN1M1)。患者于2017年5月6日在外院接受全雄激素阻断内分泌治疗(ADT)。
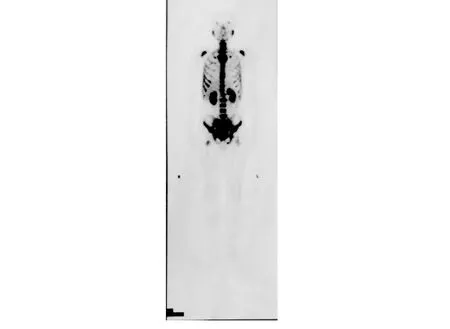
图1 2017年4月25日外院骨扫描检查见全身多发骨转移
2017年8月4日,患者至复旦大学附属肿瘤医院(以下简称肿瘤医院)就诊。既往史:平素体健。家族史:父亲患膀胱癌,2位叔叔患前列腺癌。实验室检查:PSA 22.8 ng/mL,睾酮0.13 nmol/L。前列腺特异性膜抗原(PSMA)-正电子发射型计算机断层显像(SPECT/CT):前列腺癌内分泌治疗中,前列腺原发灶未见放射性摄取增高;腹膜后、两侧髂血管旁淋巴结转移,全身多发骨转移,PSMA高表达。
考虑患者属于高转移负荷的激素敏感性前列腺癌(mHSPC),推荐ADT联合阿比特龙或ADT联合多西他赛进行化学治疗;同时考虑患者属于转移性前列腺癌,且早发,家族史显示二级亲属中有2例前列腺癌患者,参考美国国立综合癌症网络(NCCN)指南和国内专家共识,推荐行基因检测。患者选择ADT联合阿比特龙治疗。
2017年8月20日,二代基因测序显示胚系BRCA2突变,提示对聚ADP核糖聚合酶(PARP)抑制剂或铂类化学治疗敏感。9月27日,与患者讨论后其入组PARP抑制剂临床试验,开始行阿比特龙联合PARP抑制剂治疗。12月18日,检测患者血PSA降至10.98 ng/mL。PSMA-SPECT/CT:前列腺癌内分泌治疗中,前列腺未见放射性摄取增高;原腹膜后、双侧髂血管旁肿大淋巴结多数消退,仅见左侧髂血管旁小淋巴结,放射性摄取同前相仿;全身多发骨转移同前相仿,放射性摄取同前相仿,见图2。

图2 2017年12月18日PSMA-SPECT/CT检查图像
2018年3月28日,检测患者血PSA为3.71 ng/mL。PSMA-SPECT/CT:前列腺癌内分泌治疗中,前列腺体积未见增大,未见放射性摄取增高,原左侧髂血管旁小淋巴结放射性摄取增高程度同前,全身多发骨转移灶同前,放射性摄取增高程度同前相仿,见图3。
2018年6月28日,检测患者血PSA为2.1 ng/mL;PSMA-SPECT/CT为前列腺癌治疗后,全身广泛骨转移同前,仍见PSMA表达增高。9月8日,PSA为2.17 ng/mL。12月20日,PSA为1.6 ng/mL;PSMA-SPECT/CT为前列腺癌治疗后,全身广泛骨转移同前,仍见PSMA表达增高;期间睾酮均处于去势水平。
该患者目前病情稳定,不良反应有血红蛋白水平降低(<110 g/L)、疲劳(可自行恢复),轻度丙氨酸转氨酶/天冬氨酸转氨酶升高(口服多烯磷脂酰胆碱胶囊后降至正常),总体耐受性良好。

图3 2018年3月28日PSMA-SPECT/CT图像
2 病例讨论泌尿外科:该患者为mHSPC,高转移负荷(STAMPEDE研究),高危(LATITUDE研究)。最近STAMPEDE研究发布的数据显示,对于寡转移(≤3处骨转移且无内脏转移)患者,加用局部治疗(手术或放射治疗)可带来显著获益(3年生存率为81%比73%,P=0.007),但对于高转移负荷患者,加用局部治疗并未带来获益(HR=1.07,P=0.42)[1]。因此,对于该患者的治疗不推荐加用局部手术,建议给予全身治疗。
肿瘤内科:该患者同时符合CHAARTED研究高转移负荷的定义,传统观点认为对于该类患者,初始采用ADT方案,当疾病进展至去势抵抗阶段再给予阿比特龙或多西他赛化学治疗。但近年来多项大型随机对照试验结果均表明,对于mHSPC患者早期联合阿比特龙治疗,以及对于高转移负荷的mHSPC患者早期联合多西他赛化学治疗,均能够带来显著的生存获益。其中,LATITUDE研究纳入了1 191例高危mHSPC患者(满足以下标准中至少2条:Gleason评分≥8分,至少有3处骨病变,存在可测量的内脏转移),随机分为ADT联合阿比特龙组和ADT联合安慰剂组,结果显示,ADT联合阿比特龙组患者的总生存期显著延长(未达到中位生存期比中位生存期34.7个月,HR=0.62,95%CI为0.51~0.76),影像学无进展生存期显著延长(33.0个月比14.8个月,HR=0.47,95%CI为0.39~0.55),PSA无进展生存期显著延长(33.2个月比7.4个月,HR=0.30,95%CI为0.26~0.35),并且在疼痛进展、有症状骨相关事件发生、推迟化学治疗应用方面均优于ADT联合安慰剂组[2]。此外,STAMPEDE研究同时纳入了1 917例高危和低危mHSPC患者,结果仍显示加用阿比特龙治疗可显著改善总体生存情况(3年生存率为83%比76%,HR=0.63,95%CI为0.52~0.76),并使治疗失败风险降低71%[3]。另有两项随机试验证实对高转移负荷患者予ADT联合早期多西他赛化学治疗能带来生存获益。CHAARTED研究纳入了790例mHSPC患者,随机分为ADT联合多西他赛组和ADT单药治疗组。结果显示,对于513例高转移负荷(存在内脏转移或4处以上骨转移,其中包括至少1处椎体外和骨盆外骨转移)患者,ADT联合多西他赛治疗者的总生存期显著延长(51个月比34个月,HR=0.63,95%CI为0.50~0.79);而对于277例低转移负荷患者,总生存期的差异无统计学意义(中位生存期64个月比未达到中位生存期,HR=1.04,95%CI为0.70~1.55)[4]。另一项多臂随机临床试验(STAMPEDE研究)的结果也显示,与单用ADT相比,联合多西他赛化学治疗带来显著生存获益(60个月比45个月,HR=0.76,95%CI为0.62~0.92)[5]。上述临床试验的结果改变了近年来mHSPC患者的治疗模式,但对于高转移负荷患者,优先选用ADT联合阿比特龙还是ADT联合多西他赛治疗,仍需进一步探索。参照国内外最新指南,对本例患者推荐ADT联合阿比特龙或ADT联合多西他赛治疗。
精准医学:Pritchard等[6]的研究结果显示,转移性前列腺癌患者中约11.8%的患者存在DNA修复基因的胚系突变,对于中国人群转移性前列腺癌, DNA修复基因胚系突变率约为9.68%[7]。虽然DNA修复基因的突变与肿瘤更强的侵袭性和不良预后有关,但既往研究[8-9]结果表明,携带DNA修复基因突变提示对PARP抑制剂和铂类化学治疗敏感。2015年的一项研究报道了16例携带DNA修复基因突变的去势抵抗性前列腺癌患者对奥拉帕利治疗的反应率达到88%(14/16)[9];2017年Pomerantz等[8]对141例患者的临床资料进行回顾性分析,结果显示携带致病性胚系BRCA2突变患者对于铂类化学治疗的反应率显著高于非突变患者(75%比17%,HR=58%,95%CI为27%~88%)。这些研究为DNA修复基因突变患者开拓了新的治疗策略,基于这些发现,目前NCCN指南和国内专家共识对于所有转移性前列腺癌患者均推荐进行基因检测[10]。
泌尿外科:根据上述多学科讨论意见,考虑本例患者年龄为45岁,年纪轻,预期生存时间长,综合考虑联合治疗带来的药物不良反应和可能的生存获益,推荐该患者入组PARP抑制剂临床试验,早期联合阿比特龙治疗,并严密管理患者治疗期间可能出现的不良反应。
3 结 语近年来,我国前列腺癌发病率呈显著上升趋势。据估计,2018年我国前列腺癌新发病例约99 322例,死亡病例约51 895例。科学诊治前列腺癌是提高我国前列腺癌患者生存率的关键。
转移性前列腺癌的治疗模式近年来已取得重大突破,给患者带来了更长的生存获益。初发转移患者早期联合治疗的理念愈加深入人心,PARP抑制剂的应用前景值得期待。然而,对于DNA修复基因突变人群的治疗模式,仍然存在困惑之处,有待进一步研究解答,如DNA修复基因突变人群从标准治疗路径中的获益似乎与非突变患者间存在差异。最近的一项纳入14例BRCA2胚系突变患者的前瞻性临床研究结果显示,BRCA2胚系突变患者进入去势抵抗阶段时一线治疗选择阿比特龙者的肿瘤特异性生存时间(CSS)显著长于一线治疗选择多西他赛者(33.2个月比17.4个月,P=0.027),但对于其他DNA修复基因突变,如BRCA1、ATM和PALB2,尚未观察到有统计学意义的差异[11]。既往针对DNA修复基因突变患者标准治疗获益的研究结论仍然存在争议。一项纳入22例DNA修复基因胚系突变患者的研究结果显示,突变患者对一线新型内分泌治疗(阿比特龙、恩杂鲁胺)的PSA无进展生存期显著短于非突变患者(3.3个月比6.2个月,P=0.01)[12]。随后一项回顾性研究纳入了9例BRCA/ATM胚系突变患者,结果显示突变患者一线内分泌治疗的PSA无进展生存期显著长于非突变患者(10.2个月比7.6个月,P=0.07)[13]。然而后续一项纳入60例DNA修复基因胚系突变患者的回顾性研究结果显示,突变患者对于新型内分泌治疗的无进展生存期与非突变患者相似(均为8.3个月)[14]。
不同研究结果的差异性与致病性突变的解读差异、致病性突变类型、样本量大小可能存在一定关联,目前多数患者在标准治疗均失效后才接受基因检测,而这些研究的数据提示,在临床实践中基因检测的时机或许需要进一步提前,DNA修复基因突变的早期检出有利于该类患者治疗路径的调整。当然,对于DNA修复基因突变患者,去势抵抗阶段一线治疗使用阿比特龙带来的生存获益是否显著优于多西他赛仍然需要在更多随机对照研究中证实。同时,PARP抑制剂早期联合阿比特龙或多西他赛治疗能否延长患者的总生存期也有待进一步探索。

