恩度联合含铂方案治疗晚期非小细胞肺癌疗效与不良反应观察
张莲兴 李志虎 韩霞 王佳 杨燕 张秋宁 侯文沛
摘 要 目的:探究恩度联合含铂方案治疗晚期非小细胞肺癌的疗效及不良反应。 方法:将110例采用恩度联合含铂方案治疗的晚期非小细胞肺癌患者作为研究组、单纯含铂方案治疗的30例晚期非小细胞肺癌患者作为对照组,对比两组近期疗效及不良反应。 结果:研究组患者近期疗效明显优于对照组、而不良反应显著低于对照组(P<0.05);不同性别、病理类型、恩度使用方式、化疗方案患者间的ORR和DCR比例比较无统计学差异(P>0.05)。结论:恩度联合含铂方案治疗晚期非小细胞肺癌的近期疗效较好,不良反应发生率低,值得临床推广使用。
关键词 晚期非小细胞肺癌 恩度 疗效 不良反应
中图分类号:R979.19; R730.59 文献标志码:A 文章编号:1006-1533(2019)07-0019-04
The efficacy and adverse reactions of endostar combined with cisplatin in the treatment of advanced non-small cell lung cancer*
ZHANG Lianxing**, LI Zhihu, HAN Xia, WANG Jia, YANG Yan***, ZHANG Qiuning, HOU Wenpei(Department of Gastroenterology, Gansu Cancer Hospital, Lanzhou 730050, China)
ABSTRACT Objective: To explore the curative effect and adverse reactions of anti-angiogenesis drug endostar combined with platinum regimen in the treatment of advanced non-small cell lung cancer. Methods: One hundred and ten cases of patients with advanced non-small cell lung cancer treated with endostar and platinum-containing regimen were designated as a study group and another 30 cases treated with single cisplatin as a control group. The short-term efficacy and adverse reactions were compared between the two groups. Results: The short-term efficacy was significantly better while the adverse reactions were significantly lower in the study group than the control group (P<0.05). The comparison of the overall response rate (ORR) and disease control rate (DCR) ratio in the different genders, pathological types, the methods for endostar use showed no significant differences (P>0.05). Conclusion: Endostar combined with cisplatin for the treatment of advanced non-small cell lung cancer has good short-term efficacy and low incidence of adverse reactions, which is worthy of further clinical practice.
KEY WORDS advanced non-small cell lung cancer; endostar; curative effect; adverse effects
非小細胞肺癌(non-small cell lung cancer,NSCLC),是最常见的恶性肿瘤之一,目前已成为我国恶性肿瘤死亡原因的第一位[1]。据统计,NSCLC约占肺癌比例的80%,其中可通过手术切除治疗的仅为20%~30%,局部晚期患者约为30%~40%,剩余的40%患者则已出现病灶转移[2]。因大部分NSCLC患者都是在中晚期才被发现诊断的,此时已不能进行手术切除,只能采用放疗和化疗的综合疗法来进行治疗。目前,晚期NSCLC的一线治疗方案为以铂类为基础的两药联合化疗,但尽管如此,晚期NSCLC的预后也难以令人满意,其5年总生存率(overall survival,OS)仅为1%~2%[3]。
恩度是我国学者自主创新研发的新型人血管内皮抑制素,能够通过改变血管内皮素的氨基酸序列来干扰内皮细胞和细胞外机制的相互作用,从而阻止肿瘤血管网的生成,抑制肿瘤的生长增殖[4],自2005年被批准用于NSCLC的治疗以来,目前已成为晚期NSCLC的一线治疗药物。尽管恩度在临床上的应用已有多年,但是其有效性和安全性仍需要更多长期的临床试验来加以证实。本研究对我院于2010年4月—2015年6月收治的140例晚期非小细胞肺癌患者展开回顾性研究,探究恩度联合含铂方案治疗NSCLC的近期疗效及不良反应,以期为恩度药物临床使用的安全性和有效性提供相应的数据支持。
1 材料与方法
1.1 病理性资料
将140例患者分成研究组110例和对照组30例。采用奇偶号的方式随机分组。研究组中有男性65例,女性45例,年龄40~72岁,平均年龄(45.1±7.3)岁。对照组中有男性20例,女性10例,年龄39~71岁,平均年龄(46.7±7.5)岁。所有患者入院时均进行病理学或细胞学确诊为晚期非小细胞肺癌,纳入标准如下:①体力状况良好,经由ECOG评分后分值为0~2分[4];②病情预计生存期在3个月及以上;③机体及主要脏器功能良好,符合化疗要求;④对生物制剂,尤其是大肠埃希菌的基因工程产品无过敏反应。排除严重感染、精神疾病难以配合化疗治疗的患者。本研究经本院医学伦理委员会批准,且所有受试者均自愿参与并签署知情同意书。
1.2 治疗方案
研究组患者均接受恩度与第三代含铂药物的联合方案治疗,在此基础上视患者具体病情选择不同的治疗药物:培美曲塞(AP)35例,多西他赛(DP)11例,吉西他滨(GP)47例,紫杉醇(TP)17例。恩度用药剂量为15 mg/次,将其加入500 ml生理盐水中缓慢静脉滴注3~4 h,持续14 d;或15 mg静脉泵持续滴注9 d。AP用药方案:培美曲塞500 mg/m2给药1 d+顺铂25 mg/m2给药3 d。DP用药方案:多西他赛75 mg/m2给药 1 d+顺铂25 mg/m2给药3 d。GP用药方案:吉西他滨1 000 mg/m2第1天和第8天给药+顺铂25 mg/m2给药3 d。TP用药方案:紫杉醇175 mg/m2给药1 d+顺铂25 mg/m2给药3 d。对照组患者均接受顺铂25 mg/m2给药3 d。以上方案,每3周为一个治疗周期,所有患者完成两个治疗周期后评价其近期疗效。为预防恩度呕吐的不良反应,观察组和对照组的所有患者治疗前均服用止吐药物。
1.3 评价指标
2个治疗周期后患者经CT检查评价其近期疗效。评价标准为实体瘤疗效评价标准1.1:①完全缓解(CR)原有病灶完全消失,无新病灶,情况持续4周以上;②部分缓解(PR) 病灶总长径之和减少30%以上,且情况持续4周以上;③疾病稳定(SD) 病灶总长径变化基于PR和PD之间;④疾病进展(PD) 病灶总长径之和增加20%以上,其相对值增加5 mm以上,或出现新病灶。总有效率(overall response rate,ORR)为CR+ PR患者数在总患者中所占的比例;疾病控制率(disease control rate,DCR)为CR+PR+SD患者在总患者中所占比例。该方案治疗NSCLC的不良反应根据WHO抗癌药物毒性反应标准分为Ⅰ~Ⅳ四型[5]。
1.4 统计学分析
所有数据应用SPSS 18.0 进行分析。采用t检验分析计量资料;采用χ2检验分析计数资料。P<0.05认为差异具有统计学意义。
2 结果
2.1 恩度联合含铂方案的近期疗效
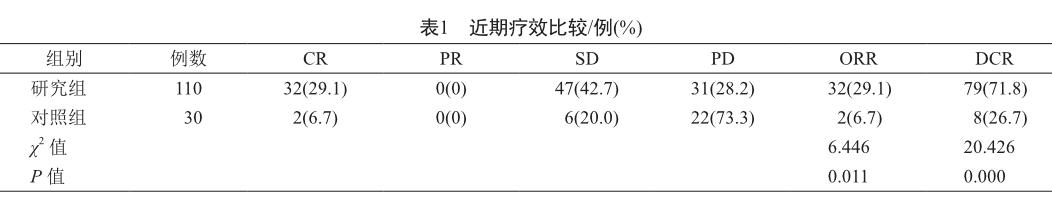
研究组治疗周期最长者为7个,最短者为2个,平均治疗周期为(4.1±2.9)周期;对照组治疗周期最长者为8个,最短者为2个,平均治疗周期为(4.2±2.9)周期,两组相比数据无统计学意义(t=0.167,P=0.867)。研究组晚期非小细胞肺癌患者ORR和DCR均明显优于对照组(P<0.05,表1)。
2.2 恩度联合含铂方案的近期疗效与临床病理特征之间的关系
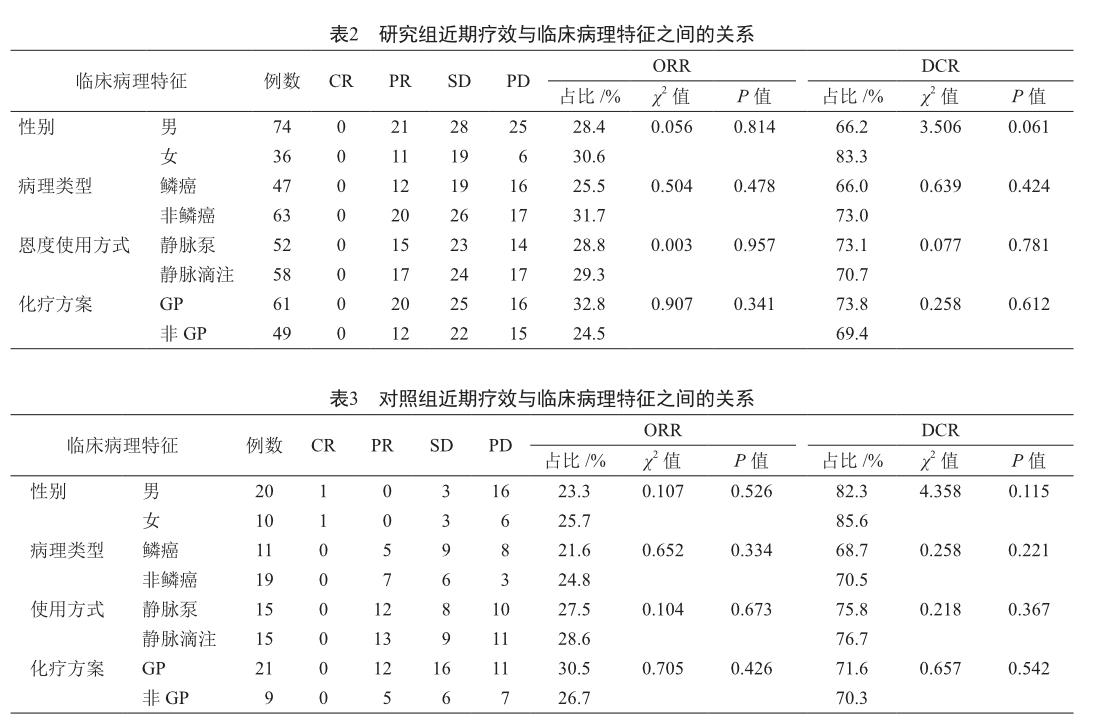
不同临床病理特征类型的患者间的ORR和DCR比较无统计学差异(P>0.05,表2、表3),单纯含铂方案治疗同样如此。
2.3 不良反应对比
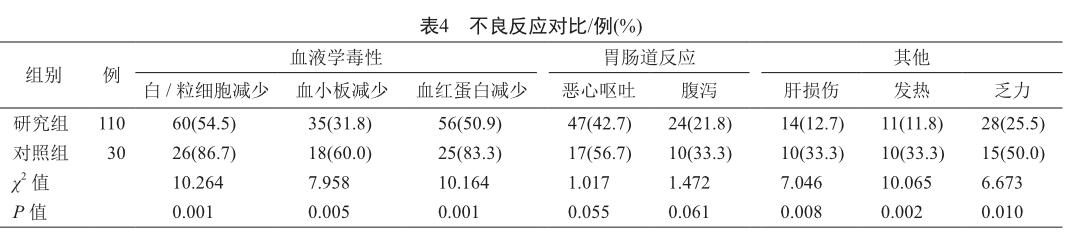
研究组晚期非小细胞肺癌患者不良反应显著低于对照组(P<0.05,表4)。
3 讨论
本次研究对接受2个治疗周期后的患者展开近期疗效评价,发现研究组近期疗效显著优于对照组。该结果与众多其他研究结果相近,说明恩度联合含铂方案治疗,相对于传统化疗药物,疗效更好。文献调研显示,研究组恩度联合含铂方案治疗的主要不良反应在于血液学毒性、胃肠道反应、皮疹和心脏毒性等[6-7]。在本研究中,研究組血液学毒性主要可以分为白/粒细胞减少、血小板减少和血红蛋白减少,发生率较高。胃肠道反应主要为恶心呕吐和腹泻。为避免呕吐反应,所有患者治疗前均服用了止吐药物,但仍有2例患者发生III级呕吐反应,因难以忍受改用其他药物,可见恩度的不良反应之强。此外,还有如肝损伤、乏力、发热等反应,但相对而言发生率较低。调查研究显示,恩度联合化疗与单用化疗的不良反应并无统计学差异[8]。本次研究发现,研究组不良反应发生率低于对照组。表明,恩度联合含铂方案可降低不良反应发生率,其具体药理研究仍需进一步探讨。本次研究中未见心脏毒性的例子,根据其他研究显示恩度的心脏毒副反应发生率较低[9],且易发于既往有冠心病、高血压病史者,因此在收治此类患者时需对其心脏功能多加注意。有研究显示[10],静脉泵持续给药可以通过调整参数,来使血浆药物浓度持续上升直至药物消除速度与给药速度相等,从而稳定相对稳定的血浆药物浓度,副反应更少。在本次研究中,静脉泵给药仅需9 d,而传统静脉滴注却需14 d,两者疗效并无差异,且前者更经济节约。因此从临床应用而言,静脉泵持续给药相较于常规静脉滴注,不仅携带方便,而且输注时间更短,药物用量更少,更经济实惠,更具推广性。
综上所述,抗血管生成药物恩度联合含铂方案治疗晚期非小细胞肺癌,相较于传统化疗,近期疗效较好,不良反应发生率较高但仍处于可控范围内可耐受,适合临床进一步实践。本次研究仍存在较多不足之处,如样本量较小,未分析远期疗效,属于回顾性研究非随机对照,化疗方案不统一等等。因此若要明确恩度治疗NSCLC的具体疗效和不良反应,仍需进一步的研究。
参考文献
[1] 徐继平, 陈奕霖, 杨卫兵, 等. 两种剂量恩度联合顺铂灌注治疗非小细胞肺癌恶性胸腔积液疗效对比[J]. 医学与哲学, 2015, 36(24): 21-24.
[2] McGowan M, Kleinberg L, Halvorsen AR, et al. NSCLC depend upon YAP expression and nuclear localization after acquiring resistance to EGFR inhibitors[J]. Genes Cancer, 2017, 8(3-4): 497-504.
[3] 王嵐, 刘畅, 巩传凤, 等. 调强放疗联合紫杉醇及恩度治疗老年局部晚期非小细胞肺癌的临床疗效[J]. 中国老年学杂志, 2014, 12(24): 6913-6915.
[4] 任柏沉, 李燕宏, 孙建, 等. 化疗联合恩度治疗ERCC1阳性晚期 NSCLC的临床疗效[J]. 重庆医学, 2015, 13(18): 2504-2505, 2508.
[5] Herbst RS, Heymach JV, OReilly MS, et al. Vandetanib(ZD6474): an orally available receptor tyrosine kinase inhibitor that selectively targets pathways critical for tumor growth and angiogenesis[J]. Expert Opin Investig Drugs, 2007, 16(2): 239-249.
[6] Manzo A, Carillio G, Montanino A, et al. Focus on nintedanib in NSCLC and other tumors[J/OL]. Front Med (Lausanne), 2016, 3: 68. doi: 10.3389/fmed.2016.00068.
[7] Lischalk JW, Woo SM, Kataria S, et al. Long-term outcomes of stereotactic body radiation therapy (SBRT) with fiducial tracking for inoperable stage I non-small cell lung cancer(NSCLC)[J]. J Radiat Oncol, 2016, 5(4): 379-387.
[8] 汪力慧. 恩度联合化疗与单纯应用化疗治疗晚期非小细胞肺癌的疗效比较[J]. 中国老年学杂志, 2013, 33(6): 1384-1385.
[9] 刘维, 哈敏文, 殷南昌, 等. 恩度联合顺铂胸腔内注射治疗非小细胞肺癌恶性胸腔积液临床研究[J]. 山东医药, 2010, 50(8): 79-80.
[10] Hall RD, Le TM, Haggstrom DE, et al. Angiogenesis inhibition as a therapeutic strategy in non-small cell lung cancer (NSCLC)[J]. Transl Lung Cancer Res, 2015, 4(5): 515-523.

