基于水滑石的全蛋液中磷吸附与解吸及动力学模型研究
迟玉杰 何 晶 赵 英 马艳秋 安瑞琪
(1.东北农业大学食品学院, 哈尔滨 150030; 2.东北农业大学农学院, 哈尔滨 150030)
0 引言
肾脏是人体内磷代谢的重要场所,当其发生病变时,机体就会出现磷代谢紊乱,并伴随许多并发症[1]。慢性肾脏病(Chronic kidncy discase, CKD)高磷血症是世界上高发病率和高死亡率的疾病之一,国外有46.7%的肾病患者存在高磷血症,国内情况更为严重,发生率高达81%[2-4]。目前,患者主要依靠透析和药物治疗维持机体的磷代谢水平,其专用饮食较为短缺,肾病患者饮食既需要优质蛋白质,又同时要求磷含量较低,磷/蛋白质(Phosphorus/Protein, P/Pro)质量比值要求控制在10~12 mg/g范围内[5-6],要求日常膳食磷的摄入量为3.3~16.0 mg/(100 kJ),透析治疗后磷的摄入量为6.0~16.0 mg/(100 kJ)[7]。全蛋液营养全面且丰富,其蛋白质生物价高达100,易被人体吸收[8-10],是患者优选的蛋白来源。全蛋液中磷质量浓度为2 268~2 289 mg/L,P/Pro质量比值为16.15~19.09 mg/g[11],基于肾病患者低磷饮食的需求,需进行全蛋液脱磷技术的开发,制备适于肾病患者的专用型食品配料。
目前,关于磷酸基团的去除方法已有一定的研究,主要包括酶法、超滤膜、离子交换树脂及吸附法等[12-16]。其中,采用吸附剂进行磷的去除易于工业化生产,是一种方便、快速的加工方式。水滑石(Layered double hydroxide, LDH)是一种常见的用于吸附磷酸盐离子的材料[17],其由带正电荷的主体层板和层间阴离子通过非共价键相互作用组装而成,层间阴离子可与各种阴离子,包括无机离子、有机离子、杂多酸离子以及配位化合物的阴离子进行交换[18]。本实验采用的吸附剂为Mg-Al LDH,是一种典型的天然矿物,其层板由镁八面体和铝氧八面体组成,具有较强的碱性[19]。相比其他吸附剂,LDH对阴离子如磷酸根离子具有吸附效率高、无二次污染及价格低廉等优点,且在高温焙烧时具有记忆效应,高温形成的无定形物可以通过水合重构结构,利于进行循环使用[20]。LDH是一种碱性材料,已广泛应用于医药和食品行业,且已作为胃药成分被收入英国药典[20]。LDH在药物缓释方面已有大量研究[20-23]。同时,利用LDH制备的食品包材具有良好的抗菌特性,可有效延长食品货架期[23]。目前,采用LDH进行磷吸附已具备一定的研究基础,学者们进行了不同层次吸附机理的探究。贾云生等[24]采用Ca-Al LDH进行磷吸附,吸附规律符合Langmuir 吸附等温方程,吸附动力学过程符合准二级动力学方程。FROST等[25]则研究了LDH吸附磷的机理,研究表明,热处理可以提高LDH对磷的吸附效率,同时层间阴离子的组成受pH值影响较大,且碱性条件下吸附较高价态的磷酸根离子。
本文通过吸附等温线、吸附动力学、吸附热力学表征LDH除磷机理,测定吸附过程中全蛋液蛋白质溶解度的变化及氨基酸含量变化,分析LDH进行全蛋液磷吸附的适用性。同时基于绿色、经济的实验原则,对LDH进行循环利用。
1 材料与方法
1.1 原料与仪器
新鲜鸡蛋,市售;Mg-Al LDH,邵阳天堂助剂化工有限公司;磷酸二氢钾标准品,纯度99.99%以上,上海阿拉丁生化科技股份有限公司;邻苯二酚、钼酸铵、亚硫酸钠、硫酸铜、氯化钠、氢氧化钠、盐酸及硫酸等均为国产分析纯。
KSW-5-12A型马弗炉,天津市中环实验电炉有限公司;日立L-8800型氨基酸自动分析仪,日本日立公司;TU-1810型紫外可见分光光度计,北京普析通用仪器有限责任公司;SHA-B型水浴恒温振荡器,常州亿通分析仪器制造有限公司;高速台式冷冻离心机,上海安亭科学仪器厂。
1.2 样品的制备
将新鲜鸡蛋经清洗、打蛋,转速135 r/min下搅拌至均匀,采用尼龙网纱(筛分粒度100目)过滤系带等杂质得到全蛋液。加入0.20 mol/L NaOH溶液,40℃搅拌(135 r/min)1.5 h,冷却恢复至室温(20℃)后采用0.10 mol/L HCl溶液调节pH值至8.5。按国家标准进行全蛋液中磷含量的测定[26],样品磷质量浓度为2 200 mg/L。采用去离子水稀释全蛋液样品,制备一系列磷质量浓度梯度的全蛋液,分别为25、50、75、100、125、150 mg/L。
1.3 LDH吸附实验
参照SHIN等[27]的方法,取稀释全蛋液100 mL至锥形瓶中,分别加入2.5、5.0、7.5、10.0、12.5、15.0 g/L的LDH,吸附温度为20、25、30、35、40、45℃,吸附时间为0、1、2、3、4、5、6、7 h,搅拌(转速135 r/min)吸附后采用尼龙网纱(筛分粒度300目)过滤混合物,并分别收集全蛋液样品和LDH,测定全蛋液中磷含量及蛋白质溶解度,LDH对全蛋液中磷的吸附量以及蛋白质溶解度[28]计算公式为
Qt=(C0-Ci)V0/m
(1)
式中Qt——t时刻吸附量,mg/g
C0——吸附初始吸附质的质量浓度,mg/L
Ci——吸附后吸附质的质量浓度,mg/L
V0——样品初始体积,L
m——吸附剂质量,g
(2)
式中S——蛋白质溶解度,%
P——样品中总蛋白质质量,g
P1——上清液中蛋白质质量,g
1.4 吸附等温式
Langmuir吸附等温式的前提条件是吸附表面均匀并且为单分子层,其线性表达式为
(3)
式中Ce——吸附质的平衡质量浓度,mg/L
Qe——吸附剂的实验平衡吸附量,mg/g
Qm——最大吸附量,mg/g
b——Langmuir常数,L/mg
Langmuir吸附等温式重要的平衡参数为RL,定义为
(4)
Freundlich吸附等温式应用于非均匀吸附剂的多层吸附,其线性表达式为
(5)
式中KF——吸附能力Freundlich常数
n——吸附强度Freundlich常数
1.5 吸附动力学及热力学模型
准一级动力学模型即Lagergren一级动力学模型,用于研究液相-固相体系的吸附过程,公式为
ln(Qe-Qt)=lnQe-tK1
(6)
式中t——吸附时间,min
K1——准一级动力学模型常数,min-1
准二级动力学模型由HO和MCKAY提出[29],方程线性化后为
(7)
式中K2——准二级动力学模型常数,g/(mg·min)
热力学参数是吸附过程实际应用中的重要指标,包括Gibbs自由能变(ΔG)、焓变(ΔH)和熵变(ΔS)。
ΔG=ΔH-TΔS
(8)
ΔG=ΔH-RTlnK
(9)
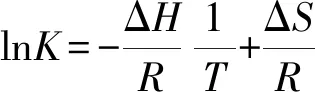
(10)
(11)
式中 ΔG——吸附自由能变,kJ/mol
ΔH——吸附焓变,kJ/mol
ΔS——吸附熵变,J/(mol·K)
R——摩尔气体常数,取8.314 J/(mol·K)
T——热力学温度,K
K——固液分配系数
1.6 LDH的解吸及重复利用
1.6.1解吸实验
将吸附后分离得到的LDH,在室温下利用0.6 mol/L的NaCl进行解吸,液料比(解吸液体积与LDH质量比)分别为0.25、0.50、0.75、1.00、1.25、1.50 L/g,解吸时间为1~8 h,解吸率计算公式为
(12)
式中Rd——解吸率,%
Cd——解吸液中吸附质的质量浓度,mg/L
Vd——解吸液的体积,L
Qd——吸附-解吸平衡的吸附量,mg/g
1.6.2重复利用
经过NaCl解吸后的LDH进行500℃焙烧4 h,冷却后使用[19],其添加量为7.5 g/L,吸附时间5 h,全蛋液磷初始质量浓度125 mg/L,吸附温度30℃,pH值8.5。按式(1)计算Qt。
1.7 氨基酸含量测定
精确称取10 mL全蛋液/脱磷全蛋液,参照WANG等[9]方法测定蛋液中各氨基酸含量。
1.8 数据处理
实验中所有结果都是3次测定的平均值,计算标准偏差,采用SPSS 19.0进行显著性分析。采用Origin 8.6软件对数据进行分析与制图,模型拟合采用Curve Expert 32软件。
2 结果与分析
2.1 LDH吸附时间对吸附量及溶解度的影响
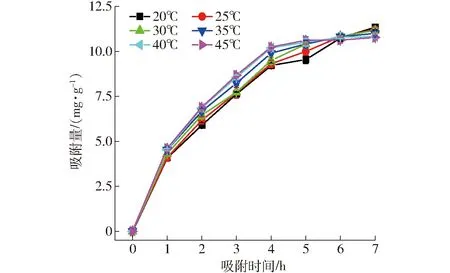
图1 LDH吸附时间对全蛋液中磷吸附量的影响Fig.1 Effect of LDH adsorption time on quantity of adsorption of phosphate in whole egg liquid

图2 LDH吸附时间对全蛋液溶解度的影响Fig.2 Effect of LDH adsorption time on solubility in whole egg liquid
图1、2分别为温度20~45℃范围内,不同吸附时间(1~7 h)LDH对吸附量及溶解度影响结果。由图1可知,随着吸附时间的增加,LDH的吸附量逐渐增加(P<0.05),实验中LDH对全蛋液中磷的最大吸附量超过10 mg/g。SHIN等[27]的研究中也采用LDH进行磷的吸附,研究得到相同的吸附趋势,随着吸附时间的增加吸附效果逐渐提高。本实验中5~7 h吸附时间内的吸附量曲线交叉重叠较多,吸附时间达到6 h时,40℃和45℃的吸附趋于饱和。LI等[30]的研究中采用天然磁黄铁矿进行磷的吸附,得到了与本实验相似的结论,较长时间吸附后增长率降低,吸附接近饱和。同时,实验中发现LDH吸附前6 h内较高温度吸附量较大,而6 h后较低温度的吸附量超过较高温度的吸附。这可能是由于在吸附初期,温度越高,分子运动越快,吸附强度也越大(P<0.05)。而长时间吸附后,热处理的蛋液发生凝固现象[31-34],严重影响吸附剂与吸附质的接触,且温度越高热凝固的影响越大。吸附6 h后各温度下吸附量数值接近,差异不显著(P>0.05)。
不同温度下,利用LDH进行全蛋液中磷的吸附,溶解度呈下降趋势(P<0.05),且各温度吸附的下降趋势相似,较低温度吸附时溶解度始终高于高温吸附(P<0.05),这也与全蛋液的热凝固密切相关。蛋白质受热后形成网状交联结构,甚至出现不溶性热聚合体,导致溶解度下降[35]。AMR等[36]研究了热处理对溶解度的影响,升高20℃溶解度损失13%。本实验中温度升高20℃后,溶解度损失不超过10%。这主要是由于全蛋液含水率高于AMR的实验,在一定程度上较高的含水率利于蛋白质稳定存在于体系中,宏观表现为溶解度较高。
2.2 初始质量浓度对吸附量及溶解度的影响
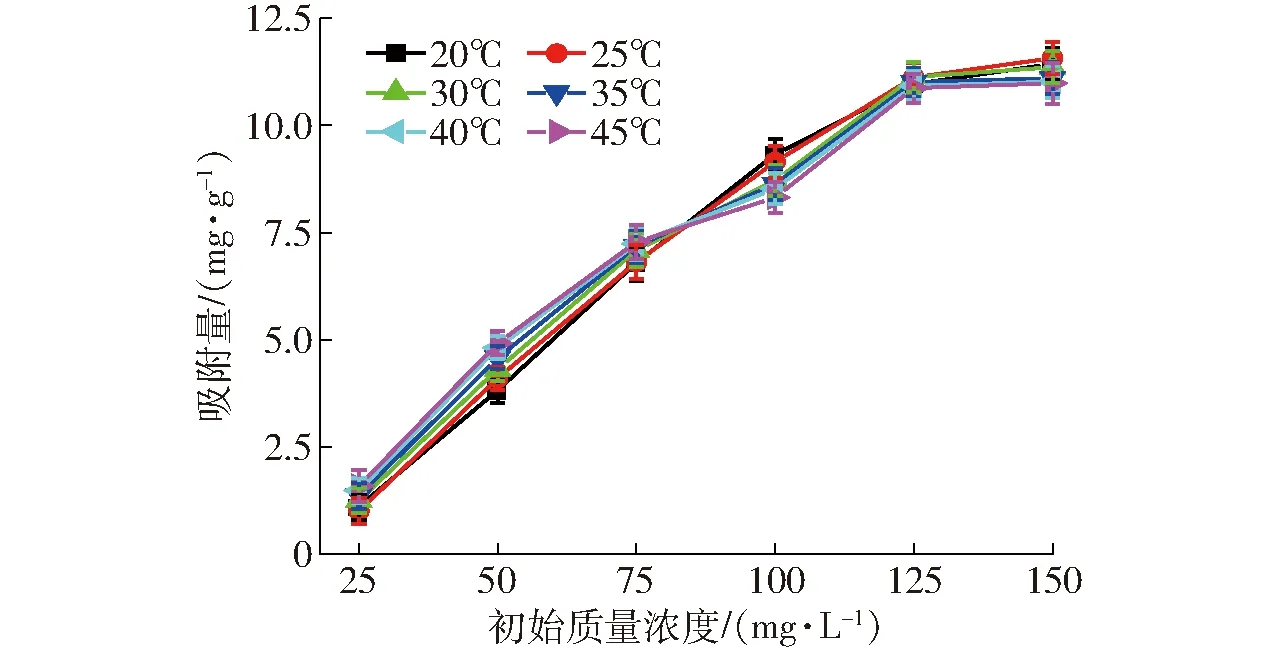
图3 磷的初始质量浓度对LDH吸附量的影响Fig.3 Effect of initial concentration of phosphate on its quantity of adsorption of LDH adsorption

图4 磷的初始质量浓度对全蛋液溶解度的影响Fig.4 Effect of initial concentration of phosphate on solubility in whole egg liquid
通过去离子水稀释得到一系列磷质量浓度梯度的全蛋液,分别为25、50、75、100、125、150 mg/L。图3、4分别为全蛋液中磷的初始质量浓度对LDH吸附量和溶解度的影响,较低初始质量浓度时,LDH分散性好,温度高的全蛋液中磷的吸附效果相对较好,但各温度下吸附量差异不显著(P>0.05)。当初始质量浓度达到75 mg/L后,较低温度(20、25、30℃)的吸附量高于较高温度吸附量(35、40、45℃)。初始质量浓度超过125 mg/L后,较高温度的吸附增长率显著降低,吸附趋于平衡,而相对低温的吸附仍具有较高的增长率。这主要是与蛋液的耐热性有关,全蛋液浓度较高时易造成热聚集,稀释的蛋液热聚集程度相对较低[31]。随着蛋液中磷质量浓度的增加,LDH对磷的吸附量逐渐增大(P<0.05)。在YAO等[37]的研究中采用红色和灰色陶瓷黏土进行磷吸附,认为磷的初始质量浓度、吸附温度、吸附量三者间的相关性较强。而本实验中磷初始质量浓度对吸附影响显著,而温度对吸附量影响较弱。这可能是由于实验所用材料的不同,本实验采用的LDH具有热稳定性,而YAO等[37]的研究中采用的陶瓷黏土更易受温度影响。在SARKAR等[38]的研究中发现吸附浓度对吸附的影响程度较弱,这可能与吸附质性质有关,SARKAR等研究中吸附质为酚类有机物(如苯酚、1,2-二羟基苯、1,3-二羟基苯和1-羟基-4-硝基苯),所带电荷小于本实验中的吸附质磷。吸附质所带电荷越高,吸附强度越大[13]。从图4可知,溶解度受磷初始质量浓度的影响显著(P<0.05),均为逐渐增加的趋势。同时,磷的初始质量浓度越小溶解度越低,这是由于过度稀释蛋液会造成蛋白质水合膜的破坏,蛋白质可溶性降低[31]。溶解度的变化与图2结果接近,且温度较低时全蛋液中溶解度较高(P<0.05)。
2.3 LDH添加量对吸附量及溶解度的影响
图5、6分别为LDH的添加量对全蛋液中磷的吸附量和溶解度的影响,随着添加量的增加,LDH对全蛋液中磷的吸附量先增加后降低,溶解度逐渐降低。当LDH的添加量在2.5~10 g/L范围内,温度对LDH吸附效果影响显著(P<0.05),且吸附温度越高其磷酸根吸附量越高。当添加量为10 g/L时,各温度下磷的吸附量均达到最高值。LDH的添加量超过10 g/L后,其对全蛋液中磷的吸附量显著下降,但此时温度对吸附效果影响不显著,各温度下LDH的吸附量无明显差异(P>0.05)。这可能是由于当添加量较大时,造成LDH的聚集现象,减小了吸附质与LDH的接触面积,降低其吸附效果。实验中发现添加量达到10 g/L时,出现结块现象,需通过搅拌辅助其分散于全蛋液体系中。陈蘅莉等[16]也研究了吸附剂添加量对吸附量的影响,其研究也表明添加量较大时,可得到较好的吸附效果。本实验还研究了全蛋液中溶解度的变化,LDH添加量对溶解度的影响与图2结果相似,随着添加量的增加溶解度逐渐下降。这可能是大量的LDH加入到全蛋液中,会造成全蛋液体系黏度增加,随着搅拌的进行,全蛋液中蛋白质等组分形成絮状物,可溶性降低[39]。与图2、4结论相似,温度对全蛋液中溶解度影响显著(P<0.05),温度较低时全蛋液中溶解度相对较高。
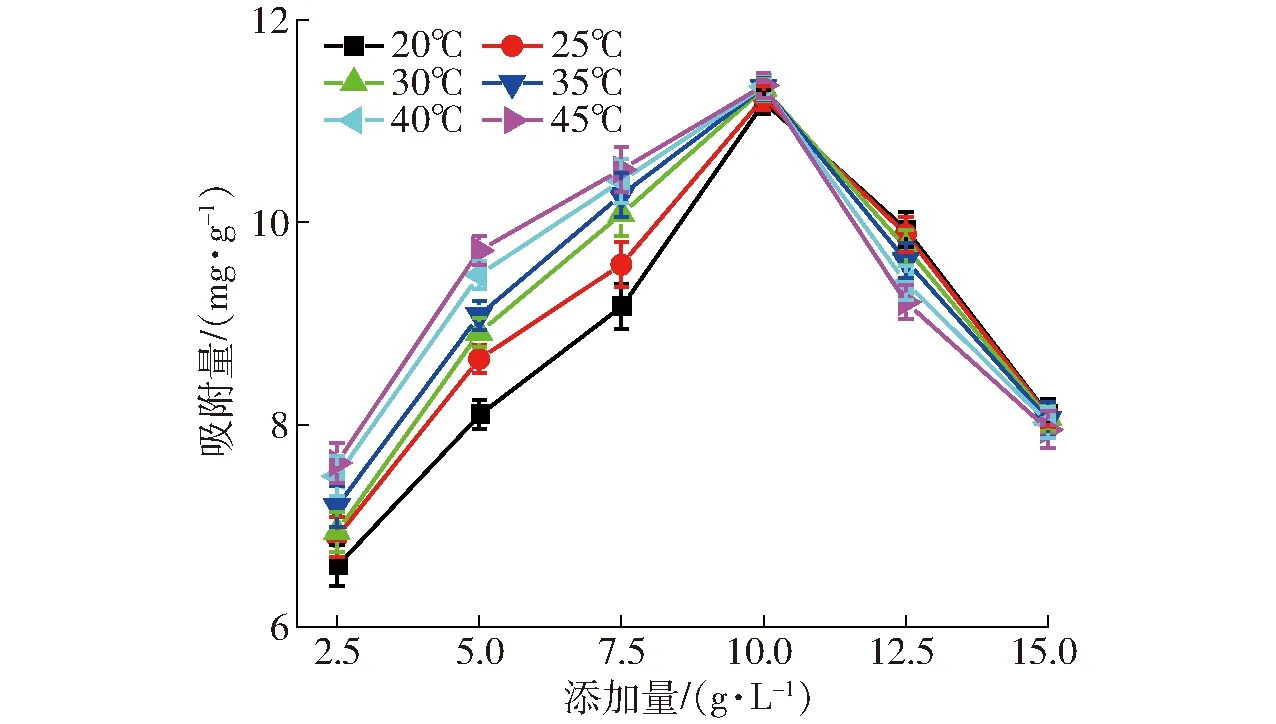
图5 LDH添加量对全蛋液中磷吸附量的影响Fig.5 Effect of LDH addition on quantity of adsorption of phosphate in whole egg liquid
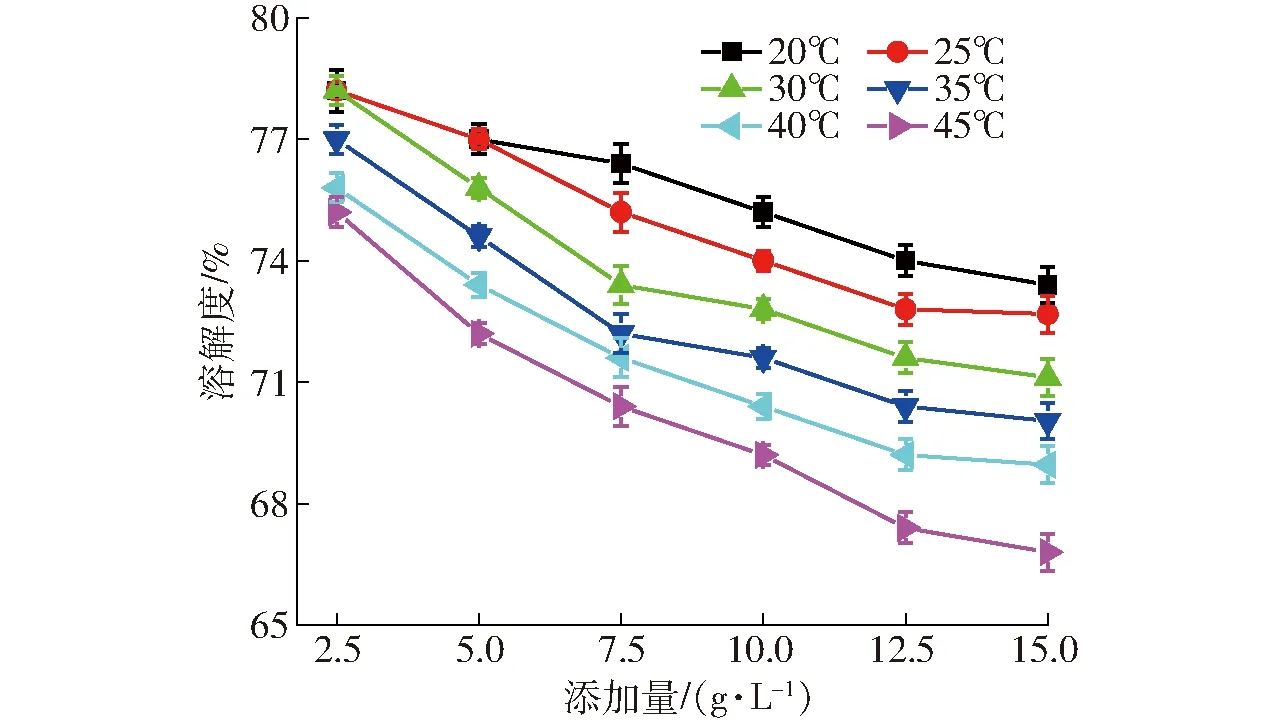
图6 LDH添加量对全蛋液溶解度的影响Fig.6 Effect of LDH addition on solubility in whole egg liquid
2.4 LDH吸附等温式、吸附热力学及吸附动力学
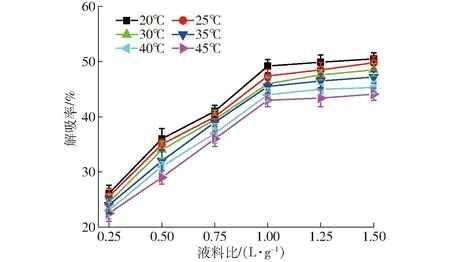
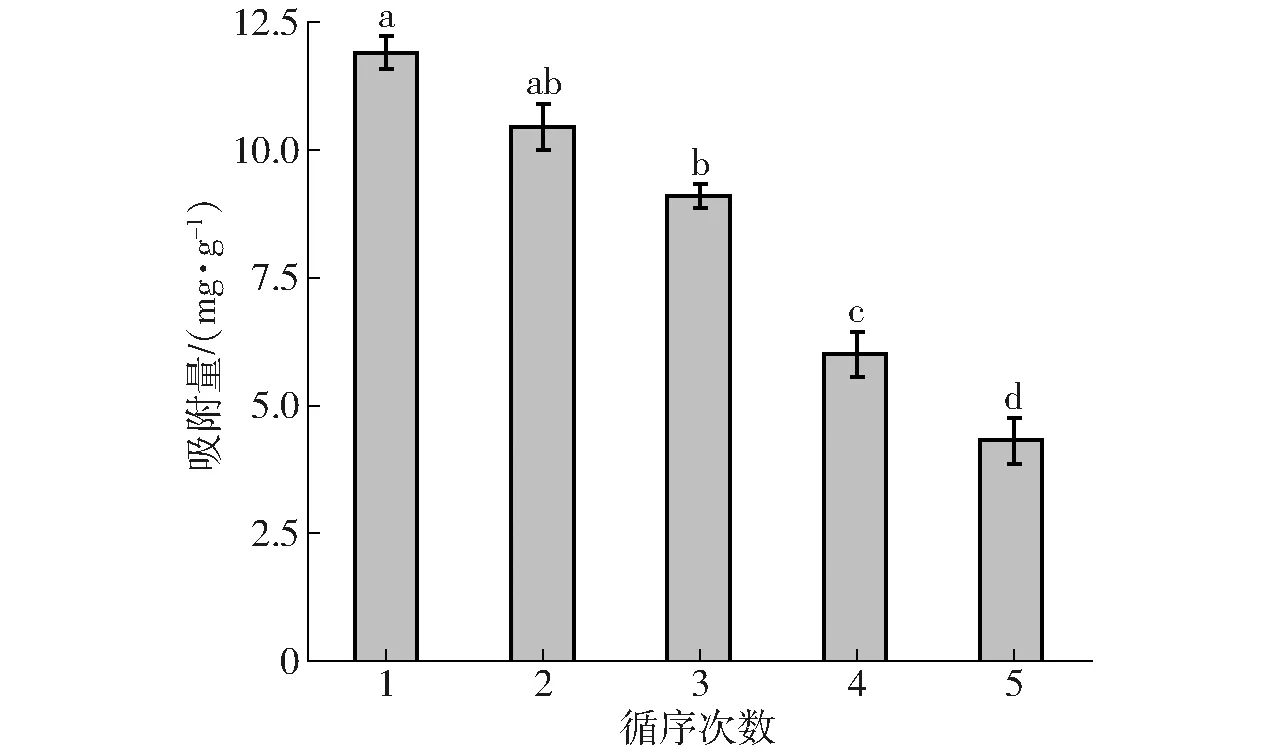
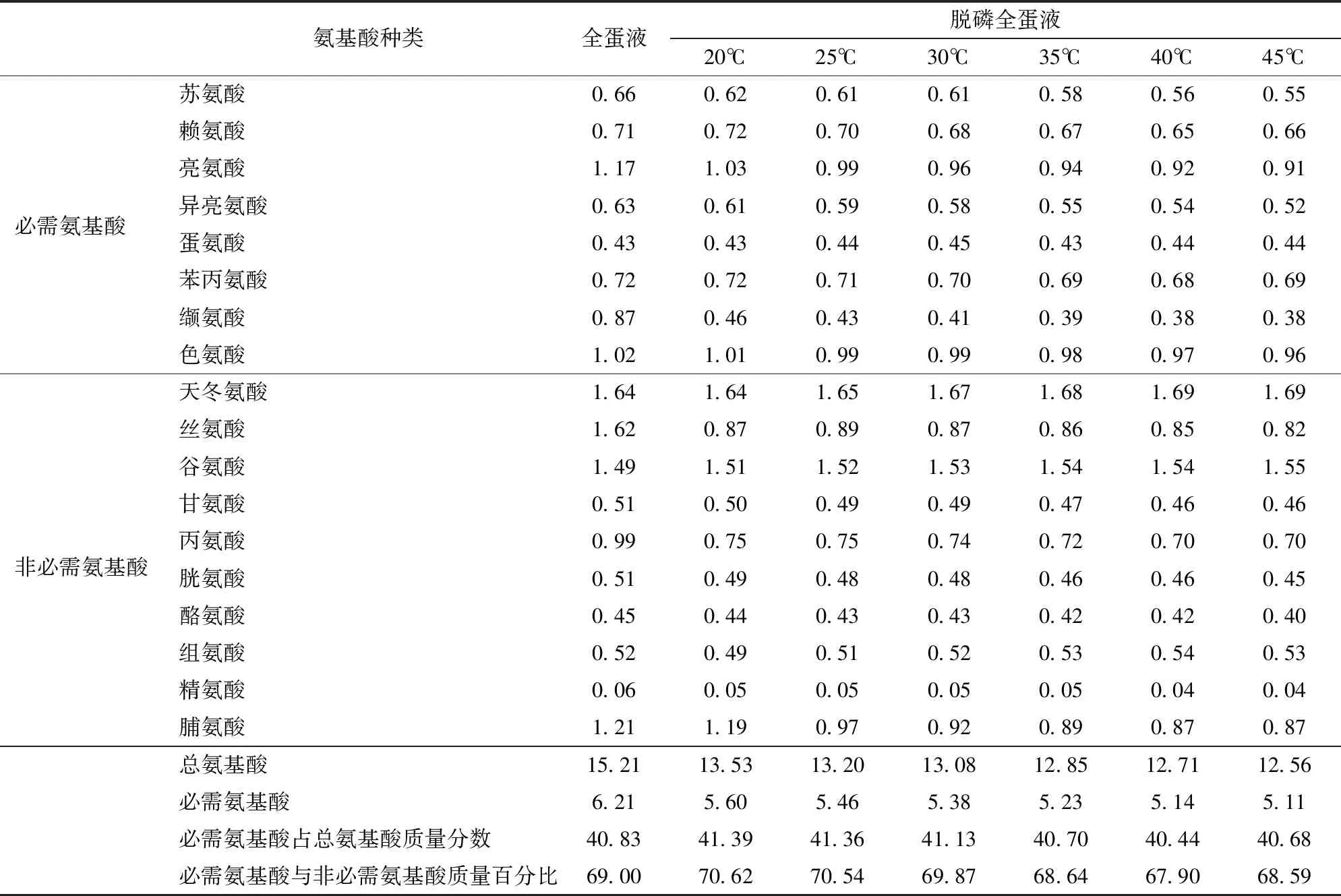
Langmuir吸附等温式的前提条件是吸附表面均匀并且为单分子层,而Freundlich吸附等温式应用于非均匀吸附剂的多层吸附[40]。Langmuir吸附等温式中根据RL的值判断吸附过程是否良好,0 图7、8为LDH解吸实验结果,由实验数据可知吸附温度对NaCl解吸磷的影响显著(P<0.05),吸附温度越低,LDH上吸附的磷的解吸效果越好,具有更大的解吸率。这是由于较低温度吸附时,磷与LDH结合方式主要为物理结合,磷吸附于LDH层板表面,结合力较低,易于解吸。吸附温度越高,化学吸附程度越大,磷与LDH层间镁离子、铝离子的结合越多,解吸难度增大。图7中随着解吸时间的增加,磷酸根解吸率逐渐增加(P<0.05),解吸5 h后解吸率增长缓慢。李克超等[47]采用LDH对棉酚进行解吸的研究中,解吸时间长达12 h。本实验达到解吸最大的时间相对较短,这可能与吸附质的性质有关。相对于棉酚,磷离子更易于被NaCl溶液解吸。通过李克超的研究可知棉酚在解吸的同时发生降解,重新吸附于LDH表面,所以需要更长的解吸时间。如图8所示,随着解吸液的增加,解吸率逐渐增加(P<0.05),各温度下初始增长呈线性,吸附温度对解吸率影响显著(P<0.05),温度越低解吸效果越好。当液料比超过1.00 L/g后解吸率增长缓慢。此时,LDH中结合较弱的磷都已脱除,继续增加解吸液用量,不能达到很好的解吸效果又会造成试剂的浪费。因此,最佳的解吸条件为:1 g LDH采用1 L NaCl解吸液进行磷解吸,解吸时间为5 h。 表1 LDH对全蛋液中磷的吸附等温式及热力学参数Tab.1 Adsorption isotherm and thermodynamic parameters of phosphorus in whole egg liquid by LDH 表2 LDH对全蛋液中磷的吸附动力学模型参数Tab.2 Adsorption kinetic model parameters of phosphate in whole egg liquid by LDH 图7 LDH解吸时间对磷解吸率的影响Fig.7 Effect of desorption time of LDH on rate of desorption of phosphate 图8 液料比对磷解吸率的影响Fig.8 Effect of ratio of desorption liquid to LDH on rate of desorption of phosphate 图9 LDH循环次数对全蛋液中磷吸附量的影响Fig.9 Effect of cycle times of LDH on quantity of adsorption of phosphate in whole egg liquid 为探究LDH的可再生性,对LDH进行循环使用,经过NaCl解吸后的LDH进行500℃焙烧4 h,冷却后使用。焙烧温度为500℃时,可以将影响磷酸根吸附的层间阴离子释放出来,增加材料的比表面积,同时焙烧产物与水混合后可以恢复原有结构[19]。将LDH焙烧产物应用于全蛋液吸附实验中,其对磷的吸附效果如图9所示。随着使用次数的增加,LDH对磷的吸附量逐渐降低。前2次对磷的吸附量差异不显著,第3次使用时降低为10 mg/g以下,在第4次和第5次使用时吸附量降低到6 mg/g以下。在循环使用中,采用高温处理水滑石,LDH片层发生断裂、移位和重排[17],形成大量微孔结构,利于物理吸附的进行。相似地,殷实等[48]研究中采用微波预处理和传统焙烧加热相结合的方式处理生物炭,形成丰富的微孔和介孔,形成了多级孔道结构。本实验进行多次循环使用时,LDH表面的吸附位点被占用,对阴离子磷的吸附效果降低。目前,关于吸附剂循环使用的研究较少,李克超等[47]对LDH进行了循环利用,在前3次吸附棉酚的效果较好。一定次数的循环使用,可以较大程度地发挥吸附剂的吸附作用。本实验中LDH最佳使用次数为2次,使用3次也基本满足吸附要求。 鸡蛋中氨基酸含量丰富,且蛋白模式与人体的蛋白模式相似,可以被人体全面吸收[49]。实验中测定了各温度下(20~45℃)磷吸附处理对全蛋液中氨基酸的影响,进而研究脱磷对蛋白质营养性的影响,如表3所示。实验结果表明氨基酸中丝氨酸含量有一定程度的降低,这是由于鸡蛋蛋白质中含有高度磷酸化的丝氨酸,特别是Ser128~Ser141之间,有14个丝氨酸残基连续排列[50]。王芳[13]的研究中得到了相同的结论,鸡蛋蛋白质脱除的磷主要来自于丝氨酸,脱磷对侧链含磷酸基团的氨基酸影响显著。根据FAO/WHO提出的优蛋白质组成条件,8种必需氨基酸占总氨基酸质量分数应在40%以上,必需氨基酸与非必需氨基酸质量百分比应超过60%。由表3可知,采用LDH进行磷吸附后全蛋液中必需氨基酸占总氨基酸质量分数始终大于40%,必需氨基酸与非必需氨基酸质量百分比也一直高于60%,表明LDH脱磷对全蛋液中蛋白质营养性的影响较小,这也对应了图2、4、6中溶解度的结果。综上可知,采用LDH进行脱磷的同时可以保持全蛋液中蛋白质的营养性,适用于低磷液蛋制品的开发。 表3 全蛋液及脱磷全蛋液的氨基酸质量分数Tab.3 Analysis of amino acids in whole egg liquid and dephosphorization whole egg liquid % (1)采用LDH进行全蛋液中磷的吸附,最佳吸附条件为:吸附时间6 h,磷初始质量浓度125 mg/L,LDH添加量10 g/L。 (2)实验中LDH的最大吸附量超过10 mg/g,同时溶解度下降幅度在10%以内;Langmuir等温式、Freundlich等温式、准一级动力学和准二级动力学模型均可表征LDH对磷的吸附,Langmuir等温式和准二级动力学模型拟合度较高,尤其在25℃和30℃吸附温度时拟合效果最佳。 (3)ΔS为31.38 J/(mol·K),ΔH为4.50 kJ/mol,ΔG小于-9 kJ/mol,在温度20~45℃范围下均能自发反应且为吸热反应。 (4)解吸实验中,最佳条件为解吸时间5 h,液料比为1.00 L/g。循环利用时,LDH最佳使用次数为2次。 (5)脱磷后全蛋液必需氨基酸占总氨基酸的质量分数大于40%,必需氨基酸与非必需氨基酸的质量百分比大于60%,LDH脱磷对蛋白质营养性的影响较小。 (6)LDH适用于全蛋液中磷的去除,其对磷的吸附效果良好且可保持蛋白质的营养性,吸附过程简单又可以进行重复使用,有利于低磷全蛋液的工业化开发。2.5 LDH的解吸特性



2.6 LDH的循环使用
2.7 对氨基酸含量的影响
3 结论

