RRLC-MS/MS同时测定食品接触材料中9种双酚类化合物迁移量
熊小婷,王继才,王海洋,黄日林,陈意光,李燕飞,谭建华,李慧勇,席绍峰
(广州质量监督检测研究院,国家包装产品质量监督检验中心(广州),广东 广州 511447)
世界各地食品安全事件频发,原因之一是食品接触材料中的化学污染物在一定条件下向食品内容物迁移而造成污染,因此,建立食品接触材料中化学污染物迁移量的检测方法具有重要意义。
双酚类化合物含有2个酚羟基,是重要的化工产品,可在环氧树脂、聚碳酸酯、酚醛树脂等高分子材料的合成中作为原料或稳定剂、促进剂等使用,也可用作阻燃剂。双酚A(bisphenol A, BPA)是目前全球范围内生产和使用量最大的双酚类化合物,“毒奶瓶”事件后,BPA受到高度关注,一些国家和组织相继出台法规限制BPA在食品接触材料中的使用,其中,欧盟法规(EU)No 10/2011[1]和我国国家标准GB 9685—2016[2]中均规定BPA在食品接触材料及制品中的特定迁移限量为0.6 mg/kg。BPA的使用受限后,一些与BPA相似结构的双酚类化合物开始作为其替代品使用,使用较多的是双酚F(bisphenol F, BPF)和双酚S(bisphenol S, BPS)。目前已有研究表明,BPA、BPF、BPS、双酚B(bisphenol B, BPB)、双酚E(bisphenol E, BPE)、四溴双酚A(tetrabromobisphenol A, TBBPA)、六氟双酚A(hexafluorobisphenol A, BPAF)均为内分泌干扰物,具有拟雌激素活性,可能对人类生殖系统及胚胎发育造成不良影响[3-4]。因其结构相似,双酚AP(bisphenol AP, BPAP)、双酚BP(bisphenol BP, BPBP)等双酚类化合物也可能对人体健康不利。
目前,双酚类化合物的检测研究主要涉及食品[5-7]、环境[8-10]、生物[11-13]等样品类型。对于食品接触材料中双酚类化合物迁移量的检测,研究对象主要为BPA及其环氧衍生物、BPF及其环氧衍生物[14-16],而对其他双酚类化合物迁移量检测研究的报道较少,覆盖范围不够广泛。
基于此,本工作拟针对性地选择高分子材料领域常用的9种典型双酚类化合物作为研究对象,各化合物的结构式示于图1,按样品的实际使用情况选择不同类型食品模拟物对样品进行浸泡,并以固相萃取的方式对浸泡液进行净化,采用高分离度快速液相色谱-串联质谱法(RRLC-MS/MS)进行分离和分析。希望为食品接触材料中双酚类化合物迁移量的检测及监控提供技术支持和方法参考。

图1 9种双酚类化合物的结构式Fig.1 Chemical structures of the 9 bisphenols
1 实验部分
1.1 仪器与装置
Agilent 1290Ⅱ-6495超高效液相色谱-串联质谱仪:美国Agilent公司产品;N-EVAP系列氮吹仪:美国Organomation公司产品;Milli-Q 超纯水器:美国Millipore公司产品;固相萃取装置:德国CNW公司产品;Oasis HLB固相萃取小柱(200 mg/6mL):美国Waters公司产品。
1.2 材料与试剂
BPA、BPF和TBBPA标准品:纯度≥98.5%,德国Dr. Ehrenstorfer公司产品;BPB和BPS标准品:纯度≥98%,美国Accustandard公司产品;BPE标准品:纯度≥98.5%,美国Sigma-Aldrich公司产品;BPAF和BPAP标准品:纯度≥98%,德国CNW公司产品;BPBP标准品:纯度均≥98%,日本TCI公司产品;甲醇:色谱纯,德国Merck公司产品;乙醇、异辛烷:均为色谱纯,美国Spectrum公司产品;实验用水:经Milli-Q净化系统过滤的去离子水;乙酸、乙酸铵:均为分析纯,广州化学试剂厂产品。
1.3 标准溶液的配制
分别准确称取10.0 mg(精确至0.01 mg)标准品于10 mL容量瓶中,用甲醇配制成1 000 mg/L单标标准储备溶液,准确移取适量各单标标准储备溶液于10 mL容量瓶中,用甲醇定容,配制成BPS、BPAF浓度为0.5 mg/L,BPBP、TBBPA浓度为5.0 mg/L,BPA、BPB、BPE、BPF、BPAP浓度为10.0 mg/L的混合标准储备液,于-20 ℃保存。使用前用50%甲醇水溶液稀释成系列浓度标准工作溶液,现配现用。
1.4 样品前处理
1.4.1迁移实验 按照GB 31604.1—2015[17]和GB 5009.156—2016[18]的要求进行迁移实验。分别选择4%乙酸溶液(V/V)、50%乙醇浸泡液(V/V)和异辛烷模拟酸性食品、含酒精类食品和含油酯类食品,以大部分食品接触材料及制品适用的60 ℃下浸泡10天作为迁移条件。食品接触材料的接触面积(S)与食品模拟物体积(V)的比值反映实际使用情形。在本实验中,对聚碳酸酯水桶、奶瓶、水杯、食品金属罐、食品金属盖等类型的食品接触材料和制品进行分析。对于空心制品,加入的食品模拟物液面与空心制品上边缘(溢出面)的距离不超过1 cm;对于扁平制品或其他S/V未知的样品,采用6 dm2食品接触材料接触1 L(或1 kg,液体模拟液密度按1 kg/L计)食品模拟物的原则进行浸泡。
1.4.2固相萃取净化 取10 mL迁移实验得到的浸泡液进行固相萃取净化。4%乙酸浸泡液(V/V)直接上柱;50%乙醇浸泡液(V/V)和异辛烷浸泡液在45 ℃水浴中经氮吹至干,加入2 mL甲醇复溶,加水定容至10 mL,混匀后上样。HLB固相萃取小柱预先依次用5 mL甲醇、5 mL水活化,上样后用5 mL水淋洗,吹干后用10 mL甲醇洗脱,定容至10 mL,取适量过0.2 μm微孔滤膜,待测。
1.5 实验条件
1.5.1色谱条件 色谱柱:Agilent poroshell 120 SB-C18柱(2.1 mm×100 mm×2.7 μm);流动相:0.1 mmol/L乙酸铵溶液(A)和甲醇(B);梯度洗脱程序:0~1 min(25%~65%B),1~5 min(65%B),5~6 min(65%~100%B),6~8 min(100%B),8~8.1 min(100%~25%B);流速0.3 mL/min;进样量5 μL;柱温30 ℃。
1.5.2质谱条件 电喷雾离子源(ESI);负离子扫描模式;多反应监测(MRM)模式检测;毛细管电压3 000 V;干燥气:氮气,温度220 ℃,流速14 L/min;雾化气:氮气,压力0.15 MPa;鞘气:氮气,温度250 ℃,流速11 L/min;碰撞气:氮气;iFunnel参数:高压90 V,低压60 V。其他质谱参数列于表1。
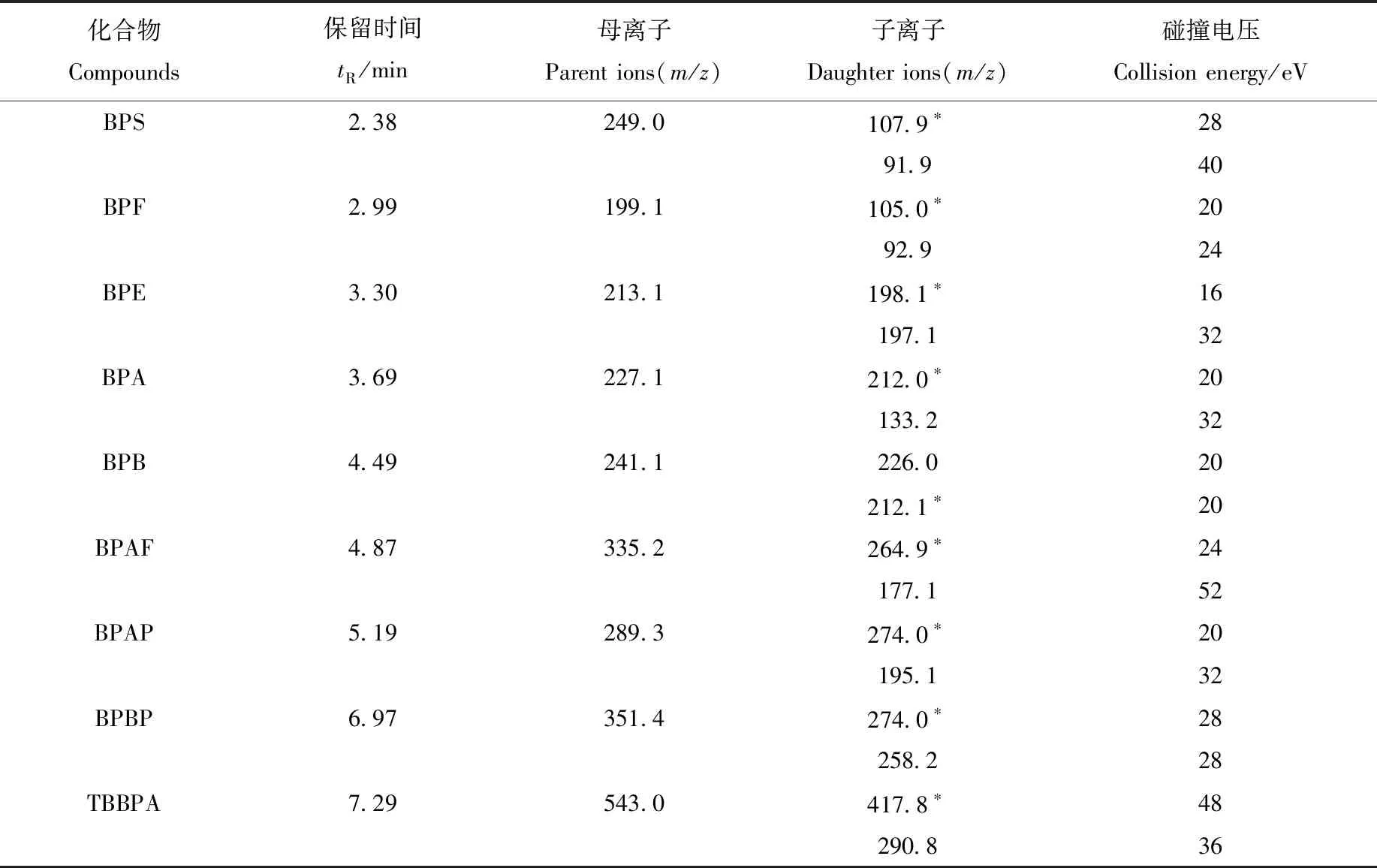
表1 9种双酚类化合物的保留时间和质谱参数Table 1 Retention times and MS/MS parameters of 9 bisphenols
注:*为定量离子
2 结果与讨论
2.1 流动相的选择
流动相对目标物的保留效果、峰形、响应均有影响。本实验所测的9种双酚类化合物的极性差异较大,其理化参数列于表2,需采用梯度洗脱的方式进行分离。分别考察了水、1 mmol/L乙酸铵溶液、0.05%氨水溶液作为流动相A的分离效果,结果显示,采用水和1 mmol/L乙酸铵溶液作为流动相A时,9种双酚类化合物均具有良好的保留效果和峰形,但采用1 mmol/L乙酸铵溶液时,可获得更强的响应。采用0.05%氨水溶液作为流动相A时,BPS、BPAF和TBBPA的保留因子明显下降,且响应减弱,可能是因为这3种双酚类化合物中酚羟基的pKa值较低,其在碱性溶液中以盐的形式存在,减弱了在反相色谱柱中的保留,同时降低了离子化效率。
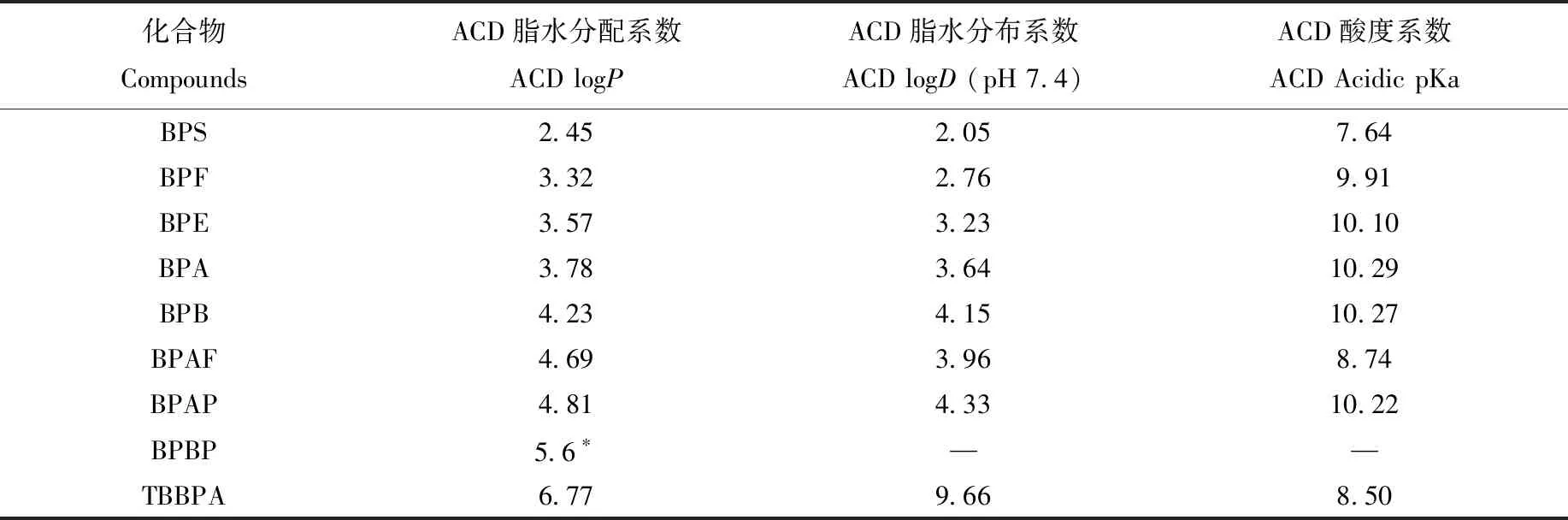
表2 9种双酚类化合物的理化参数Table 2 Physicochemical properties of 9 bisphenols
注:1.数据来源:https:∥www.ebi.ac.uk/chembl(标“*”的数据来源:https://pubchem.ncbi.nlm.nih.gov/);2. “—”表示未查询到相关数据
进一步考察不同浓度(0.1~10 mmol/L)乙酸铵溶液作为流动相时9种化合物的响应,结果表明,随乙酸铵浓度的下降,BPS、BPAF和TBBPA的响应增强,其他化合物的响应变化不明显。最终选择0.1 mmol/L乙酸铵溶液为流动相A。优化后的色谱图示于图2。
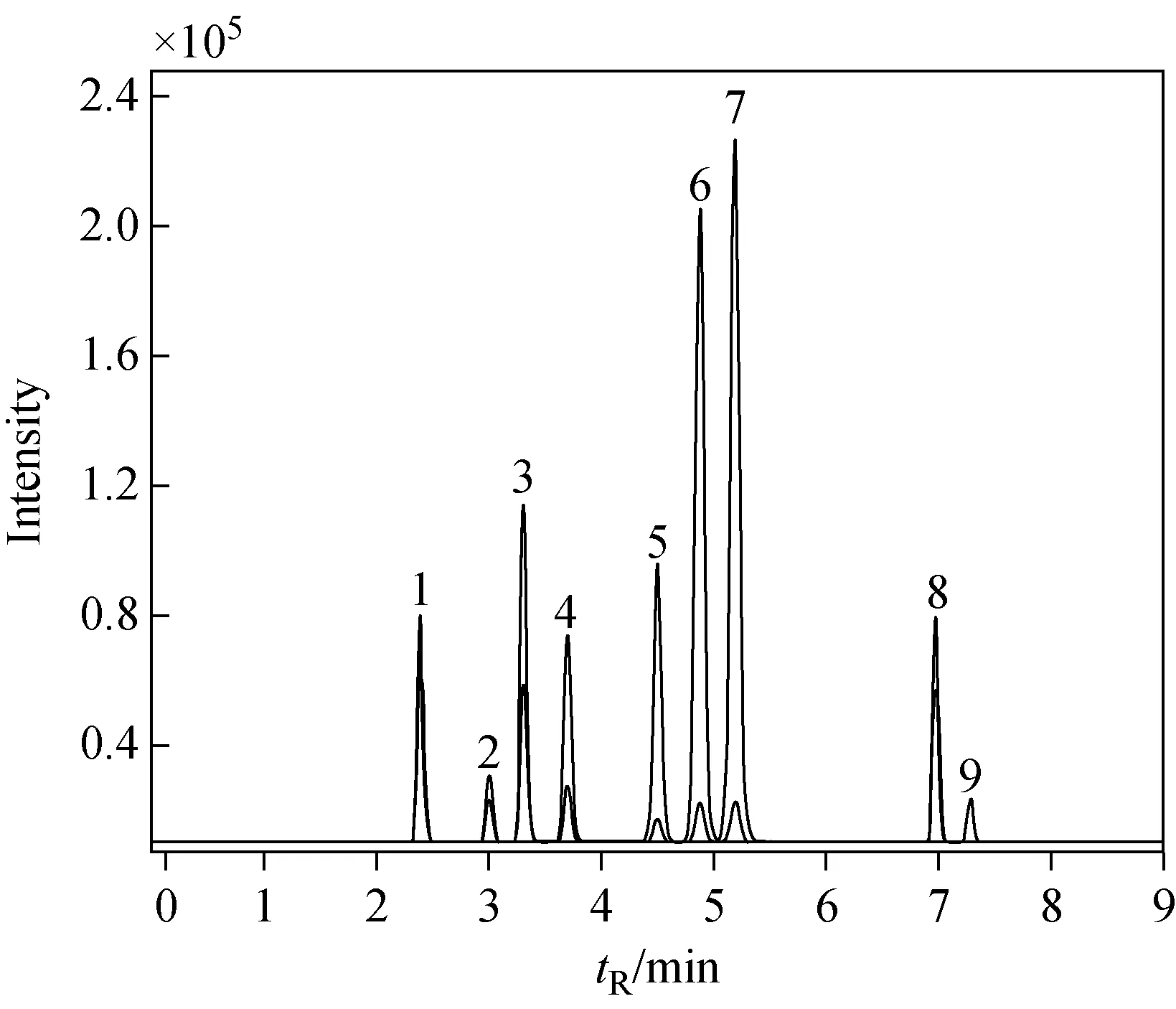
注:1.BPS(10.0 μg/L);2.BPF(200.0 μg/L);3.BPE(200.0 μg/L);4.BPA(200.0 μg/L);5.BPB(200.0 μg/L);6.BPAF(10.0 μg/L);7.BPAP(200.0 μg/L);8.BPBP(100.0 μg/L);9.TBBPA(100.0 μg/L)图2 9种双酚类化合物的多反应监测(MRM)色谱图Fig.2 Multiple reaction monitor (MRM) chromatogram of 9 bisphenols
2.2 固相萃取条件的优化
比较了2种通用型固相萃取小柱C18柱和HLB柱的净化效果。结果显示,HLB柱对9种双酚类化合物都具有良好的萃取效果,而C18柱对BPS的萃取效果不佳,加标回收率不足70%,可能是因为BPS的logP值较低,在C18柱上的保留较弱,而在具有亲水亲脂平衡特性的HLB柱上保留较强。因此,本实验采用HLB柱作为固相萃取小柱。
对上样液的甲醇比例进行考察,结果表明,采用20%甲醇-水溶液上样10 mL,9种双酚类化合物无明显损失,当甲醇比例进一步提高时,BPS和BPF会有少量损失。
2.3 方法的线性关系和检出限
以50%甲醇-水溶液为溶剂,配制9种双酚类化合物的系列混合标准溶液。其中,BPB、BPF、TBBPA浓度为1.0~200 μg/L,BPA、BPE、BPAP、BPBP浓度为0.5~100 μg/L,BPS、BPAF浓度为0.05~10 μg/L,在1.5节实验条件下测定。以峰面积(y)对相应的质量浓度(x)绘制标准曲线,9种双酚类化合物的线性范围、线性方程、相关系数、方法检出限(S/N≥3)和定量限(S/N≥10)列于表3。9种双酚类化合物在各自浓度范围内具有良好的线性关系,相关系数(R2)均大于0.99,检出限为0.01~0.2 μg/kg,定量限为0.05~1.0 μg/kg。
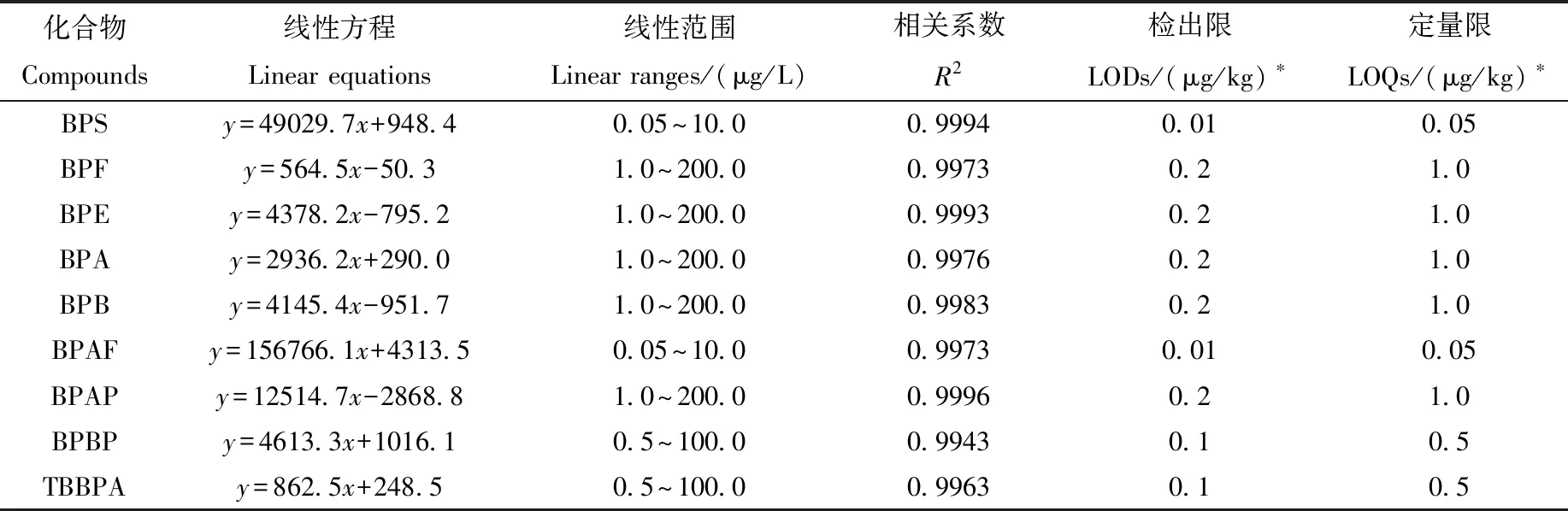
表3 9种双酚类化合物的线性方程、线性范围、相关系数、检出限和定量限Table 3 Linear equations, linear ranges, correlation coefficients (R2), LODs and LOQs of 9 bisphenols
注:*迁移量计算公式X(μg/kg)=6×(Xi-X0) ×103×(V/S),其中Xi和X0分别为样品浸泡液和空白实验中双酚类化合物的含量(mg/L),V为加入食品模拟物的体积(L),S为接触面积(dm2),6为转化系数,代表迁移量结果均转换为以6 dm2食品接触材料采用1 L(或1 kg,液体模拟液密度按1 kg/L计)食品模拟物浸泡时的迁移量,此处LOD和LOQ按S/V=6计算得出
2.4 方法的回收率与精密度
考虑到样品的代表性,选择食品金属盖作为空白样品进行加标实验。将空白样品用3种模拟物按1.4.1节进行迁移实验,分别向浸泡液中添加低、中、高3个浓度水平标准溶液,按1.4.2节处理后进行测定,每个添加浓度平行测定6次,考察方法的回收率和精密度,结果列于表4。结果显示,3个加标水平的回收率为76.9%~113.1%,相对标准偏差为1.9%~6.7%。该方法具有良好的准确度和精密度,能满足9种双酚类化合物迁移量测定的要求。
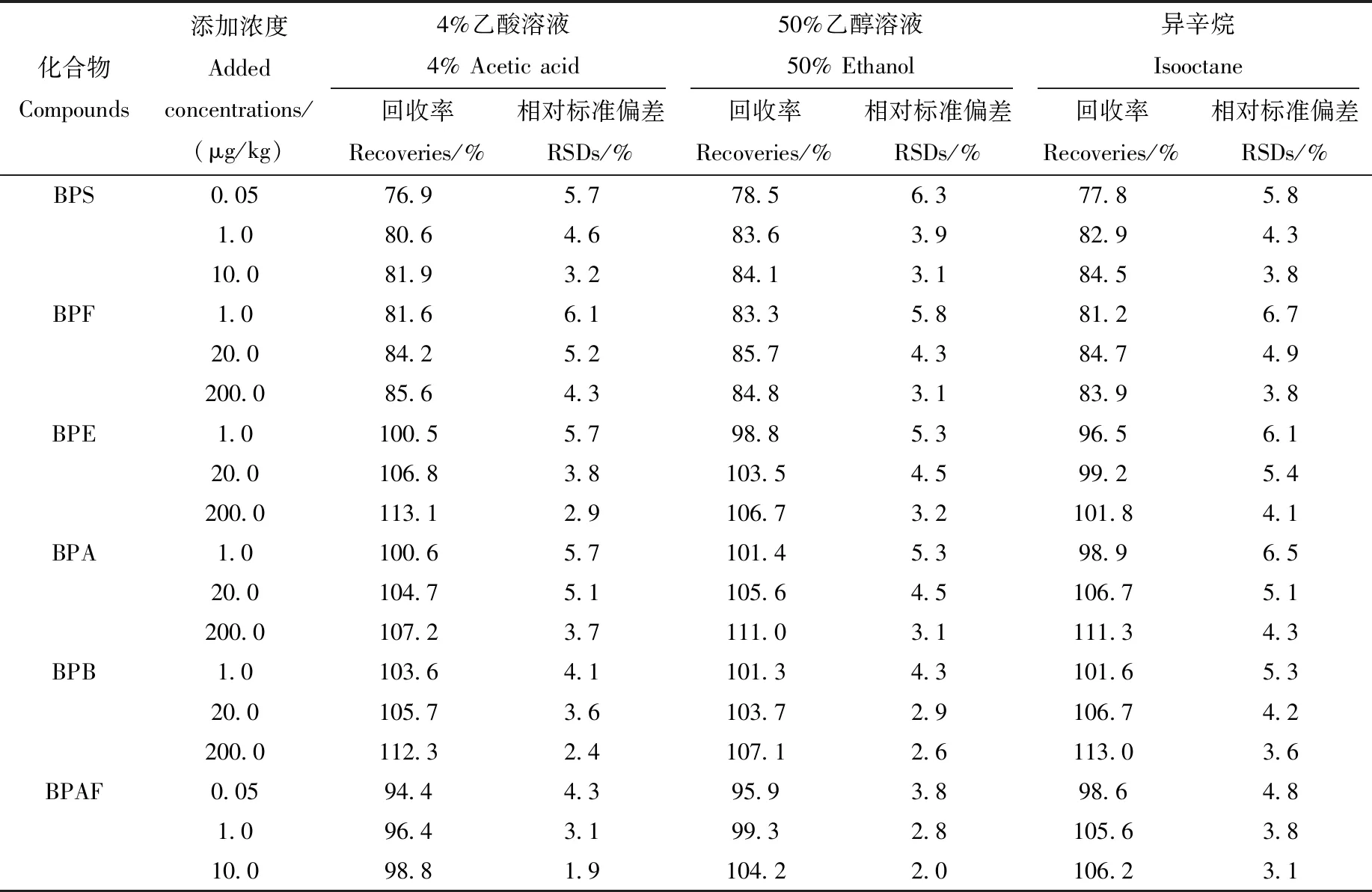
表4 9种双酚类化合物的回收率和精密度(n=6)Table 4 Recoveries and precisions of 9 bisphenols (n=6)
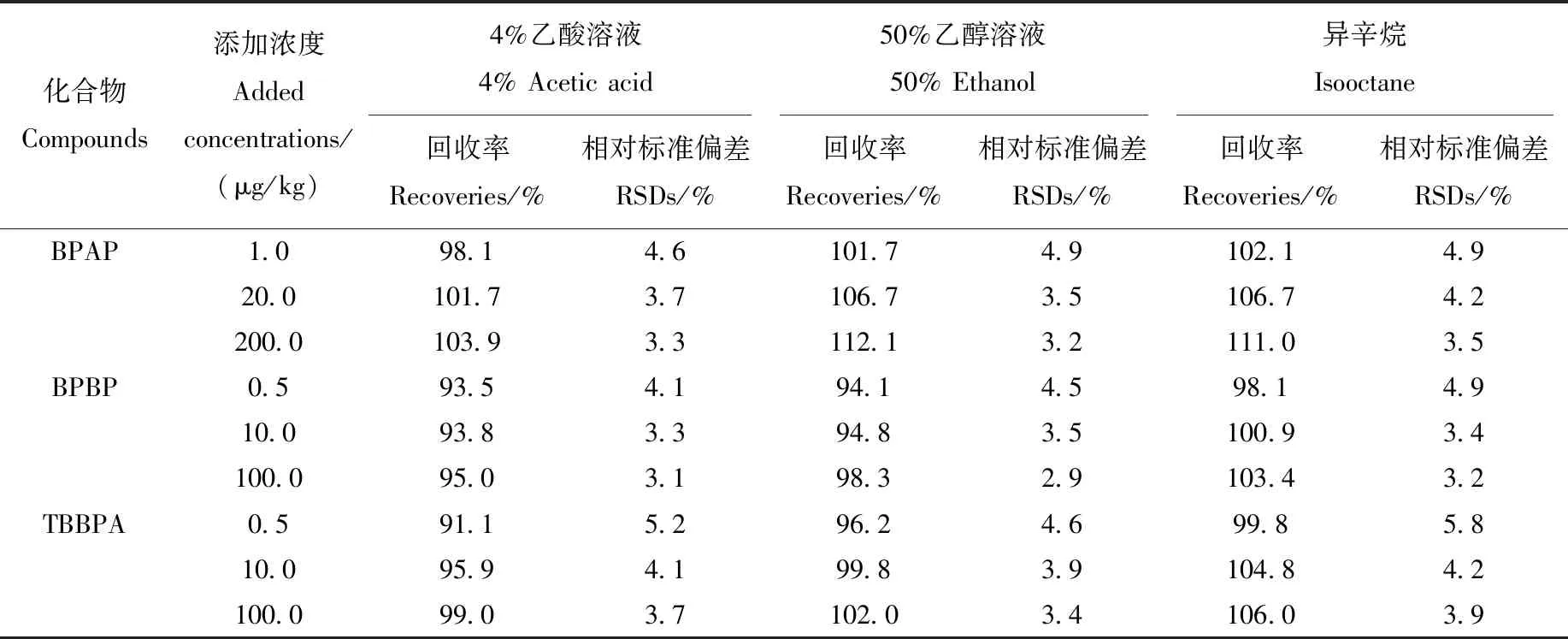
续表4
2.5 实际样品分析
采用本方法对60份食品接触材料及制品进行检测,涉及聚碳酸酯水桶、奶瓶、水杯、食品金属罐、食品金属盖等产品类型。结果显示,在4份食品金属盖样品中检出BPA迁移量,在1份食品金属盖样品中检出BPF迁移量,具体检测结果列于表5。
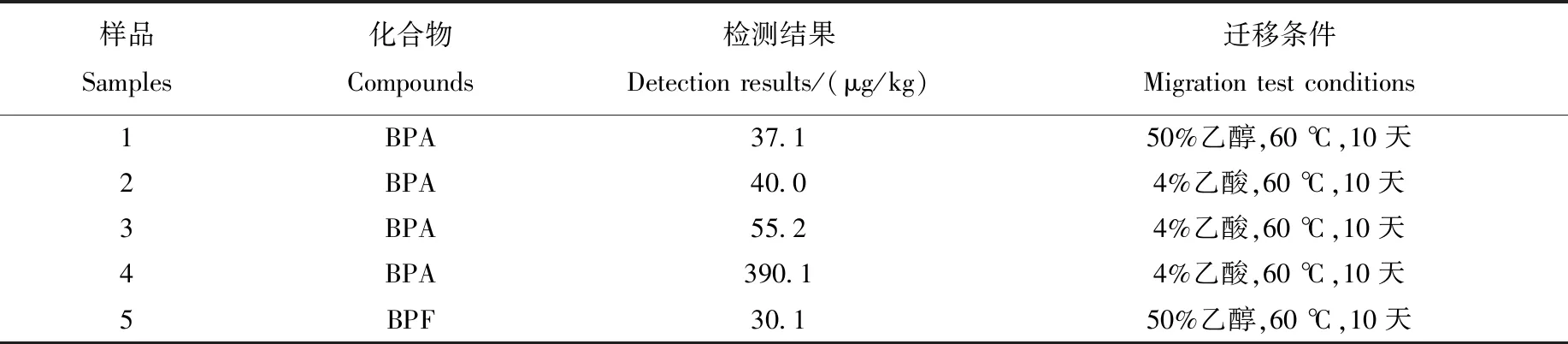
表5 阳性样品检测结果Table 5 Results of positive samples
3 结论
建立了高分离度快速液相色谱-串联质谱法测定食品接触材料中9种双酚类化合物迁移量。样品经不同类型食品模拟物浸泡后,取适量浸泡液直接净化,或经氮气吹干、甲醇复溶、纯水定容混匀后进行固相萃取净化,采用RRLC-MS/MS进行分离和分析。通过优化固相萃取净化条件以及色谱、质谱条件,9种双酚类化合物可得到有效分离,检出限可达0.01~0.2 μg/kg,加标回收率、精密度等均可满足分析要求。对聚碳酸酯水桶、奶瓶、水杯、食品金属罐、食品金属盖等60份不同类型食品接触材料及制品进行测定,结果表明,5份样品在一定条件下迁移出BPA或BPF,双酚类物质可能存在于食品接触材料及制品中,并且可能迁移至食品中,应引起关注。本方法简单、快速、准确、灵敏,可为食品接触材料及制品中双酚类化合物的迁移量检测提供技术支持。

