MIL-101(Fe)对草甘膦的吸附行为研究
蒋 实,黄 芳,林晓宇,吴桂萍,崔龙哲
(1.中南民族大学资源与环境学院,湖北 武汉,430074;2.黄石市环境保护研究所,湖北 黄石,435003)
有机磷农药(OPs)是一类高毒性合成化合物,当前广泛应用于农业生产,当其同乙酰胆碱酯酶(AchE)结合时,可以引起神经肌肉瘫痪和器官衰竭[1]。草甘膦(glyphosate,GP)是大多数有机磷农药中的有效活性化学成分,根据世界卫生组织(WHO)国际癌症研究机构2017年公布的致癌物清单,GP属于2A类致癌物,因此,如何有效去除GP已成为相关研究者重点关注的问题。目前从水溶液中去除GP 的方法主要有电化学去除、吸附、酶促生物降解和光催化降解等,其中吸附技术操作简单、成本低廉且高效安全,因此开发对水环境中的GP具有高吸附能力的吸附剂具有重要的实际应用价值。金属有机框架化合物(MOFs)是金属离子与有机配体相互作用所形成的晶体材料,具有较大的比表面积、孔隙率和结构多样性[2],已经作为新型固体吸附剂材料得到应用。与常规固体吸附剂如活性炭及介孔二氧化硅材料相比, MOFs具有可调节的孔径、多样的孔道形状和特定的活性位点等特性[3],能更有效地去除有机硫或有机氮化合物、染料和芳香族分子等有害物质。此外,为了更有效吸附OPs,不仅要求MOFs具有足够的孔隙率和孔径,而且还需要特定的活性吸附点[4],Toshitaka等[5]的研究已表明Fe2O3纳米粒子可以有选择性地捕获OPs,因此,本文采用溶剂热法合成具有大量铁氧基团的MOFs材料MIL-101(Fe),以水溶液中的GP为吸附对象,研究了溶液pH、吸附时间、溶液浓度、温度等因素对其吸附效果的影响,并对相关吸附动力学、热力学等进行了分析与探讨。
1 实验
1.1 试剂
主要试剂有六水三氯化铁、N,N-二甲基甲酰胺(DMF)、对苯二甲酸、丙酮、氢氧化钠、盐酸等,均为分析纯,草甘膦购于湖北拓楚慷元医药化工有限公司,纯度为96%。
1.2 样品的制备
参照文献[6],称取3.2243 g六水三氯化铁和1.1009 g对苯二甲酸溶于70 mL DMF中,随后转移至反应釜于383.15 K条件下反应24 h。将反应产物依次用DMF和丙酮清洗,相应清洗温度分别为333.15 K和323.15 K,经3500 r/min离心处理后再将所得固体物质于333.15 K下真空干燥、研磨,最终制得红橙色样品。
1.3 样品的表征及吸附试验
使用D8 ADVANCE型X射线衍射仪(XRD)对样品进行晶体结构分析;借助附带EDX能谱仪的ZEISS Supra 40vp型扫描电子显微镜(SEM)对样品进行微观分析;利用Autosorb-iQ型氮吸附比表面积分析仪在77 K条件下通过N2吸附-解吸等温线对样品孔结构和比表面积进行分析。
称取一定量的GP溶解在去离子水中制得浓度为1000 mg/L 的GP储备溶液,再通过用水稀释原液以制备具有不同浓度的GP使用液;称量若干样品放入盛有GP使用液的锥形瓶中,在不同的pH、吸附时间、GP溶液浓度及温度条件下于恒温震荡器中以180 r/min的转速进行单因素静态吸附实验,其中利用氢氧化钠和盐酸调节溶液pH;待吸附结束后,移取部分溶液经滤膜(0.45 μm)过滤,再根据相关标准[7],采用721E型可见分光光度计通过测定P的含量来确定吸附后溶液中的GP浓度; 使用MULTILAB 2000型X射线光电子能谱仪(XPS) 对吸附试验前后样品中的元素价态进行分析。
2 结果与讨论
2.1 结构表征
对样品进行XRD分析的结果如图1所示。由图1可见,在2θ为5.103°、8.333°、8.971°、10.205°及16.377°处均出现较明显的吸收峰,与数据库中MIL-101型的标准XRD特征峰[8-9]一致,故可确定所制样品为MIL-101(Fe),其结构式为Fe3-(μ3-O)Cl(H2O)2(BDC)3[10]。
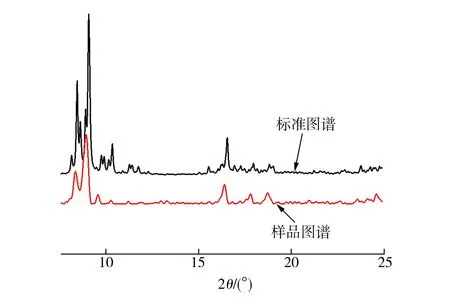
图1 XRD图谱
对样品进行 SEM 及EDX分析的结果如图2所示。结合XRD分析结果,该样品为正八面体晶体结构,正八面体上下顶点距离约为550 nm,此外,EDX分析显示样品中存在Fe、O、C和Cl元素。
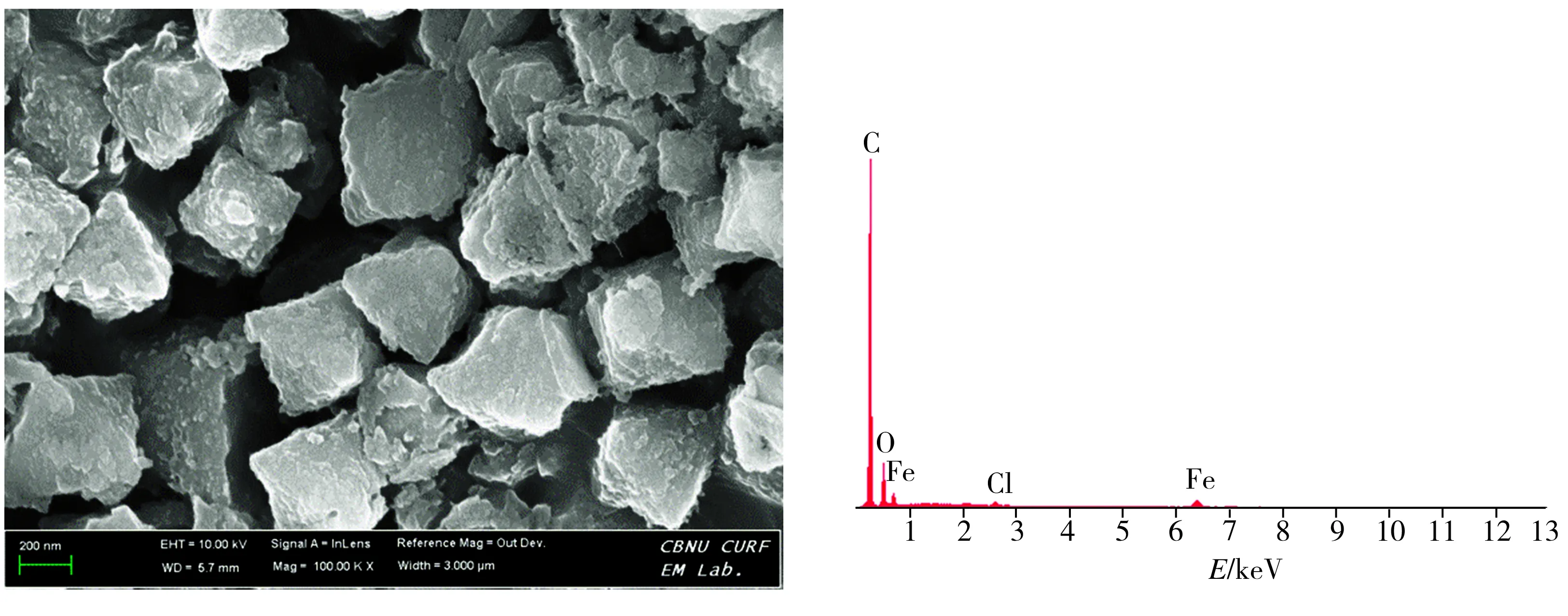
(a)SEM照片 (b)EDX光谱
图2样品的SEM照片和EDX光谱
Fig.2SEMimageandEDXspectrumofsample
图3为合成样品的N2吸/脱附等温线及孔径分布图。从图3结果可以确定样品的BET比表面积为2657.977 m2·g-1,总孔体积为2.465 cm3·g-1,平均孔径为2.6 nm,上述测试结果和文献[6]中提供的数值基本吻合,进一步证实合成样品为MIL-101(Fe)。
2.2 溶液pH对样品吸附性能的影响
溶液pH对样品吸附GP性能及Zeta电位的影响如图4所示。由于GP在不同pH值条件下的电离形态不同,故样品对其相应的吸附性能也存在明显差异[11]。由图4(a)可知,当溶液pH低于3时,样品对GP的吸附量随pH的升高而增大。这是因为此时溶液酸性较强,GP在溶液中以分子形式存在,不利于MIL-101(Fe)通过静电作用实现对GP的吸附;当pH高于3时, 样品对GP的吸附量随着pH的升高而减小。这应归因于当pH较高时,MIL-101(Fe)表面所带电荷为负电荷(图4(b)),而GP在溶液中主要以负离子形式存在,随着pH的升高,MIL-101(Fe)表面所带负电荷密度增大,导致其与GP间的静电排斥作用增加,不利于吸附的进行。与此同时,溶液中的OH-浓度逐渐升高,与GP产生竞争吸附也不利于吸附的进行。综合分析表明,当pH为3时,样品对GP的吸附能力最强。

(a)N2吸/脱附等温线 (b)孔径分布图
图3样品的N2吸/脱附等温线及孔径分布图
Fig.3N2adsorption-desorptionisothermalsandporesizedistributionofsample
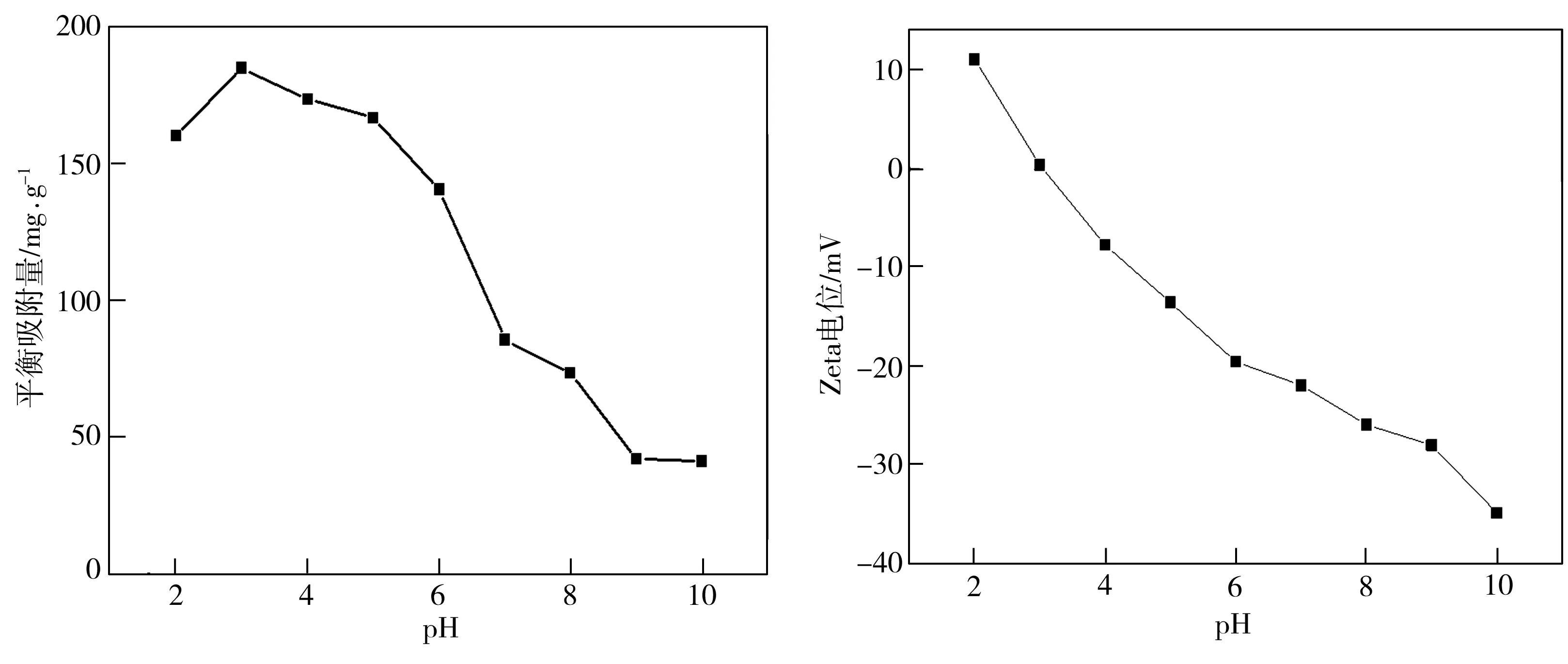
(a)pH对样品吸附GP效果的影响 (b)不同pH条件下样品的Zeta电位
图4pH对样品吸附性能及Zeta电位的影响
Fig.4EffectsofpHontheadsorptionperformanceandzeta-potentialofsample
2.3 吸附动力学
样品对GP的吸附量随吸附时间及温度变化的规律如图5所示。由图5可见, 当吸附时间少于50 min时,样品对GP的吸附速率较快,当吸附时间介于50~100 min时,吸附量仍在增加,但吸附速率增幅逐渐变缓直至达到吸附平衡,此后随吸附时间的延长,吸附量无明显变化;当吸附时间相同时,吸附速率及吸附量均随温度的上升而
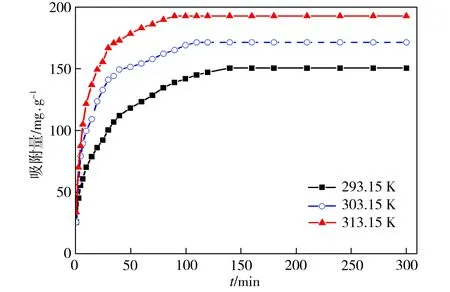
图5吸附时间及温度对样品吸附性能的影响
Fig.5Effectsofadsorptiontimeandtemperatureontheadsorptionperformanceofsample
增加,升高温度使吸附反应向正方向移动,有利于吸附的进行。该试验结果通过拟一级动力学和拟二级动力学进行拟合。拟一级动力学模型表达式为
(1)
拟二级动力学模型表达式为
(2)
式(1)~式(2)中:q为平衡吸附量,mg·g-1;t为吸附时间,min;qt为t时刻的吸附量,mg·g-1;k1为拟一级动力学速率常数,min-1;k2为拟二级动力学速率常数,g·mg-1·min-1。
经拟一级动力学和拟二级动力学方程拟合的试验结果见图6,相关拟合参数见表1。由表1可知,拟二级动力学的相关系数r更接近于1,表明拟二级动力学模型可以用于描述MIL-101(Fe)对溶液中GP的吸附过程,吸附速率的控制因素为MIL-101(Fe)与GP之间的化学反应速率。此外,动力学速率常数随温度的升高而增加,表明升高温度有利于GP向吸附剂内表面的扩散,增加了体系中GP和吸附剂吸附位点的有效碰撞次数,显著提高了吸附速率。

(a)拟一级动力学 (b)拟二级动力学

图6 吸附动力学模型
2.4 等温吸附
溶液平衡浓度对吸附量的影响见图7。由图7可见,样品对GP的吸附量随着溶液浓度的提高而增大,其可能原因是在溶液浓度较低时,吸附剂表面有大量活性位点未参与吸附。随着溶液浓度的增加,曲线斜率趋于平缓,表明MIL-101(Fe)对GP的去除率逐渐降低,这是因为当MIL-101(Fe)投放量一定时,总有效吸附面积和反应活性位点是一定的,随着GP初始浓度的增加,部分有效吸附面积与位点被占用使得有效反应位点减少[12],从而导致材料对GP的去除率降低。
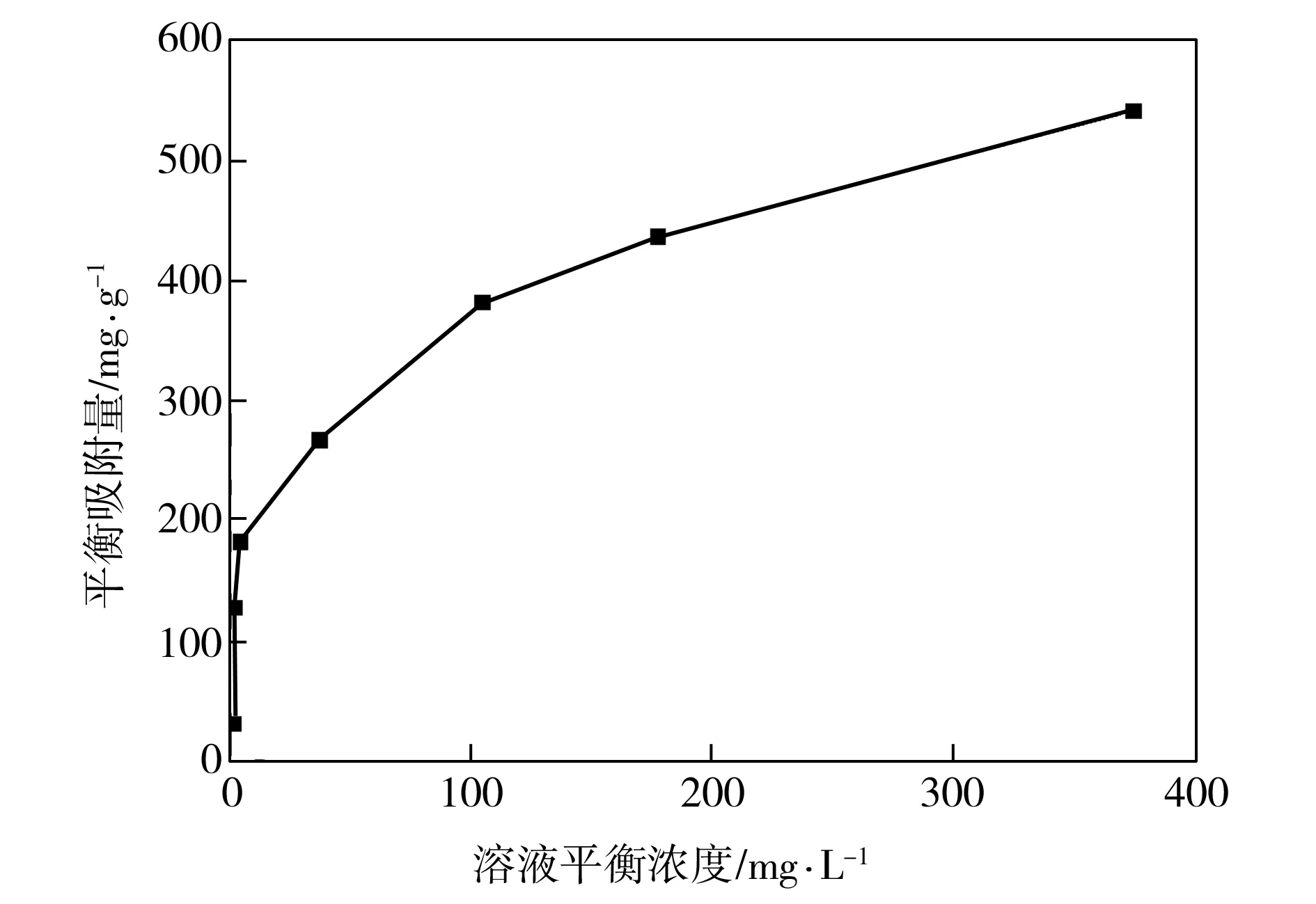
图7 溶液浓度对吸附效果的影响
Fig.7EffectsofsolutionconcentrationonadsorptionofGP
试验结果分别通过Langmuir、Freundlich、BET及Temkin模型进行拟合分析,相应模型表达式分别为
(3)
式中:c为溶液平衡浓度,mg·L-1;qmax为最大吸附量,mg·g-1;kL为Langmuir常数,mmol-1。
(4)
式中:kF为Freundlich常数,mmol1-n·Ln·g-1;n是随着材料的非均匀性变化而变化的常数,与吸附强度有关。
(5)
式中:B为与吸附质的液化热有关的常数;c0为溶液初始浓度,mg·L-1;q*为单层铺满时的吸附量,mg·g-1;
q=BT(lnA+lnc)
(6)
式中:A和BT为与温度和吸附体系性质相关的常数。
四组模型拟合结果如图8所示,相应拟合参数见表2。由表2可知,Langmuir模型的相关系数r相较Freundlich模型相应值而言更加接近于1,表明吸附属于单层吸附且吸附剂表面均匀;同BET模型相比,Temkin模型与试验数据拟合良好,表明吸附剂对GP的吸附以单层化学吸附为主,吸附热与覆盖度呈线性关系。由拟合结果可知样品对GP的最大吸附量为558.6 mg·g-1。
2.5 吸附热力学
借助式(7)~式(9)对样品吸附GP的过程进行热力学分析,分析结果如图9所示。
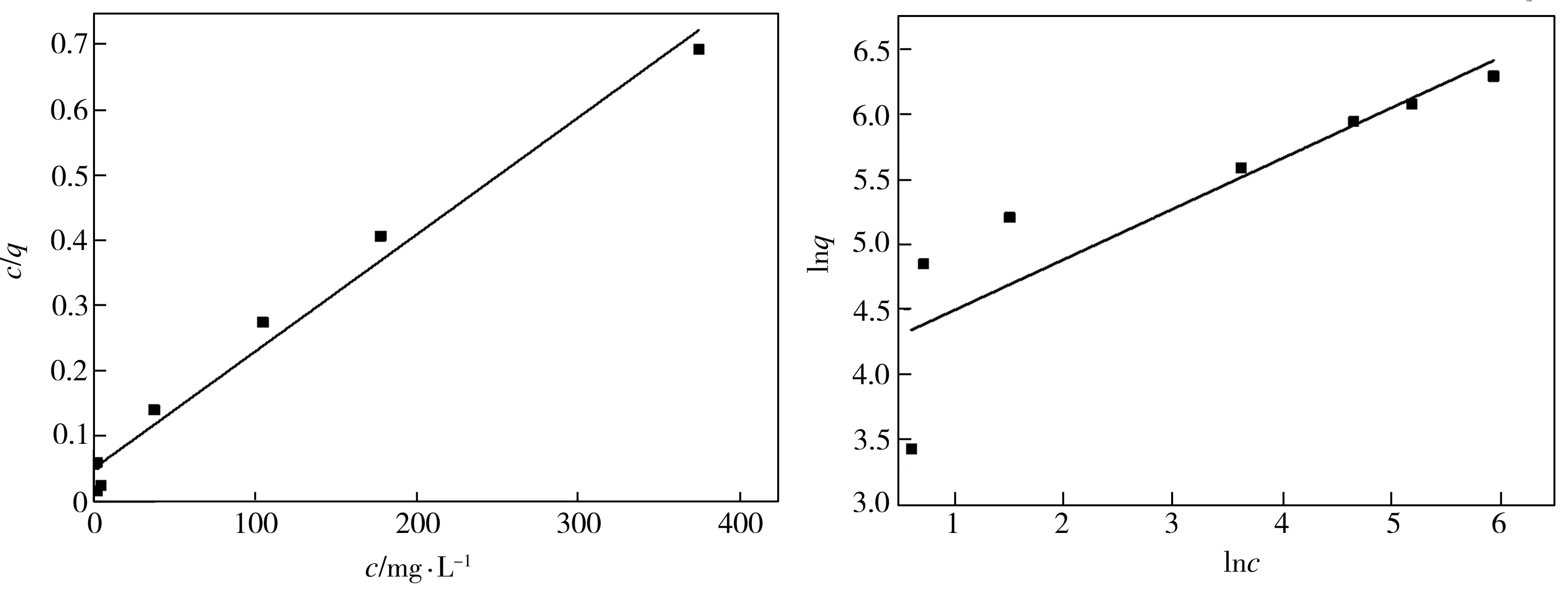
(a)Langmuir (b)Freundlich
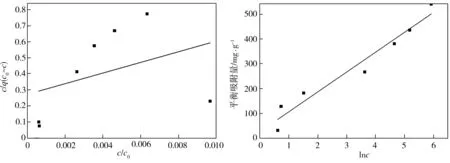
(c)BET (d)Temkin

(7)
ΔG=-RTlnKad
(8)
(9)
式中:Kad为浓度平衡常数;ΔG为吉布斯自由能变化;R为理想气体常数;T为温度;ΔH为
焓变;ΔS为熵变。
由图9(a)可知,MIL-101(Fe)对GP的吸附量随着温度的升高而升高,表明吸附过程为吸热反应,升高温度使得吸附平衡向正方向移动。基于图9(b)所示的热力学拟合曲线,其拟合相关参数如表3所示。由表3可知,ΔG<0,表明MIL-101(Fe)吸附GP是自发进行的;ΔH>0,表明吸附过程为吸热过程,升高温度使得吸附平衡向正方向移动,与实验结果相符。一般认为,当|ΔH|<20 kJ·mol-1时,表明吸附过程以物理吸附为主,当|ΔH|>40 kJ·mol-1时,吸附主要以化学吸附为主。表3中ΔH=141.2 kJ·mol-1,表明MIL-101(Fe)对GP的吸附以化学吸附为主。同时,在吸附过程中,ΔH与ΔS均大于0,表明吸附过程中自发反应的推动力源于体系混乱度的增加。

(a)温度对样品吸附GP的影响 (b)吸附热力学拟合曲线

2.6 XPS分析

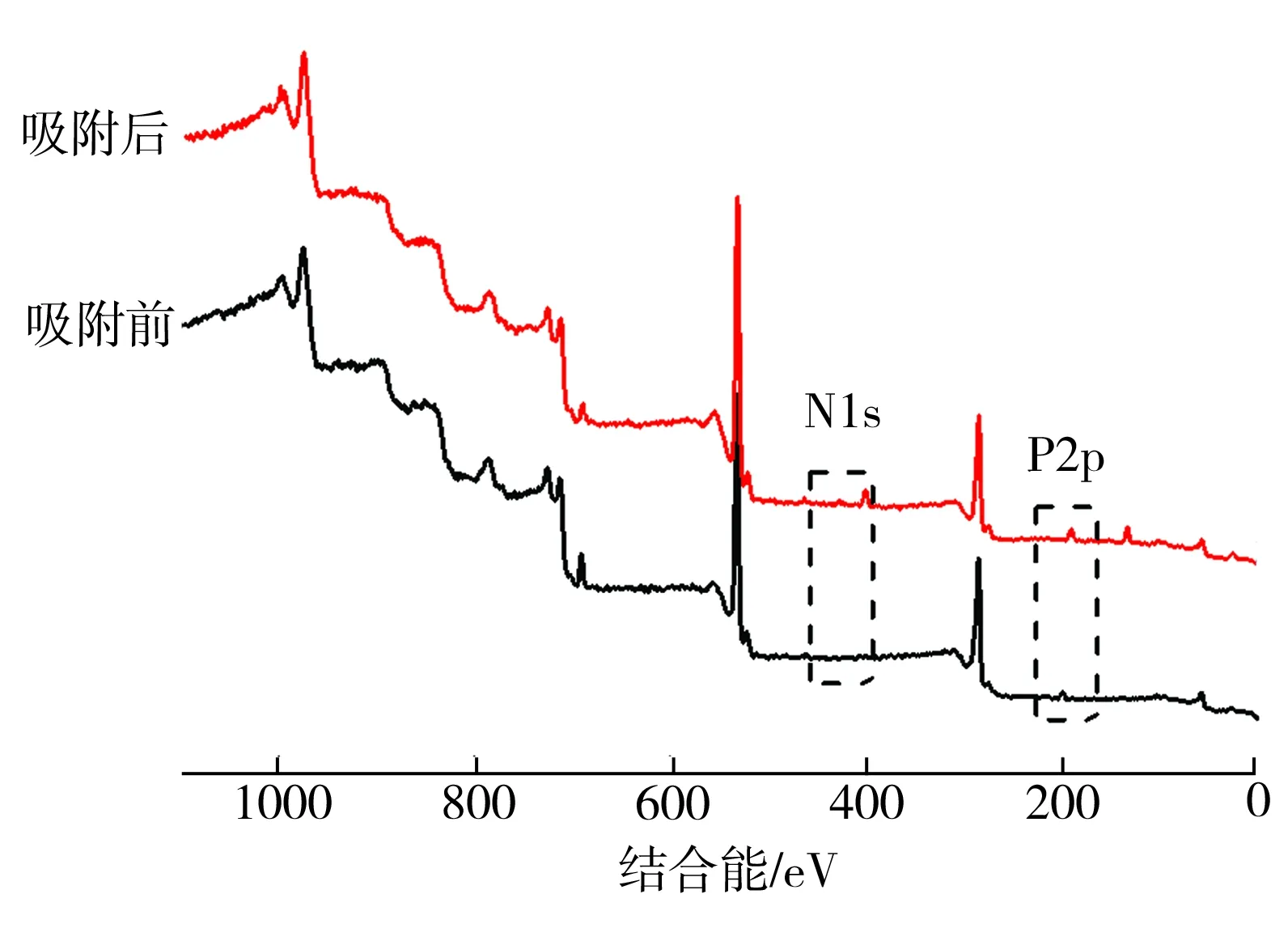
(a)样品的XPS图谱

(b)P2p精细谱
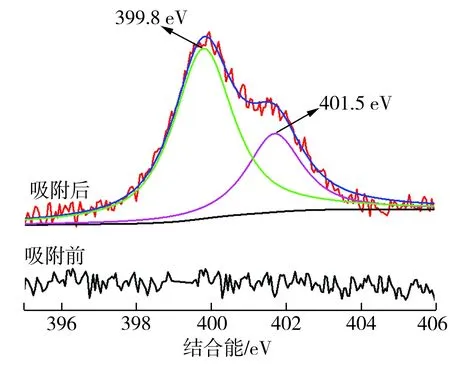
(c)N1s精细谱
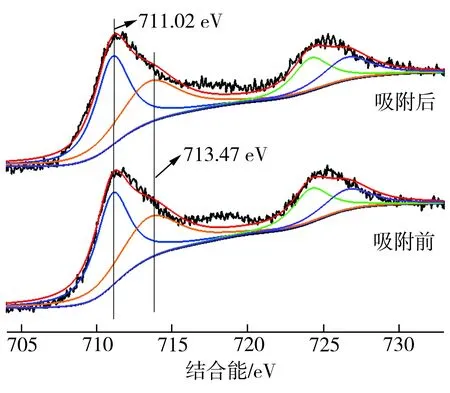
(d)Fe2p精细谱
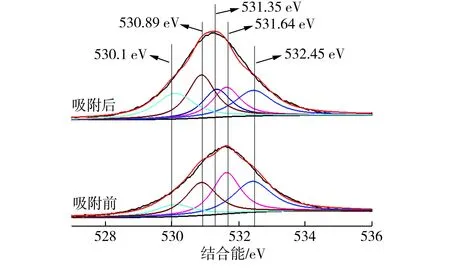
(e)O1s精细谱
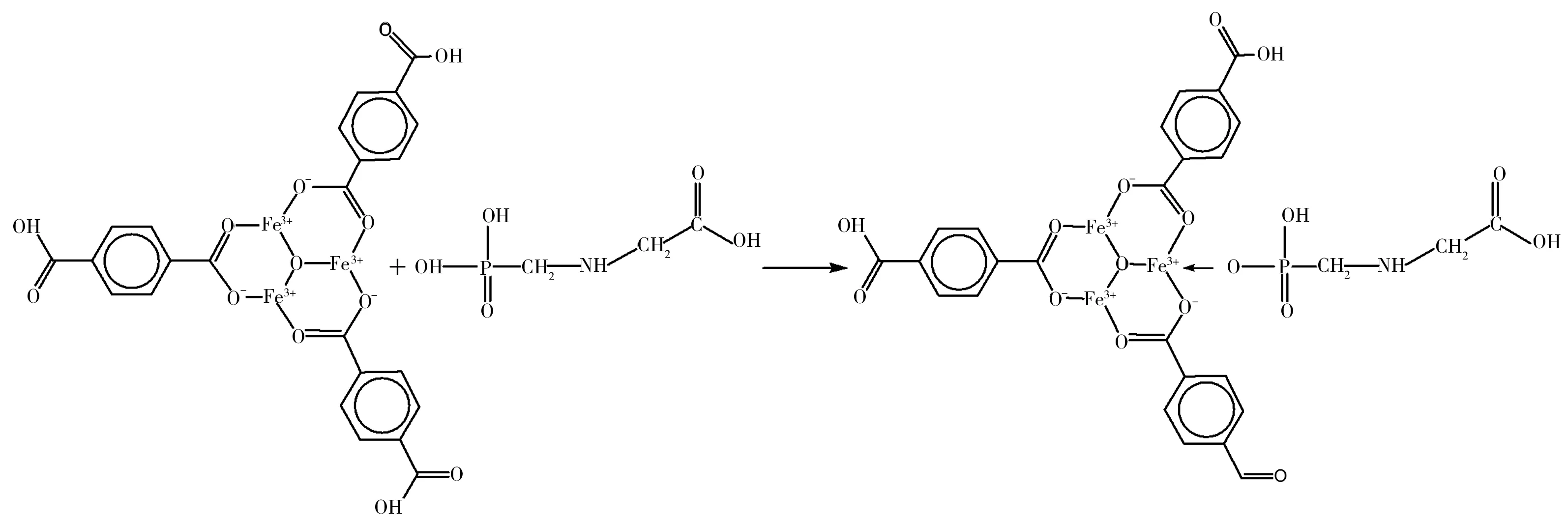
图11 吸附反应式
3 结论
(1)利用溶剂热法成功制备了金属有机框架化合物MIL-101(Fe),其晶体结构为正八面体。
(2)pH对MIL-101(Fe)吸附GP的性能影响较大,当pH为3时,MIL-101(Fe)吸附GP的能力最强,最大吸附量可达558.6 mg·g-1。
(3)MIL-101(Fe)对GP的吸附为单层化学吸附,吸附速率较快,吸附过程为自发吸热反应。
(4)MIL-101(Fe)对GP的吸附主要通过中心金属Fe与GP中的O配位从而形成GP与MIL-101(Fe)的螯合物来实现。

