形态可控合成氧化亚铜粉体及其光催化性能
徐泽忠,杨昌林,廖 凯,韩成良
(1.合肥学院分析测试中心,合肥 230601;2.合肥学院化学与材料工程系,合肥 230601)
1 引 言
氧化亚铜(Cu2O)具有良好的可见光吸收特性,是一种常见的可见光催化剂,可用做防腐剂、杀菌剂、着色剂和催化剂等[1-3]。通常,以普通铜盐为原料,在葡萄糖、抗坏血酸、果糖、水合肼、硼氢化钠和多元醇等还原剂的作用下通过还原反应可以得到不同形态的Cu2O纳米材料[4-9]。为了得到规整的Cu2O纳米晶,常在反应体系中使用一些诸如聚乙烯比咯烷酮(PVP)[10]和十六烷基溴化铵(CTAB)[11]等模板剂和表面活性剂。然而,已采用的这些还原剂和添加剂中有些在一定程度上具有一定的毒性,同时成本也较高。明胶是一种水溶性生物高分子,具有无毒、生物降解能力强和成本低等优点。在合成无机纳米材料中应用广泛[12]。Han等[13]利用明胶作为模板成功制备出了Fe3O4多孔纤维。本文以酒石酸和明胶为廉价还原剂和生物模板来可控制备Cu2O粉体。该方法无需特殊设备,具有绿色可控特征,且得到的产物量比较大。同时,获得的产物具有优异的可见光催化性能,可用于水体中有机污染物的去除。
2 实 验
2.1 合成与表征
首先,将0.005 mol CuSO4·5H2O和0.005 mol酒石酸混合后并加入到80 mL去离子水中,溶解后再将0.5 g NaOH加入到上述溶液中,得到深蓝色溶液。最后,将此深蓝色溶液转入到反应釜中并在120 ℃烘箱中反应3 h,将得到立方Cu2O粉体。在上述反应体系中添加1.5 g明胶,加热使其溶解后得到深蓝色胶体溶液,经水热反应后将获得球形Cu2O粉体。在其它条件不变的情况下,改变还原剂和模板的量,便可得到不同形态的Cu2O产物。实验得到的产物的结构、形态和光学性能分别采用X射线衍射仪(XRD)、场发射扫描电镜(FE-SEM)和紫外-可见分光光谱仪(UV-vis)等设备进行表征。
2.2 光催化实验
为了研究Cu2O粉体的光催化活性,将0.5 g Cu2O粉体加入200 mL 甲基橙的水溶液(初始浓度为10 mg/L)中,超声分散后在黑暗中搅拌60 min进行吸附实验,待吸附达平衡后,将其移到300 W氙灯(PLS-SXE300,λ>420nm)可见光源下照射。取不同时间间隔下的水溶液,并用紫外-可见分光光谱仪(UV-vis)测定其吸光度,而t时刻对应的甲基橙的浓度(Ct)可用下列式子估算:
Ct=C0×At/A0
(1)
C0(mg/L)为水体中初始甲基橙浓度,A0初始甲基橙吸光度,At为t时刻甲基橙水溶液吸光度。

图1 球形(a, b)和立方(c, d)粉体的形态和化学组成Fig.1 Morphlogy and chemical composition of spherical (a, b) and cubic (c, d)Cu2O powders
3 结果与讨论
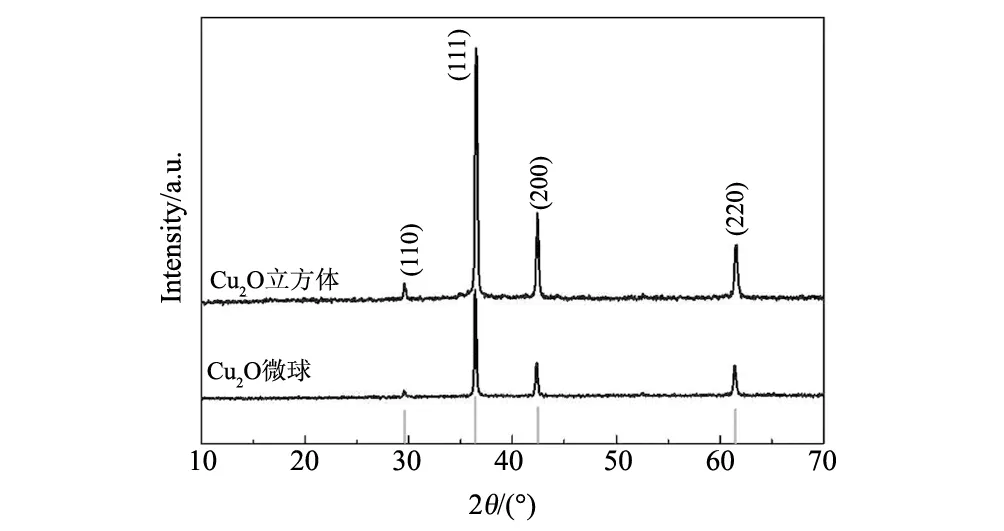
图2 不同形态产物的XRD图谱Fig.2 XRD patterns of products with various shapes
众所周知,粉体颗粒的形态在一定程度上也影响其性能。为此,首先使用扫描电子显微镜对实验所得到的产物进行形态观察和化学组成分析,其结果如图1所示。在碱性酒石酸铜体系中,当采用的实验参数恰当时,电镜观察结果表明,此时获得的产物的形状为立方(图1c所示),粒度统计分析表明,立方体的边长约为1 μm(见图1c插图),能谱进一步分析表明,立方体是由Cu和O两种化学元素组成(见图1d)。在碱性酒石酸铜和明胶构成的反应体系中,反应最后的产物的形状为球形(见图1a),统计球径约为0.7 μm(见图1a插图),且单个球的化学组成为Cu、O和少量C(见图1b)。少量的C可以认为是明胶模板组装后的残余物。
为了进一步确定上述由Cu和O两种元素组成的两种形态产物的物相,我们对两种产物进行了XRD测试分析,其结果如图2所示。与块体Cu2O标准XRD衍射谱图(PDF#:050667)对比分析后可知,实验获得的两种形态的产物均为Cu2O物相。相比之下,立方Cu2O粉体的结晶度要高于球形Cu2O粉体的结晶度。
系统研究得出,反应体系中酒石酸的用量对产物的纯度和形态具有较大的影响。酒石酸使用量较少时(<0.002 mol),产物中有少量Cu2O物相出现。这很容易理解,因为酒石酸为还原剂,其量少,还原反应不彻底。而当酒石酸使用量过高时(>0.02 mol),得到的Cu2O呈无规则。当酒石酸的使用量在0.002~0.02 mol范围内,将得到一些准立方的Cu2O产物(见图3)。而当酒石酸用量为0.005 mol时,产物为更规整的立方Cu2O(见图1a所示)。因此,可以得出结论,反应体系中酒石酸的量对最终产物的组成和形态起到了关键作用。

图3 酒石酸使用量对Cu2O粉体形态的影响(a)0.002 mol;(b)0.02 molFig.3 Effect of tartaric acid on shapes of Cu2O powders (a) 0.002 mol;(b) 0.02 mol

图4 明胶模板使用量对Cu2O粉体形状的影响(a)0.5 g;(b)1.5gFig.4 Effect of gelatin templates on shapes of Cu2O powders (a)0.5 g;(b)1.5 g
系列实验研究还得出,明胶的使用量主要影响产物的形态,在其它条件相同时,明胶的使用量在0.5~1.5 g范围内均可以获得球形Cu2O产物,使用量较少时(见图4a),获得的Cu2O球形度较低,而使用量过高时,产物中就会有明胶残余(见图4b)。因此,起模板组装作用的明胶,其使用量也必须控制在一定的范围内。
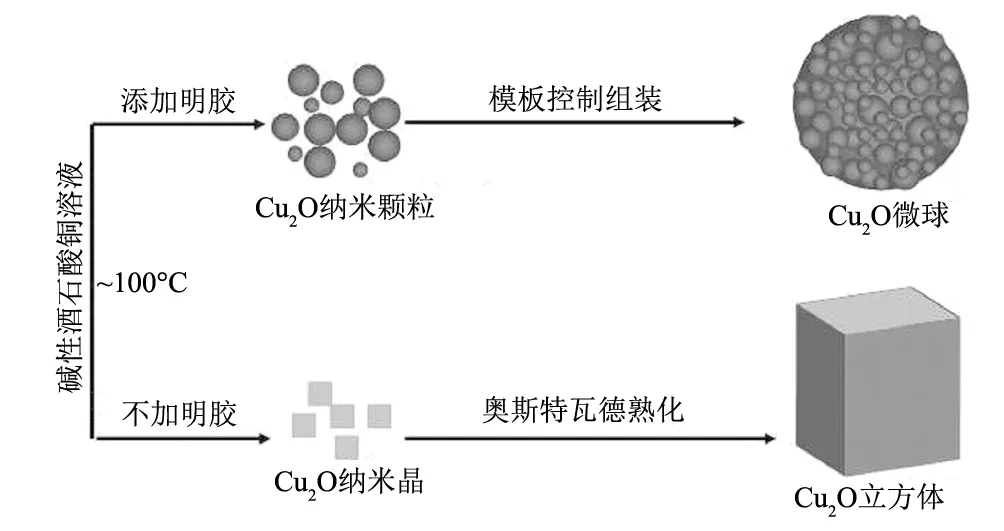
图5 球形和立方Cu2O粉体颗粒形成机理示意图Fig.5 Illustration of formation mechanisms of spherical and cubic Cu2O powders
基于以上实验结果,一般认为,在适量酒石酸根存在时,酒石酸铜中Cu2+在加热时被还原并缓慢释放出Cu+,Cu+与体系中OH-结合形成CuOH;接着,CuOH失水形成许多Cu2O小晶粒,这些单晶的Cu2O最后通过奥斯特瓦尔德熟化方式形成了尺寸较大的Cu2O立方体。其它实验参数相同时,在该反应体系中引入适量明胶,添加的明胶可起到模板的作用,将形成的若干Cu2O纳米颗粒组装成Cu2O微球,以降低整个反应体系的能量。立方体和球形Cu2O粉体的形成机理可用图5所示。
Cu2O是一种重要的半导体材料,具有良好的可见光吸收性能。两种形态Cu2O粉体的可见-紫外吸收光谱如图6a所示。可见,立方和球形Cu2O粉体的可见光最大吸收波长(λmax)均约为500 nm,由公式[14]Eg=1240/λmax可估算出两者的带隙宽度约为2.2~2.4 eV(见图6b)。
最后,以一定浓度甲基橙为目标污染物,对比研究了立方和球形Cu2O粉体的可见光催化性能,其结果如图7所示。可以看出,对于两种形态Cu2O,随着可见光辐照时间的增加,水体系中甲基橙的相对浓度(Ct/C0)将逐渐减少。进一步分析可知,两种形态Cu2O降解甲基橙的过程均符合一阶动力学模型,与文献[15-16]报道的染料降解动力学模型一致。相比之下,Cu2O微球由于其特殊的微/纳米结构具有较低的带隙,具有较高的光催化性能。因此,球形Cu2O粉体降解甲基橙的性能要优于立方Cu2O粉体。由电镜观察可知,球形Cu2O颗粒是由大量Cu2O纳米颗粒所组成,具有丰富的活性界面,加速了高氧化性OH-自由基的形成,从而增强了催化分解甲基橙的速率。
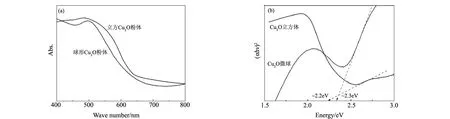
图6 不同形态Cu2O粉体的紫外-可见吸收光谱Fig.6 UV-vis spectra of Cu2O powderswith different shapes
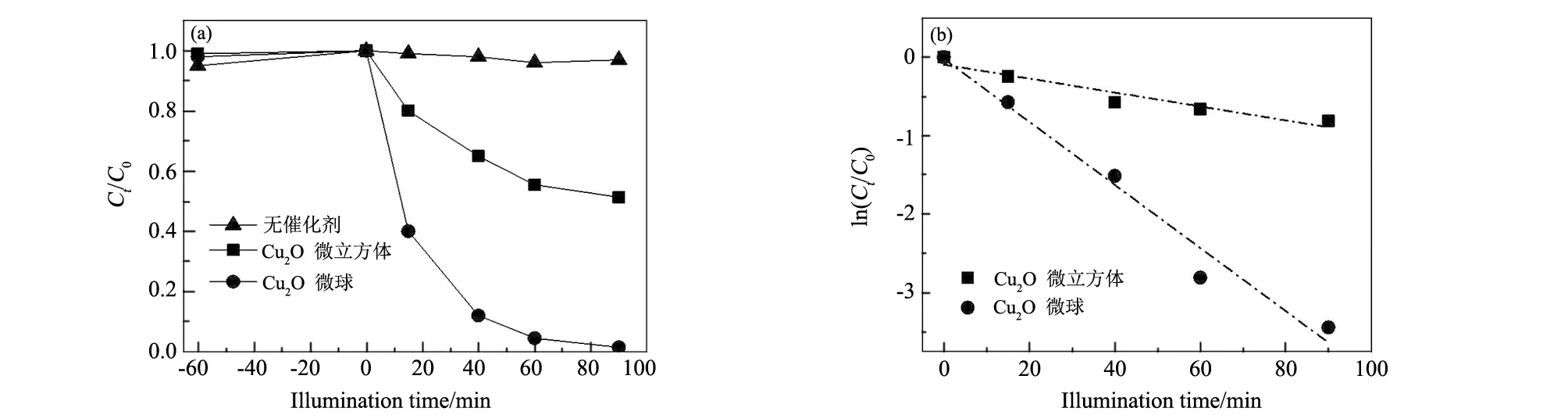
图7 (a)可见光催化降解甲基橙动力学曲线;(b)动力学曲线线性分析Fig.7 (a)Kinetic curves of degradation of methyl orange;(b)linear analysis of kinetic curves
4 结 论
采用低温水热法,在碱性酒石酸铜水体系中可以制备出Cu2O粉体,控制酒石酸的用量可以得到立方Cu2O粉体。在上述反应体系中,添加适量的明胶可以获得球形Cu2O粉体。以甲基橙为目标污染物,研究了实验得到的两种形态的Cu2O粉体的可见光降解性能。光催化实验结果表明,球形Cu2O粉体的光催化性能要优于立方Cu2O粉体的光催化性能。

