HPLC测定黄精的指纹图谱
李松涛,于 晓,耿翠翠,刘志萍,车 勇,孔 青
(山东医药技师学院,山东 泰安 271000)
黄精为百合科黄精属植物,是中国常见的中药材之一[1],主要用于治疗心血管疾病、糖尿病和提高免疫力、抗肿瘤等方面。黄精分布于华东、华北、西北、中南等区域,其药材质量随生长地理环境的不同差别很大[2],加之黄精属植物外观上形状相似,难以区分,严重阻碍高质量黄精产业的发展及应用[3]。已有研究通过测定单一成分葡萄糖含量评价黄精的质量,但该指标成分评价方法无法精确、全面地反映药材质量,其他对黄精药材质量标准方面的研究鲜有报道。
中药色谱指纹图谱方法是一种完整性、综合性质量控制方法,具有均一性和稳定性[4],在中药如雪飞、丹参质量控制方面广泛应用。本研究拟通过收集泰安不同地理位置的黄精,利用HPLC建立山东泰安的黄精指纹图谱,并与其他区域黄精指纹图谱进行对比,以期为泰安黄精药材质量评价提供参考。
1 仪器与试材
1.1 仪器与试剂
安捷伦1260二元高效液相色谱仪,安捷伦G4212B 二极管列阵检测器,安捷伦 Eclipse XDB-C18色谱柱(150 mm×4.6 mm,5 μm),KH500B型超声清洗器(昆山GRAD),明澈D24UV超纯水系统(密理博中国),HH-W420水浴锅(江苏荣华),DHG-9076A电热干燥箱(上海精宏),加热回流设备;无水乙醇(COMIO),色谱级乙腈(Fisher Scientific)。
1.2 供试材料
山东黄精采于山东泰安,共10个批次。对照黄精采于河北,共2个批次(见表1)。标准品薯蓣皂苷元(111539)、薯蓣皂苷(111707)、人参皂苷Rb1(110704),均购自中国食品药品检验研究院。

表1 12批次黄精产地及采集信息
2 黄精指纹图谱的建立与结果分析
2.1 色谱条件
安捷伦1260二元高效液相色谱仪,安捷伦G4212B二极管列阵检测器,安捷伦Eclipse XDB-C18色谱柱(150 mm×4.6 mm,5 μm),流速1 ml/min,检测波长203 nm,柱温30 ℃,进样量40 μl,以乙腈(下文用体积分数)和水为流动相,采用二元梯度洗脱,梯度洗脱程序见表2。

表2 梯度洗脱程序
2.2 对照品溶液的制备
精确称取薯蓣皂苷元、薯蓣皂苷、人参皂苷Rb1标准品适量,用80 %乙醇溶解后通过0.45 μm滤膜过滤即得对照品溶液,对照品溶液浓度分别为薯蓣皂苷元(0.306 mg/ml)、薯蓣皂苷(0.304 mg/ml)、参皂苷Rb1(0.304 mg/ml)。
2.3 指纹图谱供试品溶液的制备
黄精清洗后置于55 ℃烘箱烘干至恒重(约30 h),经粉碎机粉碎后过筛(40目),将精密称取的1 g黄精粉末加乙醇(φ=80 %)20 ml摇匀,于86℃水浴装置中回流提取3 h,热过滤取滤液,经0.45 μm滤膜滤过即得样品。
2.4 方法学考察
2.4.1 精密度试验 精密称取HJ-1批次黄精1 g,依照“2.3”方法制备样品溶液,用HPLC按照“2.1”色谱条件连续测定5次记录指纹图谱,以14号峰为内参照峰,得各共有峰相对峰面积RSD为0.134 %~1.633 %,相对保留时间RSD为0.022 %~0.182 %,结果表明,仪器具有良好的精密度[5]。
2.4.2 重复性试验 取5 份同一药材的粉末样品,依照“2.3”方法制备样品溶液,用HPLC按照“2.1”色谱条件测定, 以14号峰为内参照峰,计算16个分离度好的主组分峰的相对峰面积RSD为0.266 %~1.742 %,相对保留时间RSD为0.037 %~0.435 %之间,结果表明,该提取方法具有良好的重复性[5]。
2.4.3 稳定性试验 取同一批次黄精药材粉末,按照“2.1”色谱条件,分别于 0,3,6,9,12,24 h 依次进行进样测定,以峰14为内参比,计算出16个分离度好的主要组分的相对峰面积RSD为0.136 %~1.633 %,相对保留时间RSD为0.026 %~0.286 %,结果表明,样品在24 h内稳定性好[5]。
2.5 指纹图谱的建立与分析
对采集的10批山东泰安的黄精样品分别按“2.3”方法处理制成供试品溶液,注入高效液相色谱仪按“2.1”色谱条件测定。通过分析比较10批次样品的HPLC色谱图,将吸收强、稳定性好的16个峰标定为共有特征峰,各共有峰相对保留时间的RSD为0.21 %~1.86 %,表明以此为基准建立的黄精药材主要成分对照指纹图结果可靠。通过共有模式生成法即将10批黄精样品的指纹图谱测定结果导入中药色谱指纹图谱相似度评价软件中进行数据处理,设置参照图谱后多点校正生成对照图谱[6](见图1),各共有峰相对保留时间为0.2239,0.2544,0.276,0.3538,0.3765,0.4194,0.4848,0.51,0.5298,0.7616,0.8059,0.9363,0.9823,1,1.0762,1.1523。各批次间的相似性均在0.9以上,表明这10批次黄精药材间相似性良好。通过查阅文献,以薯蓣皂苷元、薯蓣皂苷、人参皂苷Rb1为标准品分别注入液相色谱仪进行比对[7-8],结果表明,6号峰为薯蓣皂苷元,13号峰为人参皂苷Rb1。
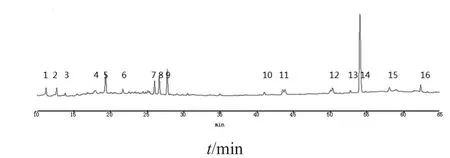
图1 山东泰安黄精参照峰图谱
2.6 不同批次黄精指纹图谱的比较
山东泰安黄精确定的16个共有峰在这10个不同批次的黄精药材中均能检测到(见图2),表明10批药材主要活性成分相似。各产地黄精样品中5,7,8,9,14峰的峰面积较大,表明5个指纹峰对应的成分在泰安黄精中占比较大为主要成分。不同批次间相同成分含量有明显差异,5,7,8,9号峰在各批次的差异明显。将10批黄精药材指纹图谱分析结果导入中药指纹图谱相似度评价体系中以16个共有指纹峰的峰面积为基本参数,对10个批次黄精的相似性进行评价,各批次黄精间相似性均在0.9以上,批次1,2,5,6四个批次的相似性在0.99以上,批次3,4,7,8,9,10六个批次的相似性在0.99以上。批次1,2和批次5,6的成分明显低于其他6个批次,初步推断海拔高度造成的地理位置差异影响药材成分含量差异,有待进一步研究。
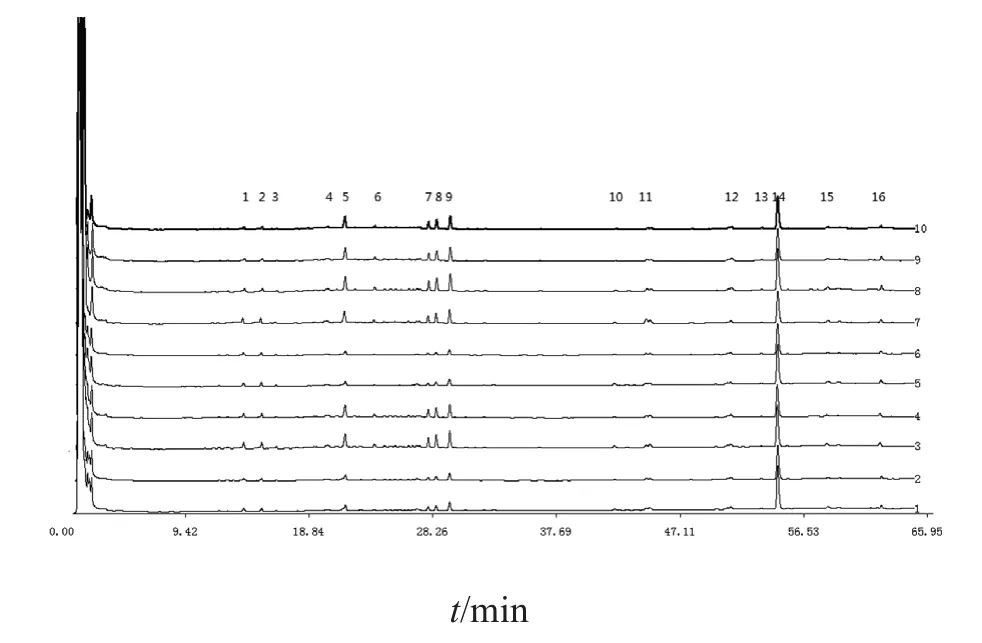
图2 不同批次的泰安黄精指纹图谱比较
2.7 不同产地黄精指纹图谱的比较
由图3可见,山东泰安黄精中共鉴定出16个共有峰,河北黄精中共鉴定出12个共有峰。山东泰安黄精中的1,2,3,6,10号峰在河北黄精中未检测到,河北黄精的3号峰在山东泰安黄精中没有检测到,其余11个峰在泰安黄精和河北黄精中均能检测到,为共有峰。综合对比,泰安黄精和河北黄精的指纹图谱差异明显,可用指纹图谱对泰安黄精和河北黄精进行区分。

图3 山东黄精和河北黄精指纹图谱对比
3 结论与讨论
3.1 黄精成分的定量评价
黄精药材在陕西、河北等地分布较为广泛,通过综合对比山东泰安黄精和河北主产区黄精指纹图谱,表明可通过指纹图谱区分两个产地的黄精。标准品匹配确定6号峰为薯蓣皂苷元,13号峰为人参皂苷Rb1,由于此两种成分在各批次中含量较少,未做指标成分评价。本研究发现5,9,14号峰在12个批次黄精指纹图谱中峰面积均较大,但仍不清楚其成分,可进一步研究其结构和物质确定以完善黄精质量评价。本研究仅通过对比指纹图谱评价黄精质量存在一定局限性,还需结合多糖多指标成分等进行定量分析以做出综合评价[9-10]。
3.2 黄精质量的影响因素
通过泰安黄精10个批次指纹图谱的对比分析,采集于海拔较高的山区的4个黄精批次和其余6个采集于平地的黄精成分含量存在明显差异,表明海拔是影响黄精成分的因素之一。由于本研究采集样品数量有限,其他生长地理环境对黄精成分的影响有待进一步展开研究。
3.3 提取方法及色谱条件的改进
分别对比了超声提取和加热回流提取两种提取方式,超声提取的样品峰较少,本试验选定加热回流方法作为黄精药材指纹图谱供试品溶液的提取方法。取多份同一产地黄精药材各1 g,以相同色谱条件下的色谱峰数目作为考察指标,提取溶液(乙醇φ=50 %,60 %,70 %,80 %,90 %,无水乙醇),提取溶液与样品量比(10倍,15倍,20倍,25倍),加热回流时间(30,60,90,120,150,180,210 min),结果表明,黄精药材用φ=80 %乙醇,20倍其质量条件下加热回流提取3 h,提取效果较好。用安捷伦1260二元高效液相色谱仪,安捷伦 G4212B 二极管列阵检测器经多波长(190~400 nm)考察后确定203 nm为本实验方法的检测波长。同时还考察了不同柱温对分离的影响,结果表明,30 ℃时分离最好。同时用甲醇-水和乙腈-水两种体系等梯度和不同梯度进行洗脱,结果表明,乙腈-水溶液作为流动相,峰形较好,分离度好。在样品处理过程中,热过滤效果明显高于冷却后过滤的效果,初步推测是黄精成分中多糖物质的干扰,有待进一步探讨。

