包埋型纳米零价铁降解水中三氯甲烷和铅(II)试验研究
成 岳,唐伟博,肖治国,余淑贞
(景德镇陶瓷大学 材料科学与工程学院,江西 景德镇 333403)
0 引 言
随着工业的不断发展,环境污染日趋严重,其中水污染最为突出,水污染中尤为突出的就是有机污染物和重金属。纳米零价铁比表面积大、表面能量较高、还原性较强[1],能够有效去除有机污染物[2-4]、重金属[5-7]等水中常见的污染物。纳米材料已经越来越多地受到研究人员的青睐,将纳米材料应用在水体修复[8]和土壤修复当中[9]。但它在实际应用中尚存在一些缺陷,纳米Fe0自身粒径较小而表面活性较强,在接触空气时会被迅速氧化,并在其表面生成一层氧化铁而使其表面失活。同时,纳米Fe0具有易团聚且易被氧化的缺点,降低了纳米Fe0的反应活性,使得纳米Fe0在实际应用中往往很难达到预期的良好效果。
针对以上问题,本试验以羟甲基纤维素(Carboxymethyl cellulose, CMC)为包埋剂,采用流变相法制备CMC包埋型纳米零价铁[10],通过正交试验方法分析溶液pH,三氯甲烷(Trichloromethane,TCM)和铅初始浓度,样品投加量和反应时间等因素对三氯甲烷和铅去除率的影响。
1 实 验
1.1 样品制备
纳米零价铁的制备和CMC包埋纳米零价铁的制备同文献[11-13];
1.2 样品表征
包埋型纳米Fe0的晶相分析 采用德国Bruker公司D8-Advance型XRD衍射仪以Cu靶,Kα为辐射源,管电压为40 千伏,管电流为100 毫安,扫描步长为0.02 °/s,扫描范围为10-70 °;形貌在JEM-2010(HR)透射电子显微镜(日本电子)上进行测定。
1.3 正交试验设计
采用正交试验方法进行试验,选择了5个可能会影响试验结果的因素:pH (A)、不同种类的反应物(B)、初始浓度(C)、投加量(D)和反应时间(E),各因素和水平见表1。
1.4 试验过程和分析方法
称取一定量的CMC、Fe0和包埋型CMC-Fe0加入到一定初始浓度的TCM和Pb(II)溶液模拟废水中,调节pH值,25 ℃条件下震荡反应一定时间后,根据设定的时间取样,通过0.45 μm滤膜过滤后,测定水样中TCM和Pb(II)浓度。
TCM的测定采用顶空气相色谱法[14](浙江福立FULI9790Ⅱ型气相色谱仪)。色谱条件:柱温为45 ℃,进样口温度和检测器温度均为200 ℃,检测器为ECD。根据标准曲线(1)计算得到样品中TCM的浓度(μg/L)

式中,S为色谱峰面积,C为溶液中TCM的质量浓度(mg/L);
Pb(II)浓度的测定采用络合滴定法[15], 溶液中Pb(II)的浓度的计算公式如(2):

式中,C为溶液中铅离子的质量浓度(mg/L);V为滴定用去的EDTA的体积(mL)。
据公式(3)计算Pb(II)的去除率E1:

式中,C0为Pb(II)初始浓度(μg/L),Ct为反应后浓度(μg/L)。
据公式(4)计算TCM的去除率E2:

式中,C0为TCM初始浓度(μg/L),Ct为反应后浓度(μg/L)。
2 结果与讨论
2.1 样品XRD和TEM表征分析
图1为包埋型纳米CMC -Fe0的的XRD分析图谱。由图1可看出,制备出的包埋型纳米CMC- Fe0并没有其他物质的衍射峰出现,说明产品纯度较高,同时也说明纳米Fe0经过CMC包埋之后未被氧化,保证了纳米Fe0的还原能力不损失。
图2为包埋型纳米CMC -Fe0的透射电镜图。由图2可知,包埋型CMC-Fe0分散较为均匀,积聚现象不明显,包埋型CMC-Fe0的颗粒直径在5-10 nm,比表面积较大,有利于CMC包埋纳米Fe0吸表附水中的TCM和铅。而且纳米Fe0颗粒完全被CMC包埋,很好的防止了纳米Fe0被氧化。
2.2 正交试验极差分析
为优化包埋型CMC-Fe0处理水中TCM和Pb(II)的试验条件,采用正交试验法考察pH,反应物,初始浓度,反应物投加量和时间五个因素,并选用五因素三水平18次试验的正交试验表,进行包埋型CMC-Fe0处理水中TCM和Pb(II),记为L18(2×37),每组试验平行进行三次,以包埋型CMC-Fe0处理水中TCM和Pb(II)的去除率作为参考指标,正交试验结果如表2所示。

图1 包埋型纳米CMC -Fe0的 XRD分析图Fig.1 XRD pattern of CMC embed nano zero valent iron

表1 因素水平表Tab.1 Factors and levels

图2 包埋型纳米CMC -Fe0的透射电镜图Fig.2 Transmission electron micrograph of embed nano CMC -Fe0
采用极差分析法来确定影响包埋型CMC-Fe0处理水中TCM和Pb(II)的主要因素。以TCM和Pb(II)的去除率为考察指标,通过极差分析结果可以看出:RB(80.1)>RD(1.2)>RC(1.0)>RE(0.7)>RA(0.1)。五个因素对处理水中TCM和铅的影响程度依次为:反应物(B)>投加量(D)>初始浓度(C)>反应时间(E)>pH(A)。反应物对去除率的影响最大,投加量、初始浓度、反应时间的影响次于反应物,pH的影响最小。为了更好的优化处理条件,还考虑了因素之间的交互作用对处理效果的影响,通过极差分析结果可知:RC×E(1.0)>RC×D(0.70)>RD×E(0.4)。各因素之间的交互作用对处理水中TCM和铅的程度依次为:C×E>C×D>D×E。C和E之间的交互作用的影响最大,C和D之间的交互作用的影响仅次于C和E之间的交互作用,D和E之间的交互作用影响最小。

表2 正交试验结果与分析Tab.2 Results and analysis of orthogonal experiment
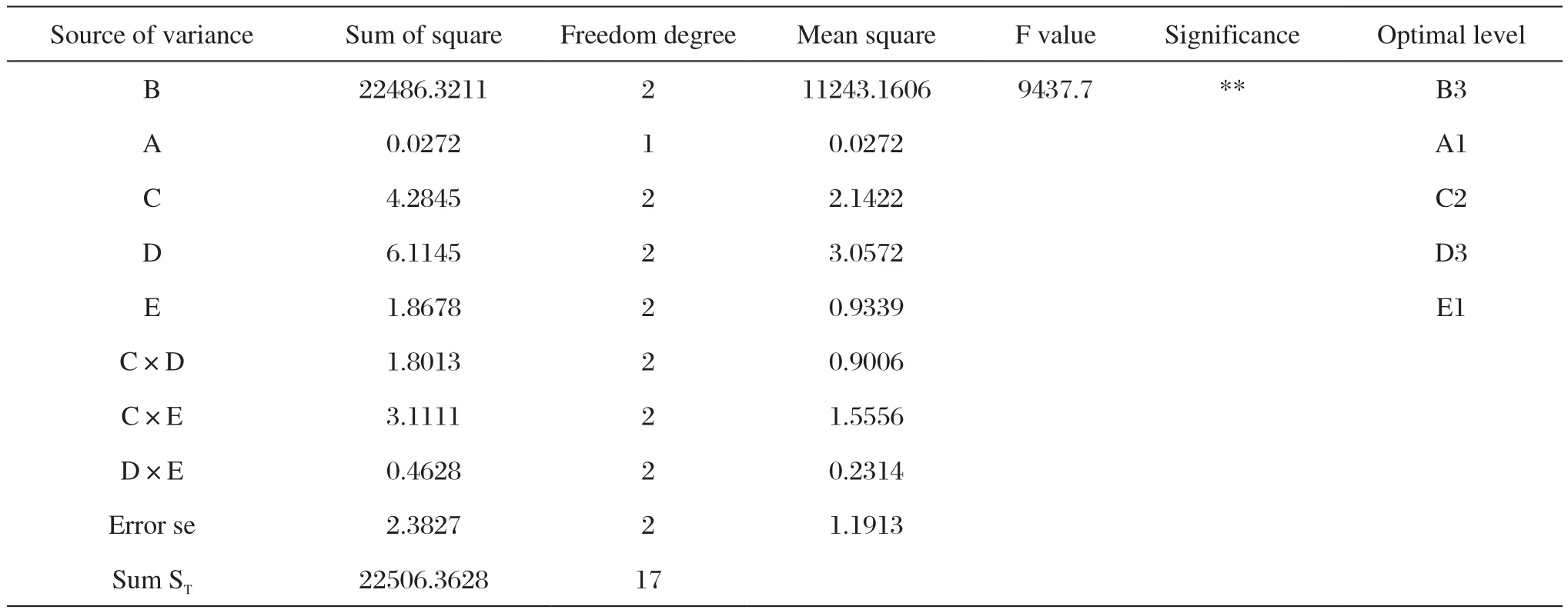
表3 方差分析表Tab.3 Results analysis of variance
2.3 正交试验方差分析
采用方差分析法来确定包埋型CMC-Fe0处理水中TCM和Pb(II)的主要因素,包埋型CMC-Fe0处理水中TCM和Pb(II)的方差分析表如表3所示。
从表3可知,因素B和因素D是显著性因素,对去除率影响比较大,在试验过程中选定合适的反应物和投加量,这样才能得到好的去除效果。
通过极差和方差分析可得试验的最佳因素组合为A1B3C2D3E1,即pH=5,反应时间为3 h,包埋型纳米CMC-Fe0,初始浓度C(CHCl3)=0.4 mg/L,C(Pb(II))=40 mg/L,投加量为1.00g/L,对TCM和铅离子的去除率分别为92.0%和96.5%,总平均去除率为94.3%。在此条件下,进行验证试验,并重复三次。在最佳条件下进行包埋型CMC-Fe0处理水中TCM和Pb(II),经3组平行试验得到TCM和Pb(II)平均去除率分别为96.1%和94.7%,总平均去除率W为95.4%与正交试验的结果接近,且去除率高,验证了所选取条件的合理性。
2.4 降解机理分析
包埋型CMC-Fe0的粒径比普通铁粉要小很多,比表面积大,还原能力强,主要是通过氧化还原反应降解水中TCM和Pb(II),能够得到良好的去除效果。本实验采用CMC包埋的形式,使得纳米Fe0周围形成一层保护膜,不易被空气中的氧化剂氧化,从而达到更高脱氯效率。包埋型CMC-Fe0去除TCM和Pb(II)的反应过程中,纳米颗粒均匀的分散在水溶液中,经过一段时间其表面的包埋剂开始溶解,使Fe0部分暴露出来,一部分同水和其中的溶解氧发生反应,过程如下:

零价铁和水中TCM和铅的反应如下:

Fe0-H2O体系反应生成的H2亦可以使TCM脱氯,反应方程式如下:

3 结 论
(1)反应物和反应物投加量是包埋型纳米CMCFe0处理水中TCM和Pb(II)的主要影响因素,反应物对处理效果的影响最大,使用CMC,TCM和Pb(II)的去除率较低,使用Fe0和CMC-Fe0有利于TCM和Pb(II)的降解。
(2)初始浓度和时间的交互作用,对包埋型CMC-Fe0处理水中TCM和Pb(II)的影响较为显著。在投加量一定时,减小初始浓度和延长反应时间,有利于还原剂与水中污染物充分接触,使反应更彻底,降解效果更好。
(3)在试验中,对反应物和反应物投加量进行控制,得到最佳的反应条件A1B3C2D3E1,即pH=5,反应时间为3 h,CMC包埋Fe0,初始浓度C(CHCl3)=0.4 mg/L,C(Pb(II))=40 mg/L,投加量为1.00 g/L进行了验证试验,对TCM和Pb(II)的去除率分别为96.1%和94.7%,总去除率为95.4%。
参考文献:
[1]GILLHAM R W, O'HNESIN S F.Enhanced degradation of halogenated aliphatic by zero-valent iron [J].Groundwater,1994,32(6): 958-967.
[2]CHEN Z X, JIN X Y, CHEN Z L, et al.Removal of methyl orange from aqueous solution using bentonite-supported nanoscale zero-valent iron [J].Journal of Colloid and Interface Science, 2011, 363: 601–607.
[3]CHEN Z X, CHENG Y, CHEN Z L, et al.Kaolin-supported nanoscale zero-valent iron for removing cationic dye-crystal violet in aqueous solution [J].J Nanopart Res, 2012, 14: 899.
[4]LIU X W, CHEN Z X,CHEN Z L, et al.Remediation of Direct Black G in wastewater using kaolin-supported bimetallic Fe/Ni Nanoparticles [J].Chemical Engineering Journal, 2013, 223:764–771.
[5]SHI L N, ZHOU Y, CHEN Z L, et al.Simultaneous adsorption and degradation of Zn2+and Cu2+from wastewaters using nanoscale zero-valent iron impregnated with clays [J].Environ Sci Pollut Res, 2013, 20: 3639–3648.
[6]HUANG R H, YANG B C, WANG B, et al.Removal of chromium (VI) ions from aqueous solutions by N-2-hydroxypropyl trimethyl ammonium chloride chitosan-bentonite[J].Desalination and Water Treatment, 2011, 50: 329-337.
[7]BRIJESH S K, RAJEEV C C.NZVI based nanocomposites:Role of noble metal and clay support on chemisorptive removal of Cr(VI) [J].Journal of Environmental Chemical Engineering,2013, 1: 320–327.
[8]罗婷, 蒋珍茂, 任志杰, 等.树脂基纳米零价铁复合材料的制备及其去除重金属铅Pb(Ⅱ)的性能研究[J].环境工程, 2015, 05:1-4+80.LUO T, JIANG Z M, REN Z J, et al.Environmental Engineering,2015, 05: 1-4+8 (in Chinese).
[9]韩晓琳.活性炭载纳米零价铁体系去除水和土壤中的多氯联苯[D].华东理工大学, 2014.
[10]成岳, 焦创, 刘海江.流变相法制备包覆型零价纳米铁及其表征[J].化学研究与应用, 2012, 03: 409-413.CHENG Y, JIAO C, LIU H J.Chemical Research and Application, 2012, 03: 409-413.
[11]UZUM C, SHAHWAN T, EROLU A E, et al.Synthesis and characterization of kaolinite-supported zero-valent iron nanoparticles and their application for the removal of aqueous Cu2+and Co2+ions [J].Appl Clay Sci, 2009, 43: 172–181.
[12]MANNINNG B A, KISKER J R, KWON H, et al.Spectroscopic investigation of Cr (III) and Cr (VI) treated nanoscale zerovalent iron [J].Environ Sci Technol, 2007, 41:586–592.
[13]樊文井, 成岳, 焦创, 等.流变相法制备包裹型Starch/Fe0及去除水中Cr(Ⅵ)的反应动力学研究[J].功能材料, 2014, 19:19035-19039.FAN W J, CHENG Y, JIAO C, et al.Functional Material, 2014,19: 19035-19039 (in Chinese).
[14]陈小丽, 陈敏, 梁春霞.顶空气相色谱法测定水中三氯甲烷及四氯化碳[J].中国热带医学, 2009, 01: 155-156.CHEN X L,CHEN M, LIANG C X.China Tropical Medicine,2009, 01: 155-156
[15]李方文, 魏先勋, 李彩亭, 等.络合滴定法测定废水中铅离子的浓度[J].工业水处理, 2002, 10: 38-39.LI F W, WEI X X, LI C T, et al.Industrial Water Treatment,2002, 10: 38-39.

