腹腔镜下G lisson蒂横断式解剖性肝切除的应用价值
(湖南中医药大学第一附属医院 肝胆外科,湖南 长沙 410007)
手术微创化是现今外科手术的一大发展趋势,腹腔镜手术作为微创外科的代表,已广泛用于腹部外科领域,并取得良好效果,但由于肝脏双重血供易出血、术野暴露困难、术中气体栓塞和肝脏内管道解剖结构复杂等原因导致腹腔镜肝脏外科发展缓慢。近年来,随着医学影像学的发展、腹腔镜外科手术技巧的成熟、肝内各管道结构解剖学特点的进一步了解及腹腔镜专用手术器械的不断更新,腹腔镜肝脏外科技术在迅速发展。本院2012年1月-2015年12月行完全腹腔镜下Glisson蒂横断式解剖性肝切除20例,取得了较好疗效。现报道如下:
1 资料和方法
1.1 一般资料
我科2012年1月-2015年12月行完全腹腔镜下Glisson蒂横断式解剖性肝切除20例。其中,原发性肝癌12例、肝内胆管结石4例、肝脏血管瘤2例、肝脏局灶结节性增生1例、肝腺瘤1例。20例患者中男14例,女6例,年龄(51.75±7.46)岁。肝功能Child-Pugh分级全部为A级。病灶直径3~8 cm。
1.2 手术方法
常规采用气管插管静吸复合全麻,患者仰卧,取头高脚低位,病变位于右肝者,右侧垫高20°~30°,脐周作1 cm切口,建立气腹,腹压维持在13~15 mmHg(1 mmHg=0.133 kPa),Trocar分布围绕病变部位呈扇形分布,一般采用五孔法,探查腹腔,左半肝切除及右肝段切除时常规先行胆囊切除。
左肝手术(左半肝、左外叶切除)手术步骤:①超声刀(美国强生,型号GEN11)切断肝圆韧带、镰状韧带、左冠状韧带、左三角韧带及肝胃韧带及部分右冠状韧带;②解剖左肝Glisson蒂,控制入肝血流:上提肝圆韧带,沿肝门板上方切开部分前腹膜,超声刀或者吸引器钝性分离肝门板,显露左、右肝蒂汇合部Glisson鞘之间的间隙,解剖出左肝蒂(附图A~C),左外叶切除时,需沿矢状部左侧解剖分离出Ⅱ、Ⅲ段Glisson蒂,可吸收生物夹夹闭后离断;③解剖第二肝门,控制出肝血流:肝内解剖出肝左静脉主干,靠近其根部用切割闭合器(泰科,型号030449)切断(附图D);④离断肝实质:按肝段、肝叶Glisson蒂阻断后的缺血标志,从肝脏面开始,在预切线上用超声刀切开肝实质,肝内所遇管道用生物夹或钛夹夹闭后离断;⑤肝创面处理:创面渗血可电凝止血,对明显的出血和胆漏予以缝扎;⑥标本取出:切除标本装入标本袋,良性疾病标本破碎后经扩大Trocar口取出,恶性疾病标本经上腹部Trocar孔扩大切口完整取出,冲洗后常规放置腹腔引流管。
右肝段切除步骤:超声刀切断肝周韧带,游离肝右叶,解剖第一肝门,右半肝切除解剖右肝蒂方法同上,如行Ⅴ、Ⅵ段等肝段切除,手术需超声刀破碎浅层肝组织后再解剖分离出肝段Glisson蒂离断,后续步骤同上。
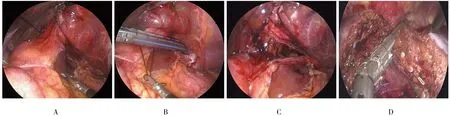
附图 左肝手术步骤Attached fig.Surgical procedure of left liver
2 结果
2.1 手术结果
20例患者均顺利完成手术,无中转开放手术,根据Couinaud分段法,其中左半肝(Ⅱ、Ⅲ、Ⅳ段)切除6例、左外叶(Ⅱ、Ⅲ段)切除5例、右半肝(Ⅴ、Ⅵ、Ⅶ、Ⅷ段)切除3例、右前叶下段(Ⅴ段)切除1例、右后叶下段(Ⅵ段)切除2例和右后叶(Ⅵ、Ⅶ段)切除3例。手术时间(144.77±24.68)min,出血量(279.00±132.70)ml,术中未发生不能控制的出血,切除肝脏重量最大985 g,最小76 g。
2.2 术后情况
全组患者术后第1天均可自行下地活动,进流质饮食,术后1 d拔除胃肠减压管,术后3~7 d拔除腹腔引流管,术后住院(8.22±1.40)d,术后发生胆漏及膈下脓肿各1例,均经非手术治疗痊愈,未发生术后出血等其他严重并发症,无住院死亡。
3 讨论
如何控制出血及在肿瘤根治性切除的基础上最大限度保留正常肝组织一直是肝脏外科医生面临的难题,为减少术中出血,传统的方法是用Pringle法阻断第一肝门,但该方法常会造成健侧肝脏的缺血-再灌注损伤[1]。解剖性肝切除是以肝段或亚肝段为肝切除的基本单位,该方法仅仅阻断患侧肝组织的入肝血流,对剩余肝组织影响小,能有效控制术中出血,TAKASAKI[2]于1998年首次报道了Glisson蒂横断式肝切除术,根据所要切除的目标肝段阻断相应的Glisson鞘,相应肝段出现缺血分界线后行解剖性肝段或肝叶切除。国内许多学者报道开腹行Glisson蒂横断式肝切除术取得良好的治疗效果[3-5],笔者也认为该方法操作相对简单,能减少肝门解剖时间,同时可降低肝门部胆管及血管损伤发生率,在肿瘤切除前阻断相应肝蒂,能减少术后复发及肝内转移机会[6]。
腹腔镜技术在其他外科领域发展迅速且日趋成熟,但在肝脏外科领域仍旧发展缓慢,其原因是:①手术视野暴露困难,尤其肝Ⅶ、Ⅷ段及尾状叶切除;②肝脏血供丰富,肝实质内管道众多,常有变异,精细解剖较困难;③创面压迫、缝合等止血技术受限,出血可能导致中转开放手术;④常规开放手术的肝门阻断技术难以应用。因此,腹腔镜肝脏切除术仍被认为是难度和风险较大的术式[7]。笔者将Glisson蒂横断式解剖肝门技术应用在腹腔镜肝切除术中取得了良好的治疗效果,本组20例患者均顺利完成手术,无中转开放手术,术后患者恢复良好,未发生术后出血等其他严重并发症。
Glisson蒂横断式肝切除术,该方法是建立在对肝脏解剖学的深入了解之上提出的,门静脉及肝动脉及胆管共同包绕在Glisson鞘内,在肝门处分成三支粗大的分支,分别进入肝左叶、右前叶及右后叶,进一步分支支配相应的肝段或亚肝段,TAKASAKI[2]将肝脏分为左段(Ⅱ、Ⅲ、Ⅳ段)、中段(Ⅴ、Ⅷ段)、右段(Ⅵ、Ⅶ段)及尾状叶4部分。该方法的技术要点和难点是肝内Glisson蒂的解剖,应先降低肝门板,肝门板下降才能显示各叶Glisson鞘,循肝门板与肝实质之间的无血管间隙操作,对于右肝前叶或后叶切除,需解剖出二级肝蒂,切除胆囊后,清除胆囊三角区的结缔组织,沿肝蒂走向切开薄层肝实质即可暴露右前叶及右后叶肝蒂。对于肝左叶切除,可直接自脐静脉窝左侧分离出Glisson系统左支发出的三级肝蒂。
有效控制和处理术中出血是腹腔镜肝切除术成功的关键[8],相对于开腹手术,腹腔镜肝切除不能用手灵活、及时地阻断肝血管,而腹腔镜下肝切除尚缺乏较为理想的器械,导致非解剖性大块肝切除时断面的出血处理困难,是腹腔镜肝切除失败的主要原因之一[9]。对于腹腔镜肝切除术,传统的肝门解剖技术操作复杂,且有导致肝门血管破裂大出血的可能,腹腔镜Glisson蒂横断式肝切除通过按肝叶、肝段的解剖学标志准确控制入肝血流,不影响健侧肝组织的血供,在没有大的血管的界面中断肝可明显减少术中出血量。术前精确的影像学评估是必不可少的,CT或磁共振影像分析了解肝门部血管及胆管的变异,避免保留侧血管及胆管的误伤。3条主肝静脉壁是判断达到正确切肝界线的重要解剖标志,可结合肝脏表面标记的边界离断肝组织[10]。
综上所述,随着手术经验的积累及手术器械、手术方法的改进,腹腔镜肝切除术将逐步得到推广,腹腔镜肝切除的适应证越来越广[11],本组资料显示,腹腔镜Glisson蒂横断式肝切除能较好地控制腹腔镜肝切除时的出血情况,确定切缘,具有安全有效等优点,是较为理想的腹腔镜肝切除术式。
[1]KATO M,SAWADA T,KITA J,et al.Erythropoietin ameliorates early ischem ia-reperfusion in jury fo llow ing the pringle maneuver[J].World J Gastroenterol,2010,16(38): 4838-4845.
[2]TAKASAKI K.Glissonean pedicte transection method for hepatic resection:a new concept of liver segmentation[J].J Hepatobiliary Pancreat Surg,1998,5(3): 286-291.
[3]唐诗彬,陈小伍,吴路杨,等.Glisson鞘解剖性肝切除术治疗肝内胆管结石[J].中华肝脏外科手术学电子杂志,2016,5(3): 148-152.
[3]TANG S B,CHEN X W,WU L Y,et al.Anatom ical hepatectomy with Glissonian approach for hepatolithiasis[J].Chin J Hepat Surg: Electronic Edition,2016,5(3): 148-152.Chinese
[4]吴宝强,江勇,朱峰,等.Glisson蒂横断式肝切除在解剖性肝切术中的应用[J].肝胆胰外科杂志,2013,25(3): 185-187.
[4]WU B Q,JIANG Y,ZHU F,et al.Application of Glisson pedicle blood occlusion in the process of precision liver resection[J].Journal of Hepatopancreatobiliary Surgery,2013,25(3): 185-187.Chinese
[5]黎焕,江勇,吴宝强,等.Glisson蒂横断式肝切除术治疗肝占位性疾病的初步应用[J].肝胆胰外科杂志,2012,24(6): 447-450.
[5]LI H,JIANG Y,WU B Q,et al.The prelim inary application of Glissonean pedicle transection method for hepatic resection in the treatment of hepatic space-occupying lesions[J].Journal of Hepatopancreatobiliary Surgery,2012,24(6): 447-450.Chinese
[6]谭新华,莫世发,韦杨年,等.美兰染色标记法联合Glisson蒂横断式肝切除与非规则性肝切除治疗肝癌的临床疗效[J].中国癌症防治杂志,2015,7(2): 104-108.
[6]TAN X H,MO S F,WEI Y N,et al.Comparison of methylene blue staining notation-Glissonean pedicle transection with irregular liver resection for the treatment of hepatocellular carcinoma[J].Chin J of Oncol Prev and Treat,2015,7(2): 104-108.Chinese
[7]X IE K L,ZENG Y,WU H.Hepatic trisectionectom y for hepatocellular carcinom a using the G lisson pedicle method combined with anterior approach[J].World J Surg,2014,38(9): 2358-2362.
[8]蔡柳新,李振宇,方哲平,等.前下入路肝后间隙解剖法处理肝短静脉在腹腔镜右半肝切除中的应用[J].中华医学杂志,2013,93(28): 2179-2182.
[8]CAI L X,LI Z Y,FANG Z P,et al.Application of anterior-inferior approach through retrohepatic tunnel for dissecting short hepatic veins in laparoscopic right hemihepatectomy[J].National Medical Journal of China,2013,93(28): 2179-2182.Chinese
[9]MATSUKAWA H,SHIOZAKI S,SATOH D,et al.Experiences of laparoscopic repeat hepatectomy for recurrent hepatic cancer after open hepatectomy[J].Gan To Kagaku Ryoho,2014,41(12): 2098-2100.
[10]仇毓东,周建新,冯伟,等.精准肝蒂离断技术在肝细胞肝癌解剖性肝段切除患者中的应用[J].中华肝脏外科手术学电子杂志,2013,2(4): 14-18.
[10]QIU Y D,ZHOU J X,FENG W,et al.Precise pedicle transection in anatom ical hepatic segm entectom y of hepatocellu lar carcinoma[J].Chin J Hepat Surg: Electronic Edition,2013,2(4): 14-18.Chinese
[11]郑树国,田驹.腹腔镜肝切除适应症再探讨[J].中国普外基础与临床杂志,2013,20(4): 352-355.
[11]ZHENG S G,TIAN J.Further discussion of indications for laparoscopic hepatectomy[J].Chin J Bases Clin General Surg,2013,20(4): 352-355.Chinese

