盐酸贝那普利片近红外光谱定性分析模型的建立
金 鹏,刘 艳,卜媛媛
(江苏省淮安市食品药品检验所,江苏 淮安 223300)
盐酸贝那普利片近红外光谱定性分析模型的建立
金 鹏,刘 艳,卜媛媛
(江苏省淮安市食品药品检验所,江苏 淮安 223300)
目的 建立盐酸贝那普利片的定性分析模型。方法 利用近红外漫反射技术采集全国4家生产企业61批样品的近红外光谱,利用化学计量学分析软件OPUS建立2层定性分析模型串联确证模型,并验证模型的准确性和专属性。结果 模型的准确性和专属性好,能准确识别21批验征集样品,区分出4个结构类似物片、假冒A企业样品及21个非结构类似物片。结论 该试验中建立的模型能快速、准确识别盐酸贝那普利片的真伪,适用于药品检测车对该品种的现场快速检测。
近红外光谱;盐酸贝那普利片;定性分析模型;快速鉴别
盐酸贝那普利是血管紧张素转换酶抑制剂(ACEI)类药物,适用于高血压、充血性心力衰竭等,临床疗效佳,安全性好,也是首个适用于肝、肾功能不全高血压患者的ACEI类药[1-3]。该药自2000年在我国上市以来,一直备受瞩目,并广泛应用于临床,被江苏省列入省级基本药物。同时,近年来也有不法分子为牟取暴利,在市场上制售假冒知名企业的盐酸贝那普利片,严重损害了患者和企业的利益。鉴于药品检测车近红外鉴别系统暂未装载该品种通用定性模型的现状,本试验中采集全国4家生产企业61批样品的近红外光谱,利用近红外漫反射技术结合化学计量学分析软件OPUS,建立2层定性分析模型串联确证模型,经过准确性和专属性验证,能快速、准确地识别样品的真伪,适用于药品检测车对该品种的现场快速检测。现报道如下。
1 仪器与试药
1.1 仪器
Matrix-F型近红外光谱仪,1.5 m光纤探头;OPUS 5.0英文版分析软件(德国布鲁克公司)。
1.2 试药
所有盐酸贝那普利片均经实验室法定方法[4-7]检验合格。4家企业(A,B,C,D)61批样品(规格为 5 mg或10 mg)来自江苏省2012年评价性抽验;盐酸贝那普利对照品(批号为100768-201102)购自中国食品药品检定研究院;卡托普利片(规格为每片 25 mg)、赖诺普利片(规格为每片 10 mg)、雷米普利片(规格为每片2.5 mg)、马来酸依那普利片(规格为每片 5 mg)4 种结构类似物片各1批,均来自日常监督抽验;4批假冒A企业样品由其他药检所提供;21个非结构类似物片来自日常快检样品。
2 方法与结果
2.1 光谱采集
每批样品随机抽取6片,用漫反射光纤探头压住药片,每片测定1次,取平均光谱作为建模光谱。光谱采集条件:以内置背景为参考;扫描范围为4 000~12 000 cm-1;扫描次数为32次;分辨率为8 cm-1;采样模式为漫反射方式;温度为25℃;相对湿度为60%。
2.2 定性分析模型建立
2.2.1训练集和验证集样品划分
对4家企业61批样品的近红外平均光谱进行聚类分析。谱段:全谱;预处理方法:矢量归一化法;光谱距离:欧式距离;聚类算法:离差平方和法(Ward′s algorithm)。由聚类分析结果可见,样品光谱较明显地被聚为两类,A企业和B企业的样品为一类,C企业和D企业的样品为一类。选择A企业和B企业的样品20批、C企业和D企业的样品20批作为训练集样品,剩下的21批样品,卡托普利片、赖诺普利片、雷米普利片、马来酸依那普利片各1批,4批假冒A企业样品及21批非结构类似物片作为验证集样品。
2.2.2谱段选择
从片剂光谱中鉴别出活性成分的特征光谱是建立片剂定性分析模型的关键[8]。首先要考虑避开7 100~7 500,5 000~5 500 cm-1波数处的水峰及 7 200 cm-1附近的滑石粉峰,将4个企业各1批样品与盐酸贝那普利对照品近红外光谱经矢量归一化处理后观察光谱的差异,结果见图1。可见,图谱在 6 000~5 700 cm-1和4 500~4 200 cm-1谱段范围匹配程度较好,受辅料的影响最小,能基本反映活性成分的差异;将4家企业训练集样品、卡托普利片、赖诺普利片、雷米普利片、马来酸依那普利片的平均光谱经一阶导数结合矢量归一化处理后观察光谱的差异,结果见图2。可见,图谱在7 000~6 900 cm-1谱段范围内最大限度体现了5个品种光谱的差异,故将 7 000~6 900,6 000~5 700,4 500~4 200 cm-1谱段范围作为定性分析模型的建模谱段。
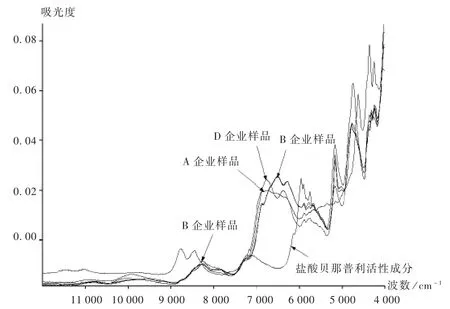
图1 4家企业各1批样品与盐酸贝那普利对照品近红外光谱图(矢量归一化)
2.2.3预处理方法选择
由于样品的性质、散射光、杂散光以仪器响应限度、人工操作的影响等,均会导致光谱的基线漂移和重复性差,因此必须对原始光谱进行预处理[9-10]。采用不同的预处理方法,对比各种方法处理后光谱的差异。由图3至图5可见,样品光谱经过矢量归一化法结合一阶或二阶导数处理后,既消除了基线漂移,降低了背景及噪声干扰,又增加了重叠峰的分辨率,使样品近红外光谱的特征信息更加突出。因此选择一阶导数或二阶导数结合矢量归一化法作为预处理方法。
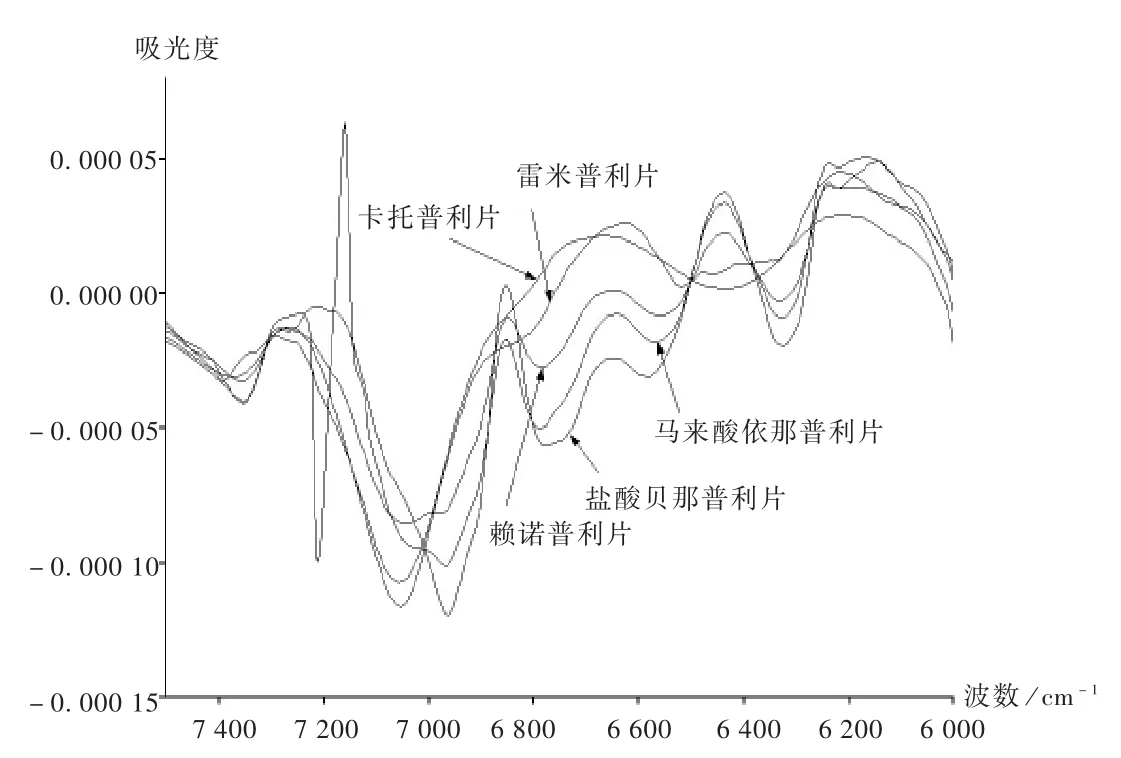
图2 盐酸贝那普利片等5个品种近红外光谱图(一阶导数+矢量归一化)
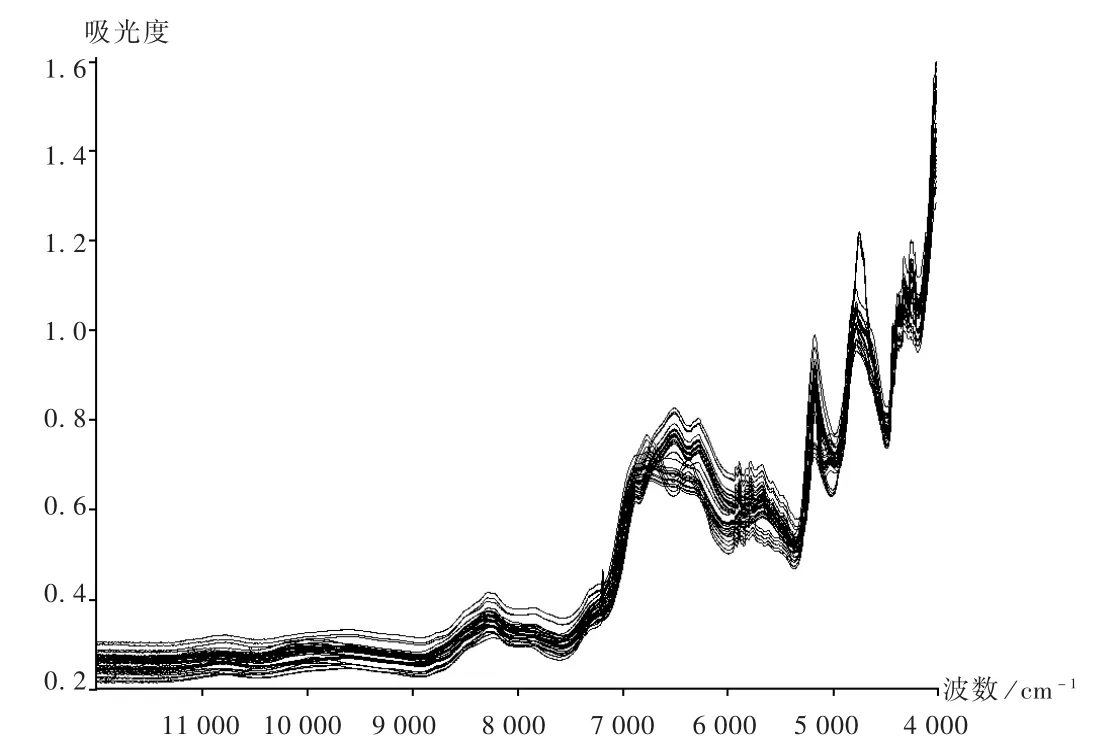
图3 4家企业样品近红外光谱图
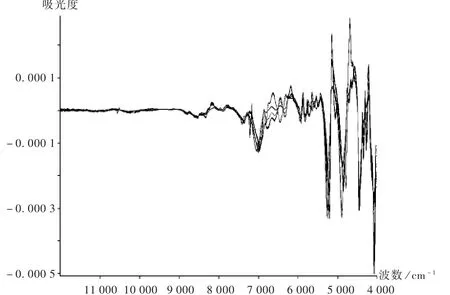
图4 4家企业样品近红外光谱图(一阶导数+矢量归一化)
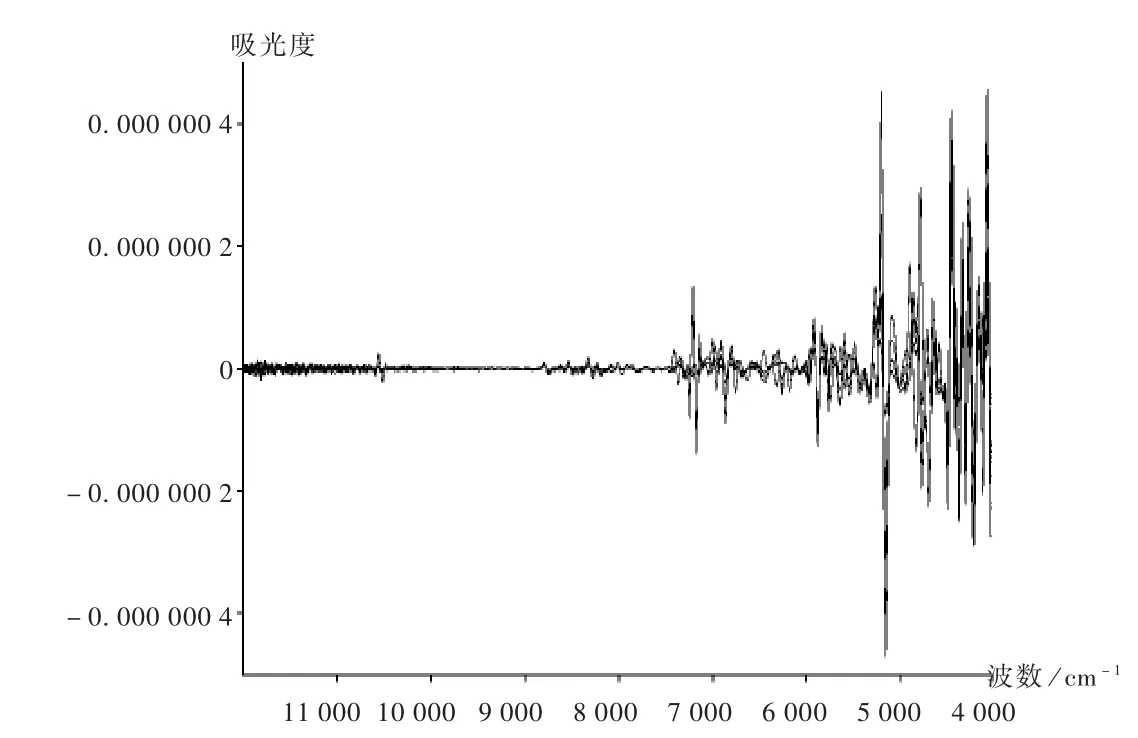
图5 4家企业样品近红外光谱图(二阶导数+矢量归一化)
2.2.4定性分析模型的建立[8-13]
通过不断优化谱段、预处理方法、平滑点数及光谱距离计算方法,最终确定盐酸贝那普利片定性分析模型。将4家企业训练集样品、卡托普利片、赖诺普利片、雷米普利片、马来酸依那普利片的平均光谱进行聚类分析,谱段为4 200~10 000 cm-1,预处理方法为二阶导数+矢量归一化(17点平滑),光谱距离计算方法选择因子法,因子数为2~3。由聚类分析结果可见,样品光谱较明显地被聚为2类,盐酸贝那普利片、赖诺普利片、马来酸依那普利片为一类,卡托普利片和雷米普利片为一类(见图6),故将模型分为盐酸贝那普利片、赖诺普利片和马来酸依那普利片、卡托普利片和雷米普利片3组,2层。
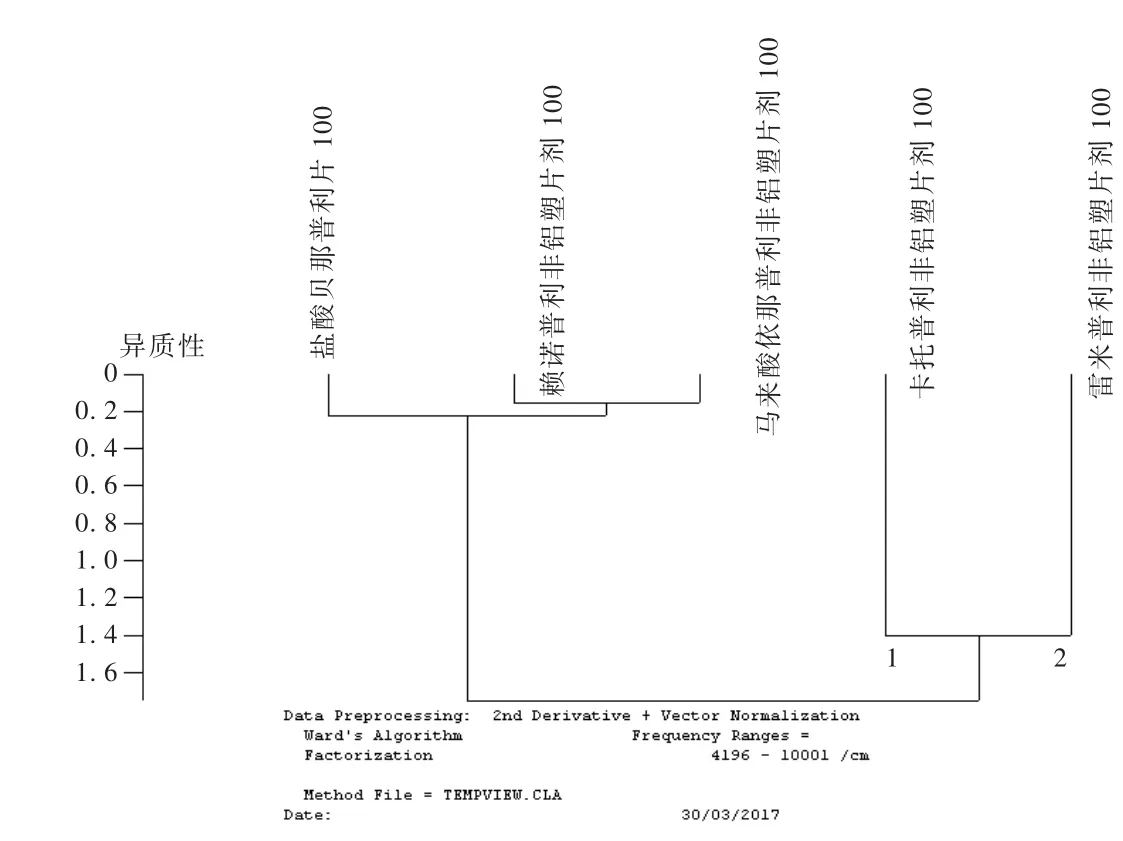
图6 盐酸贝那普利片等5个品种聚类分析图
第1层参数:谱图预处理选择二阶导数+矢量归一化(17 点平滑),谱段选择 6 001.6 ~5 696.9 cm-1和4 501.2 ~ 4 196.5 cm-1,光谱距离计算方法选择因子法,因子数为2,3组样品的阈值、标准偏差及平均距离见表1。计算结果,卡托普利片和雷米普利片组选择性值(S)为 2.21(应大于 1),盐酸贝那普利片组、赖诺普利片和马来酸依那普利片组 S均小于1,表明赖诺普利片、马来酸依那普利片不能被唯一鉴别,故将混淆品种放入第2层继续分离。
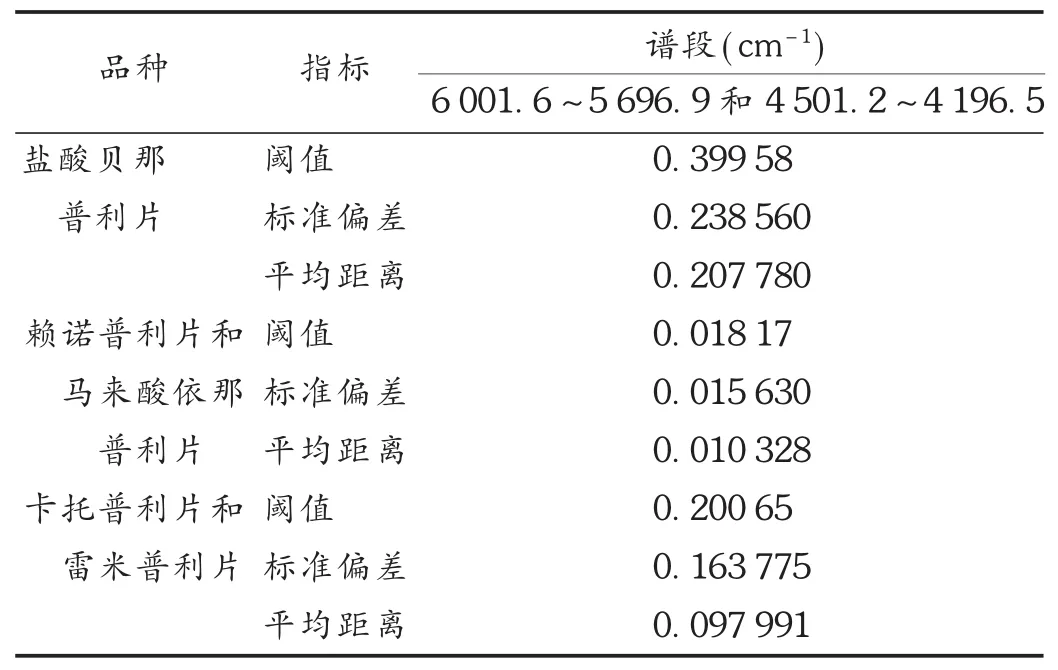
表1 第1层3组样品的阈值、标准偏差及平均距离
第2层参数:谱图预处理选择一阶导数+矢量归一化(17 点平滑),谱段选择 7 000.6 ~6 896.4.0 cm-1和4 501.2 ~4 381.6 cm-1,光谱距离计算方法选择因子法,因子数为2,两组样品的阈值、标准偏差及平均距离见表2。计算结果,盐酸贝那普利片组和赖诺普利片、马来酸依那普利片组 S分别为 2.21和 2.87(应大于 1),盐酸贝那普利片、赖诺普利片和马来酸依那普利片能够实现唯一识别。
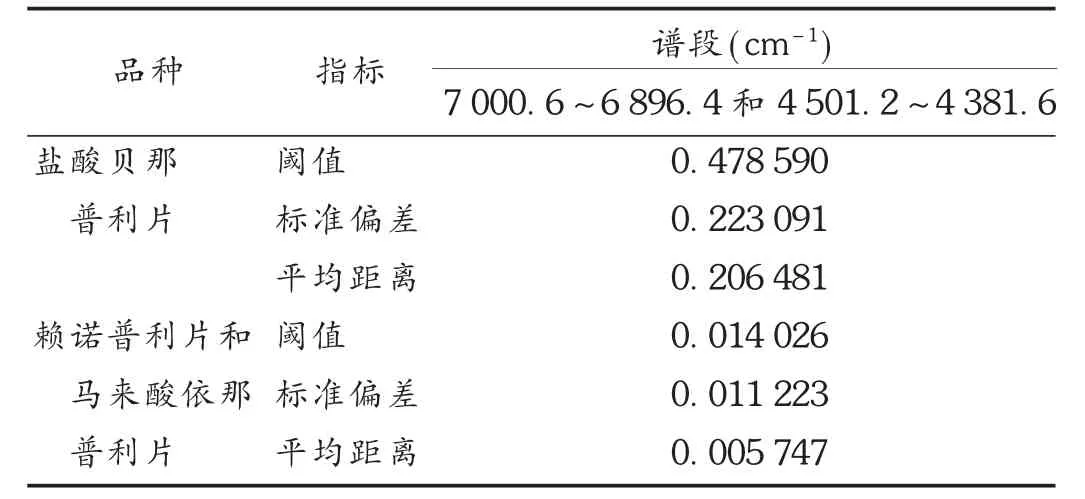
表2 第2层两组样品的阈值、标准偏差及平均距离
2.3 定性分析模型验证
准确性:选取验证集中的样品,调用定性分析模型进行测试,21批盐酸贝那普利片鉴别结果为盐酸贝那普利片,卡托普利片、赖诺普利片、雷米普利片、马来酸依那普利片均能实现唯一识别,说明模型准确性良好。
专属性:用验证集中的4批假冒A企业样品和21批非结构类似物,对所建立定性分析模型的专属性进行进一步评价。4批假冒A企业样品鉴别结果均为非盐酸贝那普利片,但发现一些活性成分含量较低的品种,如吲达帕胺片、盐酸吡格列酮片、瑞格列奈片、美洛昔康片、格列吡嗪片、非洛地平片、多潘立酮片等9个品种被错误识别为盐酸贝那普利片,说明模型对活性成分含量较低的品种鉴别能力较差。
2.4 定性分析模型调整
确定两步鉴别流程:由于在建模选择因子谱时仅考虑模型涉及品种的相互鉴别问题,加之盐酸贝那普利片在模型中的阈值较大,使得一些原本具有差异但在模型中未涉及的样品被错识鉴别,故采用两步鉴别方案,在已建好的模型基础上,再串接相应的确证模型,主要用于区分模型中的品种与模型未涉及的其他品种,进而对已建好的模型进行进一步确证。
确证模型的建立:模型分为盐酸贝那普利片、盐酸贝那普利对照品两组,谱图预处理选择一阶导数+矢量归一化(17 点平滑),谱段选择 6 001.6 ~5 696.9 cm-1和 4 501.2 ~ 4 196.5 cm-1,光谱距离计算方法选择因子法,因子数为1~2,两组样品的阈值、标准偏差及平均距离见表3。结果盐酸贝那普利片及21个非结构类似物片能被正确识别。
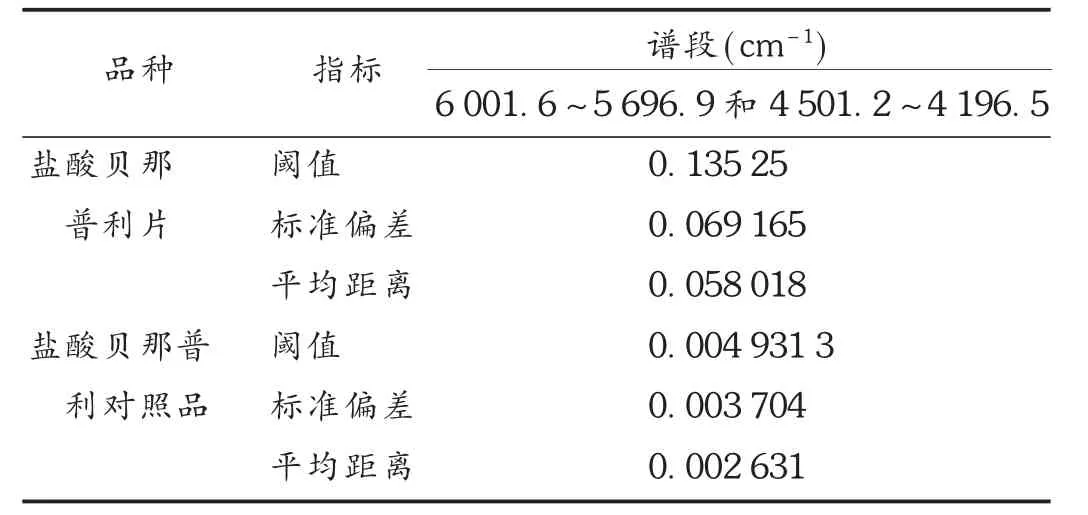
表3 确证模型两组样品的阈值、标准偏差及平均距离
串联模型的验证:在定性分析模型专属性验证中,有9个非结构类似物片被错误识别为盐酸贝那普利片,增加确证模型后,21个非结构类似物片均被正确识别为非盐酸贝那普利片。

3 讨论
近年来,近红外漫反射光谱法结合化学计量学的深入研究,在药物分析领域得到迅速发展和广泛应用,2005年版、2010年版及2015年版《中国药典》均已将“近红外分光光度法指导原则”[14-16]列入。本试验中收集的4家企业的样品均为双铝塑包装,本着“样品无损”的原则,通过隔铝塑测得近红外光谱,发现铝塑的干扰较大,样品的特征吸收明显减少,因此需拆开双铝包装直接接触样品测定其近红外光谱。片剂通常含有较多辅料,在制剂过程中通常需要经过混料、制粒、干燥等多种工艺过程;不同企业的产品,由于生产工艺、辅料种类和片子形状等均有不同,造成其近红外光谱存在差异,本试验通过选择盐酸贝那普利片的特征谱段及预处理方法,消除了不同厂家生产工艺和辅料等方面的差异,在建立定性分析模型时,选择了4个结构类似物片和21个非结构类似物片,确保一定的准确性和专属性,能准确、快速地鉴别盐酸贝那普利片的真伪。通过查询国家食品药品监督管理总局数据库,盐酸贝那普利片国内共有5家生产企业,8个批准文号,此次参与建模样品涉及4家生产企业,6个批准文号,样品范围广,模型验证良好,可装载于本所药品检测车近红外鉴别系统中,填补系统中无该品种模型的空白,用于该品种的现场快速检测。
[1]郑春忠.盐酸贝那普利药理与临床应用[J].海峡药学,2007,19(8):99 - 101.
[2]孙西征,林文清,陈代勇,等.抗高血压药物盐酸贝那普利的研究进展[J].西南国防医药,2003,13(2):216 - 218.
[3]李东军,黄 明.盐酸贝那普利片治疗原发性高血压动态血压变化观察[J].吉林医学,2009,30(9):818 - 819.
[4]YBH10332005,国家药品标准[S].
[5]YBH05862004,国家药品标准[S].
[6]YBH01662005,国家药品标准[S].
[7]YBH13652004,国家药品标准[S].
[8]胡昌勤,冯艳春.近红外光谱法快速分析药品[M].北京:化学工业出版社,2009:268 -269.
[9]褚小立,袁洪福,陆婉珍.近红外分析中光谱预处理及波长选择方法进展与应用[J].化学进展,2004,16(4):528 -542.
[10]高荣强,范世福,严衍禄,等.近红外光谱的数据预处理研究[J].光谱学与光谱分析,2004,24(12):1563 -1565.
[11]边振甲.药品快速检测技术研究与应用[M].北京:化学工业出版社,2013:35-85.
[12]韩 莹,曾文珊,赖衍清,等.采用最近邻法建立三磷酸腺苷二钠片通用型近红外定性模型[J].中国药事,2015,29(3):309 - 312.
[13]王 宇,黄巧巧,洪利娅.西洛他唑片近红外光谱定性分析模型的建立 [J].海峡药学,2015,27(8):50 - 52.
[14]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2005:附录185.
[15]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录208.
[16]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:379-380.
Establishment of Near-Infrared Spectroscopy Qualitative Model for Benazepril Hydrochloride Tablets
Jin Peng,Liu Yan,Bu Yuanyuan
(Huaian Institute for Food and Drug Control,Huaian,Jiangsu,China 223300)
Objective To establish a qualitative analysis model for Benazepril Hydrochloride Tablets.Methods Near- infrared diffuse reflectance spectrophotometry (NIRDRS) was adopted to collect near- infrared spectra (NIRS) of 61 batches of samples from 4 manufacturers,chemometrics spectral aanalysis software OPUS was adopted to establish the two- layer qualitative model and series confirmed model,and the accuracy and specificity of the model were verified.Results The model had good accuracy and specificity,it can accurately identify 21 batches of samples and distinguish 4 structural analogues,counterfeit A enterprise samples and 21 non - structural analogues.Conclusion The model established in this experiment can quickly and accurately identify the authenticity of Benazepril Hydroch1oride Tab1ets,which is suitable for the spot rapid diagnosis of the drug on the drug testing vehicles.
near- infrared spectroscopy;Benazepril Hydrochloride Tablets;qualitative analysis model;rapid identification
R927.1;R972+.4
A
1006-4931(2017)22-0024-04
10.3969 /j.issn.1006 - 4931.2017.22.008
金鹏,男,大学本科,副主任药师,研究方向为化学药品质量分析,(电话)0517-83661017(电子信箱)jcx7912@163.com。
2017-06-06;
2017-08-21)

