LC-MS/MS法测定比格犬血浆中氯吡格雷活性代谢物
赵 雪,孙 慧,张 琪,任天明,顾景凯
(吉林大学药物代谢研究中心,吉林 长春 130012)
LC-MS/MS法测定比格犬血浆中氯吡格雷活性代谢物
赵 雪,孙 慧,张 琪,任天明,顾景凯
(吉林大学药物代谢研究中心,吉林 长春 130012)
建立了一种定量测定比格犬血浆中氯吡格雷活性代谢物(active metabolize, AM)的液相色谱-串联质谱(LC-MS/MS)法。采血管中加入酯酶抑制剂敌敌畏,采样后立即离心处理,取上层血浆,加入2-溴-3’-甲氧基苯乙酮(MPB)进行衍生化,反应完成后直接加入含0.1%甲酸的冰乙腈沉淀蛋白,取上清液,测定氯吡格雷活性代谢物的衍生化产物(MP-AM)。以乙腈-0.1%甲酸为流动相,梯度洗脱,API4000电喷雾离子源,多反应监测(MRM)模式扫描。在优化的实验条件下,获得了峰宽较窄且对称的色谱峰;MP-AM的线性范围为1~1 000 μg/L,相关系数大于0.995;生物基质效应较小,提取回收率在92.8%~95.1%之间,相对标准偏差小于8.27%。该方法的准确度和精密度均符合国家食品药品监督管理总局(China Food and Drug Administration, CFDA)的相关要求,适用于比格犬血浆中氯吡格雷的药代动力学研究。
氯吡格雷;活性代谢物;液相色谱-串联质谱(LC-MS/MS);药代动力学
氯吡格雷是美国食品和药品监督管理局(FDA)批准的抗血小板药物,用于治疗心血管疾病,如动脉粥样硬化血栓、不稳定型心绞痛和心肌梗死等[1-2]。生物体内氯吡格雷(85%)经酯酶水解转化为没有活性的羧酸衍生物M1,只有少部分氯吡格雷经细胞色素P450酶(Cytochrome P450)作用产生活性代谢物(AM)。AM的巯基通过二硫键与二磷酸腺苷(ADP)的P2Y12受体的半胱氨酸残基共价结合,导致与此受体偶联的血小板糖蛋白受体的纤维蛋白原结合位点不能暴露,从而达到抗血小板的作用。15%氯吡格雷主要在CYP2C19、CYP1A2、CYP2B6的作用下氧化成M2;48%的M2被酯酶水解,产生无活性的M3;M2主要在CYP3A4、CYP2B6、CYP2C19的作用下开环形成AM。氯吡格雷的代谢通路示于图1,衍生化反应示于图2。

图1 氯吡格雷的代谢通路Fig.1 Metabolic pathway of clopidogrel

图2 AM的衍生化反应Fig.2 Derivatization reaction of AM
AM结构中含有活泼巯基,在生物体内不稳定,所以必须对巯基进行衍生化保护,再测定氯吡格雷活性代谢物的衍生化产物(MP-AM);另外,AM含有酯键,而血浆中有丰富的酯酶,故在血浆样品采集时需加入酯酶抑制剂。目前,MP-AM定量分析法存在的问题是[3-4]:衍生化前对酯键的保护没有详细的描述、液相时间较长、样品处理大多采用固相萃取和液-液萃取等繁琐的操作方法。
本实验拟采用加入酯酶抑制剂、优化色谱条件、简化样品前处理步骤等手段,对氯吡格雷活性代谢物进行分析,希望建立一种准确可靠、方便快捷的分析方法。
1 实验步骤
1.1仪器、药品及试剂
API 4000液相色谱-串联质谱仪:美国AB Sciex公司产品,配有美国Applied Biosystem公司的电喷雾离子源以及Analyst 1.6.2数据处理软件;高效液相色谱系统:美国Agilent公司产品;Sartorius BT 25 S分析天平:德国Sartorius公司产品;移液器(200、1 000 μL):美国Eppendorf公司产品;Legend Micro 17R低温高速离心机:美国Thermo公司产品;QL-901 Vortex涡流仪:海门市其林贝尔公司产品;MDF-382E(N)冰箱(-80 ℃):日本Sanyo公司产品;BCD-206TXB冰箱(4 ℃):中国海尔公司产品。
氯吡格雷(批号20150101):天士力有限公司产品;联苯双酯(批号Q01130302):北京协和药厂产品;NH4HCO3、2-溴-3’-甲氧基苯乙酮:美国Sigma公司产品;MP-AM溶液(5 mg/L):加拿大多伦多研究化学(TRC)公司产品;乙腈(色谱纯):美国Sigma公司产品;甲酸(分析纯):北京化工厂产品;敌敌畏:购于农资商店。
1.2实验条件
1.2.1色谱条件 色谱柱:Ascentis C18柱(5 cm×4.6 mm×5 μm);流动相:乙腈(A)-0.1%甲酸(B);流速1 mL/min;柱温40 ℃;自动进样器温度4 ℃;进样量20 μL;梯度洗脱程序:0~0.3 min(45%A),0.3~1.0 min(45%~95%A),1.0~2.5 min(95%A),2.5~2.7 min(95%~45%A),2.7~4.0 min(45%A)。
1.2.2质谱条件 ESI离子源,正离子检测方式;离子喷射电压5 500 V;离子源温度500 ℃;源内气体1(GS1,N2)压力0.31 MPa,源内气体2(GS2,N2)压力0.28 MPa,气帘气体(N2)压力0.17 MPa;多反应监测(MRM)扫描方式;MP-AM及联苯双酯的解簇电压(DP)分别为70 V和35 V,碰撞能量(CE)分别为26 eV和19 eV;用于定量分析的离子反应分别为m/z504.1→m/z354.1(MP-AM)和m/z436.0→m/z386.9(联苯双酯)。
1.3溶液配制
1.3.1标准系列溶液的配制 取适量5 mg/L MP-AM储备液,用乙腈-水溶液(50∶50,V/V)稀释,得到 5、15、50、150、500、1 500、5 000 μg/L MP-AM标准系列溶液;另取适量MP-AM储备液,用乙腈-水溶液(50∶50,V/V)稀释,得到60、600、20 000 μg/L质控工作液;两种溶液均存于4 ℃冰箱中,备用。
1.3.2内标工作液的配制 准确称取10.52 mg联苯双酯,用乙腈溶解并稀释至1 g/L,作为储备液于4 ℃冰箱中保存;用乙腈-水溶液(50∶50,V/V)将储备液稀释至25 μg/L,作为工作液于4 ℃冰箱中保存。
1.3.3衍生化试剂的配制 取适量MPB,用乙腈溶解并稀释至100 mmol/L,现用现配。
1.3.4NH4HCO3溶液的配制 取适量NH4HCO3,用0.5%氨水溶液稀释至200 mmol/L,备用。
1.3.5酯酶抑制剂-敌敌畏的配制 取适量敌敌畏,用1%肝素稀释至20 mmol/L,备用。
1.4标准曲线、质控样品配制及未知生物样品处理
1.4.1标准曲线、质控样品制备 分别量取20 μL MP-AM标准系列溶液,配制成含待测物MP-AM血浆浓度分别为1、3、10、30、100、300、1 000 μg/L标准曲线样品溶液;另取200 μL质控工作液,配制成含待测物MP-AM血浆浓度分别为2.4、24、800 μg/L质控样品溶液,分装、冻存于-80 ℃冰箱中。标准曲线样品溶液须现用现配。
1.4.2标准曲线、质控样品处理 取50 μL已配制好的标准曲线(质控)样品溶液,加入50 μL内标、100 μL NH4HCO3、100 μL乙腈和700 μL冰1%甲酸-乙腈溶液,涡旋振荡60 s,于4 ℃离心机以13 300 r/min离心5 min,取20 μL上清液,转移至进样瓶中,进样分析。测试结果的定量依据为MP-AM与内标峰面积之比。采用权重系数1/X2进行最小二乘线性回归分析,得到MP-AM在比格犬血浆中浓度的标准曲线,示于图3。
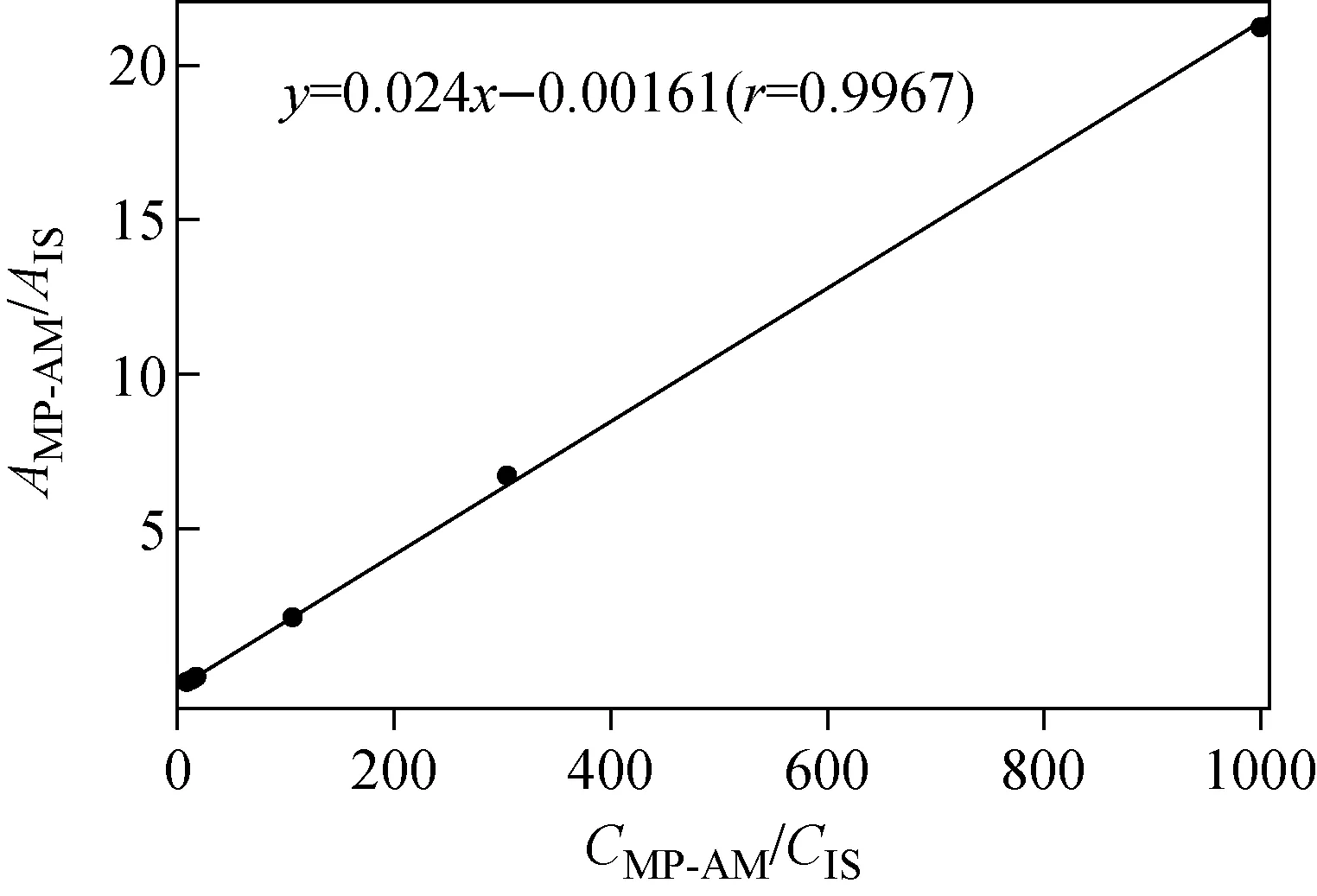
图3 比格犬血浆中MP-AM典型标准曲线Fig.3 Standard curve of MP-AM in beagle dog plasma
1.4.3生物样品采集及处理 随机选取3只比格犬,给药前12 h禁食,自由饮水。灌胃给药,给药剂量6.6 mg/kg。采用比格犬前肢隐静脉取血方式,分别于给药前0 h和给药后0.083 3、0.25、0.5、1、1.5、2、4、6、8、10、12 h采集2 mL全血,迅速加入至含酯酶抑制剂及肝素的采血管中(采血管须预冷),立即于4 ℃离心机以13 300 r/min离心1 min;取50 μL上层血浆于2.00 mL抗吸附管中,加50 μL内标、100 μL NH4HCO3和100 μL MPB,涡流振荡30 s,避光反应10 min;最后加入680 μL 冰1%甲酸-乙腈溶液,涡旋振荡60 s,于4 ℃离心机以13 300 r/min离心5 min,上清液于-80 ℃保存,待测。
2 实验结果
2.1方法学考察
2.1.1专属性 取50 μL比格犬空白血浆,按1.4.2节方法处理并进样分析;另取受试比格犬给药后采集的血浆样品,按1.4.3节方法处理并进样分析,所得色谱图示于图4。
2.1.2最低定量限 取20 μL 10 μg/L的MP-AM标准工作溶液,用比格犬空白血浆配制成1 μg/L血浆样品,按照1.4.3节方法处理并进样分析,共测定6个平行样本,定量下限数据列于表1。
从表1可以看出,MP-AM的准确度均在80%~120%之间,相对标准偏差小于20%,说明MP-AM的定量下限为1 μg/L是准确可靠的。
2.1.3精密度与准确度 用比格犬空白血浆配制2.4、24、800 μg/L 3个浓度的质控样品(每个浓度6个平行样本),以考察批内精密度和准确度;与同批随行的标准样品一同进样,考察同批内样品的准确度和精密度,连续测试3天,评价日间准确度与精密度。结果表明:日内、日间相对标准偏差均小于15%,准确度在±15%之内,说明该方法的准确度、精密度良好,可以保证未知生物样品测定的准确性。
2.1.4基质效应与提取回收率 取20 μL浓度为12、120、4 000 μg/L的MP-AM标准系列溶液,用纯净水稀释至2.4、24、800 μg/L,混合均匀后,分别取50 μL稀释好的溶液,加入50 μL内标、100 μL NH4HCO3、100 μL乙腈和700 μL 1%甲酸-乙腈溶液,涡旋混合60 s,取20 μL上清液进样分析,测定峰面积分别为AMP-AM、AIS。另取50 μL空白比格犬血浆、100 μL NH4HCO3、100 μL乙腈和700 μL 1%甲酸-乙腈溶液,涡旋混合60 s,于4 ℃离心机以13 300 r/min离心1 min后取上清液,分别加入50 μL稀释至2.4、24、800 μg/L的工作液和50 μL内标,涡旋混合60 s,进样分析,测定峰面积分别为BMP-AM、BIS。提取回收率=(随行质控峰面积/A)×100%,基质效应=(B/A)×100%。按上述方法计算得到MP-AM的内标归一化基质效应因子(matrix factor, MF)CV≤10.15%,低、中、高3个浓度的MP-AM提取回收率分别为95.1%、92.8%、94.7%,内标提取回收率为96.7%,其结果列于表2。
2.1.5稳定性 按照1.4.2节方法制备室温放置稳定性样品及自动进样器稳定性样品(2.4、24、800 μg/L,3个浓度各3个平行样本),并按1.4.3节方法处理,取处理后上清液分别于室温放置2 h、自动进样器放置2 h后进样分析;按照1.4.2节方法制备长期冻存稳定性样品及反复冻融稳定性样品,分别进行-80 ℃冰箱长期冻存30天及3次反复冻融,再按照1.4.3节方法处理,进样分析。结果表明,不同浓度(2.4、24、800 μg/L)样品测定值的准确度和相对标准偏差均小于±15%,说明该方法的稳定性良好。

注:a.空白血浆;b.定量下限(LLOQ);c.给药后血浆加内标联苯双酯图4 比格犬血浆中MP-AM(左)与内标联苯双酯(右)的LC-MS/MS色谱图Fig.4 LC-MS/MS chromatograms of MP-AM (left) and IS (right) in beagle dogs plasma
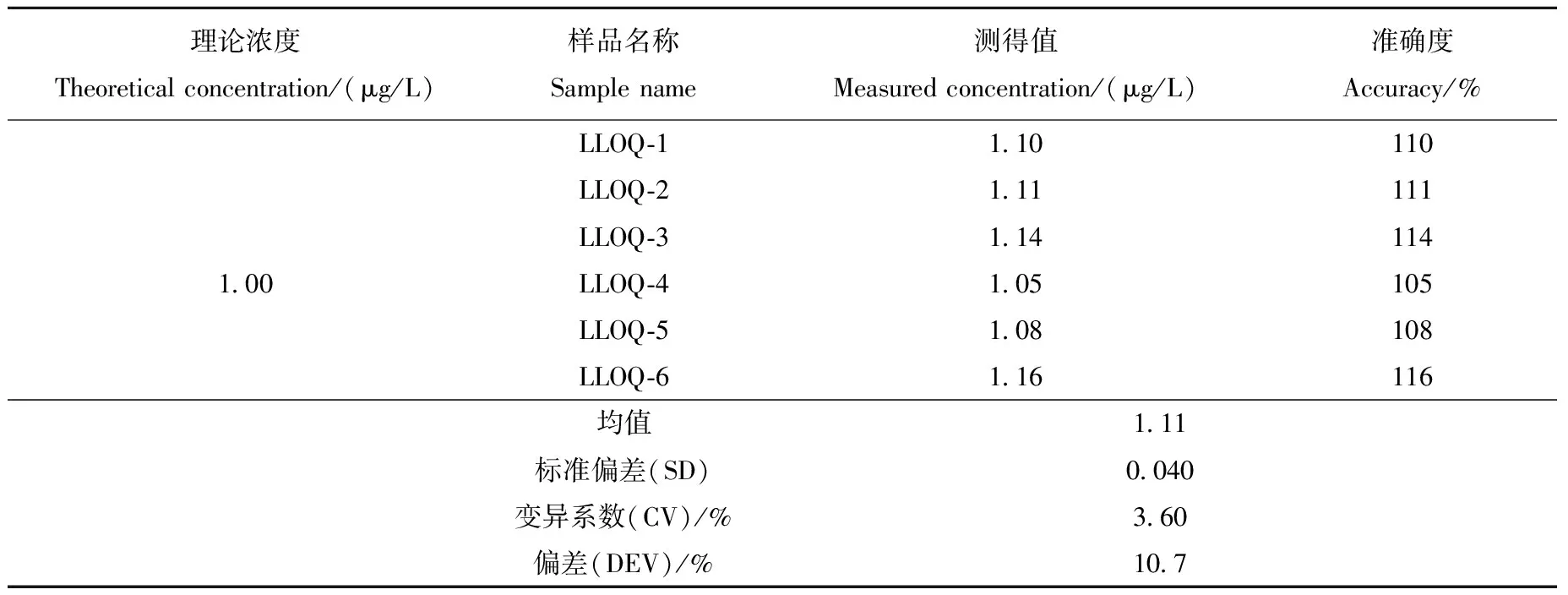
表1 MP-AM定量下限的准确度、均值及精密度Table 1 Accuracy, mean and standard deviztion of MP-AM’s LLOQ

表2 质控样品测定浓度、准确度及相对标准偏差Table 2 Concentration, accuracy and standard deviation of quality control samples
将配制好的高浓度和低浓度MP-AM和内标工作液于4 ℃放置15天后,与新鲜配制的相同浓度MP-AM和内标工作液一同进样,每个浓度重复进样3次,比较两者的峰面积。结果表明:两者平均峰面积的偏差小于±15%,说明这两种工作液于4 ℃冰箱中放置15 天后稳定。
2.2药代动力学结果
比格犬灌胃给6.6 mg/kg氯吡格雷后,MP-AM的血药浓度-时间曲线示于图5,具体的药代动力学参数列于表3。

图5 比格犬给药后血浆中MP-AM的平均血浆浓度-时间曲线(n=3)Fig.5 Plasma concentration-time curve of the active metabolite produced after oral administration of clopidogrel to beagle dogs (n=3)
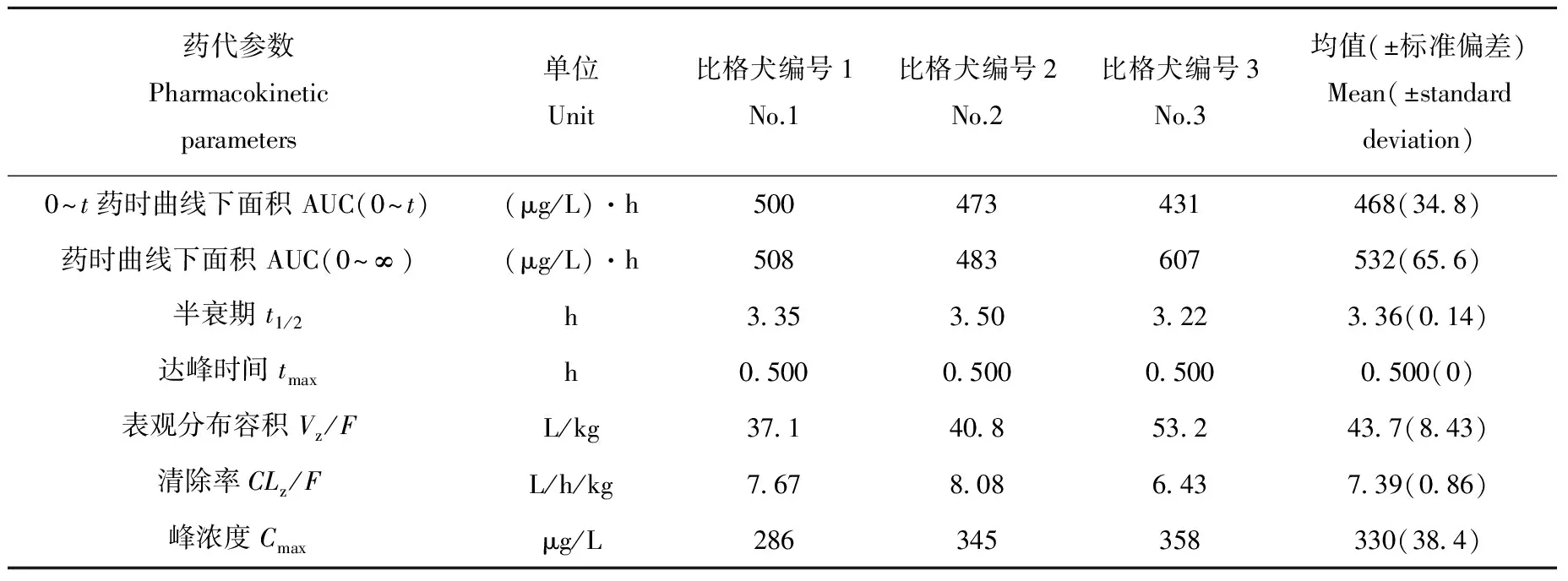
表3 比格犬血浆中MP-AM的药代动力学参数Table 3 Pharmacokinetic parameters of MP-AM in beagle dog plasma
2.3讨论
2.3.1衍生化前酯键保护 氯吡格雷为上市很多年的药物,已有很多关于氯吡格雷巯基代谢物定量分析方法的报道[5-9],但是均未对其衍生化前酯键保护做详细的描述,而这个环节会直接影响测定结果的准确性。针对这一问题,本实验采用如下操作予以解决:1) 实验操作在冰浴下进行,采血管须预冷,这是由于低温条件下,酶的活性比较低;2) 生物体内存在大量的酯酶,为了保证测定数据的准确性,须在血浆样品采集时于采血管中预先加入酯酶抑制剂。通常,有机磷、烷化剂、重金属等都可以不可逆地抑制酶的活性。本实验选用有机磷农药-敌敌畏作为酯酶抑制剂,实验过程中发现酯酶抑制剂浓度过大会导致溶血,浓度过低则达不到完全抑制酯酶活性的作用,所以在实验前进行了系列浓度水平的考察,优化了本实验中酯酶抑制剂的浓度。
2.3.2衍生化条件 氯吡格雷的活性代谢物中含有巯基,生物体内巯基不稳定,极易氧化或与其他生物大分子(如谷胱甘肽等)结合,因此需要对其进行衍生化保护。衍生化条件对于定量准确与否至关重要,为此本实验控制衍生化试剂的加入在样品采集后2 min内完成,这样可以保证不稳定的巯基在与衍生化试剂反应前不被氧化,为氯吡格雷巯基代谢物的准确定量提供了时间保证。在此基础上,还对衍生化反应时长及MPB加入量进行了考察。
1) 反应时长:取相同的生物样品,保持衍生化反应条件及样品处理方法等因素一致,考察5、10、20、30 min时间点的MP-AM浓度值。结果表明,反应10 min可确保反应完全。
2) MPB加入量:尝试在体系中加入50、100、200 mmol/L的MPB,分别命名为体系1、体系2和体系3。结果发现,相同的生物样品在体系1中的测得值低于体系2,体系2和体系3测得的结果没有差别。因此,最终选择向体系中加入100 μL 100 mmol/L烷基化试剂。由于MPB需要避光保存,本反应是在避光条件下进行的。
3 结论
本实验所建立的分析方法经过了完整的生物样品方法学确证,其准确度、精密度均可达到国家食品药品监督管理总局(CFDA)的相关要求,且操作简便、快速、灵敏,能够实现对氯吡格雷活性代谢物的准确定量分析,可满足氯吡格雷药代动力学研究的需要。
[1] 唐宁,徐向东,朱耀武,等. 不同氯吡格雷治疗检测指标的相关性及心血管事件的关系[J]. 中国循环杂志,2015,30(2):144-148.
TANG Ning, XU Xiangdong, ZHU Yaowu, et al.Correlation between different clopidogrel test indexes and cardiovascular events[J]. Chinese Journal of Circulation, 2015, 30(2): 144-148(in Chinese).
[2] 倪唤春,范维琥. 抗血小板新药——氯吡格雷[J]. 中国新药杂志,2001,10(12):888.
NI Huanchun, FAN Weihu. Antiplatelet new drug-clopidogrel[J]. Chinese Journal of New Drugs, 2001, 10(12): 888(in Chinese).
[3] ELSINGHORST P W. Quantitative determination of clopidogrel and its metabolites in biological samples: a mini-review[J]. Journal of Chromatography B, 2013, 917/918(4): 48-52.
[4] TAKAHASHI M, PANG H, KAWABATA K, et al. Quantitative determination of clopidogrel active metabolite in human plasma by LC-MS/MS[J]. Journal of Pharmeceutical and Biomedical Analysis, 2008, 48(4): 1 219-1 224.
[5] XU X Y, ZHAO X, YANG Z, et al. Significant improvement of metabolic characteristics and bioactivities of clopidogrel and analogs by selective deuteration[J]. Molecules, 2016, 21(6): 704.
[6] PARK J B, BAE S H, JANG S M, et al. Direct measurement of active thiol metabolite levels of clopidogrel in human plasma using tris(2-carboxyethyl) phosphine as a reducing agent by LC-MS/MS[J]. Journal of Separation Science, 2013, 36(14): 2 306-2 314.
[7] PEER C J, SPENCER S D, VANDENBERG D A H, et al. A sensitive and rapid ultra HPLC-MS/MS method for the simultaneous detection of clopidogrel and its derivatized active thiol metabolite in human plasma[J]. Journal of Chormatography B, 2012, 880(1): 132-139.
[8] TUFFAL G, ROY S, LAVISSE M, et al. An improved method for specific and quantitative determination of the clopidogrel active metabolite isomers in human plasma[J]. Thrombosis & Haemostasis, 2011, 105(4): 696-705.
[9] KARAZNIEWICZ-ADA M, DANIELAK D, TEZYK A, et al. HPLC-MS/MS method for the simultaneous determination of clopidogrel,its carboxylic acid metabolite and derivatized isomers of thiol metabolite in clinical samples[J]. Journal of Chromatography B, Analytical Technologies in the Biomedical & Life Sciences, 2012, 911(23): 105-112.
DeterminationofClopidogrelActiveMetaboliteinBeagleDogPlasmabyLC-MS/MS
ZHAO Xue, SUN Hui, ZHANG Qi, REN Tian-ming, GU Jing-kai
(ResearchCenterforDrugMetabolism,JilinUniversity,Changchun130012,China)
A method of liquid chromatography coupled with tandem mass spectrometry (LC-MS/MS) method was developed for determining clopidogrel active metabolite (AM) in beagle dog plasma. LC separation was performed using water containing 0.1% formic acid and acetonitrile as mobile phases with the gradient elution at a flow rate of 1 mL/min. Quantitative analysis was achieved after the chromatographic separation on an Ascentis C18 column (5 cm×4.6 mm×5 μm). The electrospray ionization (ESI) source in positive mode and multiple reaction monitoring (MRM) were used for the detection of clopidogrel AM derivative (MP-AM). The sample pretreatment conditions such as the extraction method, the derivative reagents were optimized. The alkylating reagent 2-bromo-3’-methoxyacetophenone (MPB) was used to stabilize clopidogrel AM in blood. Blood samples were centrifuged immediately after collection to take plasma and MPB was then added. Protein precipitation with iced acetonitrile (containing 0.1% formic acid) as precipitation solvent was used for sample extraction. The post-extracted samples were analyzed by LC-MS/MS. The peaks are narrow and symmetrical. The linear range of MP-AM is 1-1 000 μg/L, and the linear correlation coefficient is more than 0.995. The method has no matrix interference. The recoveries of MP-AM range from 92.8% to 95.1% at three spiked levels of 2.4, 24 and 800 μg/L with the relative standard deviations (RSD) less than 8.27% (n=6). The intra-assay/inter-assay accuracy and precision are all acceptable. The method is simple, accurate and robust, which is suitable for research the pharmacokinetic of AM in beagle dog plasma.
clopidogrel; clopidogrel active metabolite; liquid chromatography coupled with tandem mass spectrometry (LC-MS/MS); pharmacokinetic
2017-02-21;
2017-04-24
赵 雪(1991—),女(汉族),吉林磐石人,硕士研究生,微生物与生化药学专业。E-mail: zhaoxue1310@163.com
顾景凯(1963—),男(汉族),辽宁新民人,教授,从事药物代谢与药物动力学研究。E-mail: gujk@jlu.edu.cn
O657.63
:A
:1004-2997(2017)04-0460-08
10.7538/zpxb.2017.0035

