HPLC-IT-TOFMS快速区分达格列净中间体及其位置异构体
黄 钰,马 格,尹欣驰,张 健,潘远江
(1.浙江大学电气工程学院,浙江 杭州 310027;2.浙江大学化学系,浙江 杭州 310027)
HPLC-IT-TOFMS快速区分达格列净中间体及其位置异构体
黄 钰1,2,马 格2,尹欣驰2,张 健1,潘远江2
(1.浙江大学电气工程学院,浙江 杭州 310027;2.浙江大学化学系,浙江 杭州 310027)
本研究采用高效液相色谱-离子阱-飞行时间质谱法(HPLC-IT-TOF MS)对降糖药达格列净原料药中间体5-溴-2-氯-4’-乙氧基二苯甲酮(化合物1)及其异构体5-溴-2-氯-2’-乙氧基二苯甲酮(化合物2)进行区分。在不同碰撞能量下,对[M+H]+和碎片离子绘制能量分辨曲线,依据高精确度质荷比信息确定碎片离子的元素组成,并提出了可能的碎裂机理。结果表明:两种异构体的能量分辨曲线表现出明显差异,化合物1的主要碎片离子为[M+H-C6H5OC2H5]+(m/z216.90),化合物2的主要碎片离子为[M+H-C2H4O]+(m/z294.95)。推测原因可能是乙氧基取代位置的不同对质子H迁移产生了不同的影响。该方法操作简便、灵敏度高,在没有对照品的情况下也能快速区分位置异构体。
达格列净;位置异构体区分;高效液相色谱-离子阱-飞行时间质谱(HPLC-IT-TOF MS);能量分辨曲线
达格列净(dapagliflozin, ForxigaTM)是由百时美施贵宝和阿斯利康公司联合开发的抗糖尿病药物,用于治疗Ⅱ型糖尿病。该药分别于2012年11月、2014年1月在欧盟和美国上市[1]。达格列净的作用机制是通过抑制钠-葡萄糖协同转运蛋白2(SGLT2)的合成,阻断进曲小管对葡萄糖的重吸收,增加葡萄糖在尿液中的排泄,从而降低血糖[2-4]。有文献报道,达格列净合成工艺中[5,6],5-溴-2-氯-4’-乙氧基二苯甲酮(化合物1)是关键中间体,在其合成过程中往往伴随着副产物5-溴-2-氯-2’-乙氧基二苯甲酮(化合物2)的生成[7]。达格列净及化合物1和2的结构式示于图1。化合物2的存在将直接影响后续的合成进程,进而影响药物的纯度和质量。但由于化合物1和2互为位置异构体,在分离鉴定上有一定难度。因此,为提高达格列净的用药安全,达到有效控制质量的目的,对化合物1和2进行快速识别和鉴定具有重要意义。
核磁共振[8]和液质联用[9-10]是鉴定同分异构体常用的分析手段。其中,核磁共振技术所需的样品量较大,且对纯度要求较高;液质联用技术则兼具高效液相色谱的分离能力和质谱的结构分析能力,具有快速、高效、灵敏等优点,已被广泛应用于同分异构体化合物的研究。
质谱能量分辨曲线是以不同的碰撞能量为横坐标,碎片离子丰度占该能量下该化合物产生的所有离子丰度总和的比值为纵坐标建立的[11-13]。它能够提供区分异构体的裂解信息,特别是在没有对照品的情况下,可以快速高效地区分异构体[12-13]。Tai等[13]利用大气压化学电离串联质谱研究了查尔酮化合物的裂解机理,并通过绘制能量分辨曲线对异构体进行区分。Yin等[14]利用电喷雾电离串联质谱快速识别了米格列醇及其异构体,其与benzoboroxole的反应产物硼酸酯的能量分辨曲线表现出显著差异,可以通过特征碎片离子进行异构体的快速识别。
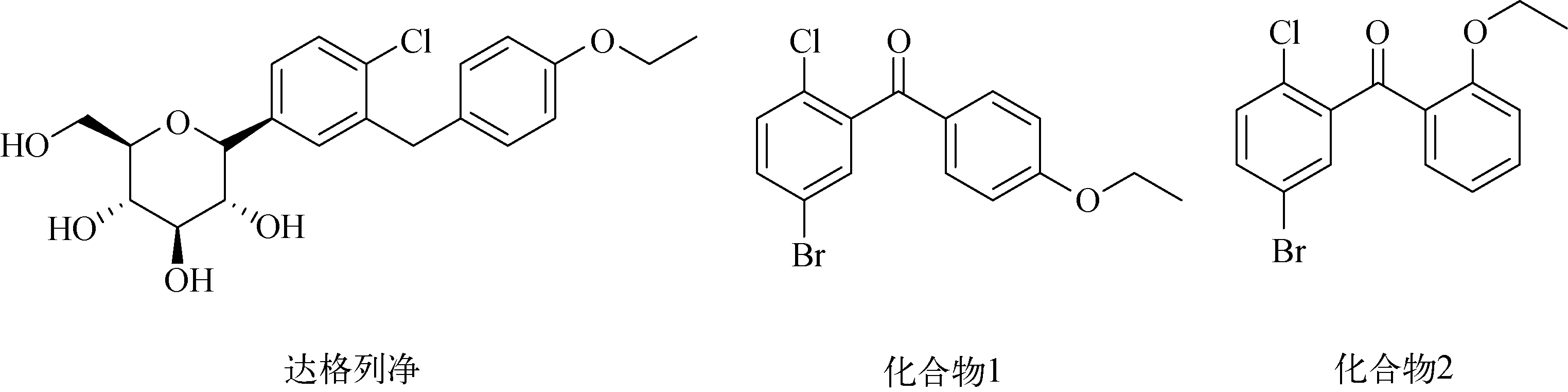
图1 达格列净及化合物1和2的结构式Fig.1 Chemical structures of dapagliflozin and compounds 1&2
本工作拟采用HPLC-IT-TOF MS技术同时采集不同碰撞能量下的二级质谱数据,绘制能量分辨曲线,快速区分达格列净中间体及其位置异构体。利用精确二级质谱数据和能量分辨曲线,进一步分析二者的质谱裂解行为,对化合物结构进行确证,希望为控制达格列净原料药的质量提供有效途径。
1 实验部分
1.1仪器与装置
LC/MS-IT-TOF质谱仪:日本岛津公司产品,配有电喷雾离子源;Milli-Q水纯化系统:美国Millipore公司产品;HPLC色谱柱:Capcell PAK C18柱(250 mm×4.6 mm×5 μm),日本资生堂公司产品;PHS-3B型pH计:上海INESA科学仪器有限公司产品。
1.2材料与试剂
乙腈、甲醇、甲酸:均为色谱纯,美国Tedia公司产品;实验用水:Milli-Q高纯水;三氟乙酸、氢氧化钠:美国Sigma公司产品。
三氟乙酸钠聚合物调谐液的制备:分别配制0.1%三氟乙酸水溶液和10 mmol/L氢氧化钠水溶液,取等体积的上述两种溶液混合均匀,并用氢氧化钠溶液调至pH 3.5后,加入等体积乙腈并混合均匀,即制得标准调谐液。
混合物样品:由本实验室根据文献报道的方法合成[5];5-溴-2-氯-4’-乙氧基二苯甲酮标准品:阿达马斯试剂公司产品。混合物样品和标准品均需用甲醇溶液稀释后进样。
1.3实验条件
1.3.1色谱条件 色谱柱:Capcell PAK C18色谱柱(250 mm×4.6 mm×5 μm);流动相:A为0.1%甲酸水溶液,B为乙腈-甲醇溶液(3∶1,V/V);流速:0.6 mL/min;梯度洗脱程序:0~15.0 min(15%~70%B),15.0~60.0 min(70%~90%B);进样量:2 μL;柱温:40 ℃。
1.3.2质谱条件 电喷雾离子源(ESI),正离子模式采样;检测电压:1.77 kV;氮气流速:1.5 L/min;曲线脱溶剂管(CDL)温度:200 ℃;氮气流速压力:100 kPa;离子累计时间:50 ms;碰撞气体:高纯氩气;二级质谱碰撞能量:10%、15%、20%、25%;一级质谱采集质荷比范围:m/z150~450;二级质谱采集质荷比范围:m/z94~400,前体离子设定为m/z338.97;高分辨质量矫正:采用三氟乙酸钠聚合物。
2 结果与讨论
2.1混合物样品的HPLC-IT-TOFMS结果分析
化合物1和2互为位置异构体,由于其理化性质相似,通常很难将二者有效分离。本实验通过条件优化,最终确定以0.1%甲酸水溶液为A相,乙腈-甲醇溶液(3∶1,V/V)为B相进行梯度洗脱。在该实验条件下,混合物的色谱图和总离子流图示于图2。色谱峰的峰形和强度较好,目标化合物在43.86 min开始出峰,峰A和峰B的保留时间分别为44.42 min和45.23 min,峰基有一定的重叠,但裸露的峰面积足够用于高灵敏度的质谱分析。
色谱峰A和峰B对应的二级质谱图示于图3,二者的质谱图具有显著差异。图3a中碎片离子m/z294.951 8丰度最高,m/z216.909 8丰度最低;图3b中碎片离子m/z216.903 9丰度最高,没有出现碎片离子m/z294.95。因此,可以将这两个碎片离子作为区分这对位置异构体的特征碎片离子。
2.2对照实验
为了归属图2a中色谱峰A和峰B,将化合物1的标准品在正离子模式下进行二级质谱解析,并在不同的碰撞能量下绘制能量分辨曲线,结果示于图4。可以发现,峰A和峰B的能量分辨曲线表现出显著差异。随着碰撞能量增大,峰A的[M+H]+离子及m/z294.95碎片离子丰度变化趋势较大,而峰B和化合物1标准品的[M+H]+离子及m/z216.90碎片离子丰度变化趋势较大。能量分辨曲线直观地体现了峰A和峰B所对应的这对位置异构体质谱裂解行为存在差异,峰B和化合物1标准品质谱裂解行为一致。进而判定峰A和峰B分别对应化合物2和1。

图2 混合物样品的色谱图(a)和总离子流图(b)Fig.2 Chromatogram (a) and total ion chromatogram (b) of the mixture sample

图3 色谱峰A(a)和B(b)在15%碰撞能量下的二级质谱图Fig.3 MS/MS spectrums of chromatographic peak A (a) and peak B (b) under 15% collision energy

图4 色谱峰A(a)、峰B(b)和化合物1标准品(c)的能量分辨曲线Fig.4 Breakdown curves of peak A (a), peak B (b) and standard compound 1 (c)
2.3碎裂机理分析
化合物1和2结构的区别在于苯环上乙氧基的取代位置。二者的高分辨质谱数据列于表1。化合物1主要产生2种碎片离子a和c,化合物2主要产生3种碎片离子a、b和c。化合物1的乙氧基在苯环上为对位取代,此时主要发生乙氧基苯的中性丢失(ion c),而当乙氧基为邻位取代(化合物2)时,主要丢失C2H4O(ion b)。质子化的化合物1和2可能的碎裂途径示于图5。
推测化合物可能的碎裂机理,碎片离子a为乙氧基上甲基H迁移至O原子发生乙烯的中性丢失而产生;碎片离子b由乙氧基上的甲基H发生1-4H迁移到苯环上中性丢失环氧乙烷(C2H4O)产生;碎片离子c的形成过程中,质子H首先发生1-4H迁移至苯环邻位,然后进行1-2H迁移丢失乙氧基苯。因此,当乙氧基为邻位取代时,由于位阻效应,质子H发生1-4H迁移难度增加,难以产生c离子。由于b、c两种碎裂途径的竞争,化合物1主要产生c离子,化合物2主要产生b离子。在两种位置异构体中,a离子丰度无明显差异。[M+H]+离子可能的碎裂机理示于图6。

表1 质子化的化合物1和2碎片离子的IT-TOF MS/MS数据Table 1 Experimental data for the product ions of compounds 1&2 by IT-TOF MS/MS

图5 质子化的化合物1和2可能的碎裂途径Fig.5 Proposed fragmentation pathway of protonated compounds 1&2

图6 [M+H]+离子可能的碎裂机理Fig.6 Proposed fragmentation mechanism of [M+H]+ ions
3 结论
本实验采用HPLC-IT-TOF MS法快速、高效地区分了降糖药达格列净中间体(化合物1)及其位置异构体(化合物2)。化合物1和2的能量分辨曲线具有显著差异,这是因为乙氧基取代位置不同,对质子H的迁移造成不同的影响,导致了异构体裂解行为的差异。当乙氧基为邻位取代时,由于位阻效应使得碎片离子c不容易形成。该方法操作简便、快速高效,能够同时获得化合物的色谱和质谱信息,可对化合物进行快速的定性鉴别和半定量分析,为控制达格列净原料药的质量提供了方法参考。
[1] 石卫峰,李晓宇,刘皋林. 治疗2型糖尿病新药达格列净[J]. 中国新药杂志,2013,22(16):1 861-1 863.
SHI Weifeng, LI Xiaoyu, LIU Gaolin. Dapaglifozin, a new anti-hyperglycemic agent for type 2 diabetes[J]. Chinese Journal of New Drugs, 2013, 22(16): 1 861-1 863(in Chinese).
[2] CHAO E C, HENRY R R. SGLT2 inhibition-a novel strategy for diabetes treatment[J]. Nature Reviews Drug Discovery, 2010, 9(7): 551-559.
[3] HAN S P, HAGAN D L, TAYLOR J R, et al. Dapagliflozin, a selective SGLT2 inhibitor, improves glucose homeostasis in normal and diabetic rats[J]. Diabetes, 2008, 57(6): 1 723-1 729.
[4] WEI M, ELLSWORTH B A, NIRSCHL A A, et al. Discovery of dapagliflozin: a potent, selective renal sodium-dependent glucose cotransporter 2(SGLT2) inhibitor for the treatment of type 2 diabetes[J]. Journal of Medicinal Chemistry, 2008, 51(5): 1 145-1 149.
[5] 禹艳坤,冀亚飞. 达格列净的合成[J]. 中国医药工业杂志,2011,42(2):84-87.
YU Yankun, JI Yafei. Synthesis of dapagliflozin[J]. Chinese Journal of Pharmaceuticals, 2011, 42(2): 84-87(in Chinese).
[6] 张帅阳,徐斌,王德才. 达格列净合成路线图解[J]. 中国医药工业杂志,2014,45(12):1 192-1 194.
ZHANG Shuaiyang, XU Bin, WANG Decai. Graphical synthetic routes of dapagliflozin[J]. Chinese Journal of Pharmaceuticals, 2014, 45(12): 1 192-1 194(in Chinese).
[7] 王彪,曹胜,杜月,等. 降糖药达格列净中2种杂质的合成[J]. 精细化工中间体,2016,46(3):24-27.
WANG Biao, CAO Sheng, DU Yue, et al. Synthesis of two impurities in dapagliflozin[J]. Fine Chemical Intermediates, 2016, 46(3): 24-27(in Chinese).
[8] 施燕红,刘松柏,宋国强. 利用NMR测定盐酸头孢吡肟中杂质的含量[J]. 波谱学杂志,2003,20(3):259-264.
SHI Yanhong, LIU Songbin, SONG Guoqiang. Measurement of the percentage of impurity in cefepime dihydrochloride by NMR[J]. Chinese Journal of Magnetic Resonance, 2003, 20(3): 259-264(in Chinese).
[9] ABLAJAN K. A study of characteristic fragmentation of isoflavonoids by using negative ion ESI-MSn[J]. Journal of Mass Spectrometry, 2011, 46(1): 77-84.
[10]OHASHI Y, KUBOTA M, HATASE H. Studies on ESI-MS/MS of a glycosaminoglycan disaccharideN-acetyllactosammine-6,6’-disulfate disodium salt-charge-localization isomers[J]. International Journal of Mass Spectrometry, 2012, 312: 179-184.
[11]李敏,王秀娟,陈娟娟,等. 质谱能量分辨曲线法区分氧化脂类前列腺素异构体[J]. 药物分析杂志,2014,34(7):1 161-1 169.
LI Min, WANG Xiujuan, CHEN Juanjuan, et al. Identification of the oxylipins prostaglandin by mass spectrometry using breakdown curves[J]. Chinese Journal of Pharmaceutical Analysis, 2014, 34(7): 1 161-1 169(in Chinese).
[12]KUURANNE T, VAHERMO M, LEINOEN A, et al. Electrospray and atmospheric pressure chemical ionization tandem mass spectrometric behavior of eight anabolic steroid glucuronides[J]. Journal of the American Society for Mass Spectrometry, 2000, 11(8): 722-730.
[13]TAI Y P, PEI S F, PAN Y J, et al. Fragmentation study of protonated chalcones by atmospheric pressure chemical ionization and tandem mass spectrometry[J]. Rapid Communications in Mass Spectrometry, 2006, 20(6): 994-1 000.
[14]YIN Q H, WANG L, SUN C R. Rapid identification of miglitol and its isomers by electrospray ionization tandem mass spectrometry[J]. Rapid Commun Mass Spectrom, 2016, 30(1): 155-161.
RapidIdentificationofDapagliflozinIntermediateandItsIsomerbyHPLC-IT-TOFMS
HUANG Yu1,2, MA Ge2, YIN Xin-chi2, ZHANG Jian1, PAN Yuan-jiang2
(1.CollegeofElectricalEngineering,ZhejiangUniversity,Hangzhou310027,China;2.DepartmentofChemistry,ZhejiangUniversity,Hangzhou310027,China)
Dapagliflozin is a sodium-glucose co-transporter-2 (SGLT2) inhibitor for treating type Ⅱ diabetes. In the process of synthesizing dapagliflozin, 5-bromo-2-chloropheny-4’-ethoxyldiphenylmethanone (compound 1) is a key intermediate. According to the literatures, there is always by-product 5-bromo-2-chloropheny-2’-ethoxyldiphenylmethanone (compound 2) in the synthesis procedure of compound 1. Due to the similarities of the two isomers in physical and chemical properties, it’s difficult to separate and differentiate compound 1 and 2. As compound 2 affects the purity of dapagliflozin, it is of great importance to establish a method to rapidly distinguish compound 1 from compound 2. In this article, high performance liquid chromatography-ion trap-time of flight mass spectrometry (HPLC-IT-TOF MS) method was used to analyze compound 1 and 2. The samples were dissolved in methanol for direct injection. Under the optimized chromatographic conditions, good separation for the two isomers was obtained on a Capcell PAK C18 column (250 mm×4.6 mm×5 μm) with a mobile phase of water (0.1% formic acid) and acetonitrile-methanol (3∶1,V/V) at a flow rate of 0.6 mL/min. The target compounds were assayed by IT-TOF MS/MS in positive mode with the spray voltage set at 1.77 kV. The nitrogen flow was set at 1.5 L/min, and the capillary temperature was set at 200 ℃. The collision gas was helium. The ion atm/z338.97 was chosen as the target to perform MS/MS experiment, and the collision energies were set at 10%, 15%, 20% and 25%, respectively. The MS/MS results under different collision energies were gained simultaneously by setting events in parallel on IT-TOF mass spectrometer. In order to visually distinguish the two isomers, breakdown curves were mapped by [M+H]+and fragment ions. The breakdown curves of the two isomers show significant differences, which provided strong support in this study. In addition, the element compositions of the three product ions were also confirmed by IT-TOF MS. Loss of C2H2from the precursor ions of [M+H]+was observed in the MS/MS spectra of both the isomers. For compound 1, the major fragmentation pathway was loss of C2H5OC6H5from [M+H]+viaa 2-step proton transfer. While, for compound 2, [M+H-C2H4O]+via1-4 H shift fromortho-substituted ethoxy group to the benzene ring was found to be the major product ion. The difference in the fragmentation pathways of the two isomers may be due to the different substitution sites of the ethoxy groups. When the ethoxy group isortho-substituted, the 2-step proton transfer is quite difficult. As a result, it goes through loss of C2H4O mainly. The method is simple, effective and accurate, which is suitable for rapidly qualitative and semi-quantitative analysis of the isomers, and also can provide a reliable and effective technique for the quality control of dapagliflozin.
dapagliflozin; isomer identification; high performance liquid chromatography-ion trap-time of flight mass spectrometry (HPLC-IT-TOF MS); breakdown curve
2017-03-14;
2017-05-10
国家自然科学基金项目(21372199)资助
黄 钰(1993—),女(汉族),四川自贡人,博士研究生,化学专业。E-mail: huangyu0402@zju.edu.cn
张 健(1980—),男(汉族),吉林辽源人,助理研究员,从事可靠性测试、仪器开发。E-mail: jianzhangzju@zju.edu.cn
潘远江(1966—),男(汉族),湖南武陵源人,教授,从事生物活性分子的质谱研究。E-mail: panyuanjiang@zju.edu.cn
O657.63
:A
:1004-2997(2017)04-0443-07
10.7538/zpxb.2017.0043

