243例参麦注射液不良反应/事件报告分析
张予军 程志 张万智(安陆市普爱医院药剂科,湖北 安陆 432600)
243例参麦注射液不良反应/事件报告分析
张予军程志张万智
(安陆市普爱医院药剂科,湖北 安陆 432600)
【摘要】目的:分析参麦注射液发生不良反应/事件(ADR/ADE)的特点,为临床安全用药提供参考。方法:收集孝感市2011-2015年参麦注射液ADR/ADE报告共 243例,并对患者的人群特征、给药途径、用法用量、ADR/ADE临床表现、严重ADR/ADE的特点等进行统计与分析。结果:243例ADR/ADE中,以女性(150例,61.73%),50岁以上患者(180例,74.08%)用药1 h内(121例,49.79%)ADR/ADE多发,累及器官及系统以循环系统反应(80例,32.92%),皮肤及附件损害(43例,17.70%)为主;严重ADR/ADE 23例(9.47%),以过敏反应为主。结论:临床应用参麦注射液时,应加强对女性、老年人和用药1 h内的监测,辨证用药,发生严重ADR/ADE时,及时停药及对症处理,转归良好。
【关键词】参麦注射液;不良反应;不良事件;分析
参麦注射液为国家基本药物目录品种,由红参和麦冬组成,具有益气固脱,养阴生津、生脉之功用。主要用于治疗气阴两虚型之休克、冠心病、病毒性心肌炎、慢性肺源性心脏病、粒细胞减少症。能提高肿瘤患者的免疫功能,与化疗药物合用时,有一定的增效作用,并能减少化疗药物所引起的毒副反应[1]。药品不良反应(adverse drug reaction,ADR)是指合格药品在正常用法用量下出现的与用药目的无关的有害反应[2],是药品使用过程中的固有风险,严重影响着药品的安全性。药品不良事件(ADE)是指药物治疗过程中所发生的任何不幸的医疗卫生事件,是与药物有联系的机体损害,而这种事件不一定与药物治疗有因果关系。参麦注射液为临床常用药品,其ADR常有报道[3-4]。本文对孝感市2011年至2015年上报国家药品不良反应中心的243例ADR/ADE报告进行分析,旨在促进临床合理用药,降低参麦注射液的用药风险。
1 资料与方法
1.1资料来源
通过国家药品不良反应监测系统下载2011 年1月 -2015年12月孝感市上报国家药品不良反应中心的参麦注射液ADR/ADE报告305份,排除可能无关、无法评价和资料不完整的报告62份,依据原卫生部ADR因果关系判断标准进行判断[5],对评价为肯定、很可能和可能的243份报告进行分析。
1.2方法
统计分析患者性别和年龄,用药剂量、给药途经和ADR发生的时间,ADR/ADE累及器官及临床表现、严重ADR发生的特点。采用Excel 2003进行统计。
2 结果
2.1一般情况
243例 ADR报告中,男 93例(38.27%),女150例(61.73%),男女比例为1∶1.61;年龄最小为20岁,最大80岁以上,平均年龄(58.96± 14.24)岁,见表1。患者无ADR/ADE家族史的238例,有ADR/ADE家族史的5例;有ADR/ADE既往史的8例,无ADR/ADE既往史的235例。按报告来源分类,一级医院 75例(30.87%),二级医院146例(60.08%),三级医院 22例(9.05%);医生 181例(74.49%),护士 36例(14.81%),药师 23例(9.47%),其他人员3例(1.23%)。引起ADR的药品来自6家药品生产企业。
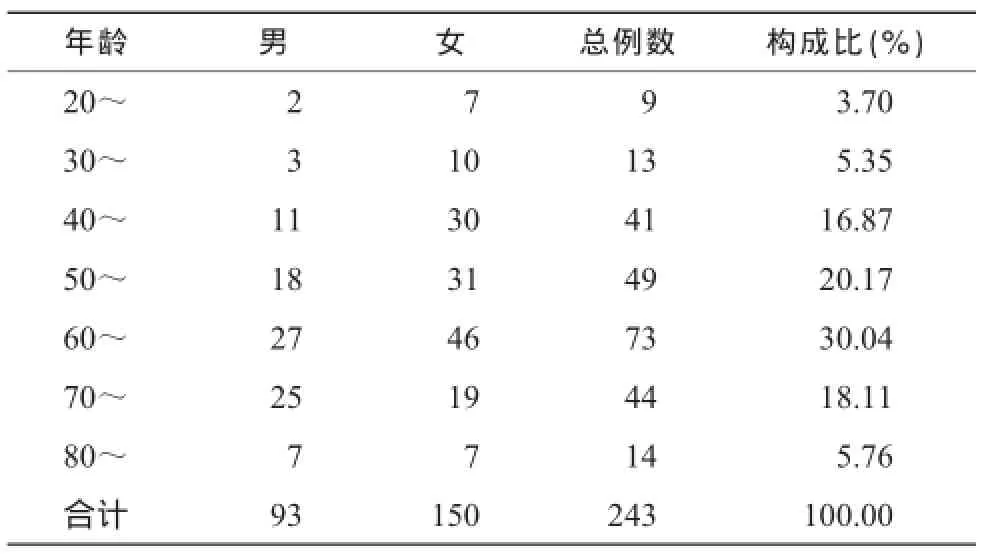
表1 243例ADR报告不同年龄分布
2.2ADR的因果关系与转归
根据ADR因果关系判断标准[5],肯定是指用药与ADR有合理的时间顺序,该反应与已知的ADR相符合,停药后反应停止,重新开始用药反应再现;很可能是时间顺序合理,该反应与已知的ADR相符合,停药后反应停止,无法用患者疾病来合理地解释;可能是时间顺序合理,与已知的ADR相符合,患者疾病或其他治疗也可造成这样的结果。在243例ADR/ADE中,很可能80例,可能77例,肯定86例;痊愈146例,好转97例。
2.3ADR发生的时间、药品用量和给药途径统计
分别见表2、表3和表4。

表2 ADR发生的时间

表3 药品用量分布
2.4引起ADR/ADE的原患疾病统计
243例ADR/ADE报告中,患者的原发疾病以心血管系统疾病最多,共140例(57.61%),见表5。
2.5ADR/ADE累及的主要器官或系统及临床表现分布
243例ADR/ADE报告中,新的ADR/ADE 35例(14.40%);一般病例 220例(90.53%),严重病例 23例(9.47%),以过敏反应多见。ADR/ADE累及的主要器官或系统见表6,严重ADR/ADE表现见表7。

表4 给药途径分布

表5 243例ADR/ADE的原患疾病分布

表6 243例ADR/ADE累及的主要器官/系统及临床表现
3 讨论
3.1ADR/ADE与性别、年龄、用药时间、药品用量和给药途径的关系
参麦注射液是中药注射剂中发生ADR频率较高的品种[6-7]。本次分析的243例ADR中,男93例(38.27%),女150例(61.73%),从年龄的分布来看,大多数的病例集中于50岁以上的年龄组,占74.08%,女性和50岁以上的老年人ADR例数较多,与文献报道基本一致[3]。究其原因,可能是中老年人心脑血管疾病发病率高,且存在不同程度的脏器功能减退,基础疾病较多,机体耐受力较差;女性也存在ADR耐受力较差等特点,故较容易发生ADR。
由表2显示,用药1 h内发生ADR者121例,占49.79%。可见参麦注射液的 ADR多为急性反应,其潜伏期短,例如皮肤及附件损害、胸闷、呼吸困难和过敏反应等,同时也提示用药初期观察ADR的重要性。
从药品用量统计看,50 mL和100 mL为参麦注射液的两个常用规格,药品说明书中用法提示可直接静脉滴注,临床使用中也是直接静脉滴注较多,出现的ADR也最多,占73.66%,这可能与参麦注射液直接静脉滴注,药物浓度过高,药物直接进入人体,缺乏屏障,容易导致ADR有关[8]。过量用药 5例(每次用量> 100 mL),用药后出现恶心、呕吐、呼吸气促、发绀、呼吸困难等临床表现,立即停药并给予对症处理,未发生严重后果。
3.2引起ADR/ADE的原患疾病统计分析
参麦注射液是临床应用较为广泛的中药注射剂,主要成分为人参皂苷、麦冬皂苷、麦冬黄酮及微量人参多糖、麦冬多糖等[9]。适用于气阴两虚的休克、冠心病、病毒性心肌炎、慢性肺心病、粒细胞减少症和肿瘤的辅助治疗。本次分析的病例中参麦注射液各科均有用药,主要用于休克、低血压、高血压、动脉硬化、冠心病、心绞痛、病毒性心肌炎(140例,57.61%),肿瘤的辅助治疗(17例,7.00%)和血液系统疾病(8例,3.29%)的治疗。参麦注射液的功能主治为益气固脱,养阴生津,生脉。用于治疗气阴两虚证,临床用药时可能存在未辨证给药的现象。建议使用参麦注射液等中药注射剂的临床医师应学习中医理论,按中医理论进行辨证施治。
3.3ADR/ADE的临床表现和严重ADR分析
中药注射剂的ADR较为常见[10]。本次调查的243例 ADR中,引起循环系统ADR的频率最高(80例,32.92%),临床表现为心悸、心慌、紫绀、潮红、心动过速等。参麦注射液循环系统的ADR与其本身兴奋肾上腺皮质系统等药理作用及用药的滴注速度有关,临床表现一般较轻,未见严重ADR。其次是皮肤及附件的损害(43例,17.70%),表现为斑丘疹、红斑疹、瘙痒、皮疹、荨麻疹、剥脱性皮炎。过敏反应(13例)是发生率最高的严重ADR[11]。参麦注射液是以中药材为原料经提纯后获得的无菌制剂,一是药品成分复杂,二是有效成分和杂质难以分离,杂质难以去除完全,高分子杂质是引发过敏反应的重要原因。不同厂家、不同批次的中药注射剂因原材料和辅料存在一定差异,发生ADR的情况也有所差异,应引起医务人员重视。建议使用参麦注射液时,注意询问患者的过敏史和家族过敏史,并准备好过敏反应的抢救药品,做好抢救准备工作,以防万一。
综上所述,参麦注射液的ADR以循环系统的ADR和过敏反应较常见,前者较轻而后者则较严重。临床用药过程中应重视按照说明书和适应证用药,注意滴注速度和询问患者的药物过敏史,对过敏体质者需谨慎用药,以减少ADR的发生。

表7 严重ADR/ADE分类
参考文献:
[1] 关溪,徐德生.参麦注射液致过敏性休克文献分析[J].药物流行病学杂志,2013,22(1):43-45.
[2] 卫生部.药品不良反应报告和监测管理办法[S].中华人民共和国卫生部令第81号.2011-05-04.
[3] 吴海雯.参麦注射液不良反应/事件分析[J].药物流行病学杂志,2014,23(9):543-545.
[4] 李万红,张蓓蓓,周婷婷.参麦注射液致36例不良反应报告分析[J].海峡药学,2015,27(6):278-279.
[5] 杜晓曦.药品不良反应报告和监测管理办法培训教材[M].北京:人民卫生出版社,2012:47-49.
[6] 张志伟,张万智,唐晓霞.2011-2014年孝感市药品不良反应/事件报告描述性分析[J].药物流行病学杂志,2015,24(8):483-487.
[7] 朱峰,郭代红,袁凤仪,等.3695例中药注射剂不良反应分析[J].药物流行病学杂志,2015,24(3):15-160.
[8] 李达,秦先涛,周艳.某院208例药品不良反应报告分析[J].中国执业药师,2016,13(1):48-51.
[9]刘存富,颜廷华.参麦注射液临床应用的安全性评估及其影响因素分析[J].中国药房,2014,25(44):4195-4197.
[10] 郭玉姝,王媛媛,韦劲,等.303例药品不良反应报告分析[J].中国执业药师,2015,12(6):45-48.
[11]汤松,张万智,唐晓霞.181例严重药品不良反应/事件报告分析[J].中国执业药师,2015,12(10):39-43.
doi:10.3969/j.issn.1672-5433.2016.08.010
收稿日期:(2016-03-29)
作者简介:张予军,男,主管药师。研究方向:医院药学。E-mail:15307296611@189.cn张万智,男,主任药师。研究方向:医院药学。通讯作者E-mail:zwz19621225@163.com
Analysis of Reports of Adverse Drug Reactions/Events Caused by Shenmai Injection
Zhang Yujun,Cheng Zhi,Zhang Wanzhi(Department of Pharmacy,Pu Ai Hospital of Anlu City,Hubei Anlu 432600,China)
ABSTRACTObjective:To analyze the characteristics of adverse drug reactions/adverse drug events(ADR/ADE)caused by shenmai injection in order to provide a reference for clinical medication safety.Methods:A total of 243 cases of ADR/ADE caused by shenmai injection reported in Xiaogan city from 2011 to 2015 were collected,in which the population characteristics of the patient,route of administration,dosage,clinical manifestations of ADR/ADE as well as characteristics of serious ADR/ADE were statistically analyzed.Results:In the 243 cases of ADR/ADE,150(61.73%)were female,and 180(74.08%)were at ages of more than 50 years.ADR/ADE occurred within 1 h after administration in 121 cases(49.79%),which involved in circulatory system in 80 cases (32.92%)and caused the damages of skin and its appendages in 43 cases(17.70%).Twenty-three cases(9.47%)of severe ADR/ADE were observed,most of which were allergic reactions.Conclusion:The monitoring on female and elderly patients and the ADR/ADE occurring within 1 h after administration as well as syndrome differentiation treatment should be strengthened.The prognosis of immediate withdrawal of the drug and symtomatic treatment is good when serious ADR/ADE occurred.
KEY WORDSShenmai Injection;Adverse Reaction;Adverse Event;Analysis

