维吾尔族肾病综合征患儿他克莫司全血谷浓度监测分析
李红健,刘金岩,刘文丽,鲍 瑞,于鲁海
新疆自治区人民医院,乌鲁木齐 830001
*通信作者
维吾尔族肾病综合征患儿他克莫司全血谷浓度监测分析
李红健,刘金岩,刘文丽,鲍瑞,于鲁海*
新疆自治区人民医院,乌鲁木齐 830001
[摘要]目的监测维吾尔族原发性肾病综合征(PNS)患儿他克莫司全血谷浓度并分析相关临床数据,以期为维吾尔族PNS患儿个体化应用他克莫司提供依据。方法对接受他克莫司治疗的70例维吾尔族PNS患儿的血药浓度、生化检验指标及合并用药进行回顾性调查分析,探讨他克莫司全血谷浓度与临床疗效的相关性,根据临床疗效分为完全缓解组(CR组)、部分缓解组(PR组)、未缓解组(NR组)。结果CR组剂量标准化谷浓度为(2.95±1.17)ng/mL/[mg/(kg·d)]、PR组剂量标准化谷浓度为(4.22±2.92)ng/mL/[mg/(kg·d)]、NR组剂量标准化谷浓度为(1.72±1.43)ng/mL/[mg/(kg·d)],三组比较差异有统计学意义(P<0.05),但三组给药剂量差异无统计学意义(P>0.05)。他克莫司治疗维吾尔族PNS患儿的缓解率为75.71%。结论他克莫司全血谷浓度与药物剂量及相关药物代谢基因相关,在全血谷浓度达5~10 ng/mL时,可达到满意的治疗效果。
[关键词]他克莫司;原发性肾病综合征;全血谷浓度;临床疗效
0引言
原发性肾病综合征(Primary nephrotic syndrome,PNS)是儿童常见的肾小球疾病,临床表现为大量蛋白尿、低白蛋白血症、高脂血症和不同程度的水肿,约占小儿时期肾病综合征总数的90%[1]。他克莫司(FK506)是一种大环内酯类免疫抑制剂,目前已广泛用于儿童PNS的治疗。由于其治疗窗窄,体内药物浓度易受各种因素的影响(如药物应用、药物之间的相互作用、制剂等因素)而产生变化,影响患者的治疗疗效。有研究表明,维吾尔族与汉族患者他克莫司的日剂量与全血谷浓度有一定的差异性[2]。来我院就诊的维吾尔族患儿众多,有关维吾尔族PNS患儿给药剂量与血药浓度及临床疗效相关性的研究未见报道。因此,本试验对在我院住院接受他克莫司治疗的维吾尔族PNS患儿的全血谷浓度、生化检验指标及合并用药进行回顾性调查分析,以期为维吾尔族PNS患儿个体化应用他克莫司提供依据。
1资料和方法
1.1临床资料选取2012年12月至2014年12月在我院儿科住院的维吾尔族PNS患儿70例,其中男41例,女29例,年龄(11.22±4.22)岁,病程1~120个月。未行肾穿刺病理检查25例,行肾穿刺病理检查45例;膜性肾病22例,微小病变11例,增生性肾小球肾炎5例,局灶节段性肾小球硬化4例,系膜增生性肾炎3例。根据临床疗效分为完全缓解组(CR组)、部分缓解组(PR组)、未缓解组(NR组)。
1.2纳入标准临床诊断为肾病综合征、年龄<18岁的患儿;患儿在出院前接受FK506治疗(剂量0.05~1.00 mg/kg),且治疗浓度达稳态(至少5 d)后,在出院前1~3 d清晨给药前采血于肝素抗凝采血管内。采用酶增强免疫分析法(美国雅培公司I1000生化仪及相关配套试剂)测定全血谷浓度。每次检测随行的高(11.4~17.7 ng/mL)、中(6.75~10.3 ng/mL)、低(3.41~5.55 ng/mL)质控均在允许的范围内。具有FK506全血谷浓度监测数据及当日实验室生化检查结果的患儿均可纳入本试验。
1.3诊断标准所有PNS患儿均符合2000年中华医学会儿科分会肾脏病学组制定的《小儿肾小球疾病的临床分类、诊断及治疗》原发性PNS的诊断标准[3]。
1.4临床指标记录患儿出院时尿素氮(BUN)、血肌酐(Scr)、血浆白蛋白(Alb)、总胆固醇(TC)、三酰甘油(TG)、凝血酶原时间(PT)、血浆纤维蛋白原(Fib)、D-二聚体等相关生化指标;记录患儿水肿消退情况。
1.5疗效判定标准根据患儿出院时病历中记录情况,按照临床评价标准进行临床疗效评价。临床评价标准[1]:完全缓解(CR):临床症状与体征消失,尿常规、尿蛋白转阴(-),血清白蛋白、胆固醇、血脂水平等指标正常;部分缓解(PR):临床症状与体征减轻,血清白蛋白、胆固醇、血脂水平等指标均明显改善,尿常规、尿蛋白阳性<(+++);未缓解(NR):临床症状与体征存在,尿常规、尿蛋白≥(+++)。

2结果
2.1患儿一般资料及生化指标比较70例维吾尔族PNS患儿纳入研究,收集记录患儿出院时的相关生化指标进行单因素方差分析,结果见表1。70例患儿根据临床疗效分为完全缓解组(CR组)20例、部分缓解组(PR组)33例、未缓解组(NR组)17例,缓解率为75.71%(53/70)。三组总蛋白、白蛋白、24 h尿蛋白定量比较差异有统计学意义(P<0.05)。
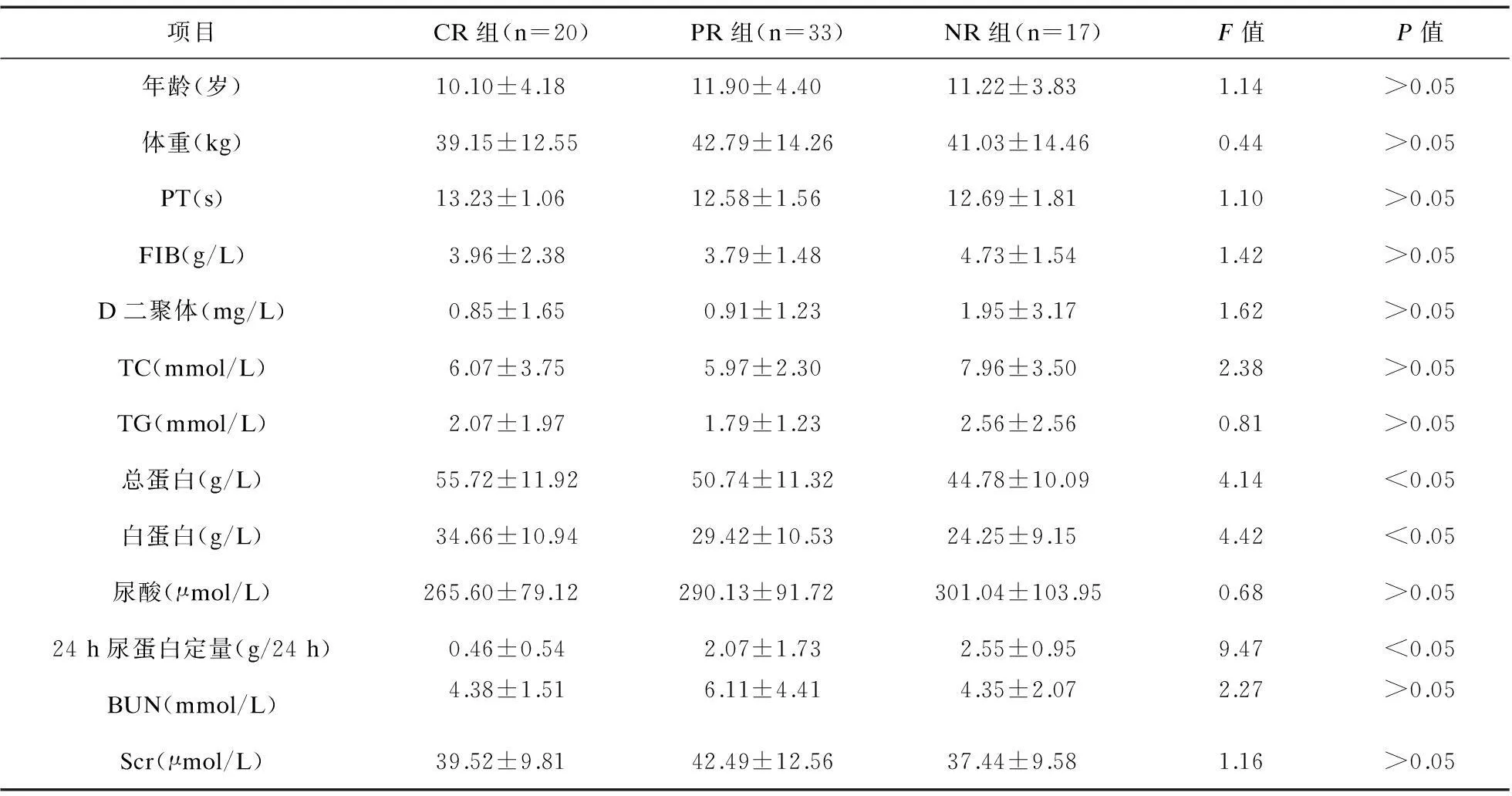
表1 维吾尔族PNS患儿临床资料及生化指标比较
2.2FK506的剂量标准化谷浓度与疗效的相关性对不同临床疗效患儿的剂量标准化谷浓度进行比较,NR组平均剂量标准化谷浓度明显比CR组、PR组偏低,三组比较差异有统计学意义(P<0.05),但给药剂量三组间差异无统计学意义(P>0.05)。FK506的给药剂量与全血谷浓度未呈现相关性(r=0.021,P>0.05),FK506的给药剂量与剂量标准化谷浓度呈负相关(r=-0.350,P<0.05)。见表2。

表2 维吾尔族PNS患儿他克莫司日剂量与全血谷浓度
2.3不良反应在本次回顾性调查中,70例维吾尔族PNS患儿未见相关药物不良反应。
2.4合并用药情况70例维吾尔族PNS患儿均有合并用药。按用药频次由高到低排列依次是甾体激素如醋酸泼尼松、甲泼尼龙(70次),抗高血压药如卡托普利、福辛普利钠、氨氯地平、硝苯地平(58次),补钙制剂如碳酸钙、阿尔法骨化醇(70次),抗凝药如双嘧达莫(36次),降脂药如辛伐他汀、普伐他汀(23次)。
3讨论
FK506是一种被推荐用于治疗儿童PNS的强效免疫抑制药,FK506的疗效、不良反应与用药剂量有一定的相关性,在药物代谢动力学、药物效应动力学上又存在明显的个体差异。有文献报道,汉族PNS患者FK506的服药剂量与全血谷浓度呈正相关[4];CYP3A5不同基因型PNS患者他克莫司血浓度与剂量比值(C/D)差异有统计学意义(P<0.05),CYP3A5*1/*1型和CYP3A5*1/*3型患者需要比CYP3A5*3/*3型患者服用更高剂量的他克莫司才能达到相同的血药浓度[5]。本研究结果显示,维吾尔族PNS患儿FK506的服药剂量与全血谷浓度不呈相关性,但CR组、PR组、NR组在全血谷浓度和剂量标准化谷浓度(C/D)等指标上差异存在统计学意义(P<0.05),与上述文献报道的结果不尽相同,考虑可能与FK506在维吾尔族PNS患儿体内代谢复杂、个体差异大有关。有文献报道,参与FK506代谢的主要是CYP3A4和CYP3A5,CYP3A5*3突变发生频率在不同种族间有所不同[6]。Roy等[7]报道,中国人CYP3A5*3的发生频率为71%~76%,非洲黑人CYP3A5*1的发生频率为55%,高加索人为10%~40%,亚洲人为33%[8]。种族间或个体间的基因多态性可能导致不同个体服用相同剂量的FK506后,药物浓度差异较大,但有关维吾尔族PNS患儿基因多态性与FK506全血谷浓度及剂量之间的关系还未见相关报道,还有待进一步的研究。
指南推荐FK506治疗肾病综合征的全血谷浓度范围为5~10 ng/mL,本文FK506治疗70例维吾尔族PNS患儿的缓解率为75.71%,与国内有关文献报道的结果相近[4],CR组、PR组的全血谷浓度与NR组差异均有统计学意义(P<0.05),CR组、PR组的全血谷浓度范围均在5 ng/mL以上,NR组血药浓度明显比CR组、PR组偏低,FK506血药浓度偏低可能是NR组临床疗效不佳的主要因素之一。
文献报道,FK506可与近150种(类)药物发生相互作用[9],主要经CYP3A4/5酶代谢的药物都会影响FK506的代谢。PNS患儿治疗合并用药较多,尤其要注意FK506与其他药物的相互作用问题,因此,在治疗时要特别关注。本次调查中发现,有2例患儿由于合并高血压,服用FK506同时服用氨氯地平,FK506给药剂量均为0.11 ng/(mL·mg),全血谷浓度为15.2 ng/mL和14.8 ng/mL。氨氯地平作为CYP3A和P-gp的底物,竞争性抑制FK506代谢而降低FK506的清除率,导致浓度明显增加[10]。因此,临床上FK506与钙拮抗剂合用时,需要根据FK506的浓度来调整FK506的用量,以期实现安全、有效的治疗。
在本次调查中,未发现患儿服用FK506后出现任何不良反应的记录,有文献报道,高FK506全血谷浓度的患者中发生药物不良反应的人数较多,常见不良反应主要表现为高血压、糖尿病、胃肠道反应、多毛症及牙龈增生等,在发生的不良反应中除血糖升高需药物控制外,其他类型不良反应经调整FK506剂量后症状消失[5]。因此,对于全血谷浓度较高的患儿,应做好用药监测,注意观察药物不良反应发生的情况。
参考文献:
[1]中华医学会儿科分会肾脏病学组.儿童常见肾脏疾病诊治循证指南(一):激素敏感、复发/依赖肾病综合征诊治循证指南(试行)[J].中华儿科杂志,2009,47(3):167-170.
[2]阿不都克依木·扎依提,迪丽达尔·克依木,米娜瓦尔·哈帕尔.维吾尔族与汉族肾移植术后患者他克莫司全血谷浓度的对比分析[J].中国临床药学杂志,2011,20(6):336-339.
[3]中华医学会儿科分会肾脏病学组.小儿肾小球疾病的临床分类、诊断及治疗[J].中华儿科杂志,2001,39(12):746-747.
[4]兰顺,叶冬梅,莫广艳.他克莫司血药浓度与肾病综合征的临床疗效相关性研究[J].中国现代应用药学,2013,30(8):896-900.
[5]叶冬梅,刘晓霞,兰顺,等.CYP3A5基因型对肾病综合征患者他克莫司血药浓度与剂量比的影响[J].中国医院药学杂志,2014,34(24):2139-2143.
[6]欧阳萌,辛华雯.他克莫司的药物基因组学研究进展[J].中国药师,2013,16(12):1785-1787.
[7]Roy JN,Lajoi EJ,Zijenah LS,et al.CYP3A5 genetic polymorphisms in different ethnic populations[J].Drug Metab Dispos,2005,33(7):884-887.
[8]Lamba JK,Lin YS,Shuetz EG,et al.Genetic contribution to variable human CYP3A mediated metabolism[J].Adv Drug Deliv Rev,2002,54(10):1271-1294.
[9]袁梅,张弋.中药成分与常见食物对他克莫司血药浓度的影响[J].药品评价,2013,10(16):20-24.
[10]周亚男,杨梦,左笑丛.钙拮抗剂与他克莫司的药物相互作用[J].中国药学杂志,2013,48(2):81-84.
Monitoring the blood trough concentration of tacrolimus in the treatment of Uygur children with nephrotic syndrome
LI Hong-jian,LIU Jin-yan,LIU Wen-li,BAO Rui,YU Lu-hai*
(Xinjiang Autonomous People′s Hospital,Urumqi 830001,China)
[Abstract]ObjectiveTo monitor the tacrolimus blood concentration in the treatment of Uygur children with nephrotic syndrome and to analyze the related clinical data in order to provide evidence for individualized application of tacrolimus in PNS patients.MethodsThe blood drug concentration,biochemical indexes and combined medication of 70 patients with PNS were retrospectively analyzed,and the relationship between tacrolimus blood concentration and clinical efficacy was evaluated.According to the clinical curative effect,patients were divided into complete remission group (group CR),partial remission group (group PR),and no remission group (group NR).ResultsThe dose normalized trough concentration of group CR,group PR and group NR was (2.95±1.17)ng/mL/[mg/(kg·d)],(4.22±2.92)ng/mL/[mg/(kg·d)]and(1.72±1.43)ng/mL/[mg/(kg·d)]respectively,there being significant difference among the three groups(P<0.05),but there was no significant difference on dose among the three groups(P>0.05).The remission rate was 75.71%.ConclusionThe blood concentration of tacrolimus in the treatment of nephrotic syndrome is correlated to the dose of tacrolimus and genetic polymorphism,and it can achieve satisfactory therapeutic efficacy on nephrotic syndrome patients in the range of 5~10 ng/mL of tacrolimus blood concentration.
Key words:Tacrolimus;Primary nephrotic syndrome;Trough concentration;Clinical efficacy
收稿日期:2015-05-08
DOI:10.14053/j.cnki.ppcr.201604023

