克唑替尼治疗进展期ALK阳性非小细胞肺癌的临床疗效研究
丁永英 朱秀华 程先鸣
430013 武汉市汉口医院(丁永英,程先鸣);442000 十堰市六里坪医院(朱秀华)
克唑替尼治疗进展期ALK阳性非小细胞肺癌的临床疗效研究
丁永英朱秀华程先鸣
430013 武汉市汉口医院(丁永英,程先鸣);442000 十堰市六里坪医院(朱秀华)
【摘要】目的探讨克唑替尼对治疗进展期ALK阳性非小细胞肺癌的临床治疗效果。方法选取60例进展期ALK阳性非小细胞肺癌(NSCLC)患者,随机分为实验组和对照组,实验组和对照组患者分别应用克唑替尼和多西他赛进行治疗。对比两组治疗效果、不良反应及生存期。结果实验组和对照组有效率分别为76.7%,20.0%;控制率分别为93.3%、60.0%,实验组较对照组具有更好的安全性和疗效。结论克唑替尼对进展期ALK阳性非小细胞肺癌有着良好的治疗效果,其能否成为一线治疗药物,有待大样本临床试验研究。
【关键词】克唑替尼;EML4-ALK基因;非小细胞肺癌
(ThePracticalJournalofCancer,2016,31:474~476)
作为世界上最为常见的恶性肿瘤之一的肺癌,其有较高的发病率与死亡率,并且呈现出逐年增加的趋势,其中约有85%的为非小细胞肺癌(non-small cell lung cancer,NSCLC)。然而传统的化疗方案对处于进展期的肺癌治疗已经处于瓶颈期。克唑替尼(XALKORI)于2011年8月26日被美国食品药品管理(FDA)批准上市,成为治疗间变性淋巴瘤酶(ALK)基因表达异常的NSCLC[1]。成为治疗肺癌的里程碑的意义。
1资料与方法
1.1一般资料
选取2013年7月-2015年3月我院收治的60例处于进展期ALK阳性非小细胞肺癌(NSCLC)的患者。
纳入标准:①NSCLC患者经组织细胞学检查确诊,同时检查ALK基因表现为阳性的;②年龄为30~60岁;③经卡式评分评定分数≥70分者;④通过CT扫描后发现病灶并可以进行测量;⑤重要组织器官(心、肝、肾、骨髓)功能均正常者;⑥患者预计生存期均大于3个月者。
排除标准:①伴有心肺或者肾功能衰竭的患者;②确诊为NSCLC但ALK基因检测呈阴性的患者。
将符合纳入标准的患者,根据随机数字表将其分为实验组和对照组两组。实验组患者30例,男性18例,女性12例,年龄为33~56岁,平均年龄为(53.2±13.8)岁,病理类型:腺癌12例,鳞癌18例;对照组30例,男性17例,女性13例,年龄为32~60岁,平均年龄为(54.1±16.8)岁,病理类型:腺癌16例,鳞癌14例。两组在性别构成、年龄、TNM分期、卡式评分以及病理类型等方面差异均无统计学意义(P>0.05),两组之间具有比较意义。
1.2治疗方法
实验组:使用克唑替尼对患者进行治疗,口服克唑替尼胶囊(250 mg/粒),1粒/次,早晚各服用一次。
对照组:给予患者多西他赛单药进行化疗,使用剂量为75 mg/m2,以静脉滴注方式给药,以21 d为1个疗程,化疗前1 d口服8 mg地塞米松,2次/d,进行常规预处理,以免出现过敏反应。
对处于治疗期间的两组患者给予定期血常规以及肝肾功能复查。治疗一个月后,对患者行影像学检查以及对疗效评估。
1.3疗效评估标准
使用WHO实体肿瘤疗效评价标准(RECIST)将治疗效果分为:完全缓解(CR),部分缓解(PR),病情稳定(SD)以及继续进展(PD)四个层次。有效率=(CR+PR)/总例数×100%。而不良反应评价则采用美国国立癌症研究所(NCI)所制定的毒性评价标准(CTCAE)进行分级评估[2]。
1.4统计学方法

2结果
2.1比较两组患者的临床疗效
有效率和控制率,实验组分别为76.7%和93.3%,明显高于对照组的20.0%以及60.0%,差异均有统计学意义P<0.05,见表1。
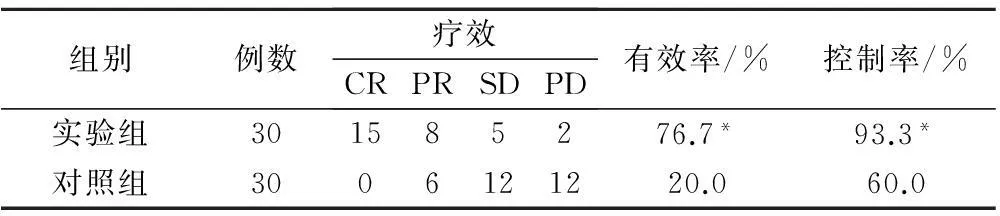
表1 两组患者在疗效方面的对比/例
注:*为P<0.05,与对照组比较。
2.2两组患者不良反应情况比较
实验组在恶心呕吐、骨髓抑制、脱发、周围神经炎以及肝功能异常方面的发生率,要明显低于对照组(P<0.05);而实验组在视觉效应以及水肿方面的发生率显著高于对照组(P<0.05)。出现不良症状后给予相应的缓解措施以缓解症状,见表2。
2.3两组患者治疗后生存情况比较
治疗结束后对患者进行,3个月随访一次的方法跟踪观察,平均随访时间为12个月。在PFS和OS评分上,实验组明显高于对照组(P<0.05),两组治疗后与治疗前比较有明显改善(P<0.05),见表3。
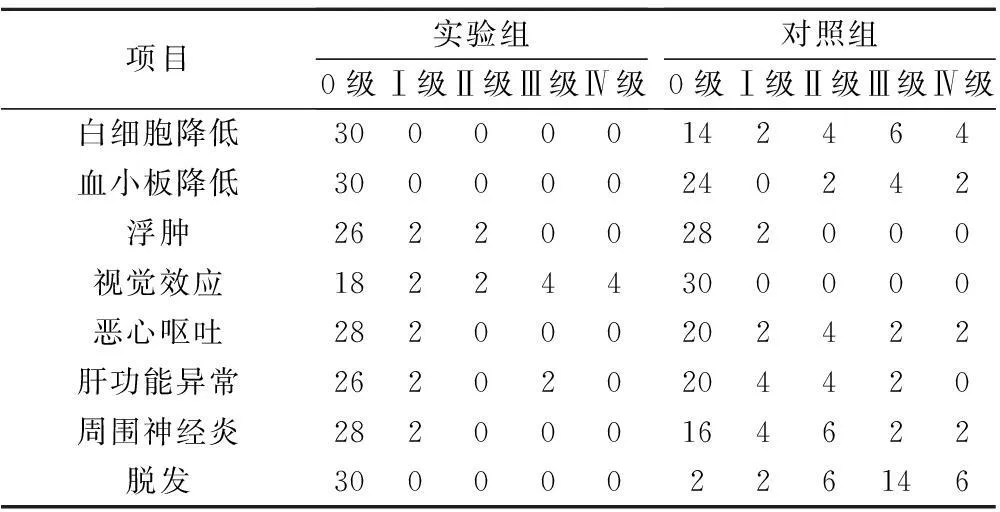
表2 两组不良反应情况比较/例
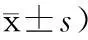
表3 PFS和OS评分比较(分,
注:*为P<0.05,与治疗前相比;△为P<0.05,与对照组相比。
3讨论
在总体肺癌的发病中NSCLC约占到了85%,并且在当NSCLC得到确诊时,便已经处于中、晚期,手术以及化疗等常规的恶性肿瘤治疗方法已经失去了治疗时机,极易出现一线标砖联合化疗药物的治疗时变,或者患者在使用一线化疗药物时出现强烈的不良反应,基于以上原因,二线治疗方案的制定在治疗NSCLC中显得尤为重要。在NSCLC患者中,ALK阳性的患者居多,在各个年龄层、吸烟或者非吸烟患者中均有表达[3-6],并且此种阳性结果的肺癌的发生率与种族、性别不呈现直接相关性关系。而通过病理学研究发现,ALK基因阳性与肺腺癌发生之间存在相关性,目前的研究表明在实性腺癌或者印戒细胞癌为主的恶性肿瘤细胞中,ALK基因为阳性表达[7-9];ALK基因阳性表达常在腺鳞癌中出现,然而在某些缺乏腺体的鳞癌中却很少发现ALK基因的阳性表达[10]。
对于ALK表达阳性的肺癌患者的治疗药物中,克唑替尼是较为有效的药物之一。此药物是一类对ATP具有竞争性抑制酪氨酸激酶的1种抑制剂,其对EML1-ALK具有特异性靶向抑制作用,从而抑制ALK基因在肿瘤细胞中的表达来达到抑制肿瘤生长加速其凋亡的目的,同时此种抑制剂对其他诸如ROS1以及c-MET等信号通路也有着一定的抑制作用。在对处于Ⅰ、Ⅱ、Ⅲ期的肺癌患者使用克唑替尼进行治疗后发现,其均得到了良好的效果,并且在不同的临床研究中被反复的研究和炎症。克唑替尼对处于进展期的ALK阳性NSCLC患者进行治疗后,患者的ORR值范
围在60%~74%,PFS范围在7.7~10.9个月[11-15]。在本次研究中,总够纳入了60例处于进展期ALK阳性的患者,其中的30例患者采用克唑替尼进行治疗,经其治疗后其结果显示,其有效率和控制率分别达到了76.7%和93.3%,明显高于传统的化疗药物进行治疗的对照组,同时也要高于之前所关于克唑替尼治疗NSCLC的报道,造成此结果的原因可能是由于本次研究所搜集的样本量不足,而导致其有效率和控制率统计上一定程度的提高,纵使如此,其结果也证明了克唑替尼对NSCLC治疗的效果。
Profle 1005以及Profile 1007的研究表明,使用克唑替尼治疗NSCLC后会存在诸如视力障碍、腹泻、恶心、水肿、呕吐、是与不正、便秘以及疲劳等不良反应症状。在本次研究中,出现不良反应主要集中在消化道方面,其次是对肝功能的损伤,而造成的谷丙转氨酶的升高等肝损伤症状。但是,其不良反应发生程度和例数与传统化疗药的对照组相比,明显的减少,发生此种情况可能是由于克唑替尼是1种具有靶向性的抑制剂有关,在发挥治疗效果时,其针对性更强,不会对其余的器官或组织造成损伤。同时,克唑替尼对患者治疗后的生活质量也有明显的提高。
综上,克唑替尼作为1种针对ALK基因阳性NSCLC患者治疗的药物是NSCLC治疗史上的一项重要的里程碑,其在治疗的有效性、安全性上均优于其他一线化疗药物,且其治疗后的不良反应较轻,更加利于患者接受。然而由于其临床上使用时间尚短,因此还缺乏临床大样本病例的研究结果,因此需要进一步对其临床效果进行研究。
参考文献
[1]董江萍.FDA批准克里唑替尼及其基因测试法治疗晚期非小细胞肺癌〔J〕.药物评价研究,2011,34(5):402.
[2]王燕,于舒飞.治疗肺癌新药cfizotinib的药理作用和临床研究进展〔J〕.中国新药杂志,2011,20(17):1602-1607.
[3]Inamura K,Takeuchi K,Togashi Y,et al.EML4-ALK lung cancers are characterized by rare other mutations,a TTF-1 cell lincage,an acinar histology,and young onset〔J〕.Mod Pathol,2009,22(4):508-515.
[4]Shaw AT,Yeap BY,Solomon BJ,et al.Effect of crizotinib on overall survival in patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement:a retrospective analysis〔J〕.Lancet Oncol,2011,12(11):1004-1012.
[5]Sun Y,Ren Y,Fang Z,et al.Lung adenocarcinoma from East Asian never-smokers is a disease largely defined by targetable oncogenic mutant kinases〔J〕.J Clin Oncol,2010,28(30):4616-4620.
[6]Zhang X,Zhang S,Yang X,et al.Fusion of EML4 and ALK is associated with development of lung adenocarcinomas lacking EGFR and KRAS mutations and is correlated with ALK expression〔J〕.Mol Cancer,2010,9(1):188.
[7]Wong DW,Leung EL,So KK,et al.The EML-4-ALK fusion gene is involved in various histologic types of lung cancers from nonsmokers with wild-type EGFR and KRAS〔J〕.Cancer,2009,115(8):1723-1733.
[8]Takahashi T,Sonobe M,Kobayashi M,et al.Clinico-pathologic features of non-small-cell lung cancer with EML4-ALK fusion gene〔J〕.Ann Sur Oncol,2010,17(3):889-897.
[9]Yoshida A,Tsuta K,Watanabe S,et al.Frequent ALK rearrangement and TTF-1/p63 co-expression in lung adenocarcinoma with signet-ring cell component〔J〕.Lung Cancer,2011,72(3):309-315.
[10]Chaft JE,Rekhtman N,Ladanyi M,et al.ALK-rearranged lung cancer:adenosquamous lung cance masquerading as pure squamous carcinoma〔J〕.J Thorac Oncol,2012,7(4):768-769.
[11]Kwak EL,Bang YJ,Camidge DR,et al.Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer〔J〕.N Engl J Med,2010,363(18):1693-1703.
[12]Camidge DR,Bang YJ,Kwak EL,et al.Activity and safety of crizotinib in patients with ALK positive non-small cell lung cancer:updated results from a phase I study〔J〕.Lancet Oncol,2012,13(10):1011-1019.
[13]Crino L,Kim D,Riely GJ,et al.Inital phase Ⅱ results with crizotinib in advanced ALK-positive non-small cell lung cancer (NSCLC):PROFILE 1005〔J〕.J Clin Oncol,2011,29(suppl 1):S7514.
[14]Shaw AT,Kim DW,Nakagawa K,et al.Crizotinib versus chemotherapy in advanced ALK positive lung cancer〔J〕.N Engl J Med,2013,368(25):2385-2394.
[15]Mok T,Kim DW,Wu YL,et al.First-line crizotinib versus pemetrexed-cisplatin or pemetrexed-carboplatin in patients (pts) with advanced ALK-positive non-squamous non-small cell lung cancer (NSCLC):results of a phase Ⅲ study (PROFILE 1014)〔J〕.J Clin Oncol,2014,32(5 suppl):Abstr 8002.
(编辑:吴小红)
Clinical Study of Crizotinib for Advanced ALK Positive Non-small Vell Lung Cancer
DINGYongying,ZHUXiuhua,CHENGXianming.
HankouHospital,Wuhan,430013
【Abstract】ObjectiveTo study the clinical efficacy of crizotinib for advanced ALK positive non-small cell lung cancer (NSCLC).Methods60 patients with advanced ALK positive NSCLC patients were randomly divided into the control group and the experiment group,The experimental group received crizotinib and the control group received docetaxel.Treatment effect,adverse reactions and survival of the 2 groups were compared.ResultsThe effective rates of the experimental group and the control group were respectively 76.7%,and 20.0%;control rates of the 2 groups were 93.3%,60.0%,the experimental group had better efficacy and safety than the control group.ConclusionCrizotinib for advanced ALK positive NSCLC is effective,and whether it can be a first-line therapy needs large sample clinical trials.
【Key words】Crizotinib;EML4-ALK gene;Non-small cell lung cancer (NSCLC)
(收稿日期2015-04-15修回日期 2015-05-04)
中图分类号:R734.2
文献标识码:A
文章编号:1001-5930(2016)03-0474-03
DOI:10.3969/j.issn.1001-5930.2016.03.038

