脑蛋白水解物片剂肽含量测定方法的改进
汤晓枢+陆志英+樊琪俊


摘 要 目的:优化脑蛋白水解物片中肽含量测定方法。方法:采用分子排阻色谱法鉴别脑蛋白水解物片中小分子肽类、高效液相色谱法测定脑蛋白水解物片中肽含量。结果:分子排阻色谱法鉴别小分子肽特异性强;高效液相色谱法测定的各种氨基酸在一定的浓度范围内与峰面积呈良好的线性关系(r>0.999),平均回收率为98.0%~102.4%。结论:该方法快速、简便、专属性强、重复性好, 结果准确可靠, 适用于脑蛋白水解物片的质量控制。
关键词 脑蛋白水解物片 质量控制 肽 分子排阻色谱 高效液相色谱
中图分类号:R282.74; R927.2; O657.72 文献标识码:A 文章编号:1006-1533(2016)03-0076-05
Optimization of a method for the determination of peptide content in cerebroprotein hydrolysate tablets
TANG Xiaoshu*, LU Zhiying, FAN Qijun
(Shanghai Greatwall Pharmaceutical Co. Ltd., Shanghai 201206, China)
ABSTRACT Objective: To optimize a method for the determination of peptide content in cerebroprotein hydrolysate tablets. Methods: A size-exclusion chromatography method and an HPLC method were used for the identification of peptide and the determination of peptide content in cerebroprotein hydrolysate tablets, respectively. Results: The result of size-exclusion chromatography method had the advantages of high specificity. The standard curve of every amino acid was linear (r>0.999)with average recovery 98.0%~102.4%. Conclusion: This method is simple, accurate, sensitive and reproducible, and can be applied in the quality control of cerebroprotein hydrolysate tablets.
KEY WORDS cerebroprotein hydrolysate tablets; quality control ; peptide; size-exclusion chromatography; HPLC
脑蛋白水解物为从健康猪新鲜大脑组织中提取的一种活性肽类水解物,其作为一种大脑所特有的肽能神经营养物质,通过作用于中枢神经,调节和改善神经元的代谢,促进突触的形成,诱导神经元的分化,并进一步保护神经细胞免受各种缺血和神经毒素的损害[1-2]。脑蛋白水解物片在临床上广泛用于改善失眠、头痛、记忆力下降、头晕及烦躁等症状,可促进脑外伤后遗症、脑血管疾病后遗症、脑炎后遗症、急性脑梗塞和急性脑外伤的康复。药理实验结果显示,脑蛋白水解物主要药效成分为小分子肽,以上肽类能通过血脑屏障,促进脑内蛋白质的合成,影响呼吸链,具有抗缺氧的保护能力,改善脑内能量代谢,激活腺苷酸环化酶和催化其它激素系统,并提供神经递质、肽类激素及辅酶前体[3-4]。
脑蛋白水解物片现行的质量标准规定药品规格为6.5 mg(按氨基氮计算)或14.4 mg(按总氮计算)[5]。在该项国家标准中,只有2项显色反应作为鉴别反应,并只采用滴定法对产品的总氮、氨基氮含量进行控制,方法落后,专属性与有效性都较差。缺乏对脑蛋白水解物片中主要药效成分小分子肽质量控制的科学方法及指标。
本研究参考文献提高了脑蛋白水解物片质量标准,通过分子排阻色谱法对小分子肽进行鉴别[6-7],并采用Waters AccQ-Tag衍生法来测定脑蛋白水解物片肽含量[8-10],制订出针对主要药效成分小分子肽合理的质量控制指标。提高了脑蛋白水解物片质量可控性,使制剂各组分达到有效剂量范围,从而保证疗效。
1 材料与方法
1.1 仪器与试药
Agilent 1100液相色谱仪,DAD检测器、自动进样器(安捷伦科技中国有限公司)。Waters 2695/2487液相色谱仪,VWD检测器、自动进样器(美国Waters公司)。Sartorius BP121S电子天平(赛多利斯科学仪器北京有限公司)。Sartorius BP121S电子天平(赛多利斯科学仪器北京有限公司)。
脑蛋白水解物对照品溶液(批号:140697-200602)、16种氨基酸对照品(批号:624-200104)和D-正亮氨酸对照品(批号:140687-200401)均购自中国药品生物制品检定所。脑蛋白水解物片(批号:20131001)为本公司产品。Waters AccQ-Fluor试剂盒(美国Waters公司,氨基酸衍生用)。乙腈和异丙醇为色谱纯,水为超纯水,磷酸氢二钾、磷酸二氢钾、乙酸钠、磷酸均为分析纯。
1.2 色谱条件
1.2.1 分子排阻色谱
采用Agilent 1100液相色谱仪和TSK GEL 2000 SWxl 型凝胶色谱柱(7.8 mm×300 mm,5 μm),流动相:磷酸盐缓冲液(取磷酸氢二钾10.63 g与磷酸二氢钾5.31 g,加异丙醇50 ml,加水至约800 ml,用磷酸调节pH至7.0,加水稀释至1000 ml)。柱温:30 ℃。检测波长:280 nm。流速:0.6 ml/min,进样量10 μl。
1.2.2 HPLC
采用Waters 2695/2487液相色谱仪和Kromasil 100-5 C18色谱柱(4.6 mm×250 mm,5 μm),流动相A:将乙酸钠19.05 g溶解于1 000 ml水,用磷酸调pH至5.00;流动相B:60%乙腈溶液。上样后按表1进行梯度洗脱。柱温:37.0 ℃。检测波长:248 nm。流速:1.4 ml/min,进样量5 μl。
1.3 溶液制备
1.3.1 对照品溶液的制备
取中国药品生物制品检定所购得脑蛋白水解物作为对照品溶液。
按表2称取需测定的16种氨基酸的对照品置于100 ml容量瓶中,以6 mol/L盐酸5 ml溶解,加水至刻度,摇匀,作为对照品贮备液;精密量取1 ml至100 ml容量瓶中,精密加入内标溶液(2 mg/ml D-正亮氨酸溶液)1 ml,加水至刻度,摇匀,作为氨基酸对照品溶液。
1.3.2 供试品溶液的制备
取脑蛋白水解物片2片,研细,加水10 ml溶解,滤过,作为脑蛋白水解物供试品溶液。
取脑蛋白水解物片20片,研细。精密称取该粉末0.72 g,置100 ml量瓶中,加1 mol/L盐酸溶液1 ml和内标溶液1 ml(2 mg/ml D-正亮氨酸溶液),加水稀释至刻度,滤过,取续滤液作为游离氨基酸含量测定供试品溶液。
精密称取同批号脑蛋白水解物片粉末0.24 g,置硬质安瓿中,加内标溶液1 ml(2 mg/ml D-正亮氨酸溶液)和盐酸2 ml,封口,110 ℃水解20 h,放冷,启封,置蒸发皿中,水浴蒸发至干,加水使残留物溶解并稀释至100 ml,作为水解氨基酸含量测定供试品溶液。
1.3.3 空白溶液的制备
取空白辅料(按处方配制,除脑蛋白水解物)适量,研细,加水10 ml溶解,滤过,作为脑蛋白水解物空白溶液。
1.4 氨基酸分析
采用AccQ-Tag氨基酸分析法,分别取对照品溶液、游离氨基酸含量测定供试品溶液、水解氨基酸含量测定供试品溶液衍生后进样,分别测定脑蛋白水解物片中游离及水解氨基酸含量,计算肽含量(肽含量=水解氨基酸含量-游离氨基酸含量)。
2 结果
2.1 方法学考察
2.1.1 系统适用性试验
取氨基酸对照品溶液和各供试品溶液,衍生后进行的系统适用性试验结果见图1。
从图1可见,在该色谱条件下,需测定的16种氨基酸均能完全分离,峰形较佳,表明该方法系统适用性好。
2.1.2 线性范围
取16种氨基酸对照品贮备液,分别稀释200倍、133倍、100倍、80倍、67倍,配制成一系列浓度的混合对照品溶液,分别取上述对照品溶液衍生后进样,并计算16种氨基酸的线性回归方程(表3)。
结果显示,在该色谱条件下,16种氨基酸均在浓度范围内与峰面积呈良好的线性关系(r>0.999)。
2.1.3 重复性试验
取同一批制备的游离氨基酸和水解氨基酸供试品溶液各6份,衍生后测定游离和水解氨基酸的含量,并计算脑蛋白水解物片肽含量(表4)。
肽含量均值为46.81 mg/片,RSD小于2.0%,表明采用该方法测定脑蛋白水解物片肽含量重复性较好,测定结果可靠。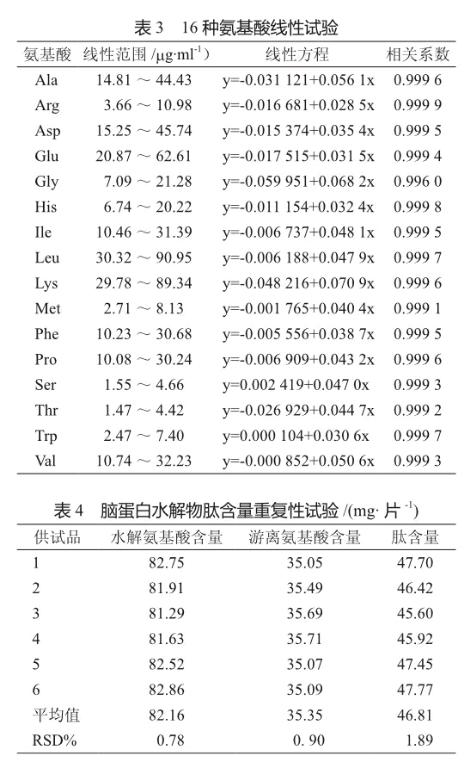
2.1.4 加样回收试验
取供试品适量,按照高(120%)、中(100%)、低(80%)三个浓度加入含16种氨基酸的对照品储备液,分别依法制备加样回收的游离氨基酸供试品溶液、水解氨基酸供试品溶液,每个浓度各3份。取上述游离和水解加样溶液衍生后进样测定,并分别计算加样回收率(表5)。
结果表明,游离和水解氨基酸含量测定中16种氨基酸的回收率均在98.0%~102.4%范围内,RSD均小于2.0%,证明本方法回收率结果良好。
2.2 肽鉴别与含量测定
2.2.1 分子排阻色谱法鉴别试验
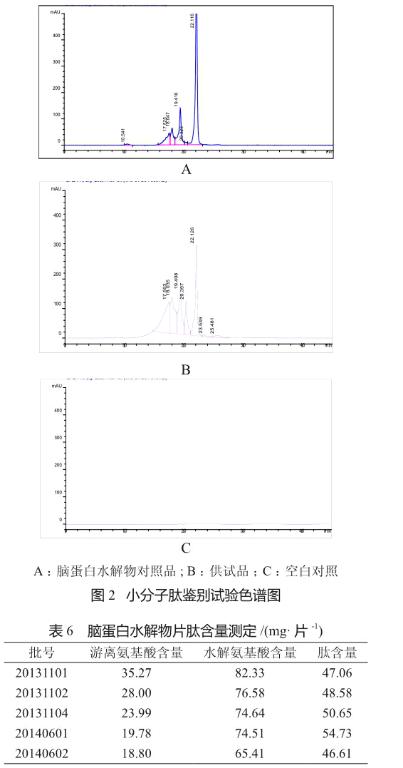
将供试品溶液肽色谱图与对照品溶液的比较,发现供试品溶液特征峰的保留时间与对照品溶液的基本一致。而脑蛋白水解物空白溶液对检测无干扰(图2),表明分子排阻色谱法鉴别脑蛋白水解物片中肽的专属性强。
2.2.2 肽含量测定
取5批次的脑蛋白水解物片制备游离和水解供试品溶液,衍生化后进样,测定并计算肽含量(表6)。
3 讨论
分子排阻色谱法的分离原理为凝胶色谱柱的分子筛机制。凝胶色谱柱的填充剂亲水凝胶表面分布着不同尺寸的孔径,药物分子进入色谱柱后,它们中的不同组分按其粒径大小进入相应的孔径内,粒径大于凝胶孔径的分子不能进入填充剂颗粒内部,在色谱过程中不被保留,最早被流动相洗脱出,表现为保留时间较短;小于所有孔径的分子能自由进入填充剂表面的所有孔径,在柱子中滞留时间较长,表现为保留时间较长;其余分子则按分子大小依次被洗脱。分子排阻色谱法可以用于高分子化合物,如蛋白质、肽类、核酸等的分离分析。脑蛋白水解物中具有生物活性及药效作用的成分为小分子肽,分子量在5 000~10 000之间,使用TSK GEL 2000 SWxl 型凝胶色谱柱进行分离,供试品与对照品在相同保留时间有相同的特征峰,显示其小分子肽类的分子量分布与对照品一致,提供了鉴别脑蛋白水解物中小分子肽类专属性更好的方式。

目前,常用的小分子肽类含量测定的方法为双缩脲比色法,其存在灵敏度差,测定结果不精确的缺点。我们对于脑蛋白水解物的成分进行分析,其主要成分为小分子肽类及游离氨基酸,小分子肽是由蛋白质中多种氨基酸以不同组成和排列方式通过肽键(也称酰胺键)相互连接形成的化合物。我们采用氨基酸分析方法(HPLC法)来测定脑蛋白水解物片中肽的含量,通过对样品进行完全的酸水解,测定脑蛋白水解物片中的氨基酸总量,并对脑蛋白水解物片中所含游离氨基酸进行含量测定,将水解后氨基酸总量减去样品中游离的氨基酸含量,准确的计算脑蛋白水解物片中的肽含量,制定出针对小分子肽含量的合理的HPLC测定方法,快速、准确、专属性强。
脑蛋白水解物片现行质量标准中规定氨基氮含量为6.5 mg/片,总氮含量为14.4 mg/片,即脑蛋白水解物片中肽的氮含量为7.9 mg/片。而肽类的含氮量一般在14%~18%之间,平均为16%。故可推算出脑蛋白水解物片中含肽约为43.9 ~56.4 mg/片。由表6中的5批测定结果可见,用氨基酸分析方法测定的肽含量在(46.6~54.7) mg/片之间,与原标准相印证,故我们脑蛋白水解物片中肽含量的限度为不少于(40~60) mg/片。
参考文献
[1] 叶良成, 毛树洲. 脑蛋白水解物的药理作用与临床应用研究进展[J]. 医药导报, 2008, 27(1): 72-73.
[2] 张荣华. 脑蛋白水解物类药物研究进展[J]. 大家健康, 2013, 7(10): 206-207.
[3] 李想. 脑蛋白水解物类药物中活性成分的比较分析[D]. 哈尔滨: 东北林业大学, 2005.
[4] 张惠敏, 王娅莉, 耿亚鹏. 猪脑蛋白水解物中小分子肽的制备及生物活性测定[J]. 河北医药, 2006, 28(3): 223-224.
[5] 国家药品标准-化学药品地方标准上升国家标准第十六册[EB/OL]. [2015-12-20]. http://pan.baidu.com/share/link?shar eid=2018922465&uk=1579445193.
[6] 汪冰, 肖新月, 程显隆, 等. 凝胶排阻色谱法研究阿胶中蛋白质及多肽相对分子质量分布规律[J]. 药物分析杂志, 2009, 29(11): 1886-1891.
[7] 连莹, 仲平. 分子排阻色谱法测定水解蛋白注射液中高分子物质[J]. 中国药品标准, 2011, 12(6): 439-441.
[8] 刘晓剑. Accq·Tag柱前衍生法分析蜂胶中的氨基酸含量[J]. 检验检疫科学, 2000, 10(6): 47-48.
[9] 庞新安, 万英. AccQ-Tag柱前衍生反相高效液相色谱法测定果品中氨基酸含量[J]. 分析仪器, 2007(4): 32-35.
[10] 陈宇堃, 梁蔚阳, 薛巧如, 等. AccQ-Tag法测定复方氨基酸注射液(18AA—V)中17种氨基酸的含量[J]. 广东药学院学报, 2008, 24(2): 243-246.

