吡格列酮/二甲双胍缓释片的处方筛选及工艺研究
·制剂研究·
吡格列酮/二甲双胍缓释片的处方筛选及工艺研究
张春红1,刘东2,3,龙朦朦2,韩邦兴2,3,陈乃富2
(1.江苏豪森药业股份有限公司,江苏 连云港 222069;2.皖西学院生物与制药工程学院,安徽 六安 237012;
3.皖西学院中药研究与开发工程技术研究中心,安徽 六安 237012)
摘要:目的确定吡格列酮/二甲双胍缓释片处方及制备工艺。方法分别以释放度及溶出度为指标对二甲双胍缓释骨架层及吡格列酮速释层进行处方和工艺研究,并对吡格列酮/二甲双胍缓释片的释放度进行考察。结果吡格列酮/二甲双胍缓释片缓释层体外释放行为与模型药物Glucophage XR(格华止)相似,速释层吡格列酮与模型药物Actos(艾可拓)体外溶出行为不相似,但30 min累计溶出药物总量相似。结论所制备的吡格列酮/二甲双胍缓释片处方组成合理,工艺可行。
关键词:吡格列酮;二甲双胍;缓释片;释放度
基金项目:国家级大学生创新创业训练计划项目(No.20141037609)
作者简介:张春红,女,研究方向:药物制剂开发,E-mail:zch76@163.com
通讯作者:刘东,男,研究方向:药物新剂型,Tel:0564-3305073,E-mail:liudong3000@126.com
中图分类号:R944.9文献标识码:A
Study on the formulation and preparation of Pioglitazone/Metformin Sustained-release Tablets
ZHANGChun-hong1,LIUDong2,3,LONGMeng-meng2,HANBang-xing2,3,CHENGNai-fu2
(1.JiangsuHansohPharmaceuticalCo.,Ltd.,Lianyungang222069,China;2.SchoolofBiologyand
PharmaceuticalEngineering,WestAnhuiUniversity,Liuan237012,China;3.CenterofTraditional
ChinesemedicineR&D,WestAnhuiUniversity,Liuan237012,China)
Abstract:ObjectiveTo ascertain the formulation and preparation of Pioglitazone/Metformin Sustained-release Tablets.MethodsThe releasing rate and dissolution rate were used as indicators to investigate the formulation and preparation of metformin layer as well as pioglitazone layer,and to investigate the releasing rate of Pioglitazone/Metformin Sustained-release Tablets.ResultsThe release behavior in vitro of sustained release layer was resemble to Glucophage XR.Though the behavior of quick release layer wasn′t resemble to the model drug,the cumulative amount of dissolution of 30 min was similar.ConclusionThe formulation of Pioglitazone/Metformin Sustained-release Tablets were feasible,and the process was reasonable.
Key words:Pioglitazone;Metformin;Sustained-release tablets;Releasing rate
吡格列酮/二甲双胍缓释片(商品名Actoplus Met XR)是一种新型的用于2型糖尿病治疗用药物[1]。本品是首个和唯一的含有缓释二甲双胍的固定剂量口服糖尿病治疗药物[2],一方面可以达到每天1次的缓释给药,另一方面可以有效改善单独使用盐酸二甲双胍治疗效果不佳病人的血糖水平。本文对吡格列酮/二甲双胍缓释片进行了处方筛选及制备工艺研究,分别对二甲双胍层及吡格列酮层的释放度和溶出度进行了考察。
1仪器与试药
1.1仪器TDP-单冲压片机(山东青州精诚机械公司);RC-8D溶出度测试仪(天津市国铭医药设备公司);Alqha-1500p紫外可见分光光度计(上海谱元仪器公司);78x-2片剂四用测定仪(上海黄浦药检仪器公司);JA2003B电子分析天平(上海越平科学仪器公司)。
1.2试药盐酸二甲双胍(广西宇泰医药科技有限公司,批号:110823,纯度:>99%);盐酸吡格列酮(西安瑞银生物科技有限公司,批号:120917,纯度:>99%);二甲双胍缓释片(Glucophage XR,美国百时美施贵宝制药公司,规格:1 000 mg,批号:MKC 90);盐酸吡格列酮片(艾可拓,日本武田制药公司,规格:15 mg,批号:0B025);欧巴代(美国卡乐康公司);乳糖(上海运宏化工有限公司,批号:K121001);微晶纤维素(MCC)(德国JRS公司,批号:120501);聚维酮(PVP-K30)、羟丙甲纤维素(HPMC-K100M,HPMC-E5)、硬脂酸镁(MS)均为安徽山河药用辅料有限公司生产;其余辅料均为药用规格,试剂均为分析纯。
2方法与结果
2.1缓释层处方筛选根据二甲双胍缓释片配方,以HPMC-K100M为缓释材料,制备规格为1 000 mg的缓释片,考察缓释效果。释放度限度以卡乐康公司初始配方库中格华止体外释放数据为依据,初步定为2 h:30%~40%,4 h:55%~65%,8 h:75%~85%。盐酸二甲双胍释放度检测方法参考《中国药典》2010年版盐酸二甲双胍片的溶出度检测方法[3],桨法,转速为50 rpm,介质为水,介质体积1 000 mL,取样时间点为2、4、8 h。由于缓释层二甲双胍层片重过大(2.0 g)不利于速释层制备,并且前期考察结果显示仅依靠HPMC作为缓释骨架在满足释放度要求的前提下,片重达到2.0 g并且无法进一步减少片重,因此选择对缓释材料硬脂酸、山嵛酸甘油酯进行考察[4,5]。
处方及试验结果如表1所示,处方2、4未能达到预定的缓释效果,处方1、3在限定片重(1.5 g)下释放度符合预定要求。结果表明,HPMC-K100M 与山嵛酸甘油酯或硬脂酸在一定比例混合使用缓释效果较好。但硬脂酸熔点较低,容易在高速压片过程中产生黏冲现象。最终筛选山嵛酸甘油酯作为混合骨架材料。 由于颗粒的堆密度较低,不利于高速压片,且会造成最终片剂的体积偏大,不利于顺应性的提高。在处方基本确定的情况下,拟通过制备工艺改进对颗粒的堆密度进行改善。

表1 盐酸二甲双胍缓释片处方及评价(批量:20片)
续表1:

处方123480%乙醇(w/w)适量适量适量适量硬脂酸镁0.3g0.3g0.3g0.3g休止角(°)36373634堆密度(g·mL-1)0.350.380.370.40颗粒水分(%)2.612.162.332.47释放度(%)2h36.541.436.840.34h59.664.164.359.88h87.584.885.382.5
2.2缓释层工艺筛选考虑通过黏合剂增加物料间结合力从而改善颗粒堆密度,将盐酸二甲双胍粉碎后,采用40% 的PVP-K30水溶液作为黏合剂,湿法工艺制备样品,结果如表2所示。加入PVP-K30水溶液可以增加颗粒堆密度,但所加入PVP-K30比例过高,并且PVP-K30对缓释片整体的释放作用无改善作用,增加其用量反而使得片重增加,降低患者使用的依从性。处方6通过考虑引入干法制粒工艺增加物料间结合紧密度,增加堆密度。结果分析:引入干法制粒后,颗粒堆密度增加,但干法制粒过程中得粒率偏低,生产效率低下。处方7中盐酸二甲双胍占总重的60%,参考Glucophage XR的处方工艺,采用40% PVP-K30水溶液对盐酸二甲双胍进行湿法制粒来改善其表面性质,增加可压性。因此将盐酸二甲双胍粉碎过200目筛后,以高浓度PVP-K30溶液先行制粒再混合其他成分进行干法制粒。结果显示该工艺在保证释放度的同时增加了干法制粒过程中的得粒率,提高了生产效率,故最终的制备工艺定为先对盐酸二甲双胍湿法制粒再混合其他成分进行干法制粒[6,7]。
2.3速释层处方及工艺研究速释层制备工艺为将处方量的氯化钠溶于20%的纯化水中,再加入80%的乙醇(w/w),边搅拌边缓缓加入处方中其他成分,持续搅拌约1 h后,过100目筛,备用。取已包隔离层的缓释片芯置包衣锅中,开启热风,片芯预热至35 ℃左右,开始包衣。包衣过程中,含药包衣液要持续进行搅拌。进风温度控制到60~80 ℃,片床控制在30~40 ℃左右,雾化压力为0.2~0.3 MPa,流量5~10 mL·min-1,中控含量,直至含量到达95%~105%范围内。以欧巴代为包衣材料,以溶出度为考察指标,处方筛选中分别考察了致孔剂的种类及比例,结果见表3。试验结果显示不同种类致孔剂对溶出度有明显的影响,氯化钠作为致孔剂效果要优于乳糖, 同时氯化钠用量增加可以提高速释层溶出度。
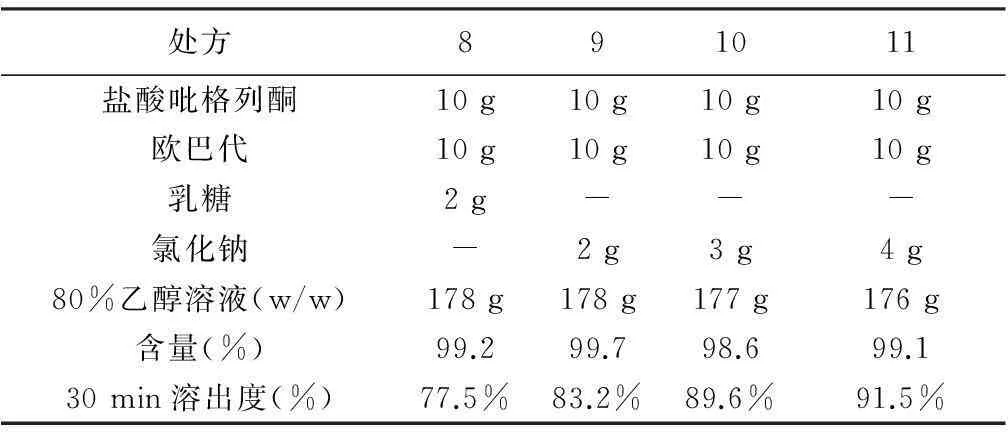
表3 盐酸吡格列酮速释层处方筛选(批量:150片)
2.4体外释放试验
2.4.1盐酸二甲双胍层体外释放试验选择纯化水为释放介质,介质体积为1 000 mL,采用桨板法,转速为50 rpm,对自制制剂及Glucophage XR进行释放度曲线的测定。取样时间点分别为1、2、4、6、8、12 h,取样时间点时分别取溶液10 mL滤过,精密量取续滤液适量,加入释放介质定量稀释为每1 mL含5 μg盐酸二甲双胍的溶液。按照释放度测定项下的方法测定[3],以f2因子作为指标,评价自研处方与模型药物Glucophage XR体外释放行为相似性,溶出曲线见图1。结果显示,盐酸二甲双胍层体外释放行为与模型药物Glucophage XR相似。
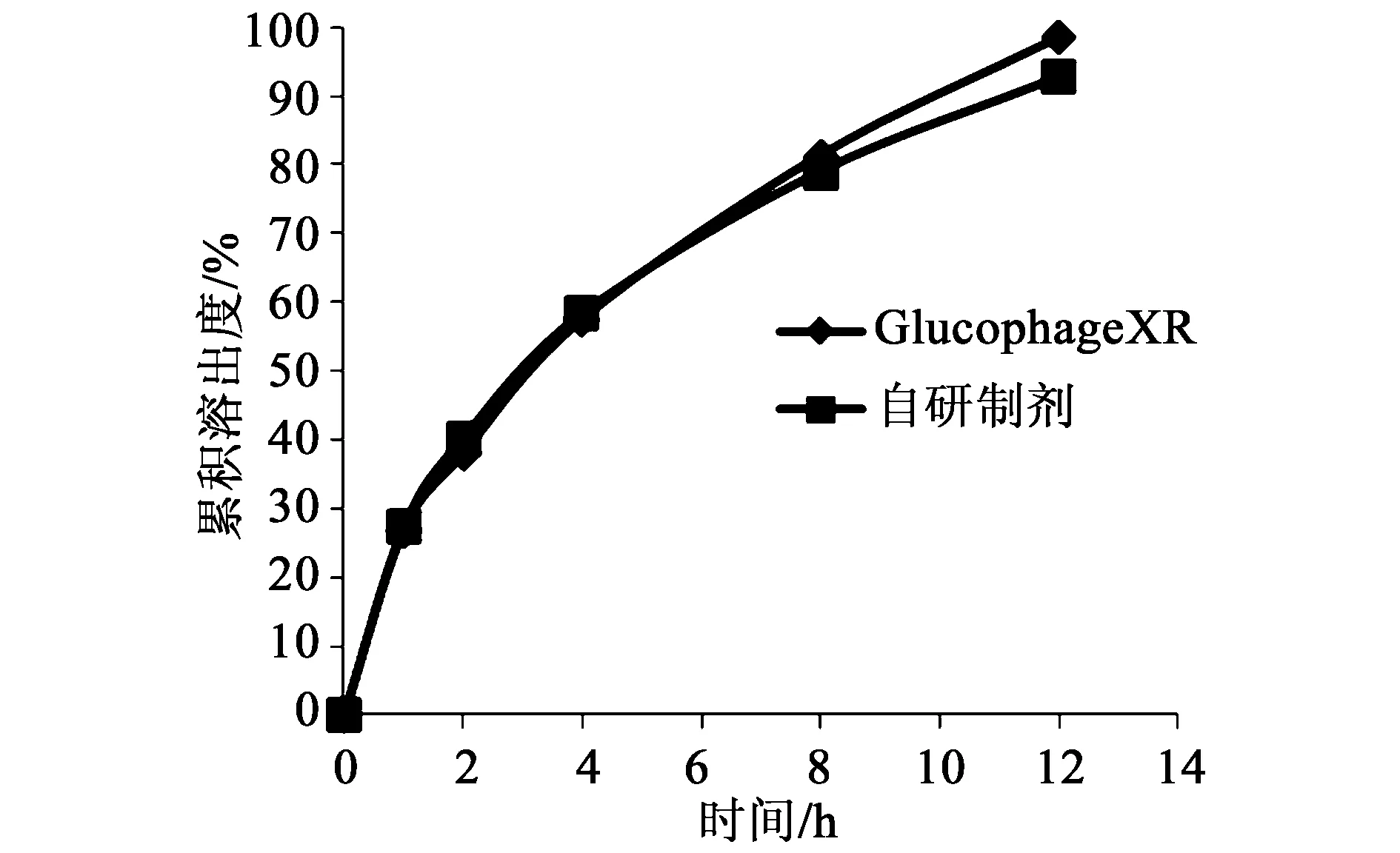
图1 盐酸二甲双胍层与Glucophage XR体外释放曲线对比
2.4.2盐酸吡格列酮层体外溶出度试验取本品[规格为15 mg·(1.0 g)-1]6片,按照盐酸吡格列酮二甲双胍缓释片溶出度测定法,选择0.1 mol·L-1盐酸溶液为溶出介质,采用转篮法,转速为50 rpm,经5、10、15、30、45 min分别取溶液10 mL,并及时补充相同体积的溶出介质。按照溶出度测定项下的方法测定不同时间点的溶出度结果[8],并以f2因子作为指标,评价自研处方与模型药物Actos体外溶出行为相似性。试验结果显示缓释层盐酸二甲双胍与模型药物Glucophage XRf2因子为75,体外溶出行为相似,速释层盐酸吡格列酮与模型药物Actosf2因子为37,体外溶出行为不相似,溶出曲线见图2。
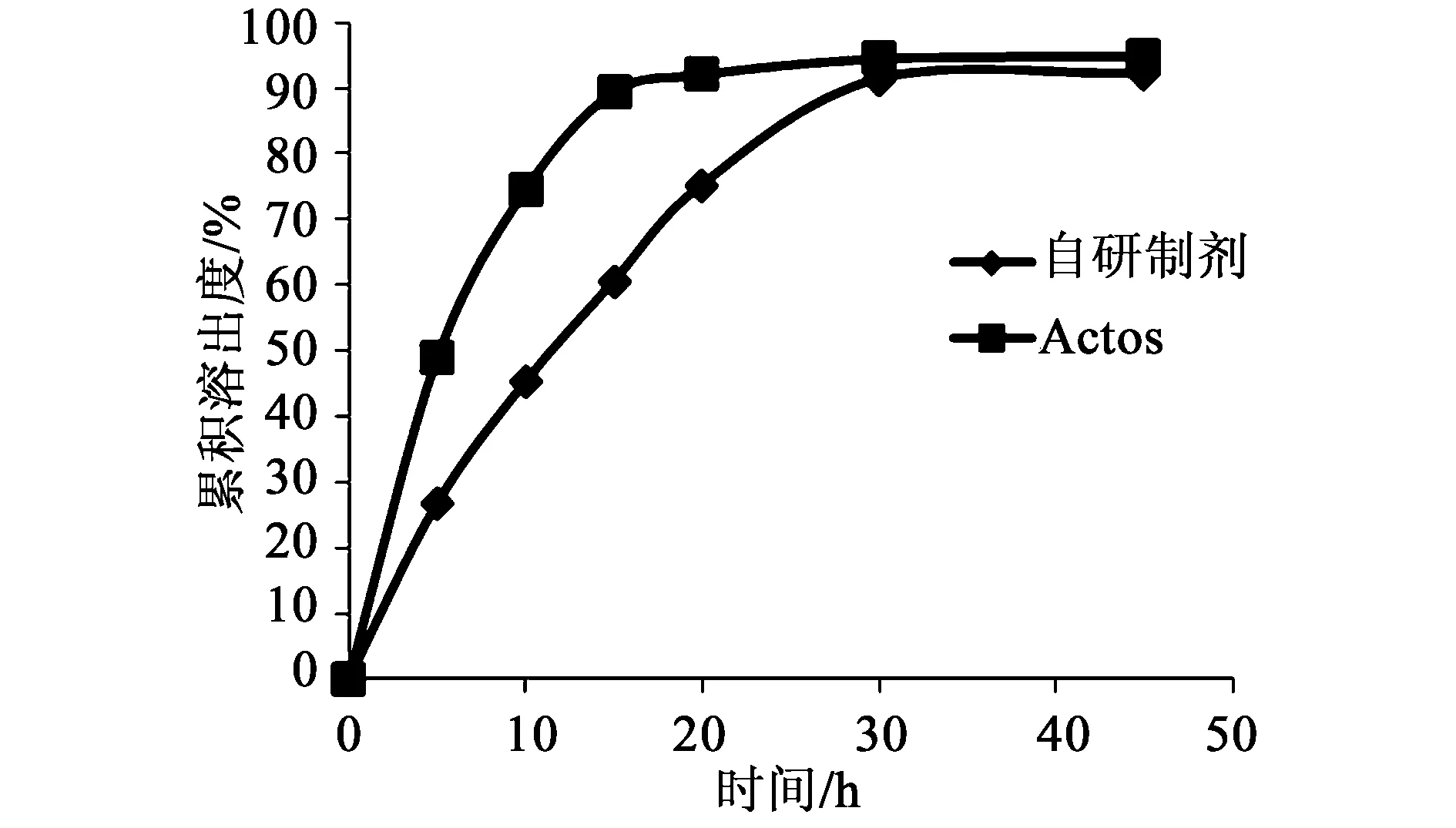
图2 盐酸吡格列酮层层与Actos体外溶出曲线对比
3讨论
本研究中盐酸二甲双胍分别采取干、湿制粒相结合的工艺与单独采用湿法或干法制粒相比,颗粒堆密度更大,更利于减小片芯体积。自研制剂速释层盐酸吡格列酮与Actos体外溶出行为不相似,其主要原因推测为两种制剂的溶出原理不同:Actos的溶出机理以崩解为主,自研制剂的溶出机理以溶解为主,机理的不同导致二者溶出行为出现一定差异,但两种制剂在30 min时溶出度均达到90%之上,累计溶出药物总量相差不大。
参考文献:
[1]Seufert J.A fixed-dose combination of pioglitazone and metformin:A promising alternative in metabolic control [J].Curr Med Res Opin,2006,22:39-48.
[2]林巧平,李薇,山莽挺,等.盐酸吡格列酮/盐酸二甲双胍缓释片的体内外评价[J].中国新药杂志,2014,23(2):154-160.
[3]国家药典委员会.中华人民共和国药典2010年版(二部)[S].北京:中国医药科技出版社,2010:625-626.
[4]林巧平,桂彬,谈颖,等.盐酸二甲双胍1 000 mg缓释片的制备及其体外释药机制考察[J].中国药房,2013,24(13):1191-1193.
[5]王智勇,纪宏宇,杜霞,等.盐酸二甲双胍缓释片的体外释放特性[J].中国医院药学杂志,2006,26(4):409-412.
[6]陆步实,侯敬文,周立新,等.非诺贝酸胆碱盐缓释片的制备及体内外评价[J].中国医药工业杂志,2013,44(9):900-903.
[7]祝侠丽,贾永艳,黄海英,等.正交设计法优化布洛芬缓释骨架片的处方工艺[J].中国药房,2014,25(9):830-832.
[8]徐芳媛,李摇娟.复方盐酸吡格列酮二甲双胍缓释片中盐酸吡格列酮溶出度的测定[J].安徽医药,2011,15(10):1230-1231.

