黄芪降浊颗粒质量标准研究
康新莉,宋英,谭睿
(1.西南交通大学生命科学与工程学院,四川成都610031;2.成都中医药大学附属医院,四川成都610075)
黄芪降浊颗粒质量标准研究
康新莉1,宋英2,谭睿1
(1.西南交通大学生命科学与工程学院,四川成都610031;2.成都中医药大学附属医院,四川成都610075)
目的建立黄芪降浊颗粒的质量标准。方法采用薄层色谱(TLC)法对黄芩、金樱子、大黄进行定性鉴别,采用高效液相色谱(HPLC)法测定制剂中黄芩甲苷的含量。结果在选定的薄层色谱条件下,层析斑点清晰,分离效果较好,阴性对照无干扰;含量测定时,黄芪甲苷质量浓度在5.42~212.52 μg/mL范围内与峰面积线性关系良好(r2=0.999 9,n=6),平均回收率为97.33%,RSD=1.85%(n=6)。结论该方法简便、准确、专属性强,可用于控制该制剂的质量。
黄芪降浊颗粒;薄层色谱法;高效液相色谱法;黄芩甲苷;质量标准
糖尿病肾病是糖尿病患者严重的并发症[1-2],其中瘀血与浊毒是其不愈或加重的症结所在。黄芪降浊颗粒由黄芪、金樱子、川芎等中药组方,是成都中医药大学附属医院经过多年的临床实践总结出来的经验方,用于糖尿病肾病患者的对症治疗,有活血化瘀、托毒排脓降浊功效[3]。根据临床需要和剂型的选择,医院将原汤剂改进为颗粒剂,旨在提高患者的用药依从性。笔者在剂型改进的基础上对黄芪降浊颗粒进行了质量标准研究,为其医院制剂注册提供依据。
1 仪器与试药
Waters 2695型高效液相色谱仪,Waters 2424 ELSD型检测器;Sartoius BS110型电子分析天平(北京赛多利斯仪器系统有限公司);KQ5200DE型超声波清洗仪(上海昆山超声波仪器厂)。黄芪降浊颗粒(成都中医药大学附属医院制剂室自制,批号为20120923,20120924,20120925);阴性对照样品(自制);黄芪甲苷对照品(批号为110781-200613)、金樱子对照药材(批号为110781-200613)、大黄对照药材(批号为110781-200613),供含量测定用,均由中国药品生物制品检定所提供;乙腈为色谱纯,其余试剂均为分析纯,水为重蒸水。
2 方法与结果
2.1 薄层色谱鉴别[4]
黄芪:取本品8 g,加60℃水20 mL,超声30 min,滤过,滤液用水饱和的正丁醇提取3次,每次20 mL,合并正丁醇液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。取缺黄芪的阴性对照样品,同法制得阴性对照品溶液。另取黄芪甲苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各5 μL,分别点于同一硅胶G板,以乙酸乙酯-甲醇-甲酸-水(10∶1∶1∶1)为展开剂,展开,取出,晾干,在紫外灯(365 nm)下检视。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱则无此斑点,见图1A。
金樱子:取本品4 g,加乙醇30 mL,超声30 min,滤过,滤液蒸干,残渣加水20 mL,乙酸乙酯振摇提取2次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加甲醇0.5 mL使溶解,作为供试品溶液。取金樱子对照药材及缺金樱子的阴性对照样品,同法制得对照药材溶液和阴性对照品溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各10 μL,分别点于同一硅胶板G板上,以石油醚-乙酸乙酯-甲醇-甲酸-水(5∶5∶1.5∶0.5∶2)的上层液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱则无此斑点,见图1B。
金樱子:取本品2 g,加甲醇40 mL,浸泡1 h,滤过,取滤液10 mL,蒸干,残渣加10 mL水溶解,再加1 mL盐酸,加热回流30 min,冷却,乙醚分2次振摇,每次20 mL,合并乙醚液,蒸干,残渣加三氯甲烷1 mL溶解,作为供试品溶液。取缺金樱子的阴性对照样品,同法制得阴性对照品溶液。取大黄酸对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法[2010年版《中国药典(一部)》附录ⅥB]试验,吸取上述3种溶液各10 μL,分别点于同一硅胶H板上,以正己烷-乙酸乙酯-甲酸(30∶10∶0.5)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,与对照品溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱则无此斑点,见图1C。
2.2 黄芪甲苷含量测定[5-11]
2.2.1 色谱条件
色谱柱:Agilent HC-C18柱(150 mm×4.6 mm,5 μm);流动相:乙腈-水(36∶64);流速:1.0 mL/min;柱温:30℃;ELSD参数:漂移管60℃,气体压力30 Psi,喷雾器加热60%模式、增益20;进样量:10 μL。理论板数按黄芪甲苷计算不低于4 000。

图1 薄层色谱图
2.2.2 溶液制备
称取黄芪甲苷对照品17.71 mg,精密稳定,置25 mL容量瓶,加入甲醇充分溶解并定容,得质量浓度为0.708 4 g/L的对照品贮备液,摇匀,待用。取颗粒5 g,研细,精密称定,加甲醇150 mL,超声1 h,滤过,蒸干加40 mL水溶解,水饱和的正丁醇振摇4次,每次40 mL,合并正丁醇液,氨试液洗涤3次,每次40 mL,弃去氨液,用正丁醇饱和的水溶液洗涤3次,每次40 mL,取正丁醇液,蒸干,加甲醇溶解,置5 mL容量瓶中定容,作为供试品溶液。取缺黄芪的阴性对照样品,研细,按供试品溶液制备方法制备,得阴性对照品溶液。
2.2.3 方法学考察
系统适用性试验:取2.2.2项下3种溶液,照2.2.1项下色谱条件进样测定,记录色谱峰,见图2。结果表明,黄芪甲苷色谱峰分离良好,且样品中其他成分对黄芪甲苷的测定无干扰。
线性关系考察:精密量取黄芪甲苷对照品贮备液0.5,1.0,1.5,2.0,2.5,3.0 mL,分别定容于10 mL容量瓶中,按2.2.1项下色谱条件进样测定,以对照品质量浓度(X)为横坐标、峰面积(Y)为纵坐标绘制标准曲线,得回归方程Y=10 984X-40 140,r=0.999 9(n=6)。结果表明,黄芩苷质量浓度在35.42~212.52 μg/mL范围内与峰面积线性关系良好。
精密度试验:精密吸取同一黄芪甲苷对照品溶液,按2.2.1项下色谱条件重复进样6次。结果峰面积的RSD=1.44%(n=6),表明仪器精密度良好。
重复性试验:取同一批样品(批号为20120923),精密称定,依法制备供试品溶液,按2.2.1项下色谱条件进样测定。结果峰面积的RSD=1.86%(n=6),表明方法的重复性较好。
稳定性试验:精密吸取同一供试品溶液,分别于0,2,4,6,8,10,12 h时依法进样测定。结果峰面积的RSD=1.14%(n=6),表明供试品溶液在制备后12 h内稳定性良好。
加样回收试验:取已知含量的同一批样品(批号为20120923),精密称定,分别加入黄芪甲苷对照品溶液适量,按供试品溶液制备方法制备溶液,依法进样测定含量,计算回收率。结果见表1。
2.2.4 样品含量测定
取3批样品,依法制备供试品溶液,按2.2.1项下色谱条件进样测定。结果批号为20120923,20120924,20120925的3批样品中黄芪甲苷含量分别为0.1336,0.1374,0.1408 mg/g。根据含量测定结果,暂订本品每1 g含黄芪以黄芪甲苷计不得少于0.12 mg。

图2 高效液相色谱图
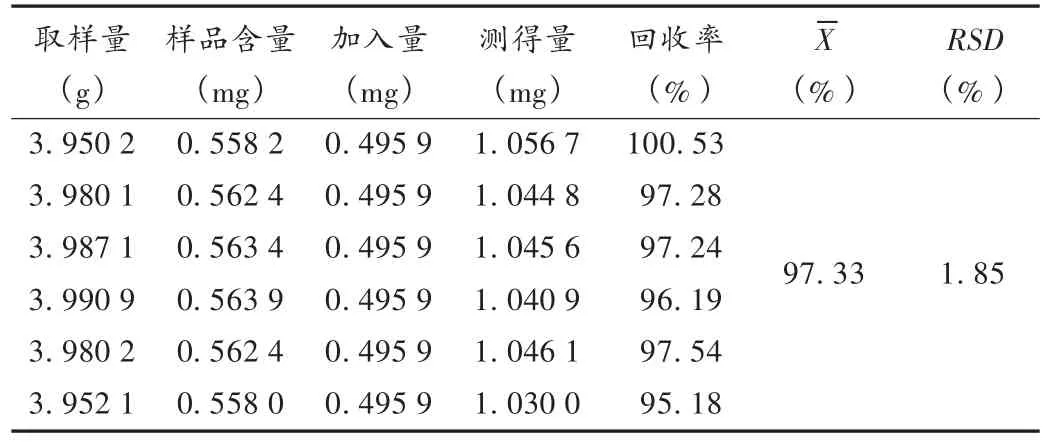
表1 黄芪甲苷加样回收试验结果(n=6)
3 讨论
根据该制剂处方组成,黄芪为主药,其主要药效成分为黄芪甲苷,故选择黄芪甲苷作为含量测定指标。曾试用色谱柱为Phenomenex C18柱(250 mm×4.6 mm,5 μm)及Agilent C18柱(150 mm×4.6 mm,5 μm),结果黄芪甲苷色谱峰分离度均良好,故选用后者。参考相关文献并考虑到蒸发光检测器的特点,温度太低不利于检测,采用柱温分别为25,30,40℃进行试验,结果柱温为30℃时分离相对较好,样品稳定,故选用柱温为30℃。
参考2010年版《中国药典(一部)》,在流速为1.0 mL/min条件下,试用乙腈-水(32∶68)、乙腈-水(36∶64)、乙腈-水(40∶60)为流动相,结果乙腈-水(36∶64)为流动相时黄芪甲苷色谱峰峰形和保留时间较好,故选用乙腈-水(36∶64)为流动相。
[1]孙胜男,赵维刚,董颖越,等.糖尿病患者自我管理现状及影响因素分析[J].中华护理杂志,2011,46(3):229.
[2]翁建平.糖尿病肾病的诊断与治疗[J].临床内科杂志,2005,22(3):150.
[3]刘仪红,田浩明.黄芪治疗糖尿病肾病的系统评价[J].中国循诊医学杂志,2007,7(10):715.
[4]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:附录XD.
[5]段立军,孙博航.黄芪甲苷研究进展[J].沈阳药科大学学报,2011,28(5):410-414.
[6]江清林,李延军,辛华,等.黄芪甲苷对胰岛素C肽分泌作用研究[J].黑龙江医药科学,1999,22(3):4.
[7]江清林,姜吉文,吕学诜,等.黄芪甲苷对类胰升血糖素肽-1作用的研究[J].中国老年学杂志,2003,23(1):52.
[8]南克祎,邢渊.胰升血糖素样肽1对胰岛β细胞的调控作用[J].甘肃医药,2011(7):405-407.
[9]刘浩文,刘嘉仪,杨妙荣,等.黄芪药材中黄芪甲苷含量测定的两种方法的比较研究[J].中药新药与临床药理,2011,22(6):659-662.
[10]翟海云,吴燕红,黄庆华,等.RP-HPLC法测定复方补气养血口服液中黄芪甲苷的含量[J].中药新药与临床药理,2006,17(2):130-131.
[11]李翔,朱臻宇,朱东亮,等.高效液相色谱法-蒸发光散射检测梯度洗脱法测定黄芪药材中黄芪甲苷的含量[J].第二军医学报,2006,27(3):331-333.
Quality Standard of Huangqijiangzhuo Granules
Kang Xinli1,Song Ying2,Tan Rui1
(1.College of Life Science and Engineering,Southwest Jiaotong University,Chengdu,Sichuan China610031;2.Teaching Hospital of Chengdu University of TCM,Chengdu,Sichuan China610075)
ObjectiveTo establish the quality standard for Huangqijiangzhuo Granules.MethodsTheRadix Astragali,Rosalaevigata Mickx,Rheum Palmatum were identified by TCL and the content of astragalosideⅣwas determined by HPLC.ResultsThe dapples in the TLC plate are clean and the result of Separation is good.and the negative control showed no interference.The mass concentration of astragalosideⅣhas a good linear relationship with the peak area in the range of 5.42-212.52 μg/mL(r2=0.999 9,n=6),the average recovery of astralosideⅣwas 97.33%,RSD=1.85%(n=6).ConclusionThe method is simple,accurate and specific,and can be used to control the quality of the preparation.
Huangqijiangzhuo granules;TCL;HPLC;astragalosideⅣ;quality standard
R284.1;R286.0
A
1006-4931(2015)20-0077-03
康新莉,女,在读硕士研究生,药师,研究方向为民族药物资源评价,(电子信箱)1315356502@qq.com;谭睿,女,博士研究生,教授,研究方向为中药质量标准规范化和新制剂研发,本文通讯作者,(电话)028-8734667(电子信箱)tanrui@swjtu.edu.cn。
2015-04-13)

