再谈“钠与乙醇反应”实验的改进
黄金泉
摘要:为使钠与乙醇反应产生较多气体且点燃后能维持稍长时间燃烧,设计了一种较为简便的实验方法。在一支摘掉橡胶乳头的滴管(无色滴瓶上的)中加入约0.2g的小钠块,然后将其慢慢倒放在一只盛有约15mL无水乙醇的50mL烧杯中反应。利用该装置钠与乙醇反应产生的气体经点燃后火焰大而明亮,持续燃烧的时间可长达30s左右,能顺利进行探究及验证气体的成分。
关键词:钠;乙醇;演示实验改进;实验探究
文章编号:1005–6629(2015)6–0070–03 中图分类号:G633.8 文献标识码:B
1 问题的提出
“钠与乙醇反应”是现行高中教材中一个重要的演示实验。笔者在教学实践中发现,不同版本教材中阐述的实验方法,尽管实验操作较为简便,产气现象也较为明显,但想要验证产生气体的成分,就显得不尽如人意。通过查阅文献发现,有同行对该实验也进行过改进,但按改进后的一些实验装置进行演示,实验效果仍不理想。究其原因主要是实验中产生气体的量不多,较难维持稍长时间持续燃烧。即便燃烧,火焰也很微弱,分别用干燥的小烧杯和蘸有澄清石灰水的小烧杯罩其上方观察现象,通过检验燃烧的产物来判断气体的成分根本无法操作。还有同行提出,只要验证产生的气体是否为氢气就行了,何必这么复杂。然而钠与乙醇反应,虽说产生的气体是氢气,但依据元素守恒思想学生会提出质疑,产生的气体为什么是氢气?难道不可以是一氧化碳?甲烷?究竟是什么气体,实验是“最高法庭”,必须通过实验来加以验证,让学生信服,这对培养学生的质疑意识很有帮助。如何才能使钠与乙醇反应产生的气体燃烧持续稍长时间且实验操作也较为简便?为此,笔者将“钠与乙醇反应”的实验进行了再改进,愿与同行们共同探讨。
2 不同版本教科书中“钠与乙醇反应”的实验方法
笔者查阅了几种不同版本的教科书,发现书中阐述的“钠与乙醇反应”的实验方法不尽相同。
苏教版化学必修2[1]“钠与乙醇反应”实验是直接向装有1~2mL无水乙醇的试管中投入一小粒金属钠,观察实验现象。
苏教版选修5《有机化学基础》[2]中“钠与无水乙醇反应”是向小烧杯中加入无水乙醇,再放入一小块切去表皮的金属钠(绿豆粒般大小),观察实验现象,并要求设法检验反应生成的气态产物。
人教版化学必修2[3]中“钠与乙醇反应”实验是采用在一支试管中加入无水乙醇和金属钠,塞上带有针头的橡胶塞,先收集一试管气体验纯后再点燃的方法,以验证所生成的气体是否是氢气,如图1所示。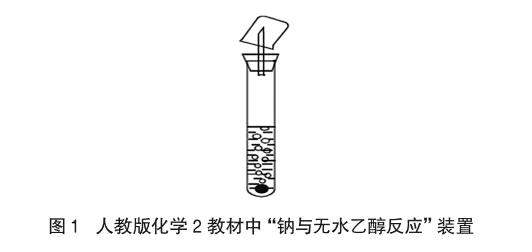
3 实际教学中的困惑
实际教学过程中,笔者发现,按苏教版化学必修2阐述的“钠与乙醇反应”实验方法进行演示,观察钠与乙醇反应的实验现象,如钠先沉在乙醇底部,而后在气体的“帮助”下可能慢慢上浮,产生气泡等不成问题,但要验证产生的是什么气体就较为勉强。通常的做法是用大拇指长时间按住试管口,然后用燃着的火柴进行点燃,用这种检验方法,笔者以为即便听到“噗”的一声或爆鸣声,也无法断定产生的气体就是氢气。因为产生的气体倘若为CO或CH4等可燃性气体,点燃后也可能会出现上述类似的实验现象;按苏教版选修5《有机化学基础》中阐述的直接在烧杯中进行实验,设法检验反应生成的气态产物,就更加困难了。按人教版化学必修2介绍的“钠与乙醇反应”实验装置(如图1)进行实验,笔者先在试管中加入大约10mL无水乙醇,然后将一粒绿豆般大小(约0.1g)的金属钠用滤纸吸干表面的煤油后投入到试管中,待反应进行大约5s后(因产生的气体量较少,收集验纯比较困难),将产生的气体直接进行点燃,看到的实验现象如图2所示,火焰较小,难以维持稍长时间的持续燃烧。在这种情形下如何验证产生气体的成分?钠与乙醇反应放热,在产生的气态产物中可能会混有乙醇蒸气,如何消除乙醇蒸气的干扰?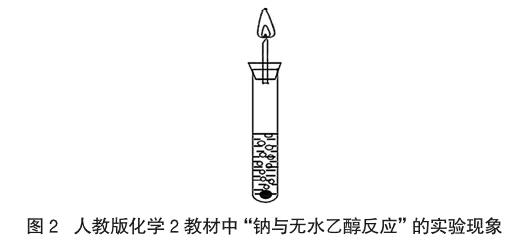
可见,无论使用教科书中哪一种实验装置,由于投入钠的量有限且钠与乙醇反应较为缓慢,产生的气体量不多,几乎不能点燃,即便点燃后燃烧起来,火焰也很微弱,随时都有熄灭的可能。因此,想要验证产生气体的成分就显得力不从心了。
4 对一些改进后的实验装置评述
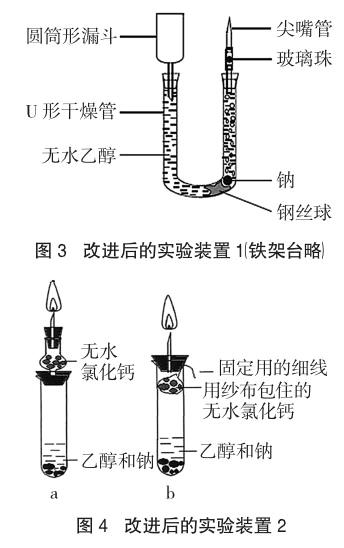
带着种种疑问,笔者查阅了相关文献资料。在2014年第10期《实验教学与仪器》期刊杂志上,笔者阅读到了由重庆市第十一中学丁昭兰老师撰写的“‘钠与无水乙醇反应实验的改进”一文[4],深受启发。丁老师在改进该实验时(改进后的实验装置如图3所示)充分展现了她在专业知识、专业智慧和实验操作技能等方面的扎实功底。丁老师在设计方案时充分考虑到一小块金属钠与无水乙醇反应,在产生有限量气体的前提下,如何确保产生的气体燃烧能持续稍长时间,又如何避免对产生的气体进行验纯这两方面动了很多心思,如用无水乙醇注满20mm×200mm的U形管,以排除U形管中混有的空气,其目的是避免验纯,以节约气体量;用连有玻璃珠和尖嘴管的塞子,使产生的气体能够聚集起来并能在尖嘴管处点燃且产生较长火焰,以便顺利检验出产生气体的成分等等。应该说丁老师设计出来的实验装置合情合理,实用性也较强。但笔者对丁老师改进后的这套实验装置有两点看法,愿与丁老师商榷:其一,该实验装置过于复杂;其二,钠与无水乙醇反应放热,在尖嘴管处燃烧的气态产物中很可能混有乙醇蒸气,另外,反应中的小钠块在产生的气体“帮助”下可能会上浮,很可能会阻塞尖嘴管通气。因此,笔者认为这套改进后的实验装置在验证产生气体成分方面仍不够理想。在2011年第3期《化学教学》期刊杂志上,笔者还关注到由湘西自治州民族中学吴国峰老师撰写的“乙醇与钠反应实验的改进”一文[5],吴老师巧用了把装入无水CaCl2的干燥管接在试管上或用纱布包住无水CaCl2放入试管中的做法以消除乙醇蒸气对检验产生气体成分的干扰。因为无水CaCl2与乙醇反应生成CaCl2·4C2H5OH[6]。实验装置如图4-a和图4-b所示。吴老师设计的方案确实技高一筹,这两种设计方案都较好地消除了乙醇蒸气的干扰。教学中,笔者曾经按图4-b进行过实验,但结果发现反应产生的气体量也不多,点燃后的火焰仍然很小,持续燃烧的时间不长,想要分别用干燥的小烧杯和蘸有澄清石灰水的小烧杯罩其上方观察现象,以检验燃烧的产物来判断产生气体的成分还是难以实现。
5 “钠与乙醇反应”实验再改进
基于以上思考,笔者对“钠与乙醇反应”实验进行了再改进。
5.1 具体操作步骤
取一支普通滴瓶上的滴管(无色的),摘去橡胶乳头,如图5-a和图5-b所示,将一小块黄豆大小的金属钠(约0.2g)用小刀切成粒状的小钠块,用镊子将这些小钠块沿口径稍大的一端慢慢地放进滴管的“大肚子”中,如图5-c所示。在一只50mL烧杯中加入约15mL无水乙醇,把装有小钠块的滴管慢慢倒放在该烧杯中,小钠块与无水乙醇接触并反应产生气体,大约经2s后(以免收集验纯),在滴管尖嘴一端直接进行点燃,火焰大且明亮,持续燃烧的时间可长达30s左右,如图5-d所示。分别用干燥的小烧杯和蘸有澄清石灰水的小烧杯罩其上方观察现象,以检验燃烧的产物来判断产生气体的成分能得以顺利实现,如图5-e所示。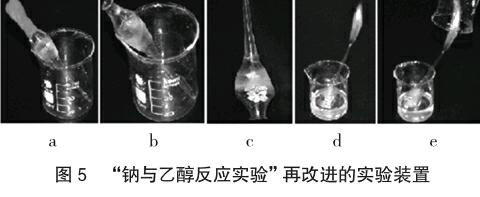
5.2 实验改进后的优缺点
优点:一是实验仪器取材简单,无需特意提前准备,实验操作也十分简便,很适合在课堂上演示或学生分组实验;二是可免去气体验纯,直接点燃(一旦反应后只需稍等几秒钟即可),增强了实验效果;三是气体燃烧产生的火焰大且明亮,持续燃烧的时间可长达30s左右,非常适合探究、验证该反应产生气体的成分。
缺点:不能判断钠与乙醇密度的大小且消耗钠和使用乙醇的量要稍多些。
5.3 一点补充说明
钠与乙醇反应放热,在产生的气体中可能会混有乙醇蒸气干扰气体的检验。如何消除乙醇蒸气的干扰?如果采用无水CaCl2来吸收,有效果,但实际操作会带来很多麻烦。注意到乙醇的沸点是78.5℃,且乙醇能使酸性K2Cr2O7溶液褪色[7]。因此,我们只要把装有无水乙醇的50mL小烧杯浸入到装有冷水的100mL烧杯中约5min左右,然后将事先装有小钠块的滴管慢慢倾斜后倒置在50mL小烧杯中,设法(如采用一种用于自行车气门芯上的小橡皮管将产生的气体导出)将产生的气体通入到酸性K2Cr2O7溶液中观察,溶液不变色,说明冷水可以防止乙醇蒸气的挥发。“把装有无水乙醇的小烧杯浸入到装有冷水的烧杯中”这一过程在上述图5-d和图5-e中都没体现出来。但在实际操作时,笔者建议不可忽略这一过程,以免乙醇蒸气造成干扰。这样可直接点燃产生的气体,然后再采用上述实验方法检验燃烧产物,若干燥的小烧杯内壁有水珠或水雾,而蘸有澄清石灰水的小烧杯内壁的液滴不变浑浊,可证明生成的气体是氢气。
对“钠与乙醇反应”的实验进行再改进,不仅能增强实验效果,提升学生的创新意识,而且在不违背实验教学功能的前提下,能让学生体验验证产生气体成分的化学学习过程,达到激发兴趣、启迪思维、培养能力、提高学生的科学素养的目的。
参考文献:
[1]王祖浩主编.普通高中课程标准实验教科书·化学2(必修)[M].南京:江苏教育出版社,2013:69.
[2]王祖浩主编.普通高中课程标准实验教科·有机化学基础(选修)[M].南京:江苏教育出版社,2014:67.
[3]宋心琦主编.普通高中课程标准实验教科书·化学2(必修)[M].北京:人民教育出版社,2007:73.
[4]丁昭兰.“钠与无水乙醇反应”实验的改进[J].实验教学与仪器,2014,(10):29.
[5]吴国峰.乙醇与钠反应实验的改进[J].化学教学,2011,(3):41.
[6][7]李景宁主编.有机化学上册[M].北京:高等教育出版社,2011:293,284.

