1-氯-3,3,3-三氟丙酮的制备与应用
戴佳亮 徐卫国 金杭丹
(浙江省化工研究院有限公司,浙江 杭州 310023)
1-氯-3,3,3-三氟丙酮的制备与应用
戴佳亮 徐卫国 金杭丹
(浙江省化工研究院有限公司,浙江 杭州 310023)
1-氯-3,3,3-三氟丙酮可用来制备医药、农药中间体和各类含氟化学品,应用广泛。介绍了1-氯-3,3,3-三氟丙酮的合成概况,并对其涉及的反应及应用进行了详细综述。
1-氯-3,3,3-三氟丙酮;合成;应用
0 前言
1-氯-3,3,3-三氟丙酮,英文名1-Chloro-3,3,3-Trifluoroacetone,分子式C3H2ClF3O,CAS号431-37-8,分子质量146.5,沸点71~72 ℃,密度1.45 g/cm3,折射率1.3445,结构式如下:

1-氯-3,3,3-三氟丙酮由于丙酮基的存在,可以在温和的条件下环合形成吡唑、噁唑、噻唑等杂环衍生物,引入三氟甲基,合成各类医药和农药中间体或原料药。也可以合成各种含氟精细化学品,在医药、农药、化工领域有着广泛的应用。
本文对1-氯-3,3,3-三氟丙酮(以下简称一氯三氟丙酮)的制备方法及其参与的各类反应及应用进行了详细综述。
1 制备
1950年,Hill等人[1]以三氟乙酰乙酸乙酯为起始原料制备一氯三氟丙酮,工艺见式1。在20 ℃温度下将氯气通入120 g三氟乙酰乙酸乙酯中,直至反应物增重26 g。通入空气去除溶液中的氯化氢气体。精馏得到25 g的前馏分和112 g产品(氯代三氟乙酰乙酸乙酯),沸点67~69 ℃。86.5 g的氯代三氟乙酰乙酸乙酯中加入200 mL 30%的硫酸回流,搅拌8 h。反应物以50 mL乙醚萃取6次,以五氧化二磷干燥,蒸馏得到23.7 g一氯三氟丙酮产品。


(1)
1955年,美国陶氏化学公司的Ruh[2]公布了涉及制备一氯三氟丙酮的专利。将92 g 1-氯-2-甲氧基-3,3,3-三氟丙烯和90 g氢碘酸回流反应一定时间后,将反应物加入水中,分离有机相,精馏后可得到21 g一氯三氟丙酮,工艺见式2。

(2)
1990年,日本中央硝子公司的Maruta等人[3]报道了以3,3,3-三氟-2-丙烯甲酸酯为原料与氯气或溴反应,温度为20~80 ℃,催化剂为五氯化锑,可制备得到一氯三氟丙酮和一溴三氟丙酮,工艺见式3。

(3)
1997年,德国拜耳公司的Lui公布了以六氟-2,3-二氯-2-丁烯(R1316)为原料制备一氯三氟丙酮的方法[4],工艺见式4。618 g 30%甲醇钠浓溶液滴加至400 g六氟-2,3-二氯-2-丁烯的甲醇(200 mL)溶液中,加热回流16 h。冷却至室温后加入150 mL 50%的硫酸,加热回流3 h。加入水,以二氯甲烷萃取有机相,干燥后除去溶剂,减压蒸馏得到178 g 2-氯-4,4,4-三氟-3,3-二甲氧基丁酸甲酯(沸点85 ℃,1 000 Pa)。在140 ℃温度下,250 g 2-氯-4,4,4-三氟-3,3-二甲氧基丁酸甲酯滴加至400 mL浓硫酸中,滴加时间2 h,同时蒸馏出产物。蒸馏物精馏后得到122 g一氯三氟丙酮,收率83%。


(4)
2 应用
2.1 制备医药中间体
1996年,日本藤泽制药的Kawai等人[5]制备了一种咪唑并[1,2-a]吡啶化合物,可作为骨吸收、骨转移的抑制剂,用于预防和治疗骨科类疾病特别是骨代谢异常,如骨质疏松症、钙血症、甲状腺功能亢进、Paget′s骨骼疾病、骨质溶解、类风湿关节炎;牙周炎、骨痛、癌症恶病质、结石病等。一氯三氟丙酮可合成咪唑并[1,2-a]吡啶化合物1,工艺见式5。6.27 g 2,3-二氨基吡啶和8.4 g一氯三氟丙酮溶于110 mL乙醇中回流20 h。旋蒸除去溶剂,加入乙酸乙酯和饱和碳酸氢钠溶液,洗涤,萃取有机相,干燥浓缩后柱层析得3.09 g固体1a。2.51 g 2,6-二氯苯甲酰氯、2.01 g固体1a、30 mL二氯甲烷在常温下搅拌1 h后回流过夜。以二氯甲烷稀释,饱和碳酸氢钠洗涤后,萃取有机相,处理后柱层析得油状物,再以二异丙醚重结晶得750 mg咪唑并[1,2-a]吡啶化合物1。
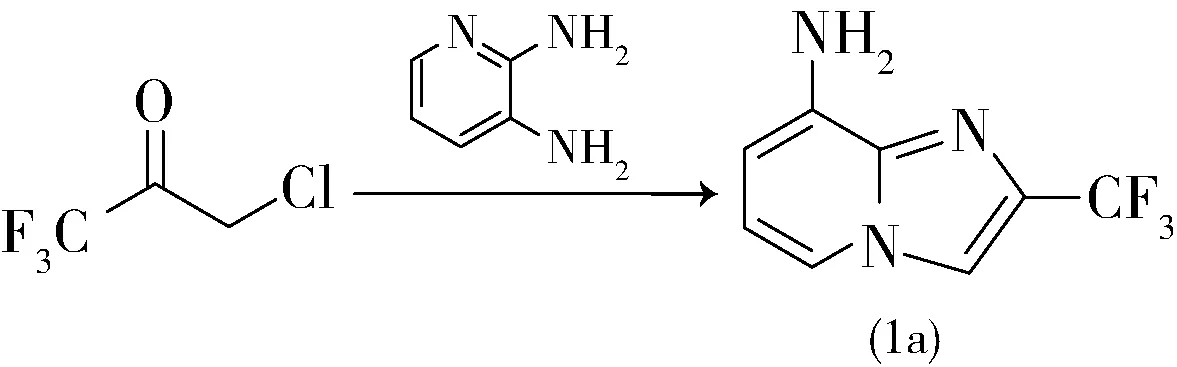

(5)
2001年,德国拜耳公司的Heil等人[6]制备了一种芳基和杂芳基的磺酸酯类化合物,是大麻酯类受体亚型CB1和 CB2(某种特定情况下)受体的高效激动剂。它们可以单独或与其他药物联合用于预防和治疗急性或慢性疼痛和神经变性疾病,特别是治疗癌症引起的疼痛和慢性神经病性疼痛,如糖尿病神经病性疼痛、带状疤疹性疼痛、外周神经损伤、中枢疼痛、三叉神经痛及其他慢性疼痛。一氯三氟丙酮可与3-甲氧基苯甲酰胺合成中间产物2a。将1.81 g(12.0 mmol)3-甲氧基苯甲酰胺和1.76 g(12.0 mmol)一氯三氟丙酮加入11 mL丙酮中,回流24 h。加入70 mL二氯甲烷,以5%碳酸氢钠水溶液洗涤至pH为9,萃取有机相,浓缩后色谱柱分离得79.5%收率的3-甲氧基-N-(3,3,3-三氟-2-丙酰)苯甲酰胺。将1.72 g(6.57 mmol)3-甲氧基-N-(3,3,3-三氟-2-丙酰)苯甲酰胺置于15 mL磷酰氯中,回流4 h,加入20 mL乙酸乙酯稀释,再倒入5 mL冰水中,萃取干燥,浓缩后柱层析得1.2 g 2a,收率53.9%。可经三溴化硼脱去甲基后与戊基磺酰氯生成具有CB1和 CB2刺激活性的磺酸酯2,工艺见式6。


(6)
2005年,美国Array生物制药的Fan等人[7]开发的类似3结构的芳基砜化合物,可以调节羟甾类脱氢酶类(HSDs),如11β-HSDs。HSDs通过将类固醇激素转换成活性代谢物的方式来调节类固醇激素受体的的活性。11β-HSDs存在于肝脏、脂肪组织、大脑、肺和其他糖皮质激素的组织,可以催化活性糖皮质激素的互变,是一个潜在的治疗疾病靶向。调节HSDs的活性,特别是11β-HSDs,可以治疗如糖尿病、肥胖症以及与年龄相关的认知功能障碍等疾病。一氯三氟丙酮可用作原料合成该类芳基砜化合物3,工艺见式7。3.74 g(39.3 mmol)一氯三氟丙酮溶于70 mL乙醇中,加入5.00 g(34.3 mmol)硫脲,回流反应9 h。减压除去溶剂,残留物溶解于水,加入5%的氢氧化钠溶液调节pH为10,以乙醚萃取有机相,洗涤干燥后浓缩,残留物以己烷重结晶得到3.2 g(19.0 mmol)黄色固体产物3a。再经NBS溴化,再与1,1,1-三氟-2-(4-巯基苯基)-2-异丙醇、mCPBA和四氢吡咯反应得到最终产物3。


(7)
德国拜耳先灵医药的Siegel等人[8-9]在2008年的专利中报道了一类咪唑并嘧啶类衍生物,为GSK3(糖原合成酶激酶3)抑制剂,属于丝氨酸/苏氨酸激酶家族,是细胞骨骼蛋白质的转录因子。抑制GSK3活性可增加造血干细胞的增生和分裂的速率,可医疗性地调停嗜中性白血球减少症。所以该类咪唑并嘧啶类衍生物可用于预防和治疗血液性疾病,特别是白血球减少症及嗜中性白血球减少症。化合物4是其中一类咪唑并嘧啶类衍生物,合成工艺见式8。5 g(28.5 mmol)的6-氯-2-甲硫基-4-氨基嘧啶和6.26 g(42.7 mmol)的一氯三氟丙酮溶于200 mL的DMF中,加热至120 ℃温度下反应16 h。结束后加入水,并用乙酸乙酯萃取,有机相经干燥后浓缩,残留物柱层析分离得到3.5 g固体产物4a,收率45%。4a经氢氧化钾脱去甲硫基后,再以三氯氧磷氯化,依次与4d和4e反应得到具有抑制GSK3活性的咪唑并嘧啶衍生物4。

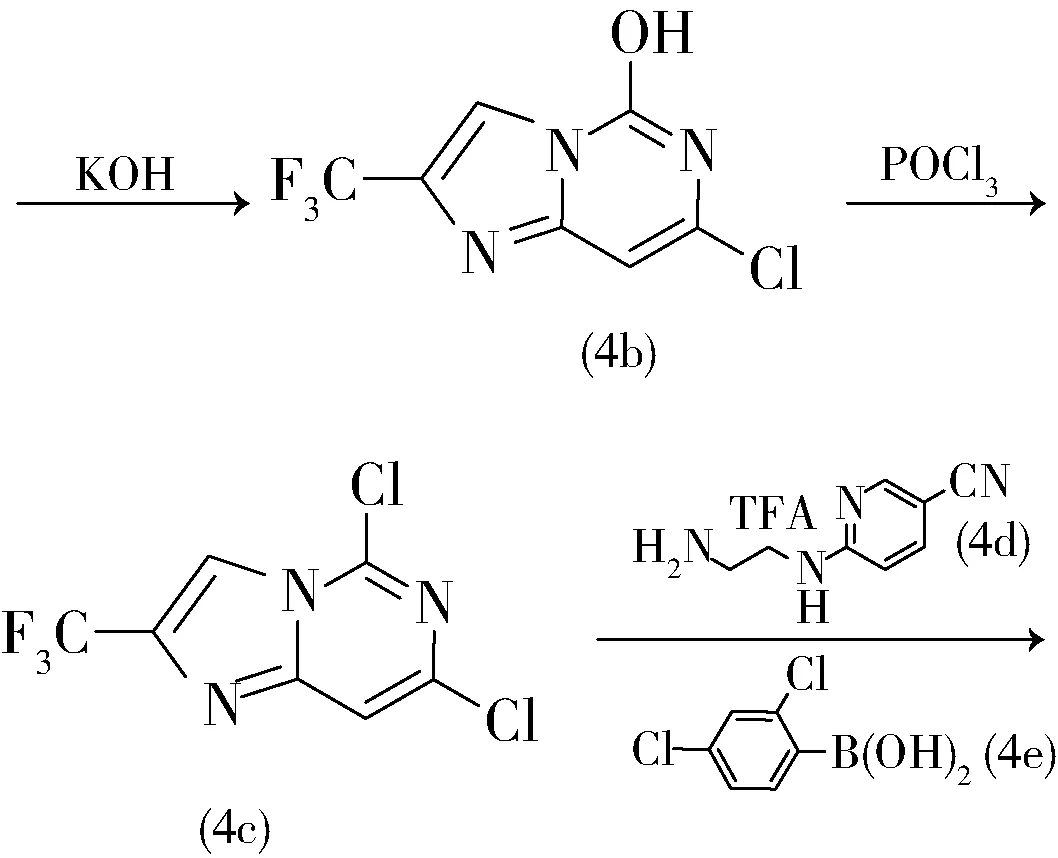

(8)
神经肽Y(NPY)广泛地分布在中枢及末梢神经系统,是神经系统中最丰富的一种肽,作为一种开胃物质能明显促进脂肪聚集。2009年,葛兰素史克集团的Biagetti等人[10]开发了一类螺环化合物,是NPY Y5受体拮抗剂,可用于预防及治疗与NPY Y5受体副型相关的障碍或疾病,较宜用于治疗饮食障碍例如肥胖、神经性厌食及其他不正常的情形,如糖尿病、高血压、高脂血症、胃肠道障碍、关节炎及免疫缺陷综合症等。一氯三氟丙酮可与6-氯-3-哒嗪胺作原料合成该类螺环化合物5,工艺见式9。0.5 g(3.41 mmol)一氯三氟丙酮和0.442 g(3.41 mmol)6-氯-3-哒嗪胺溶于10 mL乙醇中,加热至100 ℃温度过夜。除去溶剂,以二氯甲烷溶解后,洗涤干燥,浓缩得350 mg黄色固体。柱层析分离后得220 mg褐色固体即5a,在18-冠醚、氟化钾和环丁砜存在下,微波200 ℃温度照射60 min,与螺环5b在140 ℃温度下摇动反应3 h,得到目标产物5。


(9)
2012年,美国Amira制药的Roppe等人[11]开发了一类吲哚衍生物,如同6d结构,为自分泌运动因子Autotaxin(ATX)抑制剂,可治疗或预防与ATX因子活性有关的疾病,如器官纤维化、炎症、肿瘤、血管增生和疼痛等。自分泌运动因子是一种对产生脂质信号分子溶血磷脂酸(LPA)具有重要作用的分泌酶,具有将溶血磷脂胆碱转化成LPA活性。LPA是一种脂质调节剂,对许多细胞具有活化分裂素、趋化因子和存活因子的功能。ATX-LPA信号涉及了如血管发生、慢性炎症、自身免疫性疾病、纤维变性疾病、神经变性疾病、中风或心肌缺血和进行性肿瘤等疾病。一氯三氟丙酮参与合成6d的工艺见式10。2.89 g(15.29 mmol)的3-溴苯硫酚和2.35 g(16.06 mmol)的一氯三氟丙酮混合溶于80 mL THF中,冷却至0 ℃温度,加入6.65 mL(38.23 mmol)N,N-二异丙基乙基胺,反应混合物在0 ℃温度下搅拌5 min,温热至室温,搅拌过夜。往反应液中加乙酸乙酯和水,萃取有机相,浓缩得到中间产物6a。6a再与三氯苯基肼盐酸盐、1, 1′-双(二苯基膦基)二茂铁-二氯化把(II)、一氧化碳、氢氧化锂依次反应得到最终产物ATX抑制剂6d。


(10)
美国雅培公司的Gomtsyan等人[12]在2012年的专利中报道了一种脲化合物,主要结构如7所示,为TRPV1拮抗剂,可用于治疗由TRPV1通道调节引起的疼痛、咳嗽、膀胱机能过度、尿失禁或等病症。TRPV1亦称为辣椒素受体-1,皮内注射辣椒素的特点在于最初有灼烧或热的感觉,而后是持久镇痛期。人们认为,TRPVl受体止痛功能的活化是由辣椒素引起的主要感觉传入终端去敏而导致的。由此,辣椒素的长效镇痛效果使得辣椒素类似物在临床上用作止痛药。辣椒素受体拮抗剂在动物模型中可以减轻炎症引起的痛觉过敏,而注射到膀胱中的辣椒素可改善失禁症状。一氯三氟丙酮可合成TRPV1拮抗剂7,合成工艺见式11。取100 mg(0.41 mmol)7a溶于3 mL乙醇中,加入一氯三氟丙酮65 mg(0.45 mmol),将该反应混合物回流反应过夜。完毕后加入2 mL的2 N盐酸,并将该混合物回流搅拌4 h。浓缩,将残余物在二乙醚中研磨,即得到中间产物7b。7b再与7c在N,N-二甲基甲酰胺和二异丙基乙胺作用下得到最终产物TRPV1拮抗剂7。
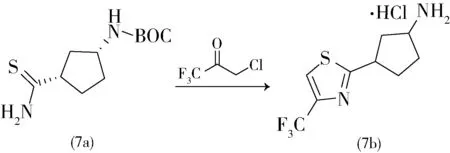

(11)
2014年,比利时杨森制药研发公司的Bartolome-Nebreda等人[13-14]开发了一类咪唑并[1,2-a]哌嗪衍生物,经过活性验证和结构分析,这类化合物能高度选择性抑制磷酸二酯酶PDE10A,且能选择性渗透大脑,在老鼠体内有良好的药物动学特征。PDE 10关系着细胞内第二信使环磷酸腺苷(cAMP)和环鸟苷单磷酸(cGMP)的转化,这两类信使调节着各种各样的生物学、神经学过程,包括消炎、离子通道、肌肉收缩、学习、细胞分裂等等。因此,该类PDE 10A抑制剂有望作为治疗精神分裂症的药物。一氯三氟丙酮可用于合成咪唑并[1,2-a]哌嗪衍生物8,合成工艺见式12。0.50 g(3.86 mmol)的3-氯-2-氨基吡嗪和4 mL(0.027 mmol)一氯三氟丙酮在100 ℃温度下搅拌16 h,反应后加入二氯甲烷和饱和碳酸氢钠,萃取有机相,干燥后旋蒸得到中间产物淡褐色固体8-羟基-2-三氟甲基咪唑并[1,2-a]吡嗪0.31 g,收率39%。取0.169 g(0.83 mmol)8-羟基-2-三氟甲基咪唑并[1,2-a]吡嗪和0.06 mL(0.006 mmol)N,N-二甲基苯胺中加入三氯氧磷0.60 mL(1 mmol),在90 ℃温度下搅拌4 h。混合物冷却至室温,得到红色固体,加入冰水和二氯甲烷,萃取有机相,干燥后旋转蒸发得到褐色固体8a 0.182 g,收率99%,不经纯化直接用于下一步反应。8a可进一步与NBS、吗啉、8d反应得到PDE10A抑制效用的最终产物8。其中产物8上的吡唑基也可被吡啶基替代,得到的产物依旧有着PDE10A抑制效用[14]。
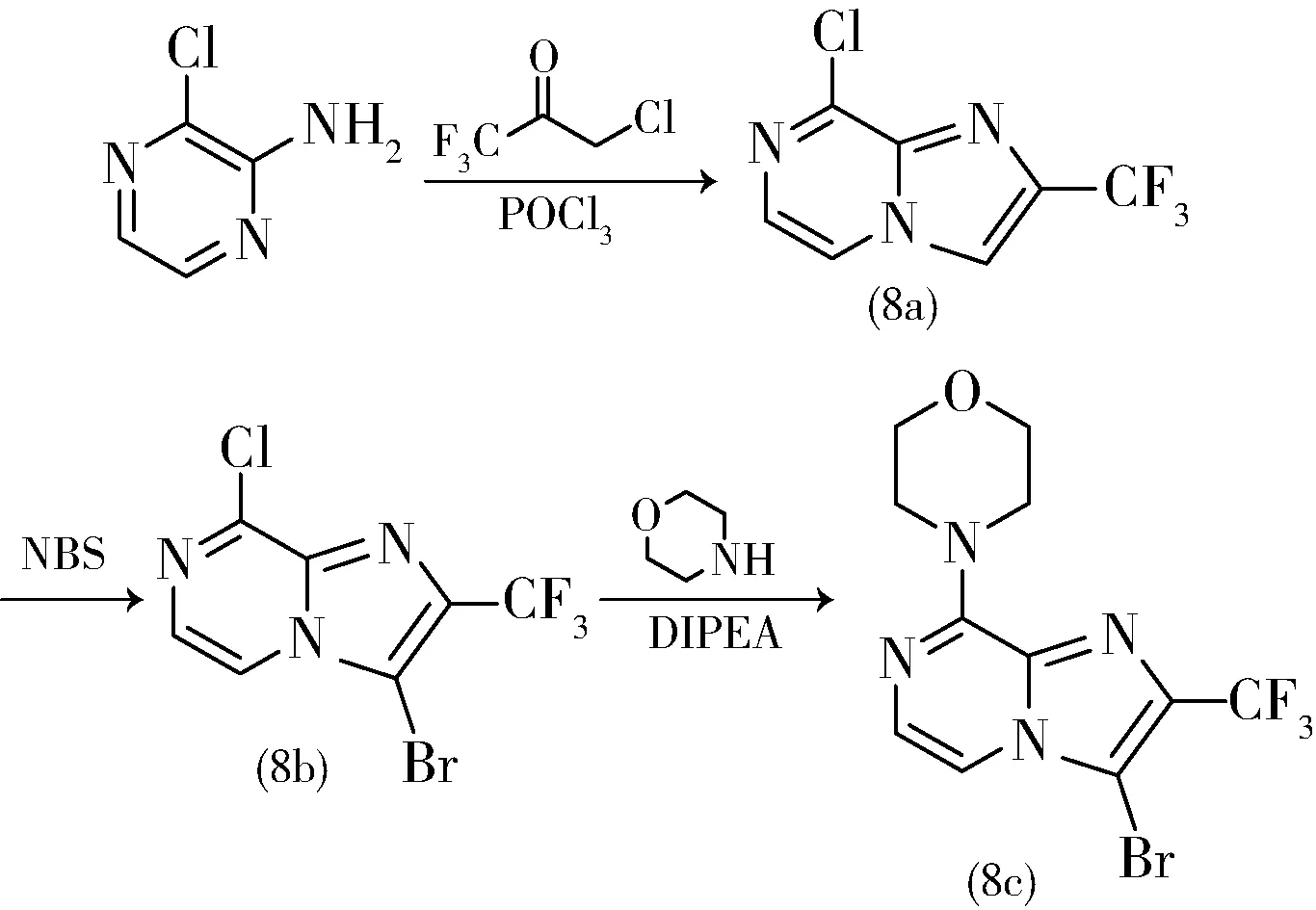
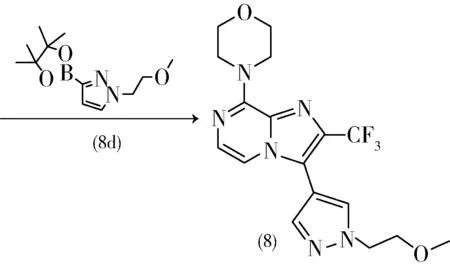
(12)
2.2 制备农药中间体
2002年,江西农业大学的刘晓庚等人[15]设计了一种含硫含氟1,2,4-三唑化合物,并对其进行了物理性质、溶解性、元素组成、生物活性试验,显示出此类化合物均有良好的杀虫活性、杀菌活性、除草活性和一定的植物生长调节等作用。一氯三氟丙酮可合成其中的三唑化合物9,工艺见式13。在反应器中加入1,2,4-三唑13.9 g(约0.2 mol)和200 mL 甲苯,搅拌使其溶解,缓慢滴加一氯三氟丙酮(约0.1 mol)。滴毕,回流反应30 min,加入适量K2CO3,搅拌反应1.5 h后减压蒸去甲苯,得白色固体。以蒸馏水洗涤,重结晶得无色晶体9a 122 g,产率68.0%。取0.03 mol中间体9a、200 mL甲苯和0.05 mol K2CO3,搅拌10 min后滴加4,4,4-三氟-1,2-丙二硫醇约0.05 mol,于85 ℃温度下反应1 h。减压脱溶,重结晶得浅黄色晶体5.10 g,产率52.6%,为目标产物三唑化合物9。


(13)
2003年,美国陶氏益农公司的Balko等人[16]制备了一系列的6-芳基吡啶甲酸及其衍生物。在目前的研究中,已经发现某些6-芳基或杂芳基吡啶甲酸和它们的衍生物是有效的除草剂,针对木本植物、禾木植物和苔草以及阔叶树具有广谱杂草控制性和优异作物选择性,且还具有优异的毒物学或环境特点。一氯三氟丙酮可制备含除草活性的该系列衍生物10和10′, 工艺见式14。2.85 g(11.8 mmol)4,5,6-三氯吡啶-2-硫代甲酰胺和2.59 g(17.7 mmol)一氯三氟丙酮加入至25 mL冰乙酸中,加热回流4 h。将得到的固体以水和碳酸氢钠溶液洗涤,最后经制备液相色谱精制得到0.7 g(2.1 mmol)化合物10和0.2 g(0.6 mmol)化合物10′。


(14)
2.3 制备含氟化学品
1998年,德国拜耳的Rock等人[17]以一氯三氟丙酮制备三氟甲基环氧乙烷11,其可用作制备抗病毒药物中间体和肿瘤细胞检测试剂。制备工艺见式15。氮气保护5 ℃温度下,12 g四氢铝锂加入至300 mL 二乙醚中,滴加147 g的一氯三氟丙酮二乙醚(150 mL)溶液,温至室温下搅拌过夜。于10 ℃ 温度下加入80 mL 0.5 M硫酸和70 mL 50%硫酸,萃取有机相,干燥后精馏得132 g一氯三氟丙醇。38.5 g氢氧化钠溶于180 mL水中,冰浴下滴加52.8 g一氯三氟丙醇,温至室温下搅拌。加热至38~39 ℃,蒸馏得到29.4 g三氟甲基环氧乙烷11,收率74%。
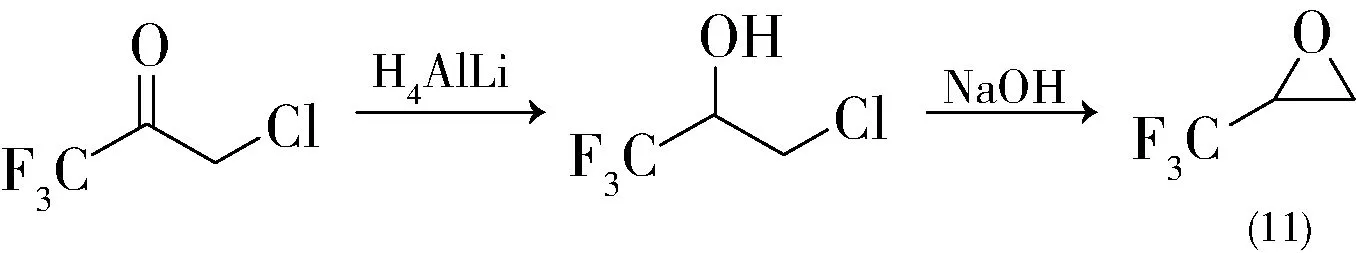
(15)
1999年,中央硝子公司的Goto等人[18]将氯代三氟丙酮与芳基化合物在质子给予试剂的存在下,制备得到医药和农药中间体3-氯代-1,1,1-三氟-2-芳基-2-丙醇。一氯三氟丙酮可合成3-氯-1,1,1-三氟-2-芳基-2-丙醇12,工艺见式16。42.7 g氯化铝和100 g苯置于反应器中,于10 ℃温度下缓慢滴加80 g一氯三氟丙酮,滴毕,自然回至室温下反应6 h。加水淬灭反应,于80 ℃温度、800 Pa压力下减压蒸馏得73.6 g 3-氯-1,1,1-三氟-2-芳基-2-丙醇12,收率60%。

(16)
2000年,中央硝子公司的Goto[19]以卤代三氟丙酮与低价态金属在质子给予体的存在下制备得到三氟丙酮。卤代三氟丙酮可以为氯代、溴代、碘代三氟丙酮等。反应温度为50~100 ℃,反应压力为0.1~2 MPa。一氯三氟丙酮为原料制备三氟丙酮的具体方法:30 g(0.46 mol)锌粉和60 g水加入具备蒸馏柱的反应器中,搅拌下悬浊液加热至85 ℃,滴加100 g 48%的一氯三氟丙酮(0.33 mol)的水溶液,滴加时间为1.5 h,三氟丙酮产生,通过蒸馏柱以-78 ℃温度冷井收集,得到31 g无色液体,气相色谱分析含82.1%三氟丙酮,15.5% 1,1-二氟丙酮和0.9%一氟丙酮,三氟丙酮收率72%。再进一步精馏可得到17.8 g三氟丙酮,纯度97%。
2003年,中央硝子公司的Tsukamoto等人[20-21]以各种卤代三氟丙酮气相氢解制备三氟丙酮。卤代三氟丙酮可以为一氯三氟丙酮、3-氯-1,1,1,3-四氟丙酮、1,1-二氯-3,3,3-三氟丙酮和1,1,1-三氯-3,3,3-三氟丙酮等。具体反应步骤:在不锈钢管式反应器内加入240 g 0.5%的Pd/C催化剂,加热至150 ℃,以0.8 L/min的速率通入氢气。将240 g一氯三氟丙酮、3-氯-1,1,1,3-四氟丙酮、3,3-二氯-1,1,1-三氟丙酮的混合物以2 g/min 的速率导入气化器内,形成含48.2%的3-氯-1,1,1,3-四氟丙酮、24.5% 一氯三氟丙酮和25.6% 的3,3-二氯-1,1,1-三氟丙酮。将此气相产物与氢气混合后,导入反应器,导入时间为2 h。再以相同速率导入氮气1 h。同时将反应中生成的产物通入1 020 g 0 ℃温度的水中,共收集得到混合物1 157 g,含87.2%的水和147 g产物,经气相色谱分析,147 g产物中含97.2%的1,1,1-三氟丙酮。
3 总结
综上所述,一氯三氟丙酮可被用来环合制备含三氟甲基的精细化学品及咪唑、噻唑、噁唑等医药或农药中间体。随着一氯三氟丙酮的应用研究越来越多,以其为原料开发的下游产品也越来越广泛。因此,开发一氯三氟丙酮新生产工艺,将会给企业带来新的经济效益增长点。
[1] Hill H M, Towne E B, Dickey J B. 3-Chloro-1,1,1-trifluoro-2-propanone[J]. J. Am. Chem. Soc., 1950, 72: 3289.
[2] Ruh R P. Hydrolysis of unsaturated fluorine-containing ethers: US, 2715144[P]. 1955-08-09.
[3] Maruta T, Murata K. Production of 1-halogeno-3,3,3-trifluoroacetone: JP, 02040338[P]. 1990-02-09.
[4] Lui N. 3,3-Dioxy-4,4,4-trifluorobutyric acid derivatives: EP, 780362[P]. 1997-06-25.
[5] Kawai Y, Satoh S, Yamazaki H, et al. Imidazo1,2-apyridine and imidazo1,2-a pyridezine derivatives and their use as bone resorption inhibitors: WO, 9634866[P]. 1996-11-07.
[6] Heil M, Meier H, Naab P,et al. Aryl and heteroaryl sulfonates: WO, 2001074763[P]. 2001-10-11.
[7] Fan P, Goto H, He X,et al. Aryl sulfones and uses related thereto: WO, 2005110980[P]. 2005-11-24.
[8] Siegel S, Wilmen A, Roehrig S,et al. Substituierte imidaz-opyrimidines and triazolopyrimidines: WO, 2008113469[P]. 2008-09-25.
[9] Siegel S, Wilmen A, Roehrig S, et al. Substitute imidazopyrimidines and triazolopyrimidines: US, 201011 3441[P]. 2010-05-06.
[10] Biagetti M, Contini S A, Genski T, et al. Spiro compounds as NPYY5 receptor antagonists: WO, 2009095377[P]. 2009-08-06.
[11] Roppe J R, Parr T A, Stock N S, et al. Autotaxin inhibitors and uses thereof: WO, 2012024620[P]. 2012-02-23.
[12] Gomtsyan A, Daanen J F, Gfesser G A,et al. TRPV1 antagonists: US, 20120245163[P]. 2012-09-27.
[13] Bartolome-Nebreda J M, Delgado F, Delgado F, et al. Discovery of a potent, selective, and orally active phosphodiesterase 10A inhibitor for the potential treatment of schizophrenia[J]. J. Med. Chem., 2014, 57(10): 4196-4212.
[14] Bartolome-Nebreda J M, Conde-Ceide S, MacDonald G J,et al. Imidazo[1, 2-a] pyrazine derivatives and their use for the prevention or treatment of neurological, psychiatric and metabolic disorders and diseases: WO, 2011110545 [P]. 2011-09-15.
[15] 刘晓庚, 黄长于, 周德红, 等. 三种含1,2,4-三唑基化合物的合成研究[J]. 江西农业大学学报: 自然科学版, 2002, 24(2): 280-283.
[16] Balko T W, Buysse A M, Epp J B, et al. 6-Aryl-4-aminopicolinates and their use as herbicides: WO, 2003011853[P]. 2003-02-13.
[17] Rock M H, Lui N. Improved process for the preparation of trifluoromethyloxirane : EP, 866064[P]. 1998-09-23.
[18] Goto Y, Kume T, Inomura H. Producing of 3-chlorinated-1,1,1-trifluoro-2-aryl-2- propanols: JP, 11228470[P]. 1999-08-24.
[19] Goto Y. Process for producing 1,1,1-trifluoroacetone: JP, 2000336057[P]. 2000-12-05.
[20] Tsukamoto M, Sakatani, Nishimiya T, et al. Method for producing 1,1,1-trifluoroacetone: JP, 2003160528[P]. 2003-06-03.
[21] Tsukamoto M, Yoshikawa F, Fujimoto M, et al. Method for producing 1,1,1- trifluoroacetone: JP, 2003342221[P]. 2003-12-03.
Progress in Preparation and Application of 1-Chloro-1,1,1-Trifluoroacetone
Dai Jialiang, Xu Weiguo, Jin Hangdan
(Zhejiang Chemical Industry Research Institute, Hangzhou 310023, China)
1-Chloro-1,1,1-trifluoroacetone can be used to synthesis of various medicine, pesticide intermediates and fluoride chemicals. It has a widely applications in various fields. This paper introduces the preparation of 1-chloro-1,1,1-trifluoroacetone, and various application of 1-chloro-1,1,1-trifluoroacetone were reviewed in detail.
1-chloro-1,1,1-trifluoroacetone; synthesis; application
戴佳亮(1984—),男,工程师,主要从事含氟精细化学品的研究开发工作。

