C-反应蛋白纯品的同位素稀释质谱法测定与国际比对
宋德伟,董晓杰,2,徐 蓓,武利庆,黄 挺,李红梅
(1. 中国计量科学研究院, 北京 100013;2. 中国疾病预防控制中心,北京 102206)
C-反应蛋白(C-reactive protein, CRP)是人类急性时相蛋白,目前已成为医院的常规检测项目,可以在很多疾病诊断上作为辅助判断的依据[1-3]。越来越多的证据表明,CRP不仅是炎症标志物,同时本身也直接参与炎症过程[4-6]。在临床应用方面,C-反应蛋白的水平检测在世界范围内越来越受到重视。但是由于免疫分析试剂具有多种产品,各厂家针对不同的目标物开发试剂和方法等因素,造成测量的偏差很大[7]。
目前,国内外临床实验室CRP的检测数据普遍具有较大偏差,没有可比性,因此使心肌梗死等疾病的临床诊断有时出现假阳性或假阴性结果[8-10]。为了使临床的检测结果具有统一的参考值和更规范的可比性,国际临床化学会和美国临床化学会设立了CRP标准化委员会,以开展相应的标准化工作[11]。欧美等发达国家已经着手进行CRP的标准物质研究。目前世界上有两种2级参比物质:1)具有世界卫生组织第一国际标准CRP (WHO IS 85/506),浓度100 mg/L[12];2)具有欧共体标准授权的有证标准物质CRP470[13]。
本次比对是基于中、日、韩国家计量组织合作框架下,并于2011年9月在中国成都的中日韩会议上提出并确认。由日本计量院负责提供比对样品,由比对参加单位自由选择方法。
同位素稀释质谱法(IDMS)具有绝对测量的性质、灵敏度高、测量动态范围宽且测量值溯源到国际基本单位制等优点,近年来被国内外实验室广泛用作蛋白准确定量的方法,也是目前公认的蛋白标准物质定值的基准方法。在本次比对中,中国计量院采用同位素稀释质谱法作为CRP的定值方法。
1 实验部分
1.1 主要仪器与装置
Agilent 6410 QQQ 液相色谱-质谱联用仪:美国Agilent公司产品;MS2型漩涡混合器:德国IKA公司产品;Mlnl-6K型掌上离心机:中国珠海黑马公司产品;UFE500烘箱:德国Memmert公司产品;3K15型台式离心机:德国Sigma公司产品;移液器(10、20、100、200、1 000 μL):法国Gilson公司产品;ME235S型天平(感量0.01 mg):德国Satorius公司产品;UMX2型天平(感量0.1 μg):瑞典Mettler Toledo公司产品。
1.2 主要材料与试剂
甲醇、乙腈(色谱纯):德国Merck公司产品;甲酸(分析纯)、盐酸(优级纯):北京化学试剂公司产品;磷酸二氢钠(分析纯):北京益利精细化学品有限公司产品;磷酸(MOS级):北京化学试剂研究所产品;氢氧化钠(分析纯):北京化工厂产品;全氟庚酸:美国Sigma-Aldirich公司产品;亮氨酸、缬氨酸标准物质:由日本计量院提供;亮氨酸、缬氨酸同位素标记物:美国剑桥同位素实验室产品。
1.3 实验条件
1.3.1色谱条件 色谱柱:Agilent Zorbax SB-Aq(2.1 mm×150 mm×3.5 μm);柱温30 ℃,进样体积2 μL,流速0.2 mL/min;流动相:A为0.8 mmol/L全氟庚酸和0.05%三氟乙酸的水溶液,B为乙腈;进样量2 μL;洗脱梯度:0~5 min,15%B,5~20 min,30%B,20~30 min,30%B,30~40 min,70%B。
1.3.2质谱条件 多反应监测模式(MRM);监测离子对:m/z117.1>m/z72.1(缬氨酸),m/z122.1>m/z75.1(C5-缬氨酸),m/z132.1>m/z86.1(亮氨酸),m/z142.1>m/z96.1(D10-亮氨酸);碰撞诱导解离电压100 V;碰撞能量8 eV。
1.4 样品前处理方法
取100 μL CRP于安瓶中,按质量比1∶1分别加入缬氨酸和亮氨酸标记溶液,真空干燥。然后加入800 mL 6 mol/L HCl,混合均匀后,通氮除氧,密封,在110 ℃烘箱中水解,每隔12 h涡旋混匀1次。水解48 h后取出,氮气吹干,用含有0.1%盐酸的水溶液复溶,溶液经过0.22 μm滤膜过滤后,上机测定[14]。
1.5 结果计算
按照低标—样品—高标—样品—低标的顺序测定,同位素比例分别为0.9和1.1。
样品的氨基酸浓度为:
c氨基酸=
其中:m标为样品溶液中氨基酸同位素标记物的质量;I样为样品氨基酸与氨基酸标记物的峰面积比;W1为高标溶液氨基酸与氨基酸标记物的质量比;W2为低标溶液氨基酸与氨基酸标记物的质量比;I1为高标溶液氨基酸与氨基酸标记物的峰面积比;I2为低标溶液氨基酸与氨基酸标记物的峰面积比;M为样品质量;P为氨基酸标准物质的纯度。
根据C-反应蛋白的结构和测得的氨基酸浓度,计算对应蛋白的浓度。
2 结果与讨论
2.1 比对样品测量结果
本次比对样品为同一浓度的2个样品,分别记为A样和B样。氨基酸标准品和蛋白水解样品在液相色谱-同位素稀释串联质谱上的分离情况示于图1、图2。
从2个样品中分别取3份子样进行同位素稀释质谱法的测定,结果列于表1~3。
1号实验室是韩国计量院,2号实验室是中国计量院,3号实验室是日本计量院,日本计量院采用了气相和微波消解两种方法。与日本计量院的结果相比,韩国计量院的测定结果稍低,
中国计量院的测定结果稍高,但都处于日本计量院的测定结果不确定度范围内。
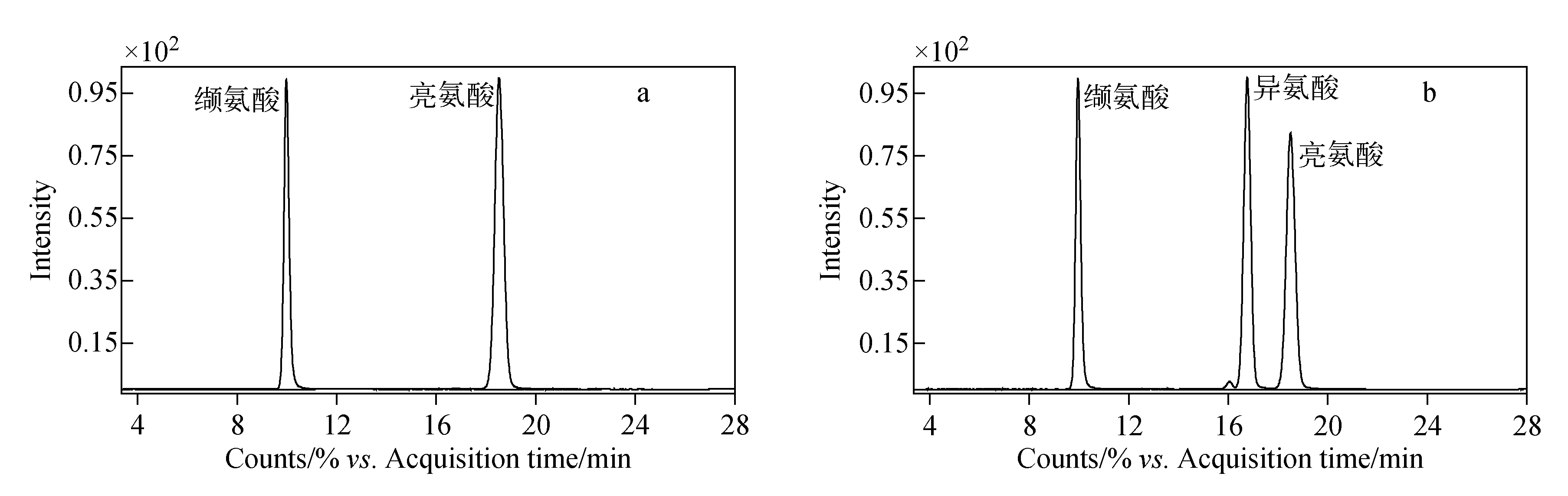
图1 标准品(a)和C-反应蛋白检测样品(b)的氨基酸分离Fig.1 Amino acid separation of standard sample(a) and CRP sample(b)
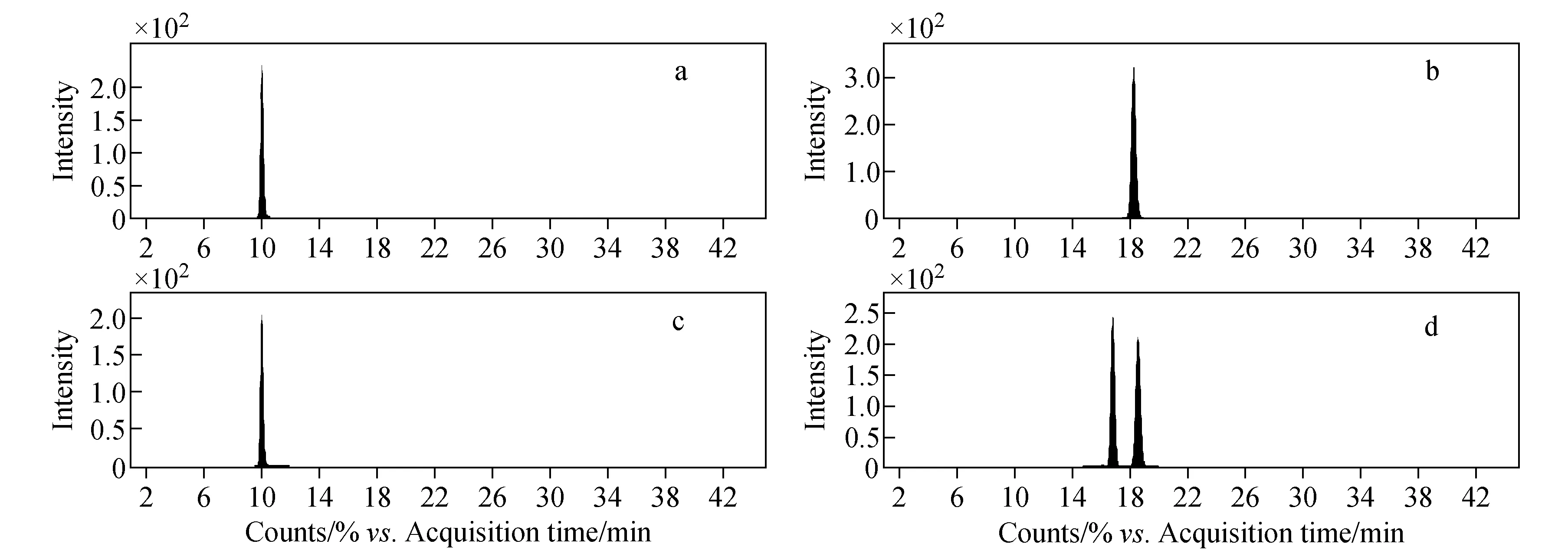
注:a.缬氨酸标准物质;b.亮氨酸标准物质;c.人CRP标准物质的缬氨酸分离;d.人CRP标准物质的亮氨酸分离图2 人C-反应蛋白标准物质样品的氨基酸分离Fig.2 The amino acid separation for CRP CRM

样品编号样品浓度/(mmol/kg)A样41.56B样41.48平均值41.52不确定度0.91(k=2)
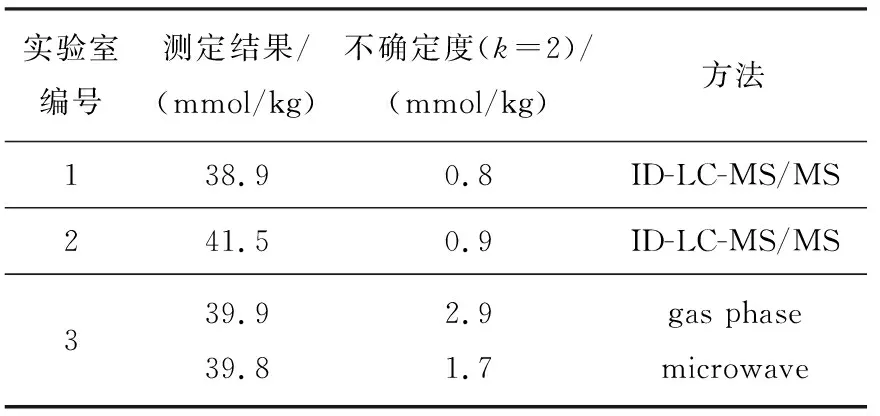
表3 中日韩C-反应蛋白比对结果Table 3 The comparison results of C-reactive protein international for Japan, South Korea and China
2.2 测量结果不确定度
将各个不确定度分量合成,由式(1)计算得
到标准不确定度:
(1)
对应95%置信水平,取包含因子k=2,则扩展不确定度为U=k·u。方法重复性为A类不确定度,其余为B类不确定度,计算结果列于表4。
3 结论
此次重组人C-反应蛋白纯蛋白标准物质量值比对由日本计量院组织发起,韩国计量院和日本计量院的结果与中国计量院测定的结果取得了等效一致。证明了三家计量院在人C-反应蛋白纯蛋白标准物质上的测定能力,同时也证明了中国计量院所使用的定值方法准确可靠。本次比对研究了可能影响标准物质定值结果的各种因素,为研究蛋白质类大分子标准物质积累了宝贵经验,同时验证了国内CRP纯品标准物质的定值方法,并为相关研究奠定了基础。
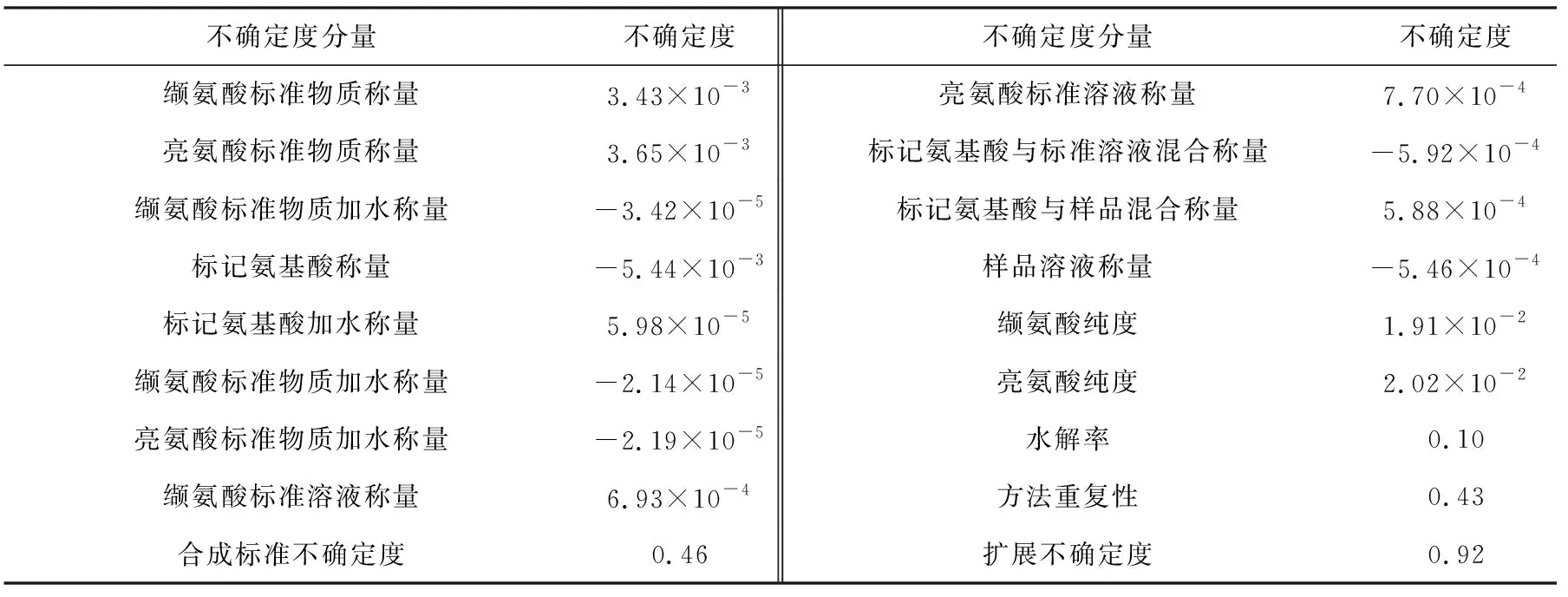
表4 C-反应蛋白不确定度计算
参考文献:
[1] FILEP J G. Platelets affect the structure and function of C-reactive protein[J]. Circ Res, 2009, 105(2):109-111.
[2] CRANE A M, FEUER W, GALOR A. C-reactive protein levels and tear function parameters[J]. Ophthalmology, 2013, 120(5):1 099-1 112.
[3] MARTINS C, FREITAS I J R, PIZARRO A, et al.Cardiorespiratory fitness, but not central obesity or C-reactive protein, is related to liver function in obese children[J]. Pediatr Exerc Sci, 2013, 25(1):3-11.
[4] PRADEEP A R, KUMARI M, KALRA N, et al. Correlation of MCP-4 and high-sensitivity C-reactive protein as a marker of inflammation in obesity and chronic periodontitis[J]. Cytokine, 2013, 61(3):772-777.
[5] MCTNTYRE C, HARPER I, MACDOUGALL I C, et al. Serum C-reactive protein as a marker for infection and inflammation in regular dialysis patients[J]. Clin Nephrol, 1997, 48(6):371-374.
[6] LIBBY P, RIDKER P M. Inflammation and atherosclerosis: Role of C-reactive protein in risk assessment[J]. Am J Med, 2004,116 (6):9-16.
[7] DIAR H A, NAKWA F L, THOMAS R, et al. Evaluating the QuikRead C-reactive protein test as a point-of-care test[J]. Paediatr Int Child Health, 2012, 32(1):35-42.
[8] DOMINICI R, LURASCHI P, FRANZINI C, et al.Measurement of C-reactive protein: Two high sensitivity methods compared[J]. J Clin Lab Anal, 2004,18(5):280-284.
[9] ARMIN I, MARGIT F, HANNELORE L, et al. Distributions of C-reactive protein measured by high-sensitivity assays in apparently healthy men and women from different populations in Europe[J]. Clinical Chemistry, 2003,4 (4): 4 669-4 672.
[10] WALD D S, KASTURIATNE A, BESTWICK J P, et al. The value of C-reactive protein in screening for future coronary heart disease events[J]. J Med Screen, 2009,16(4):212-214.
[11] WHO Expert Committee on Biological Standardization, (WHO technical report series ; no. 963)[R]. WHO Press, World Health Organization 1 211 Geneva 27, Switzerland, www.who.int/bookorders.
[12] WHO international standard human C-reactive pr-otein 1st international standard NIBSC code: 85/506 instructions for use (Version 3.0, Dated 19/03/2008)[S]. Medicines and Healthcare Products Regulatory Agency, 2008.
[13] JOHNSON A M, LEDUE T B, COLLINS M F, et al. Commutability of the CRM 470 C-reactive protein value in the Dade Behring N High Sensitivity CRP assay[J]. Clin Chem Lab Med, 2003, 41(2):177-182.
[14] MUNOZ A, KRAL R, SCHIMMEL H, et al. Quantification of protein calibrants by amino acid analysis using isotope dilution mass spectrometry[J]. Anal Biochem, 2011, 408(1):124-131.
[15] RIDKAR P M, BURING J E, COOK N R, et al.C-reactive protein,metabolic syndrme,and risk of incident cardiovascular evnts:An 8 year follow-up 14 719 initially healthy American women[J]. Circulation, 2003, 107(3): 391-397.
[16] FUJII T, YAJIMA R, TABE Y, et al. Elevated C-reactive protein is associated with the tumor depth of invasion but not with disease recurrence in stage II and III colorectal cancer[J]. Hepatogastroenterology, 2013, 60(126):1 343-1 347.

