L-叔亮氨酸的合成和应用
董凌政 廖诗雨(西北民族大学,甘肃 兰州 730100)
1 L-叔亮氨酸的性质
天然氨基酸和非天然氨基酸之间结构相似但手性不同。L-叔亮氨酸分子式为C6H13NO2,外观为白色至近乎于白色的粉末状物质,别称L-2-氨基-3,3-二甲基丁酸,分子量131.17,是一种化学物质。其密度为1.038g/cm3,熔点300℃,沸点217.7℃,闪点85.5℃,折射率-9°,水溶解性125.5g/L(20℃),蒸汽压0.0499mmHg (25℃)。图1为L-叔亮氨酸的结构式示意图。

图1 L-叔亮氨酸的结构式
2 L-叔亮氨酸的功能
L-叔亮氨酸是合成抗病毒药物阿扎那韦的关键侧链。抗癌药物 BB-2516、抗艾滋病药物阿扎那韦、抗炎药物 RO-31-9790、抗丙肝病毒药物特拉匹韦等药物的制备都需要借助L-叔亮氨酸进行合成。L-叔亮氨酸常常替代其他氨基酸:如缬氨酸、亮氨酸等应用于多肽合成中,L-叔亮氨酸用作不对称反应的催化剂,在用作不对称氨化还原反应中化学酶催化剂的配体时能很好地提升其催化效率。图2为L-叔亮氨酸的应用示意图。
3 L-叔亮氨酸的合成
3.1 化学制备法
3.1.1 有机拆分
Wittig反应是指羰基用磷叶立得变为烯烃,该反应又称为叶立得反应或维蒂希反应,它主要用于将醛、酮直接合成为烯烃。为了制得L-叔亮氨酸,可以将三甲基乙醛作为反应原料,通过叶立得反应,将合成的烯烃经过加成,再在有醋酸钠-醋酸的条件下发生取代,经过水解后在催化加氢最常用的Pd/C催化剂作用下即可发生加成反应生成L-叔亮氨酸。该方法反应流程如图3所示。

图2 L-叔亮氨酸的应用
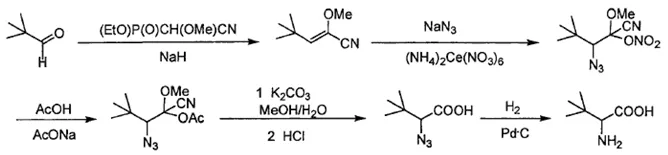
图3 三甲基乙醛反应生成L-叔亮氨酸的流程示意图
由该反应的流程图可以看出,用此方法制备L-叔亮氨酸步骤繁琐,且制备过程中会有对环境造成污染的有机物参与,随着工业技术的发展,目前这种方法已经由更为简便的其他方法逐渐取代。
3.1.2 有机合成
手性合成也称不对称合成,是研究向反应物引入一个或多个具手性元素的化学反应的有机合成分支。
利用化学合成方法中的不对称合成,将(R)-苯基甘氨酸酰胺或手性α-苯乙胺作为手性诱导剂,分别与特戊醛或叔丁基酮酸经过一系列反应合成L-叔亮氨酸。由于参与此化学过程中的催化剂成本高昂,并且会对环境造成较大污染,也不提倡用此法进行大规模生产。该方法反应流程如图4所示。

图4 不对称合成法生成L-叔亮氨酸的流程示意图
最早用于制备L-叔亮氨酸的方法便是化学制备法,它的优势是易扩大到工业水平,但同时因为制备操作复杂、产物产率较低、工艺价格昂贵、造成环境污染等诸多问题制约了该方法的开展和应用。
3.2 生物制备法
近年来,生物制备法逐渐成为制备叔亮氨酸的热门研究课题。利用生物法制备L-叔亮氨酸主要分为两大类,一种是生物催化直接合成法,另一种是生物酶法。
3.2.1 生物催化直接合成法
根据材料和方式的不同,生物催化可分别使用全细胞和游离酶作为催化剂制备L-叔亮氨酸。
选用HPLC直接检测法作为表征方法,细菌全细胞作为催化剂对以三甲基丙酮酸和甲酸铵为底物的反应进行催化,将L-叔亮氨酸从三甲基丙酮酸中还原出来。也可将L-亮氨酸脱氢酶作为催化剂对以三甲基丙酮酸和甲酸铵为底物的反应进行催化,从底物甲酸铵中获取氢原子和氨分子,再在辅酶NADH的作用下将L-叔亮氨酸从三甲基丙酮酸中还原出来。
3.2.2 生物酶法
生物酶法需要作用的条件温和,收率、光收率均很高,与化学合成法不同的是,在利用生物酶法制备目标物时不会对环境造成污染和危害,这也是生物酶法最大的优势。目前在工业和市场中,生物酶法具有更大的发展潜力和更广阔的发展空间。
人们首次使用生物酶法制备L-叔亮氨酸时用到的酶是纯化的猪肾酰胺水解酶,但其目标物产率很低。赫斯特公司用青霉素G酰化酶辅助一些工艺也合成了L-叔亮氨酸,但其工艺十分复杂,不便操作。在前人研究的基础上,后来还有研究人员探究出一种新的制备方法,即通过水解酶或者消旋酶对对映体进行选择性水解,但因其成本巨大、步骤繁琐也没有得到广泛的应用。
α-酮酸成本低廉、容易获得,且其制备过程操作简单,所以常作为生物酶法的原始底物。由于制备反应过程中辅酶NADH(其结构式如下图5所示)的成本昂贵,通常在实验中引入甲酸脱氢酶或葡萄糖脱氢酶来解决辅酶再生的问题,从而在辅酶NADH的作用下,三甲基丙酮酸能够高效地从亮氨酸脱氢酶的作用中得到还原。德国的德固赛公司使用游离的甲酸脱氢酶(FDH)和亮氨酸脱氢酶,在25℃和pH8.0的条件下,利用甲酸脱氢酶将NAD+还原为NADH,从而实现辅酶的再生,该反应最大的优势是可以实现使用酶的回收再利用,其反应原理如下图6所示。美国一家领先的蛋白质工程公司(Codexis)使用游离的酮基还原酶和亮氨酸脱氢酶,在40℃和pH9.0的条件下进行了L-叔亮氨酸的合成,游离酮基还原酶的使用也是为了实现辅酶的再生。

图5 NADH的结构式
4 结语
文章介绍了L叔亮氨酸的物化性质、结构特点及应用前景,阐述了制备L-叔亮氨酸的各类方法。随着工业技术和科学研究的发展,制备L-叔亮氨酸从最初的化学合成法到现在的生物催化法,实现了从高成本到低成本,高污染到低污染,高能耗到低能耗的转变。化学反应条件苛刻,步骤繁琐,需要用到的大量有机溶剂都需经过多次拆分或多次合成,操作过程中会产生对环境污染较大的有害物质,且收率极低。生物催化法条件温和,步骤简单,产物光学纯度大于99%,收率极高,且不会产生对环境造成污染或危害的物质,是一种绿色、环保的生产工艺。
L-叔亮氨酸作为很多药物合成的中间体,在生物领域、化工领域、医药领域等都具有十分重要的作用,因此对L-叔亮氨酸合成路线的研究将一直作为热门项目,吸引一批又一批的科学家及研究人员不断探索、不断创新。

