FPS-1306的合成研究
翟世重,姜乃才
(烟台大学药学院,山东 烟台 264005)
戊聚糖钠(Arixtra,fondaparinux sodium,磺达肝癸钠)是赛诺菲圣德拉堡集团和欧加农公司联合研究开发出的新一代抗血栓制剂,是第一个以Xa 因子为主要靶点的全合成戊糖抗凝血剂[1].2001年获得FDA批准[2],2008年在中国上市.戊聚糖钠由5个单糖片段(ABCDE,结构见图1)构成,其结构复杂,全合成需要50多步化学反应.
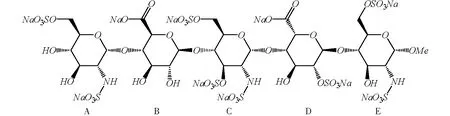
图1 戊聚糖钠的结构
戊聚糖钠常见的合成策略是A+BC+DE,关于各片段的合成文献已有报道[3],其中,DE片段是戊聚糖钠合成重要组成部分之一,该片段的合成已有文献报道[3-4],本研究报道了二糖AB片段FPS-1306(1)的一种新的合成路线.
文献报道化合物1的合成是以1,2,4-三-O-乙酰基-4-O-苄基-L艾杜糖醛酸甲酯(2)为原料经溴化、原乙酸酯化、脱乙酰基、上氯乙酰基后与化合物3成苷、脱去氯乙酰基制得(图2).在对文献报道的方法进行实验条件考查以后,发现该路线反应步骤多(6步)、产率较低(17.4%)、中间体不稳定且难于纯化.

图2 文献合成路线
本研究以化合物2为原料采用溴代物方法[5]制得溴代物(4),后者与化合物3在银盐的催化作用下形成糖苷键得到化合物5,脱乙酰化产物6再经选择性乙酰化反应得到化合物1(图3),该合成路线以化合物2计算共计4步反应,与文献报道的6步反应比,具有步骤少、收率高(38.9%)、中间体稳定等特点.

图3 化合物1的合成路线
1 实验部分
1.1 仪器和试剂
熔点用WRS-1B数字熔点仪;核磁共振谱数据由Bruker AVANCE-400型核磁共振仪测定(TMS为内标,CDCl3为溶剂);质谱数据由TSQ QUANTUM ACCESS质谱仪测定(乙腈为溶剂);HPLC图谱由Agilent 1100型高效液相色谱仪测定(90%乙腈,ODS柱,25 ℃,210 nm),测试试剂均用色谱纯;TLC跟踪化学反应和分离过程,所用柱层析硅胶及薄层层析硅胶板均由烟台化学工业研究所提供;其他化学试剂均为分析纯;2个单糖化合物2和3由本课题其他研究小组提供.
1.2 化合物4和化合物5的合成
称取化合物2(2.0 g,4.7 mmol)按照文献方法[5]合成得透明黄色浆状物 4(2.2 g),收率95%,直接用于下步反应.
称4A分子筛(2.7 g)和化合物3(3.3 g,7.2 mmol)于内含化合物4(2.2 g)的圆底烧瓶中,加入二氯甲烷(38.5 mL),室温搅拌30 min,降至0 ℃,加入三氟甲基磺酸银(1.6 g,6.0 mmol),剧烈搅拌1 h(TLC,V正己烷∶V乙酸乙酯=1∶1),反应液过滤,滤液减压浓缩得到黄色浆状物.经硅胶柱层析(V正己烷∶V乙酸乙酯=3∶1~2∶1),得到透明浆状物5(2.2 g),收率56%.
1H NMR (400 MHz,CDCl3),δ: 7.40~7.14 (m,15H,-3 Ph),5.14 (s,1H,H-1′),4.86 (br s,1H,H-5′),5.06 (t,1H,J=3.0 Hz,H-2′),5.01 (m,2H,-CH2Ph),4.82 (d,1H,J=10.0 Hz,-NH),4.72 (m,2H,-CH2Ph),4.67 (d,1H,J=11.3 Hz,-CH2Ph),4.66 (br s,1H,H-1),4.50 (d,1H,J=11.3 Hz,-CH2Ph),4.49 (d,1H,J6a,6b=12.2 Hz,H-6a),4.22 (dd,1H,J6b,6a=12.2 Hz,J5,6=3.2 Hz,H-6b),4.03 (ddd,1H,J2,N=J2,3=10.0 Hz,J1,2=3.2 Hz,H-2),3.94 (t,1H,J=10.0 Hz,H-4),3.80 (m,2H,H-3′,H-5),3.54 (t,1H,J=10.0 Hz,H-3),3.43 (s,3H,-COOMe),3.35 (s,3H,-Ome),2.12 (s,3H,-OAc),2.03 (s,3H,-OAc),2.00 (s,3H,-OAc).
1.3 化合物6的合成
称化合物5(2.2 g,2.7 mmol)和碳酸钾(0.10 g,0.76 mmol)于圆底烧瓶中,加入甲醇(34 mL),室温反应12 h(TLC,V正己烷∶V乙酸乙酯=1∶1),减压蒸干,得到微黄色固体,加入乙醚(100 mL)静置2 h后.抽滤,滤饼用乙醚(50 mL)洗涤3次,得到白色固体化合物6(1.7 g),收率90%,HPLC纯度为92%.mp:163~164 ℃.
1H NMR (400 MHz,CDCl3),δ: 7.52 (d,1H,J=9.2 Hz,-NH),7.41~7.11 (m,15H,-3 Ph),5.47 (d,1H,J=6.2 Hz,-OH),5.14 (d,1H,J=7.8 Hz,-OH),5.01 (d,1H,J=3.6 Hz,H-1′),4.97 (AB system,2H,-CH2Ph),4.88 (t,1H,J=5.6 Hz,-OH),4.73~4.57 (m,6H,H-1,H-2′,-2 CH2Ph),3.84 (m,1H),3.66(m,7H),3.84 (m,1H,H-6a),3.76~3.55 (m,7H),3.47 (d,1H,J=9.6 Hz,H-2),3.31 (s,3H,-COOMe),3.29 (s,3H,-OMe);
1H NMR (400 MHz,CDCl3+D2O),δ: 7.52 (d,1H,J=9.2 Hz,-NH),7.41~7.11 (m,15H,-3Ph),5.01 (d,1H,J=3.6 Hz,H-1′),4.97 (AB system,2H,-CH2Ph),4.68~4.48 (m,6H,H-1,H-2′,-2 CH2Ph),3.81(br s,1H,H-4′),3.62(m,7H),3.47(d,1H,J=9.6 Hz,H-2),3.25(br s,6H,-COOMe,-OMe);
13C NMR(100 MHz,CDCl3),δ: 169.3,156.1,138.7,138.6,136.9,128.2,128.1,127.7,127.6,127.5,127.5,127.3,127.0,126.8,100.4,98.3,77.9,74.3,73.2,71.5,69.9,68.9,67.8,65.3,59.5,55.1,54.8,54.4
1.4 化合物1的合成
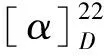
1H NMR (400 MHz,CDCl3),δ: 7.40~7.21 (m,15H,-3 Ph),5.10 (br s,1H,H-1′),4.99 (AB system,2H,-CH2Ph),4.97 (d,1H,J4′5′=1.8 Hz,H-5′),4.94 (br s,1H,H-2′),4.86 (d,1H,J2N=10.0 Hz,N-H),4.76 (d,1H,J=11.6 Hz,-CH2Ph),4.74 (d,1H,J=11.2 Hz,-CH2Ph),4.67 (br s,1H,H-1),4.66 (d,1H,J=11.6 Hz,-CH2Ph),4.53 (d,1H,J=11.2 Hz,-CH2Ph),4.47 (d,1H,J6a,6b=12.1 Hz,H-6a),4.24 (dd,1H,J6b,6a=12.1 Hz,J5,6=3.7 Hz,H-6b),4.07 (td,1H,J2,N=J2,3=10.0 Hz,J1,2=3.2 Hz,H-2),3.97 (br s,1H,H-4′),3.93 (m,1H,H-4),3.81 (m,1H,H-5),3.73 (m,1H,H-3’),3.59 (t,1H,J2,3=J3,4=10.0 Hz,H-3),3.50 (s,3H,-COOMe),3.37 (s,3H,-OMe),2.13 (s,3H,-OAc),2.09 (s,3H,-OAc).
13C NMR (100 MHz,CDCl3),δ: 169.1,169.4,170.6,155.7,138.0,137.3,136.1,128.4,128.2,128.1,128.1,128.0,127.9,127.4,127.2,98.8,98.1,79.1,77.3,77.0,76.7,75.2,74.5,72.3,74.3,69.2,68.5,67.7,67.2,67.0,62.3,55.2,54.6,52.0,29.6,22.6,20.8.
MS(ESI),m/Z: 804.21 [M+Na]+.
2 结 论
实验结果表明本研究设计的新路线较文献[3-4]报道的路线减少两步化学反应,总收率提高21.5%,反应步骤少,总收率高,中间体相对稳定,在规模化制备方面具有较大的优势.2条路线所得化合物1波谱分析数据与文献报道值[3-4]相符.
参考文献:
[1] Susan J K,Karen L G. Fondaparinux sodium[J]. Drugs,2002,62(11): 1673-1685.
[2] Alban S. From heparins to factor Xa inhibitors and beyong[J]. European Journal of Clinical Investigation,2005,35(Supple1):12-20.
[3] Jacquinet J C,Petitoi M,Duchausso P,et al. Synthesis of Heparin fragments: A chemical synthesis of the trisaccharide[J]. Carbohydr Res,1984,130:221-241.
[4] Petitou M,Duchaussoy P,Lederman I,et al. Synthesis of heparin fragments: A methylα-pentaoside with high affinity for antithrombin III [J]. Carbohydr Res,1987,167: 67-75.
[5] Gavard O,Hersant Y,Alais J,et al. Effcient preparation of three building blocks for the synthesis of heparan sulfate fragments: towards the combinatorial synthesis of oligosaccharides from hypervariable regions[J]. Eur J Org Chem,2003,18:3603-3620.

