聚离子液体膜修饰电极检测厚朴酚
李春涯,郑芙蓉,黄奕娜,李 婷,李丽卿,杨 婷,陆俭洁*
(1中南民族大学化学与材料科学学院国家民委分析化学重点实验室,武汉430074;2广东省潮州市质量计量监督检测所,潮州521011)
离子液体是由有机阳离子和无机阴离子或有机阴离子组成的,在室温附近呈液体或熔点<100℃的盐类,因而也称作室温离子液体.离子液体具有不挥发、液程宽、溶解性强、热稳定性高、导电性好、电位窗口宽等特性,广泛用于有机合成、材料科学、生物化学、电化学及分析化学[1].电分析化学研究表明,离子液体能促进电子转移速度,改善电极的传感特性,提高传感器的选择性及灵敏度[2-4].然而,即使采用1-丁基-3-甲基咪唑六氟磷酸盐这种疏水性离子液体构建膜修饰电极,仍很难保持离子液体膜的长期稳定性[5].鉴于此,拟通过电化学聚合1-[3-(N-吡咯)丙基]-3-己基咪唑四氟硼酸盐离子液体至电极表面,以提高修饰膜的稳定性.结果表明,该聚离子液体膜仍会在水相中溶解.因此,采用十二烷基磺酸钠处理该聚离子液体膜修饰电极,实现其阴离子交换,构建疏水性聚合物界面.考察了厚朴酚在该聚离子液体疏水界面上的电化学行为,并建立高灵敏分析方法.
厚朴酚是中药厚朴皮中抗菌作用的有效成分,其结构如图1.《中国药典》规定中药厚朴质量以厚朴酚含量为标准.因此,建立高效、选择性强的厚朴酚检测方法,对确保厚朴药材的质量以及合理用药有重要的意义.厚朴酚检测方法主要有毛细管电泳法[6],液相色谱法[7]和液相色谱/质谱联用法[8]等.由于厚朴酚中的酚羟基可被电化学氧化,故电化学法[9]也用于其检测,且因灵敏、快速而倍受关注.

图1 厚朴酚的化学结构Fig.1 Chemical structure of magnolol
1 实验部分
1.1 仪器与试剂
在CHI660C电化学工作站(辰华仪器公司,上海)上进行电化学测试,采用三电极体系进行:聚离子液体膜修饰电极(3 mm)为工作电极,参比电极为饱和甘汞电极(SCE),对电极为铂柱电极;核磁共振谱在AVANCE III 400 NMR spectrometer(Bruker,Switzerland)上测得.
厚朴酚(Magnolol,阿拉丁试剂公司)溶于无水乙醇配成1.0×10-2mol/L标准溶液,置于4℃冰箱储存备用,使用时稀释到所需浓度;磷酸盐缓冲液由Na2HPO4和KH2PO4配成;除特别标注外,所有试剂均为分析纯,试剂未经纯化而直接使用,实验用水为超纯水,所有实验在室温下完成.
1.2 实验方法
1.2.1 离子液体合成
吡咯逐滴加至含1,3-二溴丙烷和NaH的DMF溶液中,并搅拌过夜.加入适量二次水,无水乙醚萃取,乙醚层以无水硫酸镁干燥,旋转蒸发溶剂.初产品经硅胶柱分离纯化,得褐色油状液体,N-(3-溴丙基)吡咯.
搅拌条件下将N-(3-溴丙基)吡咯甲苯溶液逐滴加入3-己基咪唑甲苯溶液中,反应12 h.减压蒸出甲苯溶剂,以CH2Cl2/CH3OH(1:1)为淋洗剂,硅胶柱分离得溴化1-[3-(N-吡咯)丙基]-3-己基咪唑离子液体.搅拌条件下,将该离子液体加入四氟硼酸钠水溶液中,60°C反应30 min,CH2Cl2萃取分离,无水硫酸镁干燥,蒸出溶剂,即得1-[3-(N-吡咯)丙基]-3-己基咪唑四氟硼酸盐离子液体(1H NMR(D2O):8.42(s,1H),7.34(s,2H),6.68(s,2H),6.08(s,2H),4.11(t,2H),4.05(t,2H),3.97(t,2H),2.30(tt,2H),1.75(tt,2H),1.21(tt,6H),0.78(t,3H).
1.2.2 聚离子液体膜修饰电极制备
用 6#金相砂纸打磨玻碳电极,再用 0.3 μm α-Al3O2抛光,分别在硝酸、乙醇、二次水中超声清洗,晾干备用.将洁净的玻碳电极置于含0.5 mmol/L1-[3-(N-吡咯)丙基]-3-己基咪唑四氟硼酸盐离子液体的四氟硼酸钠溶液中,在0 V和1.2 V间进行电位阶跃聚合,修饰电极在十二烷基磺酸钠溶液中浸泡,实现阴离子交换,获得疏水性聚1-[3-(N-吡咯)丙基]-3-己基咪唑十二烷基磺酸盐离子液体膜修饰电极(PIL/GCE).
1.2.3 样品制备
中药厚朴购买于武汉市中南民族大学校医院.厚朴样品在60℃下干燥4 h后研磨成粉.厚朴酚的萃取过程按照文献[10]进行:称量2.0 g已研磨好的厚朴粉末,加入100 mL甲醇,60℃静置3 h.冷却至室温,超声30 min,过滤,收集滤液.
1.2.4 电化学测试方法
将PIL/GCE电极置于磷酸缓冲溶液中,在-0.2~1.0 V电位范围内循环伏安扫描至基线稳定,洗净,室温晾干.将PIL/GCE电极置于厚朴酚溶液中,0 V 条件下搅拌富集120 s,记录-0.2~1.0 V电位区间内的微分脉冲伏安曲线,氧化峰峰电流用于厚朴酚测定.
2 结果与讨论
2.1 厚朴酚在聚离子液体膜修饰电极上的循环伏安行为
图2为3.0×10-6mol/L厚朴酚在聚离子液体膜修饰电极(a)和裸玻碳电极上的循环伏安曲线.在-0.20~1.0 V电位范围内,厚朴酚在聚离子液体膜修饰电极和裸玻碳电极上都呈现出一个氧化峰,其氧化峰峰电位分别位于0.64 V和0.56 V.在负电位方向扫描过程,没有观察到相应的还原峰,由此可知,厚朴酚的电化学氧化是一个不可逆过程.与裸电极相比,厚朴酚在聚离子液体膜修饰电极上的氧化峰电位略有正移,表明聚合物膜对其电子传递有阻碍作用;但其氧化峰峰电流比在裸电极上显著增强,表现出明显的增敏效应.
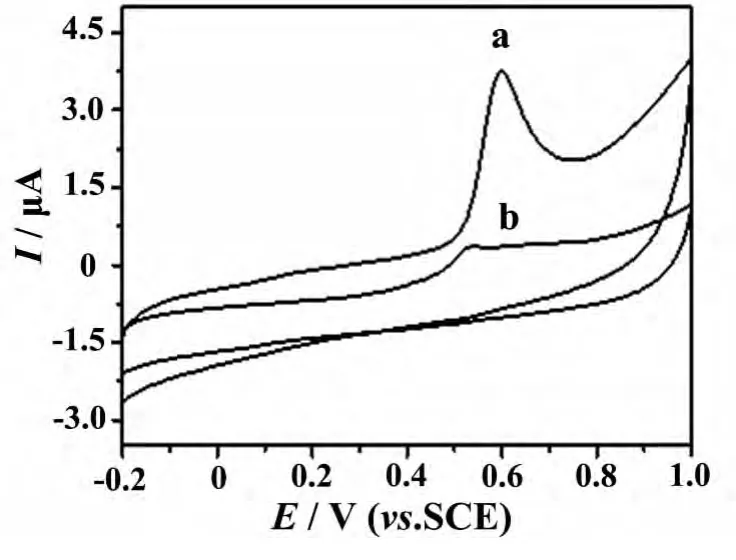
图2 厚朴酚的循环伏安曲线Fig.2 Cyclic voltammograms of magnolol
2.2 扫描速度的影响
以聚离子液体膜修饰电极为工作电极,在0.025~0.5 V/s范围内考察了不同扫描速度对1.0×10-6mol/L厚朴酚的伏安行为的影响,其循环伏安曲线见图3.如图3所示,从0.025 V/s(图3 a)到0.5 V/s(图3 h),随扫描速度增加,峰电位正移,峰电流逐渐增加.厚朴酚的氧化峰峰电流(I)与扫描速度(v)之间有良好的线性关系,线性方程为I(μA)=14.22 v(V/s)+0.2560(r=0.985),说明厚朴酚在聚离子液体膜修饰电极上的电化学反应受吸附过程控制.
2.3 电位阶跃次数对厚朴酚响应电流的影响
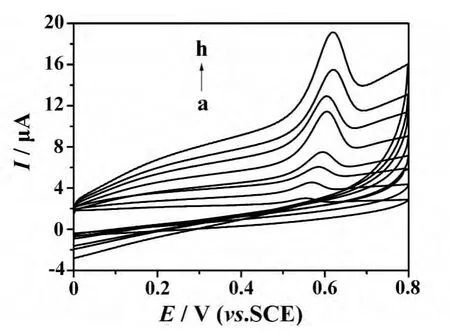
图3 不同扫描速度下厚朴酚在聚离子液体膜修饰电极上的循环伏安曲线Fig.3 Cyclic voltammograms of magnolol on the polymerized ionic liquid film modified electrode at different scan rate
电位阶跃次数(n)直接影响聚聚离子液体膜厚度,从而影响厚朴酚在该膜修饰电极界面的电化学响应,进而改变其检测灵敏度.在不同电位阶跃次数条件下,制备聚离子液体膜修饰电极,采用微分脉冲伏安法研究1.0×10-6mol/L厚朴酚的电流响应,如图4.当阶跃次数由5次增加至10次时,其氧化峰峰电流显著增加;而阶跃次数由10次增加至30次时,厚朴酚氧化峰峰电流逐渐降低;阶跃次数大于30次后,氧化峰峰电流趋于稳定.氧化峰峰电流降低的原因,可能是聚合物膜厚度增加导致界面电荷传递电阻增加,从而导致电流响应下降.

图4 电位阶跃次数对厚朴酚氧化峰峰电流的影响Fig.4 Influence of the potential step number on the oxidation peak current of magnolol
2.4 pH值对厚朴酚响应电流的影响
以聚离子液体膜修饰电极为工作电极,考察了缓冲溶液pH值对厚朴酚在聚离子液体膜修饰电极上的电化学响应的影响.结果表明,当磷酸盐缓冲溶液pH值由4.0到6.0时,氧化峰峰电流逐渐增加;在pH值7.0~12.0范围内,峰电流逐渐减小;在pH值为6.0时,峰电流最大,故选择 pH 6.0的磷酸盐缓冲溶液为支持电解质溶液.
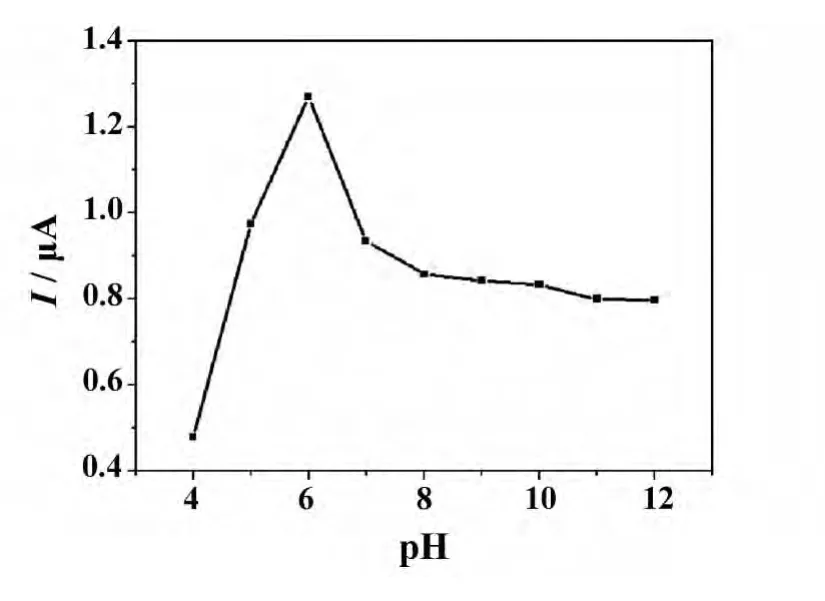
图5 pH值对厚朴酚在聚离子液体膜修饰电极上的氧化峰峰电流的影响Fig.5 Influence of pH values on the oxidation peak current of magnolol at the polymeric film electrode
2.5 富集电位和富集时间的影响
在–0.4~0.5 V内考察了富集电位对厚朴酚在聚离子液体膜修饰电极上的氧化峰峰电流的影响.在–0.4~0 V范围内,峰电流随富集电位增加而增加;进一步升高富集电位,峰电流逐渐降低,故选择0 V作为最佳富集电位.

图6 富集电位对厚朴酚在聚离子液体膜修饰电极上的氧化峰峰电流的影响Fig.6 Influence of accumulation potential on the oxidation peak current of magnolol at the polymeric film electrode
在0~270 s内考察了富集时间对厚朴酚在聚离子液体膜修饰电极上的氧化峰峰电流的影响,结果在0~210 s范围内峰电流逐渐增加,210 s后峰电流逐渐趋于稳定,故选择210 s为最佳富集时间.

图7 富集时间对厚朴酚在聚离子液体膜修饰电极上的氧化峰峰电流的影响Fig.7 Influence of accumulation time on the oxidation peak current of magnolol at the polymeric film electrode
2.6 重现性和干扰实验
平行制备7支聚离子液体膜修饰电极,分别测定1.0×10-6mol/L厚朴酚溶液,相对标准偏差(RSD)为2.09%,表明制备该聚离子液体膜修饰电极具有良好的重现性.考察了该聚离子液体膜修饰电极测定1.0×10-6mol/L厚朴酚时的干扰情况,实验发现 100 倍的 Cd2+,Pb2+,Mg2+,Fe3+,Zn2+,Cu2+;50倍的次黄嘌呤,苯酚,邻苯二酚,赖氨酸,尿酸;100倍的多巴胺,抗坏血酸和儿茶酚对厚朴酚的氧化信号不产生任何干扰(SD<5.0%),故该聚离子液体膜修饰电极用于检测厚朴酚具有较好的选择性.
2.7 分析应用
在优化条件下,用微分脉冲伏安法考察了氧化峰峰电流与厚朴酚浓度之间的关系,发现厚朴酚的氧化峰峰电流与其浓度在 1.0×10-8~5.0×10-6mol/L和5.0×10-6~2.0×10-5mol/L 范围内呈良好的线性关系,线性方程为Ip(μA)=0.7169 c(μmol/L)+0.3123(R2=0.999)和 Ip(μA)=0.1593 c(μmol/L)+3.0864(R2=0.999),其检测限为7.1 ×10-9mol/L.
在最优条件下,按照2.5的方法对实际样品中厚朴酚的含量进行测定,结果见表1.

表1 实际样品中厚朴酚的的测定结果(n=3)Tab.1 Results for magnolol determination in real samples(n=3)
3 结语
本文合成了四氟硼酸1-[3-(N-吡咯)丙基]-3-己基咪唑离子液体,采用电位阶跃技术在玻碳电极表面可控制备了聚离子液体膜修饰电极,考察了厚朴酚在该聚离子液体膜修饰电极上的电化学行为,并用微分脉冲伏安法实现了厚朴酚的测定.结果表明:厚朴酚在该聚离子液体膜修饰电极上只有一个不可逆氧化峰,其氧化峰峰电流与裸电极相比显著增加,具有增敏效应.该方法用于实际样品中厚朴酚含量测定,结果满意.
[1]Rogers D R,Voth G A.Ionic liquids[J].Accounts of Chemical Research,2007,40:1077-1078.
[2]Ratel M,Provencher-Girard A,Zhao S S,et al.Imidazolium-based ionic liquid surfaces for biosensing[J].Analytical Chemistry,2013,85:5770-5777.
[3]Li R,Liu C X,Ma M,et al.Synthesis of 1,3-di(4-amino-1-pyridinium)propane ionic liquid functionalized graphene nanosheets and its application in direct electrochemistry ofhemoglobin[J].Electrochimica Acta,2013,95:71-79.
[4]詹国庆,涂晓婧,苏恩琪,等.聚1-[3ˊ-(N-吡咯)丙基]-3-丁基咪唑离子液体膜电极测定双酚A[J].中南民族大学学报:自然科学版,2012,31:5-9.
[5]Chang J L,Wei G T,Zen J M.Screen-printed ionic liquid/preanodized carbon electrode:Effective detection of dopamine in the presence of high concentration of ascorbic acid[J].Electrochemistry Communications,2011,13:174-177.
[6]Chen C L,Chang P L,Lee S S,et al.Analysis of magnolol and honokiol in biological fluids by capillary zone electrophoresis[J].Journal of Chromatography A,2007,1142:240-244.
[7]Wu X N,Chen X G,Hu Z D.High performance liquid chromatographic method for simultaneous determination of honokiol and magnolol in rat plasma[J].Talanta,2003,59:115-121.
[8]Xu F G,Liu Y,Zhang Z J,et al.Rapid simultaneous quantification of five active constituents in rat plasma by high-performance liquid chromatography/tandem mass spectrometry after oral administration[J].Journal of Pharmaceutical and Biomedical Analysis,2008,47:586-595.
[9]Liu T,Zheng X J,Huang W S,et al.Voltammetric detection of magnolol in Chinese medicine based on the enhancement effectofmesoporousAl/SiO2modified electrode[J].Colloids and Surfaces B:Biointerfaces,2008,65:226-229.
[10]Chen G,Xu X J,Zhu Y Z,et al.Determination of honokiol and magnolol in Cortex Magnoliae Officinalis by capillary electrophoresis with electrochemical detection[J].JournalofPharmaceuticaland Biomedical Analysis,2006,41:1479-1484.

