Pt/SBA-15催化硝基苯选择性加氢合成N-苯基羟胺
刘安双 张群峰
(浙江工业大学工业催化研究所,绿色化学合成技术国家重点实验室培育基地,杭州310014)
N-芳基羟胺是重要的化工中间体,可用于合成生物活性物质、有机试剂、阻聚剂、抗氧化剂等[1-3]。N-芳基羟胺的合成方法主要有金属还原法、生物合成法及催化加氢法等[4-8]。在金属还原法中,金属不能重复使用,并产生大量的含胺废料。生物合成法则会产生大量有害废液,污染环境。催化加氢法是在金属催化剂作用下,芳香族硝基化合物加氢选择性地生成N-芳基羟胺,它具有操作简便、成本低廉、且环境友好的特点。
芳香硝基化合物催化加氢生成芳胺化合物是个多步骤的反应,经历2种中间产物,即亚硝基芳香化合物和N-芳基羟胺。Takenaka等提出的反应机理如下[9]:


若要芳香硝基化合物高选择性加氢合成N-芳基羟胺,就需要在反应体系中加入毒化剂,抑制反应c,即N-芳基羟胺进一步加氢生成芳胺。常用的毒化剂是有机碱、3价或5价磷类化合物、亚砜类化合物等[10-12]。其中,后2种毒化剂对反应c的抑制能力较强,明显地降低催化剂活性;有机碱的抑制能力相对较差。但是,当有机碱与后2种毒化剂一起使用时,它们的供电子能力会有效地提高反应速度[9,11]。
近年来,国内外研究比较多地侧重于有机碱和毒化剂的选择以及它们之间协同效应,而对催化剂的研究鲜有报道。目前,所用的催化剂多以铂族金属为活性组分,尤其是Pt具有更高的选择性。载体一般选用活性炭或SiO2,其中活性炭载体具有比表面积大、Pt金属颗粒易分散的特点,但活性炭微孔多,目标产物分子在催化剂微孔内的扩散困难因而降低了反应的选择性;SiO2孔径较大,可有效消除内扩散的影响,但SiO2比表面积较小,不利于制备分散度高、活性好的Pt/SiO2催化剂。因此,研究制备一种具有较高比表面积和较大孔径的载体负载的高分散型Pt催化剂对高转化率、高选择性催化加氢合成N-芳基羟胺是很有意义的。
本研究采用具有较大比表面积、规整介孔结构的SBA-15分子筛为载体,考察了制备方法(嫁接及浸渍方法)对Pt/SBA-15催化剂结构和性能的影响,获得了1种在硝基芳香化合物催化加氢合成N-芳基羟胺反应中具有高选择性及高活性的Pt/SBA-15催化剂。
1 实验部分
1.1 载体和试剂
SBA-15,A=417m2/g;实验中所用试剂均为分析纯试剂;氢气及氮气纯度均≥99.99%。
1.2 催化剂制备
1.2.1 SBA-15的嫁接
将1.0 g SBA-15在110℃下真空干燥2 h;然后加入到100 mL无水乙醇和3 mL的3-氨丙基三乙氧基硅烷(APTES)中,在78℃下搅拌回流24 h;随后过滤、洗涤、干燥,得到的样品记为SBA-15-gra。反应式如下:
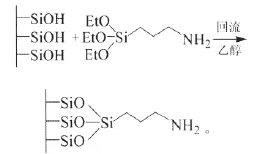
1.2.2 浸渍法
称取已干燥除水的SBA-15和SBA-15-gra各1.0 g,分别将其与适量的水混合形成浆液,在83℃下缓慢滴加化学计量比的H2PtCl6·6H2O溶液,搅拌5 h后,于100℃下干燥16 h,然后在400℃焙烧4 h。焙烧后的Pt/SBA-15和Pt/SBA-15-gra催化剂分别用一定计量比的水合肼溶液在40℃下进行还原,再过滤、洗涤、干燥,得到的样品记为Pt/SBA-15和Pt/SBA-15-gra。
1.2.3 等体积浸渍法
测量SBA-15和SBA-15-gra的饱和吸水量,然后量取等体积的去离子水并在水中溶解化学计量比的 H2PtCl6·6H2O溶液,在室温条件下逐滴加入H2PtCl6·6H2O水溶液到相应的SBA-15和SBA-15-gra中,滴毕后,在100℃下干燥16 h,其余步骤与浸渍法相同。得到的催化剂记为Pt/SBA-15-iwi和Pt/ SBA-15-gra-iwi。
1.3 催化剂表征
1.3.1 XRD
采用X′Pert PRO型X射线衍射仪(XRD)测定催化剂样品的衍射峰,X射线源为Cu靶Ka射线(λ=0.154 056 nm),电压40 kV,电流40mA。
1.3.2 BET
采用Micromeritics ASAP2020型比表面积测试仪测定催化剂样品的比表面积及孔结构等参数。首先将压力抽至2 Pa,保持10 min,然后将温度升至110℃,恒温6 h进行脱气预处理,除去样品上的吸附物种。在-196℃下由N2物理吸附法进行测定,比表面积采用BET方程由N2吸附等温线求得,样品的孔径分布根据Barrett-Joyner-Halenda(BJH)模型计算。
1.3.3 TEM
采用Tecnai G2 F30 S-Twin型透射电子显微镜(TEM)对样品进行扫描,工作电压300 kV。金属粒子的平均颗粒大小用ds表示,通过计算机平台选取几百个颗粒的大小用公式ds=Σnid/(Σnid)得到[13]。
1.4 催化反应评价
硝基苯(NB)催化加氢合成N-苯基羟胺(PHA)反应在100 mL三口烧瓶中进行。用氮气吹扫装置1min,停止通气。将催化剂、反应物、溶剂及添加剂(毒化剂DMSO和异丁胺)依此装入烧瓶中,用氮气置换空气3次,再用氢气置换氮气3次,调节温度和压力,开启搅拌。当吸氢量达到理论值停止反应。冷却过滤催化剂,产物采用Agilent 1100 series高效液相色谱分析,VWD检测器,ODS-2色谱柱(4.6 mm×250mm)。
2 结果与讨论
2.1 催化剂表征
图1~图4是4种Pt/SBA-15催化剂的吸脱附曲线及孔径分布。
从图1~图4可以看出,所有等温线都是IV型曲线,在较高相对压力下均出现H1型滞后回线[14]。吸附曲线的一步毛细凝聚现象表明4种催化剂具有均匀介孔结构,经BJH模型计算可得4种催化剂的平均孔径均为8 nm左右[15]。
4 种Pt/SBA-15催化剂的小角度XRD谱图如图5所示。

从图5可以看出,焙烧之后,除Pt/SBA-15-graiwi催化剂以外,其余3种催化剂的XRD谱图均出现3个衍射峰,分别对应SBA-15特有的100、110和200晶面[16]。说明负载Pt金属后的这3种催化剂均保持了SBA-15高度有序的介孔结构。然而,小角度区域峰强度却各不相同。Pt/SBA-15-gra催化剂的峰强度最小,这可能是Pt纳米粒子进入孔道,降低了孔道和孔壁之间的散射对比度[17-19]。
尽管Pt/SBA-15-gra-iwi催化剂没有观察到明显的衍射峰,但是吸脱附曲线及TEM图(图4)皆表明其有序介孔结构的存在。因此推测可能是由于Pt纳米颗粒大量进入孔道,部分堵塞孔道,明显改变了孔道和孔壁之间的散射对比度。
图6为4种Pt/SBA-15催化剂的广角XRD图谱。
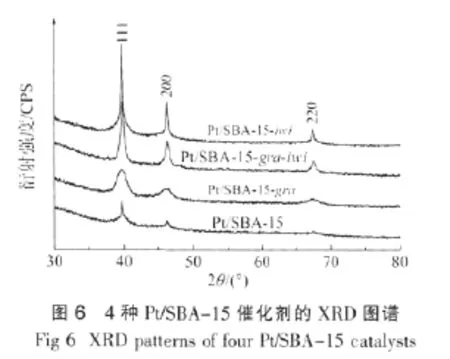
从图6可以看出,4种催化剂的3个特征峰的2θ为39°、46°和68°,分别对应Pt的111、200和220晶面,这表明Pt在SBA-15载体上形成的是面心立方晶体结构[20];Pt/SBA-15-gra催化剂的衍射峰出现了明显宽化的现象,这表明Pt/SBA-15-gra催化剂中有小晶粒的出现,晶粒度较小。
表1是4种Pt/SBA-15催化剂的比表面积及颗粒尺寸。
从表1可以看出,尽管4种催化剂的比表面积变化不大,但颗粒尺寸却变化比较明显。浸渍法制备的Pt/SBA-15和Pt/SBA-15-gra催化剂Pt金属颗粒尺寸较小,而等体积浸渍法制备的Pt/SBA-15-iwi和Pt/SBA-15-gra-iwi催化剂Pt金属颗粒尺寸较大。这可能是因2种浸渍方法的不同特点所致[21]。

表1 不同方法制备的Pt/SBA-15催化剂比表面积及颗粒尺寸Tab 1 Specific surface area and particle size of Pt in Pt/SBA-15 catalysts prepared by differentmethods
透射电镜提供了直接观察Pt纳米颗粒在SBA-15载体上的分布规律。图7分别为4种典型Pt/ SBA-15催化剂的TEM照片。
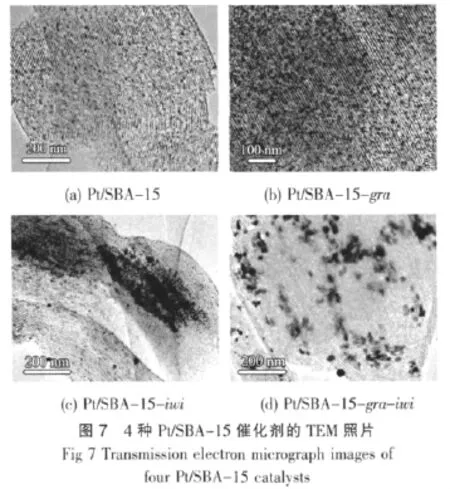
从图7可以看出,4种催化剂的TEM图均能观察到SBA-15载体高度有序的孔道结构。Pt/SBA-15和Pt/SBA-15-gra催化剂的Pt颗粒分散度较好,均一度较高。4种催化剂的Pt颗粒平均尺寸为7 nm、6.4 nm、22 nm和19.5 nm。
2.2 催化性能测试
表2列出了4种催化剂在NB催化加氢合成PHA反应中的催化性能。
从表2可知,4种催化剂的PHA选择性都较高,这可能是由于4种催化剂均保持了SBA-15高度有序的孔道结构,有效消除了内扩散的影响,从而使得在DMSO的作用下,选择性较高。然而反应时间却变化较大,Pt/SBA-15-gra催化剂的反应时间最短(80min),说明其在反应中活性最高。这可能是由Pt/SBA-15-gra催化剂最小Pt纳米颗粒、较好分散度和均一度所致。
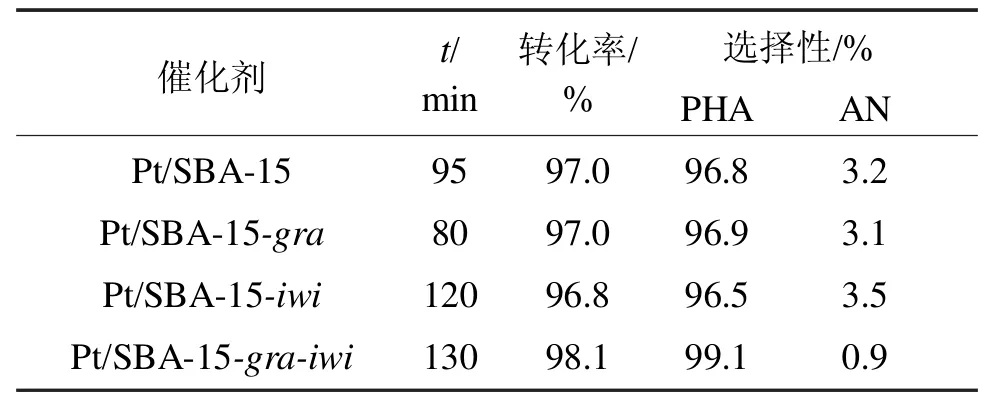
表2 4种Pt/SBA-15催化剂的NB催化加氢性能Tab 2 Nitrobenzene catalytic hydrogenation properties of four Pt/SBA-15 catalysts
3 结论
经嫁接法预处理SBA-15载体且通过浸渍法负载Pt催化剂,获得了1种在NB加氢合成PHA反应中具有高活性及高选择性Pt/SBA-15催化剂,实现了反应进行80min的时候,收率达到94%。该催化剂还可以应用于其他取代NB类化合物高选择性催化加氢合成N-芳基羟胺的反应中。
[1]Vyas P M,Roychowdhury S,Woster P M,et al.Reactive oxygen species generation and its role in the differential cytotoxicity of the arylhydroxylamine metabolites of sulfamethoxazole and dapsone in normal human epidermal keratinocytes[J].Biochemical Pharmacology,2005,70(2):275-286.
[2]Yadav J S,Reddy B V S,Sreedhar P.Three-Component One-Pot Synthesis ofα-Hydroxylamino Phosphonates using Ionic Liquids[J].Advanced Synthesis&Catalysis,2003,345(5):564-567.
[3]Niu D,Zhao K.Concerted Conjugate Addition of Nucleophiles to Alkenoates.Part I:Mechanism of N-Alkylhydroxylamine Additions[J].Journal of the American Chemical Society,1999, 121(11):2456-2459.
[4]ShiQ X,Lu RW,Jin K,et al.Ultrasound-promoted Highly Chemoselective Reduction of Aromatic Nitro Compounds to the Corresponding N-Arylhydroxylamines Using Zinc and HCOONH4in CH3CN[J].Chemistry Letters,2006,35(2):226-227.
[5]Li F,Cui J,Qian X,etal.A novel strategy for the preparation of arylhydroxylamines:chemoselective reduction of aromaticnitro compounds using bakers′yeast[J].Chem Commun,2004, 20:2338-2339.
[6]Li F,Cui J,Qian X,et al.Highly chemoselective reduction of aromatic nitro compounds to the corresponding hydroxylamines catalysed by plantcells from a grape(Vitis vinifera L.)[J].Chem Commun(Camb).2005,14:1901-1903.
[7]S.D Kushch,E N Izakovich,M L Khidekel,et al.Mechanism of catalytic hydrogenation of nitrobenzene in an aprotic medium in the presence of quinones[J].Russian Chemical Bulletin,1981,30(7):1201-1206.
[8]Kushch S D.Selective hydrogenation of nitrobenzene in aproticmedia[J].Russian ChemicalBulletin,1991,40(1):33-36.
[9]Takenaka Y,Kiyosu T,Choi JC,et al.Selective synthesis of N-arylhydroxylamines by the hydrogenation of nitroaromatics using supported platinum catalysts[J].The Royal Society of Chemistry,2009(9):1385-1390.
[10]江茂修,路春茂.固定床上硝基苯Pt/C催化加氢合成苯基羟胺探索研究[J].精细石油化工,1999(4):31-34.
[11]Freudenreich J,Stohrer J.Method for producing organic hydroxylamines:US,6211410[P].2001-04-03.
[12]Rylander P N,Karpenko I M,Pond G R.Selective hydrogenation of nitroaromatics to the corresponding N-arylhydroxylamine:US,3694509[P].1972-09-26.
[13]刘维桥,孙桂大.固体催化剂实用研究方法[M].北京:中国石化出版社,2001.
[14]Gregg SJ,Sing K SW.Adsorption,surface area,and porosity [M].London:Academic Press,1982:1-303.
[15]Meynen V,Beyers E,Cool P,et al.Post-synthesis deposition ofV-zeolitic nanoparticlesin SBA-15[J].Chemical Communications,2004(7):898-899.
[16]Zhao D,Huo Q,Feng J,et al.Nonionic triblock and star diblock copolymer and oligomeric surfactant syntheses of highly ordered,hydrothermally stable,mesoporous silica structures[J].Journal of the American Chemical Society, 1998,120(24):6024-6036.
[17]Gu J,Shi J,You G,et al.Incorporation of highly dispersed gold nanoparticles into the pore channels of mesoporous silica thin films and their ultrafast nonlinear optical response[J].Advanced Materials,2005,17(5):557-560.
[18]Winkler H,Birkner A,Hagen V,et al.Quantum-confined gallium nitride in MCM-41[J].Advanced Materials,1999,1 1(17):1444-1448.
[19]周志平,孔祥涛,盛维琛,等.复合材料PAA-PNIPA/APSSBA-15的制备及其药物缓释性能[J].江苏大学学报:自然科学版,2010,31(5):544-548.
[20]Yang C,Liu P,Ho Y,et al.Highly dispersed metal nanoparticles in functionalized SBA-15[J].Chemistry of Materials,2003,15(1):275-280.
[21]王尚弟,孙俊全.催化剂工程导论[M].北京:化学工业出版社,2001:53-58.

