胶原酶优化消化法对退变椎间盘纤维环细胞分离培养的作用
冯 旭 ,禹宝庆,刘 莉 ,李承 ,陈安民
(1.上海市浦东医院复旦大学附属浦东医院骨科、麻醉科,上海 201399;2.华中科技大学同济医学院附属同济医院矫形外科,湖北 武汉 430030)
胶原酶优化消化法对退变椎间盘纤维环细胞分离培养的作用
冯 旭1,禹宝庆1,刘 莉1,李承1,陈安民2
(1.上海市浦东医院复旦大学附属浦东医院骨科、麻醉科,上海 201399;2.华中科技大学同济医学院附属同济医院矫形外科,湖北 武汉 430030)
目的 通过观察不同浓度Ⅰ、Ⅱ型胶原酶对退变椎间盘纤维环组织消化效果,探讨适合于纤维环细胞分离培养的优化消化法。方法 收集16例退变椎间盘纤维环组织,Ⅰ、Ⅱ型胶原酶单独消化并在0.1%,0.05%,0.01%浓度下联合消化。消化4、8、16、24 h时倒置显微镜下计算纤维环细胞数,台盼蓝染色检查其活力,并观察其生长情况。结果 Ⅰ、Ⅱ型胶原酶联合消化细胞数多于单独消化细胞数。联合消化4、8 h时,细胞数随胶原酶消化浓度增加而增多,16、24 h时极低浓度组纤维环细胞数逐渐增多,细胞活力维持在较高水平。结论 极低浓度Ⅰ、Ⅱ型胶原酶优化消化法能节省酶量,对细胞损伤小,更适合纤维环细胞分离培养。
胶原酶;优化消化法;纤维环细胞;分离培养
酶消化法是分离椎间盘纤维环组织细胞的常 用方法,有报道采用链酶蛋白酶消化[1],但成本偏高。实验中常用胰蛋白酶和胶原酶分离消化椎间盘组织。胶原酶(Collaganase)属于基质金属蛋白酶家族,在一定的PH及温度下能溶解椎间盘纤维环组织。但在何种优化条件下充分发挥胶原酶的活性,对消化分离的纤维环细胞损伤更小,值得进一步探讨。本文采用I型、Ⅱ型胶原酶单独和联合消化分离纤维环细胞,在消化分离效果好的方式中,探讨在不同浓度下对纤维环细胞生物学行为的影响,观察其对纤维环细胞数、活力生长情况的影响,优化选择最佳浓度的酶消化方法,探讨更有利于纤维环细胞的培养方法。
1 材料与方法
1.1 一般资料
我院2010-12-2012-12收治的16例腰椎间盘突出症患者术中切除的椎间盘纤维环组织,男9例,女7例;年龄32~52岁,平均36.6岁;其中L4-510例,L5-S16例。
1.2 实验方法
1.2.1 试剂 采用胰蛋白酶、Ⅰ型和Ⅱ型胶原酶由DMEM/F12培养基配制。
1.2.2 取材 手术切除腰椎间盘突出症突出椎间盘髓核组织的同时,突出部位和毗邻髓核的部分纤维环常常被切除。无菌条件下取出纤维环取出后,立即置入4℃生理盐水中送实验室,在无菌操作台上用4℃ D-Hanks液冲洗2~3次以清除血液,超净工作台下将髓核与纤维环、纤维环交界区用眼科剪分离,剔除软骨和肉芽组织,分离出纤维环组织再放入装有D-Hanks液的培养皿中,用小剪刀将其剪碎成约1 mm3的组织块。
1.2.3 细胞分离 将无菌的纤维环组织碎块放入3倍体积的0.25%的胰蛋白酶液中,室温下消化20 min,胎牛血清中止消化。1000 rpm离心5 min,弃上清液,用DMEM/F12培养基洗涤2次。
1.2.4 实验分组 根据分组情况单独或联合加用Ⅰ型、Ⅱ型胶原酶进行消化,同时加入10%的胎牛血清。
1.2.4.1 不同类型胶原酶分组 观察Ⅰ型、Ⅱ型胶原酶对纤维环细胞的分离效果,0.25%胰蛋白酶消化20 min后,分别换成Ⅰ型、Ⅱ型胶原酶单独或Ⅰ型+Ⅱ型胶原酶联合继续消化,分别称为:Ⅰ组(0.2%Ⅰ型胶原酶)、Ⅱ组(0.2%Ⅱ型胶原酶)和Ⅲ组(0.1%Ⅰ型胶原酶+0.1%Ⅱ型胶原酶),观察各组消化酶的消化分离效果。
1.2.4.2 不同浓度胶原酶分组 探讨纤维环细胞分离的最适消化酶浓度,0.25%胰蛋白酶消化20 min后,分别换用浓度为0.1%(Ⅲa组,高浓度组)、0.05%(Ⅲb组,低浓度组)、0.01%(Ⅲc组,极低浓度组)的Ⅰ型+Ⅱ型胶原酶联合消化。
1.3 细胞计数与细胞活力测定 Ⅰ组、Ⅱ组、Ⅲ组,Ⅲa,Ⅲb,Ⅲc各组在 37℃消化后 4、8、16、24 h 各时间点进行细胞计数和细胞活力测定。
1.3.1 细胞计数方法 用平板计数器在相差显微镜下计数,观察细胞的分离和生长情况,计数方法参照《体外培养的原理与技术》[2]。
1.3.2 细胞活力测定方法 细胞分离过程中通过台盼蓝染色计算细胞存活率判断细胞活力。步骤如下:将细胞置于等容积的DMEM/F12培养基和0.4%台盼蓝溶液中染色,用平板计数器显微镜下观察并记录细胞被染色及未被染色的数量,蓝染细胞为死亡细胞,按未被蓝染细胞所占细胞总数的百分比即可初步得到细胞活力的数据。计算细胞存活率(染色纤维环细胞数/高倍视野纤维环细胞总数×100%)。
1.4 细胞培养 在纤维环细胞消化后4、24 h分别经1000 rpm离心5 min,弃去上清液,加入DMEM/F12培养基,经孔径为74 μm的无菌尼龙滤网过滤,计数并按1×104 ml密度接种于含10%胎牛血清和DMEM/F12培养基的一次性培养瓶中。各组在胶原酶消化的同时即加入10%胎牛血清,37℃,5%CO2的培养箱中培养,每3 d换液1次。细胞融合80%时用胰蛋白酶消化并进行细胞传代。
1.4.1 体外培养的纤维环细胞纯化 培养过程中,采用“反复贴壁法”即将碎块经胶原酶消化后,加入DMEM/F12培养液,分别接种至3个培养皿中,第1皿接种5 min后,轻轻倾斜吸出培养液,再接种至第2皿中,同法处理,最后接种第3皿。
1.5 统计学分析 所有数据均以x±s表示,用单因素方差分析进行处理。数据表中*表示P<0.05;#P<0.01。
2 结果
2.1 纤维环细胞计数 在37℃消化4、8、16 h、24 h后各组纤维环细胞计数结果(见表1)相同胶原酶浓度和相同消化时间点比较,Ⅲ组细胞数多于Ⅰ、Ⅱ组。在Ⅲ组相同消化时间点比较,消化4、8 h时,细胞数Ⅲa>Ⅲb>Ⅲc,16 hⅢc细胞数明显增多,Ⅲa,Ⅲb轻度增多,24 h时Ⅲa,Ⅲb组纤维环细胞减少,Ⅰc组细胞活力较其他两组高。
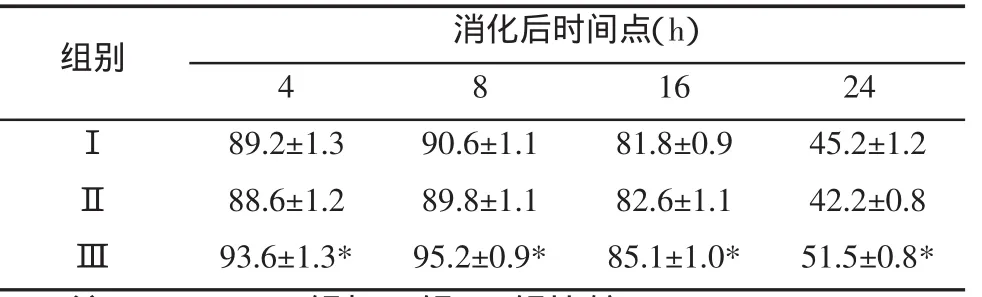
表1 Ⅰ型、Ⅱ型胶原酶单独或联合消化后不同时间点纤维环细胞数(×104/ml)
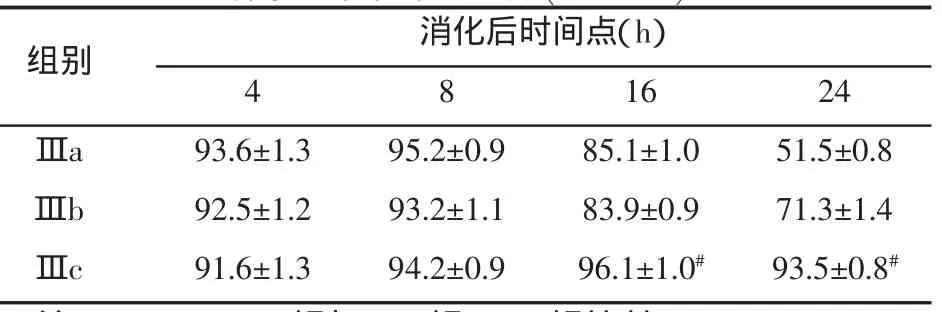
表2 不同浓度Ⅰ+Ⅱ型胶原酶联合消化后不同时间点纤维环细胞数(×104/ml)
2.2 细胞活力测定
Ⅰ型、Ⅱ型、Ⅰ+Ⅱ型胶原酶消化后各时间点对纤维环细胞存活率的影响无统计学差异(P>0.05);Ⅰ+Ⅱ型胶原酶联合消化不同浓度组(Ⅲa,Ⅲb,Ⅲc)消化纤维环细胞后各时间点细胞存活率计算结果:不同分离方法的细胞存活率在接种培养后24 h与接种时相比,均不同程度降低,其中Ⅲa组细胞存活率降低幅度最大,表明其毒性较大,在消化24 h后Ⅲc组和Ⅲa组、Ⅲc组和Ⅲb组间均有显著性差异(P<0.01)。
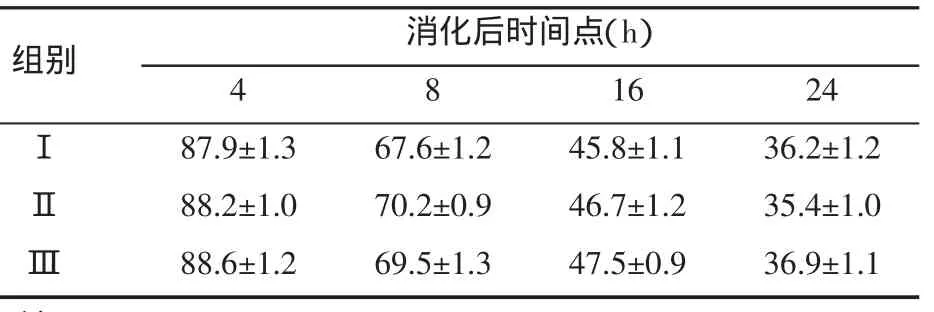
表3 Ⅰ型、Ⅱ型、Ⅰ+Ⅱ型胶原酶消化后不同时间点纤维环细胞存活率(%)
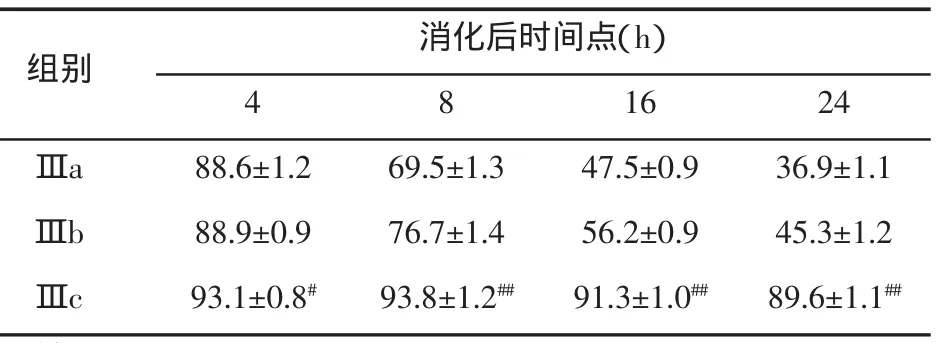
表4 不同浓度Ⅰ+Ⅱ型胶原酶联合消化后不同时间点纤维环细胞存活率(%)
2.3 形态学观察 Ⅲa,Ⅲb两组贴壁速度相对缓慢,72 h后Ⅲc组细胞贴壁多于Ⅲa,Ⅲb组。细胞呈短梭形,轮廓清楚,细胞核呈圆形(见图1)。2周后细胞贴壁数目明显增多,但细胞生长及分裂增殖慢,大约24 d左右,细胞长满瓶壁,即进行传代。传代后细胞同样需要6 d左右贴壁,且生长较传代前稍慢,呈现相对稳定的生长状态。

图1 纤维环细胞原代培养3 d贴壁生长
3 讨论
椎间盘纤维环细胞由间充质细胞分化而来,是一种纤维环软骨细胞,常被描述为纺锤形态的成纤维样细胞,其形态常根据局部的力学环境改变而发生变化[3,4]。体内椎间盘纤维环细胞表达Ⅰ、Ⅱ、Ⅴ型胶原和蛋白聚糖亚单位PGS等成分[5]。除了培养基、pH值等影响因素外,其中取材、酶消化法对纤维环原代细胞培养存在重要影响[6]。本实验培养基采用F12/DMEM加10%胎牛血清,每3 d换液一次,以保证细胞有良好的生长环境。贴壁后,细胞呈梭形,传代后细胞有向梭形演变的趋势,体现了细胞有成纤维化的趋势。
胶原酶是从溶组织梭状细胞芽孢杆菌提取制备的,能特异性水解胶原蛋白的三维螺旋结构,在一定的pH及温度下能溶解椎间盘纤维环组织。主要用于消化骨、肾等组织。纤维环组织的基质成分主要是胶原蛋白、蛋白多糖和弹性蛋白等成分。由于粗酶含有各种不同的蛋白酶,也会消化细胞表面的蛋白,所以对细胞有一定的损伤。
由实验结果可知,在分离纤维环细胞时,Ⅰ型与Ⅱ型胶原酶联合消化比单独用Ⅰ型、Ⅱ型胶原酶的酶活性更强。细胞活力的测定说明刚分离的细胞活力较强,培养一段时间后活力最强,传代培养后活力逐渐减弱,符合细胞的生长周期。
高浓度消化酶对细胞数和细胞活性产生一定影响,实验证实,极低浓度的Ⅰ、Ⅱ型胶原酶联合消化后16 h的纤维环细胞数和细胞活力更高,而高浓度和中等浓度的胶原酶消化后的细胞数开始减少,活力显著降低,可能是高浓度的消化酶对细胞的损伤作用,甚至导致细胞的死亡。
人退变椎间盘细胞的贴壁时间为5~7 d甚至更长,对数生长期短,细胞生长周期较长,说明退变的椎间盘细胞的生长活力低下。传代后纤维环细胞生长相对较快,约24 d可以传1代,但当传至第2代时其细胞内空泡增多,分泌颗粒增多,细胞开始呈现衰老迹象。在Ⅰ型与Ⅱ型胶原酶联合消化中,极低浓度(0.01%)更适合于消化纤维环细胞。一方面,胶原酶在极低浓度时消化力较弱,克服了酶活性过强对纤维环细胞活性的影响,对细胞的损伤程度相对较小,这有助于后续细胞培养中纤维环细胞活力的恢复和提高;另一方面,极低浓度胶原酶消化法操作简单,省略了第一次消化时除去消化酶时离心等步骤。由于胶原酶的效价不象胰蛋白酶那样受胎牛血清的影响,这就允许在含胎牛血清的培养基培养细胞的同时,加入胶原酶同步消化纤维环组织,而极低浓度的胶原酶可在培养的过程中自然消耗掉。
本实验报告的极低浓度胶原酶消化法,具有操作方法简单、获得细胞数量多且纯度高的优点。极低浓度消化酶对纤维环细胞造成损伤程度较小,有利于其成活及维持较活跃的功能。
[1] Shingo M,Shoichi K.Changes with age in proteoglycan synthesis in cells cultured in vitro from the inner and outer rabbit annulus fibrosus:responses to interleukin-1 and interleukin-1 receptor antagonist protein[J].Spine,2000,25(2):166.
[2] 司徒镇强,吴军正.细胞培养[M].西安:世界图书出版公司,2001.186-187.
[3] Roberts S,Evans H,Trivedi J,et al.Histology and pathology of the human intervertebral disc[J].J Bone Joint Surg(Am),2006,88(2)10-14.
[4] Clare C G,Eugene Y S,Sebastien B G,et al.Challenges and strategies in the repair of ruptured annulus fibrosus[J].Eur Cell Mater,2013,25(1):1-21.
[5] Henriksson H,Thornemo M,Karlsson C,et al.Identification of cell proliferation zones,progenitor cells and a potential stem cell niche in the intervertebral disc region:a study in four species[J].Spine,2009,34(10):2278-2287.
[6] 潘勇,周跃,郝勇,等.不同接种方法构建组织工程化椎间盘纤维环细胞支架复合体的对比研究[J].颈腰痛杂志,2009,30(1):3-7.
Effection of optimized digestion of collagenase on the culture of annulus fibrosus cells of degenerated intervetebral disc.
FENG Xu,YU Bao-qing,LIU Li,et al.
(1.Department of Orthopedics、Anesthesia,Pudong Hospital of Shanghai,Shanghai 201399,China;2.Department of Orthopedics Surgery,The Tongji hospital HuaZhong University of Science and Technology TongJi Hospital.)
ObjectiveTo explore the optimized digestive method of collagenase to annulus fibrosus(AF)cells by observing the digestive effects of type I,II collagenase in different concentrations on AF of degenerated intervetebral disc.Methods16 AF samples from human herniated intervertebral disc were collected and digested by type I,II collagenase individually or combined in different concentration.The AF cells were counted with inverted microscope and their activities were checked with trypan blue staining at 4 h、8 h、16 h、24 h after digestion.The growth of AF cells was also observed.ResultsThe amount of AF cells with combined collagenases was more than that seperatedly in the identical concentration.With combined collagenases in 4,8 hours,the higher concentration of collagenases,the more AF cells.The amount of cells in extremely low concentration of collagenases increased at 16 h、24 h,and their activities kept in higher level.ConclusionThe optimized digestion at extremely low concentration of typeⅠand Ⅱcollagenase combination could save enzyme,and is less harmful to AF cells,which is more adapted to separate and culture of AF cells.
collagenase;optimized digestion;annulus fibrosus cell;seperation and culture
Q556.9 文献辨识号:A
1005-7234(2013)05-0361-04
10.3969/j.issn.1005-7234.2013.05.004
2013-07-02;
2013-07-30
冯旭(1971-),男,湖北籍,副主任医师,博士
研究方向:脊柱外科
禹宝庆
电 话:18918790021
电子邮箱:fengalectj@163.com
·临床论著·

