食用油烹饪过程中苯并[a]芘含量的变化
金文娟,程 鹏,胡志雄,齐玉堂,,谢 明,张维农,
(1.武汉工业学院食品科学与工程学院,湖北武汉430023;2.武汉工业学院油脂及植物蛋白工程技术研发中心,湖北武汉430023;3.浙江泰谷农业科技有限公司,浙江杭州310012)
多环芳烃类化合物主要是指2个以上苯环稠合在一起的芳烃化合物,由煤炭、石油、木柴等不完全燃烧或工业中利用这些燃料进行热加工处理时产生的一种化合物,存在于大气烟尘、空气、水、土壤以及烟熏食物中。目前已发现200多种多环芳烃化合物或其衍生物具有致癌性[1]。
苯并[a]芘是多环芳烃中毒性最大的一种强致癌物,缩写为:B(a)P。苯并[a]芘可诱发皮肤、肺和消化道癌变。高剂量时甚至能够引起免疫抑制,对健康造成潜在的威胁。
目前检测苯并[a]芘的方法主要有[2]:荧光分光光度法、薄层层析法、高效液相色谱法和气相色谱—质谱联用法。其中高效液相色谱法因简便快速,安全性好,灵敏度高,线性范围宽,精确度高而被广泛采纳。
据报道,食用油加热到270℃时产生的油烟中,含有苯并[a]芘等化合物,吸入人体后可以诱发肿瘤和导致细胞染色体的损失;而食用油如果加热温度低于240℃时,其损害作用较弱。也就是说,温度越高,加热时间越长,苯并[a]芘产生得越多[3]。国家标准GB2716-2005《食用植物油卫生标准》规定,食用植物油类产品中苯并[a]芘的安全限量为不超过10 μg/kg。欧盟208/2005号文件规定食用油脂中苯并[a]芘的最大限量为 2 μg/kg[4]。
因此本文欲在建立简单易行的高效液相色谱检测法的基础上,选用制备工艺不同的四种油脂,简单模拟烹饪条件,对未加热,高温加热和加入食盐加热的食用油进行检测,从而得出在三种不同条件下食用油中苯并[a]芘含量的变化规律。研究结果可用于指导食用油在烹饪过程中采用合适的方式以减少苯并[a]芘的产生;对于油脂加工过程中采用合适的工艺参数避免或减少苯并[a]芘的生成亦有参考价值。
1 实验材料及方法
1.1 实验原材料及试剂
实验原材料:浸出大豆油、热榨茶叶籽油(由浙江泰谷农业科技有限公司提供)、特级初榨橄榄油(超市购买)、冷榨茶籽油(采用武汉新概念农业机械设备制造有限公司双螺杆冷榨机制备)。
实验试剂:苯并芘标品(纯度≥96%);甲苯(天津市科密欧化学试剂有限公司,色谱纯);四氢呋喃(天津市科密欧化学试剂有限公司,色谱纯);乙腈(天津市科密欧化学试剂有限公司,色谱纯)。
1.2 实验仪器
高效液相色谱仪:配有Waters 2475荧光检测器、Waters 1525二元泵、Empower色谱工作站(美国Waters公司产品),DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器厂)。
1.3 苯并[a]芘的检测方法
本实验主要从流动相、流速、检测器条件等几个方面来进行色谱条件的优化。反相色谱的流动相常见的是甲醇、乙腈、四氢呋喃,但是综合考虑溶剂的黏度、紫外吸收强弱以及样品的相互作用、使用方便等条件,得出乙腈最适合;本实验通过降低流速来提高分离度,但是会使色谱峰变宽,柱效明显下降,延长了分析时间。根据文献的报道[5],选择乙腈和水作为流动相,激发波长384 nm,发射波长406 nm。并根据实验室条件,对检测方法进行了适当的调整,具体如下。
1.3.1 色谱条件
(a)色谱柱:LiChrospherⓇPAH(5 μm),4.0 mm×250 mm。
(b)进样量:20 μL。
(c)流动相:乙腈∶水 =95∶5(体积比)。
(d)流速:1.0 mL/min。
1.3.2 苯并[a]芘标准贮备溶液
准确称取12.5 mg苯并[a]芘于25 mL容量瓶中,用甲苯溶解,定容。此溶液浓度0.528 mg/mL。
1.3.3 标准溶液
用苯并[a]芘标准贮备液,分别配制浓度为0.001056 μg/mL,0.01056 μg/mL,0.1056 μg/mL,0.528 μg/mL,1.056 μg/mL,2.112 μg/mL 的标准溶液。
1.3.4 油样的处理
取10 mL容量瓶准确称取2.5 g样品,加入5 mL四氢呋喃后,用乙腈定容,摇匀后过0.2 μm有机滤膜,按照选定的色谱条件进样分析。
1.4 样品加热处理
浸出大豆油、特级初榨橄榄油、热榨茶叶籽油、冷榨茶籽油4种食用油,第一批处理方法是将每种食用油取少量在270℃下加热1 h;第二批处理方法是将每种食用油取少量,加入油重1%的NaCl(配成20%的水溶液)并在270℃下加热1 h。由此未加热、加热、加盐加热的处理方法共得到了12组样品。
2 结果与分析
2.1 标准曲线的绘制
将标准溶液经有机滤膜过滤后,进样检测,进样量为20 μL。以苯并[a]芘浓度为横坐标,对应峰面积为纵坐标,绘制校正曲线。实验结果表明,苯并[a]芘含量与峰面积的线性范围为0.001056—2.112 μg/mL;回归方程为 y=1.08465 ×10-9x,相关系数为0.99967。标准曲线见图1。
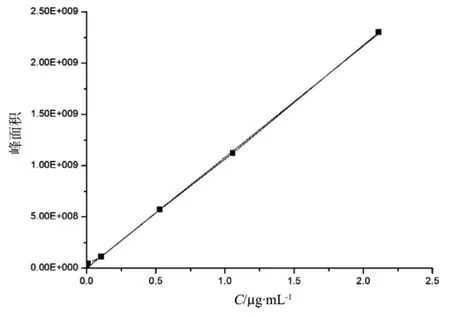
图1 苯并[a]芘标准曲线
由相关系数可知,苯并[a]芘在0.001056—2.112 μg/mL的浓度范围内具有良好的线性关系。
2.2 加样回收实验
取经过1.3.4处理过的油样,分别加入0.1056 μg/mL、1.056 μg/mL 的苯并[a]芘标准溶液 0.1 mL、0.3 mL、0.5 mL,定容到 2 mL,经有机滤膜过滤后,进样检测,进样量为20 μL。根据峰面积绘制校正曲线,如图2所示。
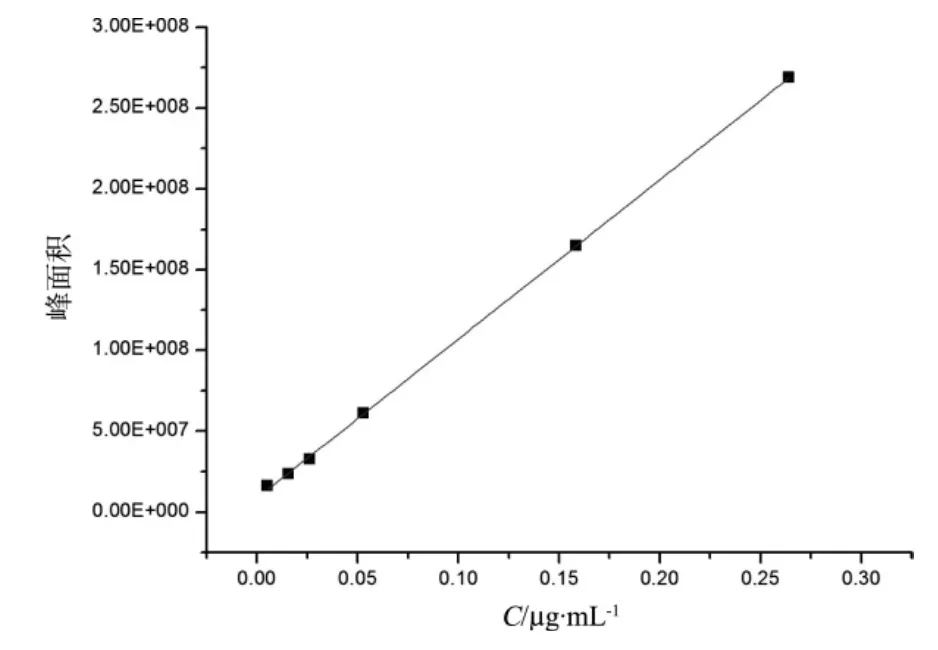
图2 加样回收校正曲线
与标准曲线的斜率相比较,可知方法的精确度在一定程度满足实验要求。
2.3 苯并[a]芘HPLC检测图谱
由图3可以看到,苯并[a]芘标品在11—12 min会出现色谱峰,以此作为检测油样中苯并[a]芘含量的依据。
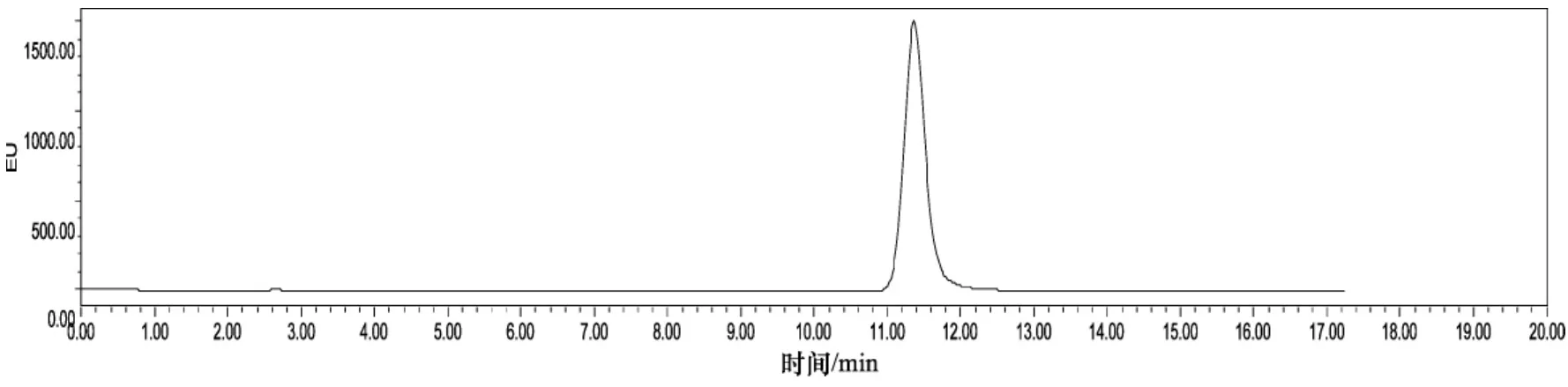
图3 苯并[a]芘标品荧光检测图
图4—图6为浸出大豆油样品中苯并[a]芘的HPLC分析图谱。

图4 未加热浸出大豆油中苯并[a]芘的HPLC分析图

图5 经270℃高温处理浸出大豆油中苯并[a]芘的HPLC分析图
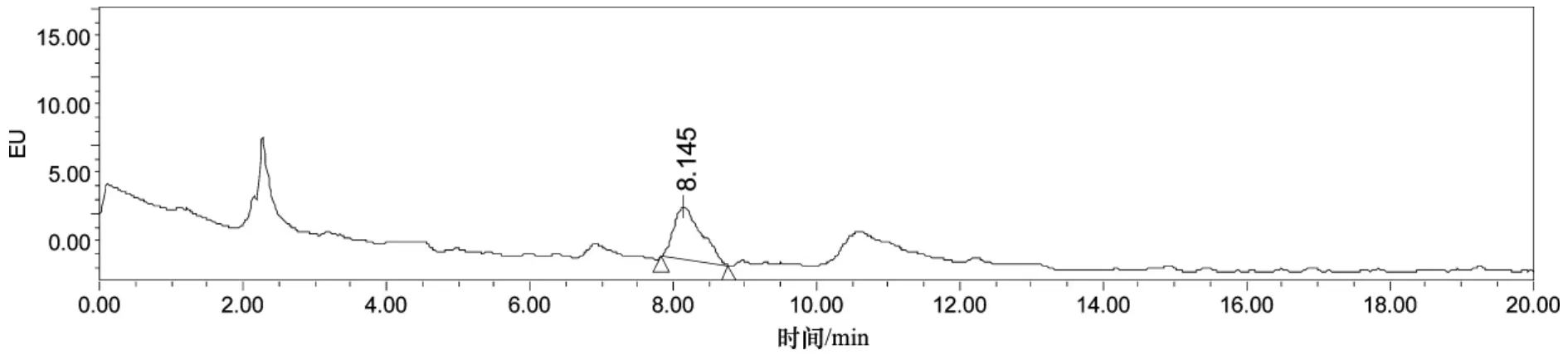
图6 加入食盐水并经270℃加热处理浸出大豆油中苯并[a]芘的HPLC分析图
通过向样品中加入苯并[a]芘标样发现色谱峰增大可知,8—10 min所出的峰即是苯并[a]芘的峰。本实验油样前处理采用四氢呋喃溶解,乙腈定容,简单易行。样品前处理过程中没有进行中性氧化铝过柱,除油和净化的效果稍差,从而导致保留时间的改变,但只要对色谱条件进行很好的优化,使目标物与杂峰在色谱图上得以分离就不会影响到检测的准确性。
2.4 不同油样苯并[a]芘含量的测定结果
2.4.1 未加热处理油样中苯并[a]芘含量的测定结果
根据图7所示的检测结果可以看出,未加热处理油样中均含有少量的苯并[a]芘,但都在我国食用植物油类产品中苯并[a]芘的安全限量之内。有研究报道,油料作物易受到大气污染,从而引发苯并[a]芘不断向食用油迁移,因此大气污染是食用油中苯并[a]芘的来源之一;其次,油料干燥过程中与热解燃气直接接触,从而引发苯并[a]芘向植物油迁移;再次,油料在机械收获、运输、加工等过程中因接触污染物而受到苯并[a]芘污染,从而引发苯并[a]芘向食用油迁移;Scimko等[6]报道,植物油用聚乙烯材料包装贮藏时,植物油中PAHs与贮藏时间的平方根成正比;Grob等[7]报道,油菜籽用黄麻袋包装运输,油菜籽中PAHs含量逐渐升高,其压榨油中PAHs含量最高达到194 mg/kg。此外,浸出溶剂中残留的芳烃类物质,也是造成食用油中苯并[a]芘污染的原因之一。2010年6月1日起,GB16629-2008《植物油抽提溶剂》新标准强制实施,规定苯质量分数不大于0.1%。我国食用油抽提溶剂中存在潜在的高苯并[a]芘污染风险。但从我们的实验结果看,油中苯并[a]芘的含量主要与原料的污染有关,制备工艺对其影响不大,因为采用溶剂浸出的大豆油中的苯并[a]芘含量并不高。

图7 未加热油样中苯并[a]芘含量的测定结果
2.4.2 高温加热油样中以及高温加热加盐油样中苯并[a]芘含量的测定结果
由表1可知,与未加热油样相比,大部分处理油样测得的苯并[a]芘含量较低,但并不意味着经处理后油中苯并[a]芘含量减少了。同时,加热油样与加热加盐油样相比较,苯并[a]芘含量有所增加。据相关文献报道,食用油加热到270℃时,产生的油烟中含有苯并[a]芘等化合物,吸入人体可诱发肿瘤和导致细胞染色体的损害;高温加热时,油脂易发生聚合反应,产生杂质,从而吸附苯并[a]芘。同理,因为加入食盐水,在高温加热的情况下,会有食盐颗粒析出,吸附苯并[a]芘,也会对实验结果产生影响。并且,日光和荧光都使其发生光氧化作用,这些均会影响苯并[a]芘的检测结果,但若想获得准确的信息,必须对植物油做进一步的研究,找出根源,从而使得油中苯并[a]芘含量小于国家标准。在模拟家庭烹饪的条件下,我们可以知道煎炸时所用油温越高,产生的苯并[a]芘也越多,因此,在家庭烹饪的情况下要注意控制油温,并且不要反复使用食用油。

表1 高温加热油样以及高温加热加盐油样中苯并[a]芘含量的测定结果 /μg·kg-1
3 结论
本实验采用反相高效液相色谱法测定食用油中苯并[a]芘含量,通过模拟家庭烹饪的条件,检测四种不同油脂在不同的处理条件下苯并[a]芘的含量,可得知,煎炸油温越高,苯并[a]芘的含量越高,且食盐亦会在一定程度上增加苯并[a]芘的含量。对烹饪条件下苯并[a]芘含量变化规律进行探索,可以指导人们在日常饮食中正确使用食用油,从而减少苯并[a]芘的生成,减弱苯并[a]芘对人们健康带来的恶劣影响。
[1] 杨美娟.浅析3,4-苯并芘的危害及其预防[J].实验研究,2011(10):71-72.
[2] 王丹,曹维强,王静.食品安全隐患——苯并(a)芘的研究进展[J].食品研究与开发,2006,1(27):132-135.
[3] 王民.烹炸时油和油炸品中苯并(a)芘及脂肪酸含量变化的实验研究[J].中国卫生检验杂质,1997,7(1):17-19.
[4] GB 2716-2005,食用植物油卫生标准[S].
[5] 吴海智,周丛,袁烈江,等.高效液相色谱法快速测定植物油中苯并芘的研究[J].安徽农业科学.2011,39(10):6075-6076.
[6] Scimko P, Khunova V, Simon P, et al.Kinetics of sunflower oil conta mination with polycyclie aromatic hydrocarbons from conta minated recycled low density polyethylene film[J].Int J Food Sci Technol,1995:30:807-815.
[7] Grob K,Biederman M,Caramaschi A,et al.LC-GC analysis of the aromatics in a mineral oil fraction:batching oil for jute bags[J].J High Reso Chromatogr,1991,14:33-39.

