慢性胰腺炎患者胰管支架堵塞及其相关因素分析
王新涛 邹多武 李兆申 廖专 赖晓伟
·论著·
慢性胰腺炎患者胰管支架堵塞及其相关因素分析
王新涛 邹多武 李兆申 廖专 赖晓伟
目的分析慢性胰腺炎(chronic panreatitis,CP)患者胰管支架的堵塞率及影响支架通畅的相关因素。方法收集2006年11月至2010年1月间64例CP患者经内镜下取出的胰管支架77根,应用自制的支架通畅率检测装置,在10 cm水柱压力下,测15 s,连测4次。使用Kaplan-Meier统计方法对风险因子和支架堵塞的相关性进行单变量分析研究。通过Cox regression生存分析法进行风险因子对于支架堵塞风险影响的多因素分析。结果64例CP患者入组,其中男性43例,女性21例,年龄4~80岁,平均38岁。支架置入时间为26~759 d,平均263 d;支架直径5~10 F,平均8F。10 cm水柱压力下支架总堵塞率为67.5%(52/77)。90、180、360、540 d的通畅率分别为96.1%(74/77)、72.7%(56/77)、58.4%(45/77)和35.1%(27/77)。通过Cox回归分析,支架直径≥8.5F是支架堵塞的唯一的独立风险因素。结论支架放置180 d仍有较高的通畅率,明显低于国外相同研究97%的堵塞率;选择≥8.5 F的胰管支架更容易发生堵塞现象。
胰腺炎,慢性; 胰管; 支架; 回顾性研究; 支架堵塞率
内镜下胰管支架植入治疗慢性胰腺炎(CP),尤其是对于胰管结石无法取出以及胰管狭窄患者具有良好的短、中、长期临床效果。但围绕内镜治疗的并发症,如支架移位、支架短期内的堵塞、内镜胰胆管逆行造影(ERCP)术后急性胰腺炎以及比较严重的胰管损伤、胰腺脓肿等尚有争议。目前只有2个前瞻性研究[1-2]关注胰管支架的堵塞率。 本研究回顾分析77根胰管支架的治疗状况,总结CP患者胰管支架的堵塞发生率及导致其发生的危险因素。
资料与方法
一、研究对象及记录项目
收集2006年11月至2010年1月间符合M-ANNHEIM诊断标准[3]且在我院住院期间行ERCP下胰腺导管塑料支架置入治疗的CP患者64例。采用相同的随访表记录患者年龄、性别、家庭住址、联系电话、CP确诊时间;是否吸烟、饮酒、病情是否影响工作、支架置入时间、是否长期规律口服胰酶制剂、是否口服止痛药以及疼痛评分;血常规、肝功能、CEA、CA19-9等实验室检查结果。疼痛评分主要包括:(1)腹痛的频率:每天都有持续性腹痛为100 pts,每周1次以上为75 pts,每月1次以上为50 pts,无明显腹痛为0;(2)疼痛剧烈程度(izbicki pain score):从0 至100 pts;(3)是否需要镇痛药物:1周使用1次以上阿片类止痛药为100 pts,1周1次阿片类止痛药为75 pts,1周使用1次以上非类固醇类(NSAIDs)止痛药为75 pts,1周1次NSAIDs止痛药为50 pts,1月使用1次以上阿片类或NSAIDs止痛药为50 pts,1年使用1次以上阿片类或NSAIDs止痛药为25 pts,无需规律口服镇痛药物为0。
二、支架取出及检测
支架取出的适应证:(1)支架置入后出现反复发作的腹痛者;(2)支架置入后出现新发的胰腺假性囊肿或者出现不适合支架放置的CP并发症等;(3)部分患者支架3个月定期更换。支架通过十二指肠镜使用圈套器仔细取出。
支架取出时应避免损坏支架侧翼以及前端,若支架有明显损坏、扭曲以及折断的,则该支架不纳入本研究中。取出的支架先用肉眼观察有无堵塞及堵塞部位(如支架侧翼、支架十二指肠端等),并立即用自制的检测装置(图1)检查支架是否通畅。如无法立即检测,则将支架置于8℃冰箱恒温保存,但保存时间不超过12 h。
正常胰管压力是7~16 mmHg(1 mmHg=0.133 kPa),相当于9~22 cm水柱,因此检测压力为10 cm水柱,测15 s,连测4次。有水流自胰管支架十二指肠端或侧翼流出者为通畅,无水流者为堵塞。
三、统计方法
研究的主要终点是支架的通畅时间,支架堵塞为研究的终止事件。使用Kaplan-Meier统计方法对风险因子和支架堵塞的相关性进行单变量分析研究。通过Cox regression生存分析法进行风险因子对于支架堵塞风险影响的多因素分析。所有分析均采用SAS 9.0版本统计软件包,P<0.05为差异有统计学意义。

图1 胰管支架通畅率的检测装置
一、患者基本资料
64例CP患者入组,其中男性43例,女性21例,年龄4~80岁,平均38岁。患者饮食规律59例(92.1%);正常工作58例(90.6%);并发糖尿病12例(18.8%);伴脂肪泻5例(7.8%);支架置入期间有饮酒史17例(26.6%),有吸烟史15例(23.4%);根据剑桥分级,38例(59.4%)有重度的胰管形态改变,22例(34.4%)有中度的胰管形态改变, 1例(1.6%)有轻度的胰管改变,3例(4.7%)无明显胰管的形态改变。
二、支架堵塞的单因素分析
共收集胰管支架77根,其中11根5F支架,21根7F支架,25根8.5F支架,20根10F支架,支架长3~12 cm,平均6.3 cm,支架置入时间26~759 d,平均263 d。肉眼见23根支架的十二指肠出口端堵塞,29根支架的侧翼侧孔处堵塞,支架胰腺端未见堵塞。10 cm水柱压力下总堵塞率达67.5%(52/77),90、180、360、540 d的通畅率分别为96.1%(74/77)、72.7%(56/77)、58.4%(45/77)和35.1%(27/77)。肉眼未见支架堵塞物被水流冲出。用Kaplan-Meier生存率计算法统计的支架堵塞的单变量风险因素见表1。随着支架置入时间的延长,堵塞率逐渐升高,但是临床症状以及实验室检查与支架堵塞无明显关联。
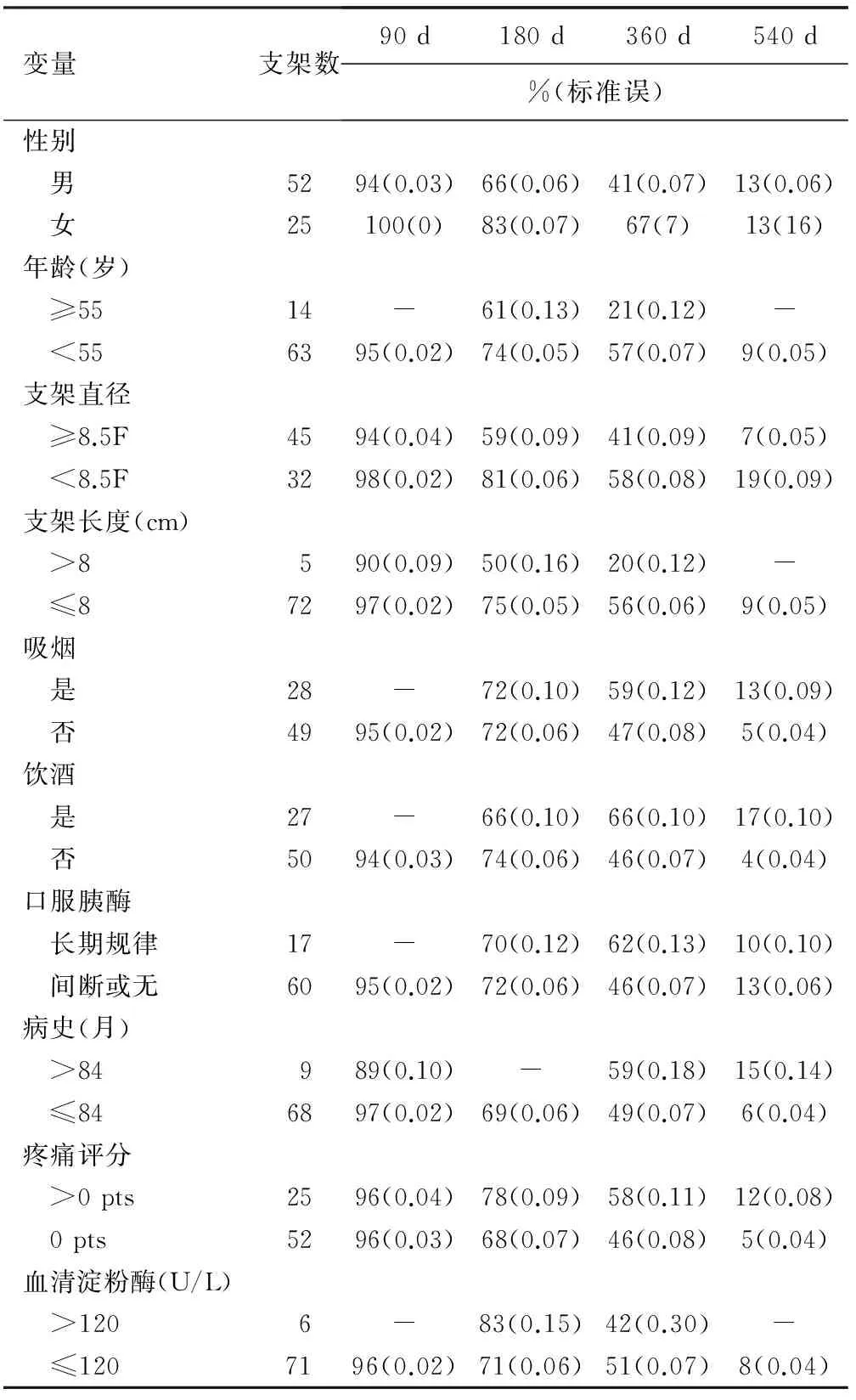
表1 不同时间段胰管支架通畅率
三、支架堵塞的多因素分析
通过Cox回归分析,支架直径≥8.5F被认为是支架堵塞的唯一的独立风险因素(表2)。

表2 支架堵塞多因素分析
讨 论
CP患者由于胰腺实质慢性炎症改变,导致胰腺解剖形态改变,造成胰管梗阻、胰管内压力增加或胰腺周围神经炎症等,这些因素共同作用导致腹痛[4-11],这一结论成为内镜下胰管支架治疗CP的理论基础。内镜介入治疗由于其低侵入性而成为了一种被广泛接受的治疗手段,但对其并发症、长期疗效和风险研究较少。为了尽量减少支架置入相关并发症的发生以及降低患者的ERCP费用,应该选择最佳的支架体内放置时间[12-13]。考虑到这一点,采取一定的标准,预测支架堵塞时间,针对不同患者的胰管支架取出或置换时间采取个体化治疗就非常有意义。
本实验结果显示,支架总堵塞率为67.5%,6个月内支架的通畅率相对较高,为72.7%,可以达到较好地引流作用,起到了良好的临床治疗效果。但随着置入时间的延长,支架堵塞的概率增加,1年半时的通畅率降至35.1%。根据Hagen-Poiseuille定律,流体在水平圆管中作层流运动时,流动阻力与管子半径的4次方成反比,与管子的长度和粘滞系数成正比;Bernoulli′s方程告诉我们,流体总是从高压处(支架胰腺端)向低压处(支架十二指肠端)流动,压力差越大,流体流动越快。随着支架直径的增加,支架置入后支架两端压力差就减小,胰液在支架内的流动速率逐渐降低,这也许是导致支架堵塞的一个重要因素。本结果显示,支架直径≥8.5F是支架堵塞的唯一的独立风险因素,所以我们认为,选择≥8.5F的胰管支架更容易发生堵塞现象。
Farnbacher等[2]的研究显示,胰管支架置入超过3个月,堵塞率高达97%。本组结果显示,支架置入3个月内通畅率超过90%,6个月内仍有70%以上的通畅率,明显高于国外研究报道,至于其中差别,仍需进一步对照研究。本组胰管支架置入后的6个月内有较高的通畅率,支架放置时间最长达2年多,因此,在没有明确的取支架适应证时不一定需要3个月定期更换。国外研究[2]指出,支架直径 (≥8.5F)是支架堵塞的独立风险因素,本实验结果显示,支架直径 (≥8.5F)是支架堵塞的唯一的独立风险因素,与上述文献报道结果一致。但国外研究同时指出女性患者、支架长度>8 cm及患者规律、长期口服胰酶补充制剂是支架堵塞另外3个独立风险因素。而本研究的结果与其不同,没有发现这3个因素与胰管堵塞的相关性,尚需要更多的前瞻性大样本量研究证实。
[1] Ikenberry SO,Sherman S,Hawes RH,et al.The occlusion rate of pancreatic stents.Gastrointest Endosc,1994,40:611-613.
[2] Farnbacher MJ,Radespiel-Troger M,Konig MD,et al.Pancreatic endoprostheses in chronic pancreatitis:criteria to predict stent occlusion.Gastrointest Endosc,2006,63:60-66.
[3] Schneider A,Lohr JM,Singer MV.The M-ANNHEIM classification of chronic pancreatitis:introduction of a unifying classification system based on a review of previous classifications of disease.J Gastroenterol,2007,42:101-119.
[4] Ammann RW,Akovbiantz A,Largiader F,et al.Course and outcome of chronic pancreatitis.Longitudinal study of a mixed medical-surgical series of 245 patients.Gastroenterology,1984,86:820-828.
[5] Bockmann DE,Büchler M,Malfertheimer P,et al.Analysis of nerves in chronic pancreatitis.Gastroenterology,1988,94:1459-1469.
[6] Di Sebastiano P,Di Mola FF,Di Febbo C,et al.Expression of interleukin 8 (IL-8) and substance P in human chronic pancreatitis.Gut,2000,47:423-428.
[7] Widdison AL,Alvarez C,Karanjia ND,et al.Experimental evidence of beneficial effects of ductal decompression in chronic pancreatitis.Endoscopy,1991,23:151-154.
[8] Conwell DL.Motion-pancreatic endoscopy is useful for the pain of chronic pancreatitis: arguments against the motion.Can J Gastroenterol,2003,17:61-63.
[9] Di Sebastiano P,Friess H,Di Mola FF,et al.Mechanisms of pain in chronic pancreatitis.Ann Ital Chir,2000,71:11-16.
[10] Karanjia ND,Widdison AL,Leung F,et al.Compartment syndrome in experimental chronic obstructive pancreatitis:effect of decompressing the main pancreatic duct.Br J Surg,1994,81:259-264.
[11] Lewis MP,Lo SK,Reber PU,et al.Endoscopic measurement of pancreatic tissue perfusion in patients with chronic pancreatitis and control patients.Gastrointest Endosc,2000,51:195-199.
[12] Kozarek RA.Pancreatic stents can induce ductal changes consistent with chronic pancreatitis.Gastrointest Endosc,1990,36:93-95.
[13] Smith MT,Sherman S,Ikenberry SO,et al.Alterations in pancreatic ductal morphology following polyethylene pancreatic stent therapy.Gastrointest Endosc,1996,44:268-275.
2010-02-27)
(本文编辑:屠振兴)
Riskfactorsofstentocclusioninchronicpancreatitis
WANGXin-tao,ZOUDuo-wu,LIZhao-shen,LIAOZhuan,LAIXiao-wei.
DepartmentofGastroenterology,ChanghaiHospital,SecondMilitaryMedicalUniversity,Shanghai200433,China
ZOUDuo-wu,Email:ronaldowxt@126.com
ObjectiveTo investigate the stent occlusion rate and its risk factor in chronic pancreatitis (CP).MethodsFrom November 2006 to January 2010 a total of 77 pancreatic endoprostheses from 64 patients with CP were tested by simulating the pathophysiologically increased main pancreatic duct (MPD) pressure. The water flow during 15 seconds was recorded 4 times at a pressure of 10 cm water. Kaplan Meier method was used to evaluate the univariate relationship between risk factor and stent occlusion, and Cox regression survival analysis was used to evaluate the multivariate relationship between risk factor and stent occlusion.Results64 patients with CP were included, with 43 males and 21 females, the mean age was 38 years (range, 4~80 years). The stents had been placed for a mean of 263 days (range 26~759 days). Average stent diameter was 8F (range, 5~10 F). The overall occlusion rate was 67.5% (52/77), the non-occlusion rates at 90, 180, 360, 540 d were 96.1% (74/77), 72.7% (56/77),58.4% (45/77) and 35.1% (27/77). In the Cox regression analysis, endoprosthesis diameter ≥8.5F was shown to be the only risk factors for stent occlusion.ConclusionsA significant proportion of stents placed after 180 d were not occluded, and were significantly lower than those reported from similar studies overseas. Pancreatic endoprosthesis diameter ≥8.5F was prone to occlusion.
Pancreatitis,chronic; Pancreatic ducts; Stents; Retrospective studies; Stent occlusion rate
10.3760/cma.j.issn.1674-1935.2010.04.001
200433 上海,第二军医大学长海医院消化内科
邹多武,Email:ronaldowxt@126.com

