丹参川芎嗪注射液联合西医常规治疗急性脑梗死临床疗效的Meta分析
彭世雄 危聪 雷静颖 杜泽 凃晋文 丁砚兵

摘要 目的: 系统评价丹参川芎嗪注射液联合西医常规治疗急性脑梗死的有效性和安全性。 方法: 计算机检索中国知网(CNKI)、万方、维普、中国生物医学文献数据库(CBM)、PubMed、Web of Science、和 EMbase等数据库,收集建库至2022年5月31日有关丹参川芎嗪联合西医常规治疗急性脑梗死的临床随机对照试验。采用《Cochrane干预措施系统评价手册》对纳入的研究进行质量评价,采用RevMan 5.4软件进行Meta分析。 结果: 共纳入16项研究,涉及1 693例病人。Meta分析结果显示,与对照组比较,试验组美国国立卫生研究院卒中量表(NIHSS)评分降低[MD=-3.75,95%CI(-5.46,-2.05), P <0.000 1],临 床总有效率[RR=1.20,95%CI (1.15,1.25), P <0.000 01]、 日常生活活动能力[MD=10.39,95%CI(8.94,11.83), P <0.000 01]提高,血小板聚集率[MD=-15.31, 95%CI(-20.23,-10.40), P <0.000 01]、纤维蛋白原[MD=-0.86,95%CI(-1.39,-0.32), P =0.002]、血浆黏度[MD=-0.34,95%CI(-0.55,-0.13), P =0.002]降低。两组不良反应发生率比较,差异无统计学意义[RR=1.35,95%CI(0.62,2.88), P =0.44]。 结论: 现有证据表明,在西医常规治疗基础上联用丹参川芎嗪注射液治疗急性脑梗死可提高临床疗效,但纳入文献质量不高,需更多的多中心随机对照试验支持。
关键词 急性脑梗死;丹参川芎嗪注射液;随机对照试验;Meta分析
doi: 10.12102/j.issn.1672.1349.2024.10.005
脑卒中是全球第二大死亡原因,具有较高的发病率、致残率和复发率 [1] 。其中急性缺血性脑卒中(acute ischemic stroke,AIS)约占全部脑卒中的85%,是导致成年人致残、致死的首要原因 [2] 。急性脑梗死治疗的重点在于尽早开通阻塞血管 [3] 。目前,国内外指南均推荐发病3.0~4.5 h采用静脉溶栓治疗 [4] ,受限于溶栓的严格时间窗、禁忌证及症状性颅内出血等不良反应,我国溶栓普及率较低,治愈率不高,实际获益人群有限 [5] 。中医药治疗急性脑梗死历史悠久,中医药具有多靶点调控、不受时间限制等优点。近年来,随着研究的进步,较多关于中药注射液的随机对照试验(RCT) 在临床开展 [6] 。有指南提出,部分活血化瘀类中药注射液联合西医常规治疗可改善病人神经功能缺损 [7] 。
丹参川芎嗪注射液是由盐酸川芎嗪和丹参素组成,药理学研究表明,两者合用可显著升高大鼠血清超氧化物歧化酶(SOD)活性,改变脑缺血大鼠海马非受体型酪氨酸激酶(SRC)、丝裂原活化蛋白激酶(MAPK).1 mRNA表达水平,保护脑细胞 [8.9] 。丹参川芎嗪注射液自上市后被纳入众多指南中,广泛用于临床 [10] 。鉴于部分病人临床使用丹参川芎嗪注射液存在过敏反应、高质量的循证证据较少,既往文献对联用的西医治疗欠规范,因此,对丹参嗪注射液联合西川芎 嗪注射液联合西医常规治疗的疗效和安全性进行系统评价是有必要的。本研究系统评价丹参川芎嗪注射液联合西医常规治疗的有效性和安全性,根据相关指南 [11] 对西医常规治疗进行规范限定(同时使用抗血小板聚集和 调脂),旨在西医常规治疗的基础上对丹参川芎嗪注射液联用西医治疗的临床应用提供循证医学证据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型
临床RCT,语种不限。
1.1.2 研究对象
确诊为急性脑梗死的病人(发病2周以内),不限年龄、种族、国籍。脑梗死的部位和类型不限。
1.1.3 干预措施
对照组给予西医常规治疗(包括抗血小板聚集、调脂稳斑、血压血糖常规控制、降颅脑压、改善脑代谢等)或在西医常规治疗基础上联合其他常规药物或联合安慰剂治疗,其中西医二级预防中的抗血小板聚集、调脂为必要措施。试验组在对照组基础上加用丹参川芎嗪注射液治疗,干预措施、疗程不受限制。两组接受的西医常规治疗一致。
1.1.4 结局指标
纳入研究至少包含以下结局指标的1种,1)神经功能缺损指标:美国国立卫生研究院卒中量表(NIHSS)评分。2)总有效率:根据NIHSS评分进行评定,基本痊愈:NIHSS评分减少91%~100%;显著进步:NIHSS评分减少46%~90%;进步:NIHSS评分减少18%~45%;无变化:NIHSS评分减少及增加18%以内;恶化:NIHSS评分增加18%以上及死亡;基本痊愈、显著进步、进步为总有效,无变化、死亡为无效。3)日常生活活动能力:采用Barthel指数量表进行评定。4)血液流变学指标(包括纤维蛋白原、血小板聚集率、血浆黏度)。5)不良反应。
1.1.5 排除标准
无法获取全文的文献;采用静脉溶栓或机械取栓的病人;对照组未使用抗血小板聚集和调脂治疗;重复发表的文章,以公开发表的第一项研究为主;数据缺失或数据有严重错误的文献。
1.2 文献检索
对中国知网(CNKI)、万方、维普、中国生物医学文献数据库(CBM)、PubMed、Web of Science和EMbase等数据库进行计算机检索。检索时限从建库至2022年5月31日,对丹参川芎嗪注射液联合西医常规治疗急性脑梗死的临床RCT进行检索。采用自由词和主题词结合进行全面检索,中文检索词包括丹参川芎嗪注射液、脑梗死、急性脑梗死、缺血性脑中风、缺血性脑卒中、缺血性中风、RCT、随机对照等22个关键词;英文检索词包括salvia ligustrazine injection, Danshen Chuanxiongqin injection,cerebral infarction, cerebral stroke,random等20个关键词。
1.3 文献筛选与资料提取
应用NoteExpress进行文献管理和查重,再由2名循证医学研究员严格按照纳入与排除标准,独立完成文献筛选和提取,汇总结果,确定最终纳入的文献。若在筛选和提取过程中出现分歧,与第3方协商解决。提取资料的条目包括作者与发表年份、发病时间、研究对象的特点(各组例数、性别比例、年龄等)、川芎嗪注射液用法、频次、疗程、结局指标及影响偏倚风险的要素(随机方法、有无盲法、有无脱落等)。
1.4 纳入研究的偏倚风险评价
由2名研究员根据《Cochrane干预措施系统评价手册》评估纳入临床RCT的方法学质量,根据“是否随机、是否隐藏分配方法、是否采取双盲、结局数据有无缺失、选择性报告研究结果及其他偏倚来源”7个方面对文献进行评估;根据 “是(低风险)”“否(高风险)” “不清楚(缺乏相关信息或偏倚风险不确定)”评估纳入研究的偏倚风险。
1.5 统计学处理
采用RevMan 5.4软件进行Meta分析。连续性变量以均方差(MD)、95%置信区间(confidence interval,CI)表示;二分类资料以相对危险度(risk ratio,RR)及95%CI表示。异质性使用Cochrane Q 法及 I 2法进行分析, P >0.1、 I 2≤50%,认为各研究间异质性可接受,采用固定效应模型进行分析;反之,认为各研究间异质性较大,采用敏感性分析或亚组分析确定异质性来源,若无法确认异质性来源,采用随机效应模型进行分析。对结局指标>10项的研究绘制漏斗图进行发表偏倚分析。
2 结 果
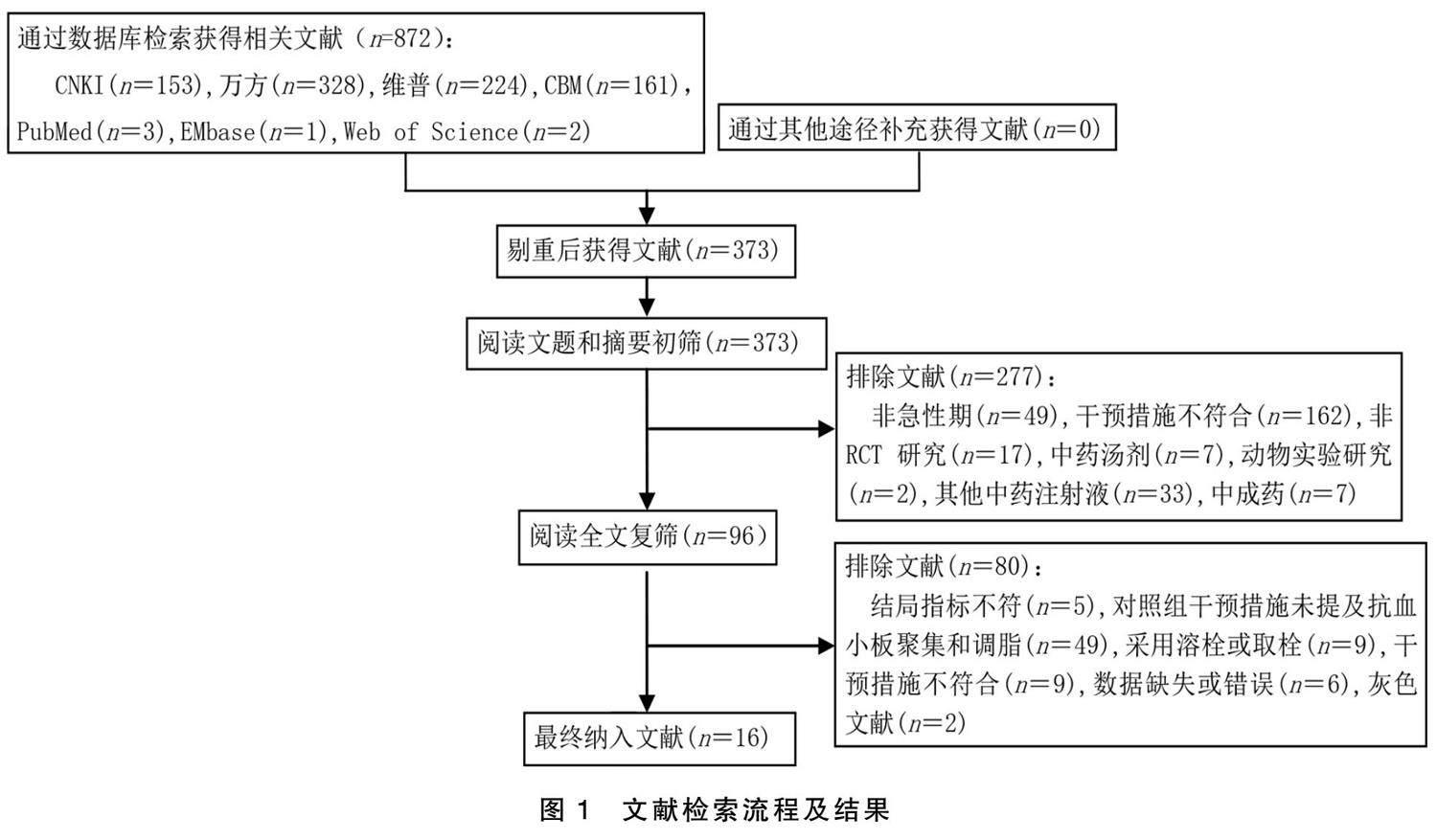
2.1 文献检索流程及结果
检索数据库获得相关文献872篇,经Note Express 3.4软件查重后删除499篇,阅读题目和摘要后删除277篇,阅读全文后再删除74篇,最终纳入16篇文献 [12.27] 。文献检索流程及结果见图1。
2.2 纳入研究的基本特征
纳入的16项研究 [12.27] 均为在我国进行的双臂RCT,涉及1 693例病人,其中对照组843例,试验组850例。1项研究 [26] 未提及对照组和试验组男女比例,其余15项研究男女比例为1.375∶1。关于急性脑梗死的诊断标准,10项研究 [14.16,18.20,22,24,26.27] 采用脑血管病诊断标准,4项研究 [12.13,21,25] 采用脑卒中指南中的诊断标准,1项研究 [17] 采用《神经病学》标准,1项研究 [23] 未提及诊断标准。由于对照组治疗急性脑梗死的干预措施复杂,故将抗血小板聚集、调脂稳斑、控制血压、降糖、脱水降颅脑压、改善脑代谢等对症治疗等作为西医常规治疗便于提取信息。纳入研究的基本特征见表1。
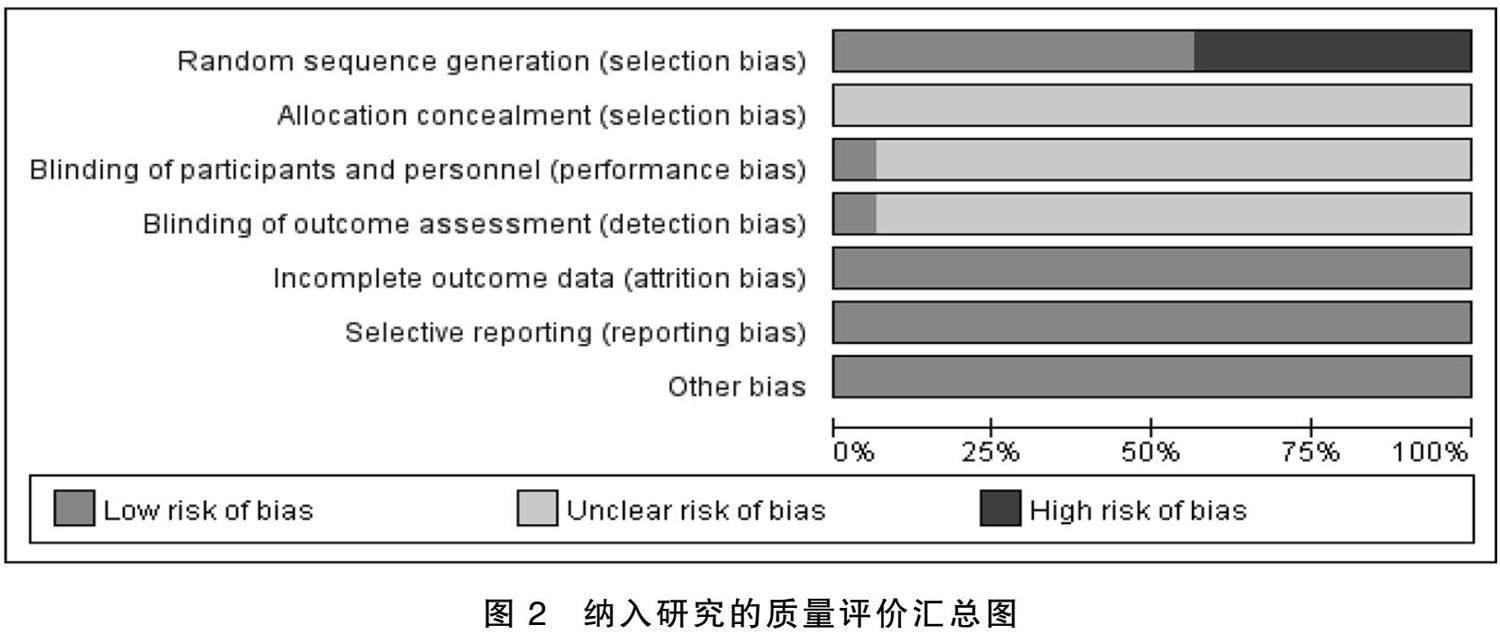
2.3 纳入研究的质量评价
纳入的16项研究中,7项研究 [13,21.25,27] 采用随机数字表法,1项研究 [26] 采用单双号法,均评为“低风险”,8项研究 [12,14.20] 未提及随机方法,评为“不确定”;所有研究均未详细描述分配隐藏方法,均评为“不确定”;1项研究 [14] 采用双盲法,评为“低风险”,其余研究均未提及盲法,评为“不确定”;所有研究均报道方案指标,无缺失数据,无部分报告情况,均评为“低风险”;所有研究未提及其他偏倚,均评为“低风险”。纳入研究的质量评价见图2。
2.4 Meta分析结果
2.4.1 NIHSS评分
共14项研究 [12.18,20,22.27] 报道了NIHSS评分,涉及1 50 9例病人。异质性检验结果, I 2=97%, P <0.000 01, 提示各研究间异质性较大,采用敏感性分析法逐项剔除14项研究,未发现明显的异质性来源。14项研究中,7项研究 [12.15,22.23,27] 采用5%葡萄糖注射液作为溶液,另外7项研究 [16.18,20,24.26] 采用生理盐水作为溶液,考虑溶液不同可能是异质性来源, 故根据丹参川芎嗪注射液配伍溶液的不同进行亚组分析。结果显示,应用葡萄糖注射液配伍时, I 2=94%, P <0.000 01,Meta分析结果显示,试验组NIHSS评分低于对照组[MD=-3.03, 95%CI(-4.50,-1.56), P <0.000 1];应用生理盐水配伍时, I 2=96%, P <0.000 01,Meta分析结果显示,试验组NIHSS评分低于对照组[MD=-4.49,95%CI (-7.60,-1.39), P =0.005],提示各研究间异质性较大,故溶液无法解释异质性来源。考虑病人年龄、病程及既往史可能为异质性来源。采用随机效应模型进行Meta分析,结果显示,试验组NIHSS评分 低于对照组,差异有统计学意义[MD=-3.75,95%CI(-5.46,-2.05), P <0.000 1]。详见图3。
2.4.2 总有效率
共14项研究 [13.15,17.27] 报道了临床总有效率,涉及 1 521例病人。异 质性检验结果显示, I 2=0%, P =0.99, 提示异质性可接受,采用固定效应模型进行Meta分析。结果显示,试验组总有效率高于对照组,差异有统计学意义[RR=1.20, 95%CI(1.15,1.25), P <0.000 01]。 详见图4。
2.4.3 Barthel指数
共5项研究 [14.15,20,22,26] 报道了Barthel指数,涉及 653例病人。异质性检验结果显示, I 2=94%, P < 0.000 01,提示各研究间异质性较大,详见图5。逐一剔除文献后发现,删除文献 [20] 后异质性变小, I 2=17%, P =0.30,故采用固定效应模型进行Meta分析。结果显示, 试验组Barthel指数高于对照组,差异有统计学意义[MD=10.39, 95%CI(8.94,11.83), P <0.000 01]。 详见图6。
2.4.4 血液流变学
共2项研究 [14,21] 报道了血小板聚集率,涉及307例病人。异质性检验结果显示, I 2=59%, P =0.12,采用随机效应模型 进行Meta分析,结果显示,试验组血小板聚集率低于对照组,差异有统计学意义[MD=-15.31, 95%CI(-20.23,-10.40), P <0.000 01]。共4项研究 [14,23,25.26] 报道了纤维蛋白原含量,涉及527例病人。异质性检验结果显示, I 2=97%, P <0.000 01,采用随机效应模型进行Meta分析,结果显示,试 验组纤维蛋白原含量低于对照组,差异有统计学意义 [MD=-0.86,95%CI(-1.39,-0.32), P =0.002]。共4项研究 [14,23,25.26] 报道了血浆黏度,涉及527例病人。异质性检验结果显示, I 2=83%, P =0.004,采用随机效应模型进行Meta分析,结果显示,试验组血浆黏度低于对照组,差异有统计学意义[MD=-0.34,95%CI(-0.55,-0.13), P =0.002]。
2.4.5 不良反应
共7项研究 [14.15,17,20.21,23,25] 报道了不良反应,其中1项研究 [15] 报道无不良反应,其余6项研究 [14,17,20.21,23,25] 均有不良反应。其中试验组10例病人出现皮疹,2例皮疹无特殊处理后自行消退;1例病人出现一过性头痛,调慢滴速后症状缓解;2例病人出现恶心呕吐,1例病人出现血压偏低,1例病人出现嗳气;对照组出现8例皮疹,8例胃肠道反应(恶心、呕吐、食欲减退等) ,1例转氨酶升高,未经特殊处理于停药10 d 后自 行恢复。异质性检验结果显示, I 2=0%, P =0.73, 异质性可接受,采用固定效应模型进行Meta分析;结果显示,试验组和对照组不良反应发生率比较,差异无统计学意义[RR=1.35,95%CI(0.63,2.88), P =0.44]。详见图7。
2.5 发表偏倚分析
对NIHSS评分及总有效率进行发表偏倚分析,漏斗图显示较对称,在无效线两边,提示存在发表偏倚的可能。详见图8、图9。其余结局指标不足10项研究,故未进行发表偏倚分析。
3 讨 论
3.1 本研究选题依据及临床意义
脑卒中已成为我国第一大死因。目前,静脉溶栓 [28] 和机械取栓 [29] 为首选措施,受限于其严格时间窗 [30] 、严重不良反应 [31] ,我国溶栓率仅为2.4%。有共识提出,错过静脉溶栓或有禁忌证的急性脑梗死病人,中医早期干预可提高临床疗效 [32] 。丹参川芎嗪注射液作为活血化瘀类中药广泛用于急性脑梗死病人的治疗中,其有效成分丹参素可穿过血脑屏障 [33] ,改善微循环,减缓神经元凋亡 [34] ,缓解脑缺血大鼠的脑组织损伤,对脑梗死急性期挽救缺血半暗带发挥多靶点 [35] 协同作用。丹参川芎嗪注射液作为多靶点调控的中药,引起的药物不良反应 [9] 较多,如皮疹、消化道症状等。丹参川芎嗪注射液联合西医的有效性和安全性值得深入探讨。查阅相关文献发现,关于丹参川芎嗪注射液与西药联用的循证医学仅2项研究 [36.37] 。既往相关Meta检索时间最晚为2019年 [36] ,本研究将检索时间更新至2022年5月,增补近3年的空白,将发病时间扩展到14 d,根据指南对西医治疗进行规范限定(同时运用抗血小板聚集、调脂),旨在提高相关纳入文献的质量,探讨丹参川芎嗪注射液联用西医常规治疗的有效性和安全性。
3.2 本研究结果分析
本研究纳入16项研究,与对照组比较,试验组NIHSS评分降低[MD=-3.75 ,95%CI(-5.46,-2.05), P <0.000 1],临床总有效率[RR=1.20,95%CI(1.15,1.25), P <0.000 01]、日常生活能力[MD=10.39,95%CI(8.94,11.83), P <0.000 01]提高,血小板聚集 率[MD=-15.31,95%CI(-20.23,-10.40), P < 0.000 01]、纤维蛋白原[MD=-0.86,95%CI(-1.39,-0.32), P =0.002]、血浆黏度[MD=-0.34,95%CI(-0.55,-0.13) , P =0.002]降低。两组不良反应发生率比 较,差异无统计学意义[RR=1.35,95%CI(0.62,2.88), P =0.44]。 故丹参川芎嗪注射液联合西医治疗可提高急性脑梗死病人的临床疗效,不良反应较少。
3.3 本研究的不足与建议
本研究存在的不足:1)纳入文献质量不高,结局可靠性的应用需谨慎对待;2)纳入研究的部分结局指标,如NIHSS评分异质性较高,采用敏感性分析及亚组分析未降低异质性,考虑可能由病人的年龄、发病时间、病情严重程度及西药不同造成的,今后需开展更多设计严谨、方法科学的RCT,明确年龄范围、发病时长、合理运用盲法等;3)报道不良反应的文献仅为纳入文章的50%,可见部分纳入文献在结局指标方面存在不足,今后应丰富完善有关不良反应的结局指标;4)部分结局指标的相关文献较少,结果可靠性的应用需谨慎对待。
现有证据表明,在西医常规治疗基础上联合丹参川芎嗪注射液治疗急性脑梗死可提高临床疗效,有较高的安全性。今后仍需更多的多中心RCT支持。
参考文献:
[1] GUZIK A, BUSHNELL C.Stroke epidemiology and risk factor management[J].Continuum,2017,23:15.39.
[2] 王陇德, 刘建民,杨弋,等.我国脑卒中防治仍面临巨大挑战——《中国脑卒中防治报告2018》概要[J].中国循环杂志,2019,34(2):105.119.
[3] WARNER J J, HARRINGTON R A,SACCO R L, et al .Guidelines for the early management of patients with acute ischemic stroke:2019 update to the 2018 guidelines for the early management of acute ischemic stroke[J].Stroke,2019,50(12):3331.3332.
[4] WANG W Z, JIANG B,SUN H X, et al .Prevalence,incidence,and mortality of stroke in China:results from a nationwide population.based survey of 480 687 adults[J].Circulation,2017,135(8):759.771.
[5] ADIBHATLA R M, HATCHER J F.Tissue plasminogen activator(tPA) and matrix metalloproteinases in the pathogenesis of stroke:therapeutic strategies[J].CNS & Neurological Disorders Drug Targets,2008,7(3):243.253.
[6] 谢倩文, 肖晶旻,邓雪仪,等.建立中医药治疗缺血性卒中核心结局指标集的初步研究[J].中医杂志,2022,63(3):220.228.
[7] 倪小佳, 陈耀龙,蔡业峰.中西医结合脑卒中循证实践指南(2019)[J].中国循证医学杂志,2020,20(8):901.912.
[8] 孙佳, 张静雅,李容,等.川芎嗪.丹参配伍前后对药动学及CYP450酶的影响及其相关性[J].中国中药杂志,2022,47(23):6348.6354.
[9] 段凯旋, 刘志强,王博龙.基于网络药理学的丹参川芎嗪注射液入血成分治疗脑梗死机制分析[J].药学研究,2020,39(10):605.608.
[10] 高阳, 王桂倩,王健,等.丹参川芎嗪注射液临床应用专家共识[J].中国中药杂志,2019,44(14):2937.2942.
[11] 中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组.中国缺血性脑卒中和短暂性脑缺血发作二级预防指南2014[J].中华神经科杂志,2015,48(4):258.273.
[12] 董琦, 富奇志.丹参川芎嗪注射液对急性脑梗死患者血清TNF.α、hs.CRP、 IL.6水平的影响[J].中国实验诊断学,2020,24(8):1238.1240.
[13] 李丹琪. 丹参川芎嗪注射液治疗急性脑梗死疗效及对SOD、Hcy及神经功能恢复的影响[J].亚太传统医药,2018,14(6):175.176.
[14] 李婷, 王煜,张立,等.丹参川芎嗪注射液联合阿托伐他汀治疗急性脑梗死的疗效观察[J].现代药物与临床,2017,32(10):1872.1875.
[15] 李春丽, 扎西草,孙燕辉.丹参川芎嗪注射液对急性脑梗死老年患者血清血管细胞间黏附分子.1、细胞间黏附分子.1、内皮素.1和一氧化氮水平的影响[J].现代中西医结合杂志,2016,25(19):2088.2090.
[16] 林翔东, 吴红星,邵爱民.丹参川芎嗪注射液对急性脑梗死患者的治疗作用及血清vasostatin.2、sICAM.1水平的影响[J].中国卫生检验杂志,2014,24(21):3079.3081.
[17] 刘梅. 依达拉奉单用、联用丹参川芎嗪治疗急性脑梗死疗效及安全性评估[J].现代中西医结合杂志,2014,23(19):2105.2107.
[18] 叶植放, 程玉珠.丹参川芎嗪注射液联合阿托伐他汀治疗40例急性脑梗死的疗效观察[J].医学理论与实践,2013,26(16):2155.2156.
[19] 凌家艳, 刘庆,吴家顺,等.丹参川芎嗪注射液对急性脑梗死患者PAC.1和CD62p的影响[J].中西医结合研究,2013,5(2):60.62.
[20] 张勇, 侯静,胡勇,等.丹参川芎嗪注射液联合依达拉奉治疗急性脑梗死临床观察[J].中西医结合心脑血管病杂志,2012,10(2):168.169.
[21] 邢春丽, 闫桂珍,郭松霞.丹参川芎嗪注射液联合阿托伐他汀对急性脑梗死患者Hcy、hs.CRP及血小板聚集率的影响[J].临床医学研究与实践,2020,5(27):20.22.
[22] 张叶飞, 周黎琴.丹参川芎嗪注射液联合阿托伐他汀钙片治疗糖尿病合并急性脑梗死临床研究[J].新中医,2020,52(6):74.77.
[23] 李震亮, 姚冬梅,幺桂兰.丹参川芎嗪注射液联合低分子肝素治疗急性脑梗死的疗效观察[J].现代药物与临床,2016,31(8):1184.1187.
[24] 俞珺, 胡勇,高杰,等.丹参川芎嗪联合瑞舒伐他汀对急性脑梗死患者血浆脑钠肽、miR.223及短期预后的影响[J].中国医院用药评价与分析,2019,19(11):1335.1338.
[25] 王明朋, 罗文成,杨金球.依达拉奉联合丹参川芎嗪治疗急性脑梗死疗效观察[J].现代中西医结合杂志,2015,24(14):1533.1535.
[26] 张东伟, 孙如,张莎莎.中西医结合治疗对脑梗死病人血液流变学、超氧化物歧化酶活性和神经功能的影响[J].中华中医药学刊,2017,35(2):507.509.
[27] 宋秋英, 方红丽,吴滨.丹参川芎嗪注射液治疗急性脑梗死的临床研究[J].重庆医学,2017,46(A01):246.247.
[28] JADHAV A P, MOKIN M,ORTEGA.GUTIERREZ S, et al .An appraisal of the 2018 guidelines for the early management of patients with acute ischemic stroke[J].Interventional Neurology,2020,8(1):55.59.
[29] SILVA G S, NOGUEIRA R G.Endovascular treatment of acute ischemic stroke[J].Continuum,2020,26(2):310.331.
[30] 中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组.中国急性缺血性脑卒中诊治指南2018[J].中华神经科杂志,2018,51(9):666.682.
[31] HU Y Z, JI C M.Efficacy and safety of thrombolysis for acute ischemic stroke with atrial fibrillation:a meta.analysis[J].BMC Neurology,2021,21(1):66.
[32] 孔令博, 王淑燕,廖晓凌,等.中医药治疗神经内科领域临床优势病种的探讨[J].中国实验方剂学杂志,2021,27(13):172.178.
[33] 杨莹, 薛霞,刘兆平.丹参素对大鼠局灶性脑缺血再灌注损伤的保护作用[J].食品与药品,2009,11(1):24.26.
[34] 李占鹰, 贾林,袁丽君,等.丹参素药理作用的研究进展[J].华西药学杂志,2021,36(5):600.603.
[35] 杨倩, 吕莉莉,孙蓉.基于网络药理学的丹参川芎嗪注射液作用机制分析[J].中草药,2018,49(11):2606.2613.
[36] 姜言红, 田颖,练佳颖,等.丹参川芎嗪注射液辅助治疗72 h内急性缺血性卒中的系统评价[J].中草药,2021,52(18):5663.5675.
[37] 谢保城, 陈世春,王清辉,等.丹参川芎嗪注射液辅助治疗急性脑梗死疗效与安全性的系统评价[J].中国中药杂志,2018,43(17):3573.3581.
(收稿日期:2023.01.05)
(本文编辑 薛妮)

