信迪利单抗分别联合白蛋白结合型紫杉醇与吉西他滨治疗鳞状非小细胞肺癌的效果对比
杨红叶,林明珠,李丹,师宇,张宁
(安阳市肿瘤医院 药学部,河南 安阳 455000)
鳞状非小细胞肺癌(squamous non-small cell lung cancer,sqNSCLC)为肺癌中常见类型,多见于老年男性,由于其起病隐匿,大部分患者就诊时已进入中晚期,丧失最佳手术切除时机[1]。化学治疗和免疫治疗是治疗晚期sqNSCLC患者的重要方法,二者联合或可给患者带来更显著的获益,化学免疫治疗应用前景广阔[2]。信迪利单抗是我国自主研发的免疫检查点抑制剂,能激活免疫T淋巴细胞,增强免疫系统识别并杀伤肿瘤细胞的能力,从而控制肿瘤生长[3]。白蛋白结合型紫杉醇或吉西他滨联合铂类是临床常用一线化疗方案,既往大量临床试验已证实其治疗sqNSCLC的有效性[4]。目前,国内关于信迪利单抗联合白蛋白结合型紫杉醇或联合吉西他滨治疗sqNSCLC的相关研究均不多见,两种化学免疫治疗方法的疗效比较研究更是鲜有报道。基于此,本研究通过回顾性分析,论证信迪利单抗分别联合白蛋白结合型紫杉醇与吉西他滨的应用效果,旨在为sqNSCLC患者治疗方案选择提供参考。
1 对象与方法
1.1 研究对象
回顾性分析安阳市肿瘤医院2021年1月至2023年6月收治的76例sqNSCLC患者的临床资料,根据治疗方案将其分为两组,其中32例接受信迪利单抗联合白蛋白结合型紫杉醇方案治疗的患者纳入T组,44例接受信迪利单抗联合吉西他滨治疗的患者纳入G组。(1)纳入标准:①符合sqNSCLC相关诊断标准[5];②恶性肿瘤国际临床病理分期[6]为ⅢA~Ⅳ期;③无法采用手术切除;④存在不低于1个可测量病灶;⑤美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体能状态评分[7]0~1分;⑥治疗及随访资料完整。(2)排除标准:①未完成治疗周期者;②妊娠或哺乳期妇女;③合并其他重要器官功能障碍者;④合并认知障碍、精神疾病者。
1.2 治疗方法
1.2.1T组
白蛋白结合型注射用紫杉醇[齐鲁制药(海南)有限公司,国药准字H20193309,规格100 mg]150 mg·m-2,静脉滴注,第1、8天。信迪利单抗[信达生物制药(苏州)有限公司,国药准字S20180016,规格100 mg(10 mL)/瓶]200 mg,静脉滴注,第1天。顺铂(云南植物药业有限公司,国药准字H53021740,规格2 mL∶10 mg)38 mg·m-2,静脉滴注,第2、3天;或卡铂(齐鲁制药有限公司,国药准字H20020180,规格10 mL∶100 mg)5 mg·mL-1·min-1的浓度-时间曲线下面积,静脉滴注,第2天;或奈达铂(齐鲁制药有限公司,国药准字H20050563,规格10 mg)27~33 mg·m-2,静脉滴注,第1、2、3天。以21 d为1个治疗周期,连续治疗2个周期。
1.2.2G组
盐酸吉西他滨(仁合熙德隆药业有限公司,国药准字H20213148,规格0.2 g)1 250 mg·m-2,静脉滴注,第1、8天。信迪利单抗、铂类用药方案同T组。以21 d为1个治疗周期,连续治疗2个周期。
1.3 观察指标
(1)临床疗效[8]:统计两组患者治疗结束后的客观缓解率(objective response rate,ORR)和疾病控制率(disease control rate,DCR)。ORR为完全缓解、部分缓解例数占总例数的百分数,DCR为完全缓解、部分缓解、疾病稳定占总例数的百分数。
(2)肿瘤标志物:收集患者治疗前后次日血清鳞状上皮细胞癌抗原(squamous cell carcinoma,SCC)、细胞角质蛋白19片段抗原21-1(cytokeratin 19 fragment antigen 21-1,CYFRA21-1)、癌胚抗原(carcinoembryonic antigen,CEA)检测结果。
(3)用药不良反应:统计患者治疗过程中消化道反应、肝肾功能异常、骨髓抑制、血钠减少、免疫相关肺炎、甲状腺功能异常等不良反应发生情况。
(4)无进展生存期(progress free survival,PFS):统计两组患者PFS,定义为从治疗开始到第1次病情进展或因任何原因死亡的时间。
1.4 统计学方法
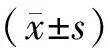
2 结果
2.1 一般资料
G组和T组患者在年龄、性别、ECOG、吸烟史、疾病分期、铂类选择、既往治疗方案方面比较,差异无统计学意义(P>0.05)。见表1。
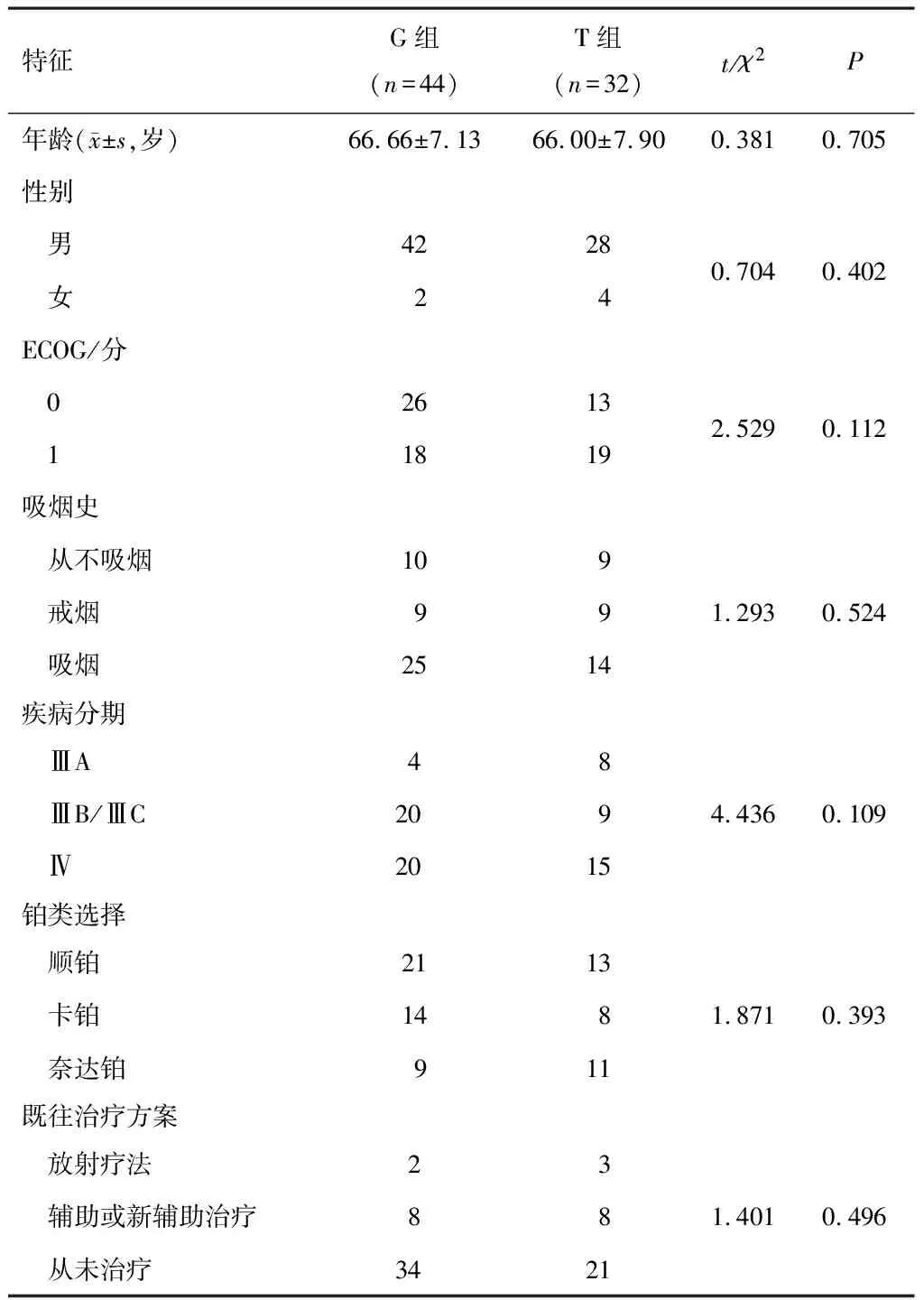
表1 两组患者一般资料比较(n)
2.2 临床疗效
治疗后,G组和T组患者ORR和DCR比较,差异无统计学意义(P>0.05)。见表2。

表2 两组患者临床疗效比较(n,%)
2.3 肿瘤标志物
治疗后,G组和T组患者SCC、CYFRA21-1、CEA均较治疗前降低(P<0.05),但两组组间比较差异无统计学意义(P>0.05)。见表3。
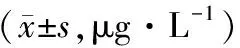
表3 两组患者肿瘤标志物比较
2.4 用药不良反应
治疗过程中,G组和T组患者消化道反应、骨髓抑制、血钠减少、免疫相关肺炎、甲状腺功能异常发生率比较,差异无统计学意义(P>0.05);T组肝肾功能异常发生率低于G组,差异有统计学意义(P<0.05)。见表4。
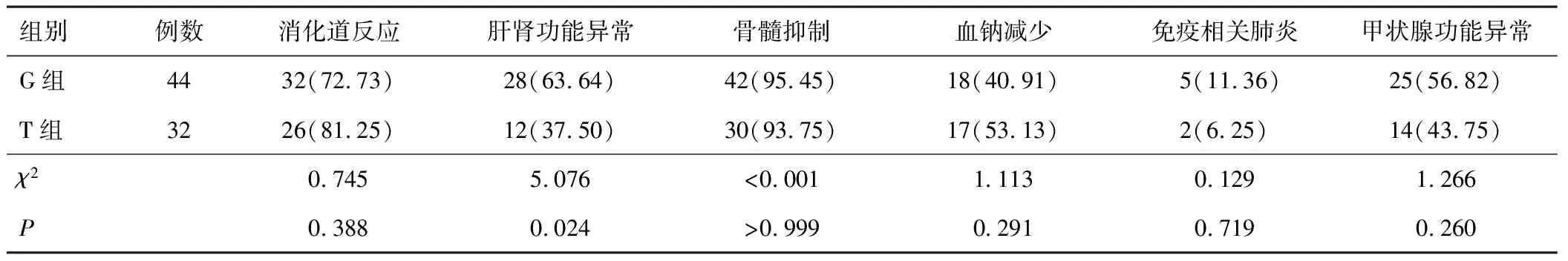
表4 两组患者用药不良反应比较[n(%)]
2.5 PFS
G组PFS为1.4~7个月,中位PFS为5.6个月;T组PFS为1.4~5.6个月,中位PFS为5个月,两组PFS、中位PFS比较,差异无统计学意义(log-rankχ2=0.312,P=0.576)。
3 讨论
晚期sqNSCLC患者通常会出现咯血、胸部疼痛、吞咽困难、气短喘促等临床症状,疾病无法治愈,治疗目的是缓解患者临床症状,提高生存质量及延长生存期[9]。在过去几十年里,化疗都是攻击肿瘤的主要武器,近年来,随着分子生物学、肿瘤免疫学的飞速发展,免疫治疗凭借特异性强、不良反应少的优势迅速成为肿瘤治疗领域的研究热点[10]。信迪利单抗属于程序性细胞死亡受体-1(programmed cell death protein-1,PD-1)抑制剂,能中断肿瘤细胞表面PD-1配体作用通路,解除免疫抑制并激活人体自身免疫监察机制,保持T淋巴细胞的持续活化状态,发现并攻击肿瘤细胞,阻止肿瘤细胞免疫逃逸的发生,抑制肿瘤细胞生长,发挥优越抗癌效果,控制并缓解sqNSCLC患者病情[11]。从肿瘤治疗的发展趋势来看,以免疫治疗为基础的化学免疫治疗方案有望成为晚期癌症的主要治疗模式。
白蛋白结合型紫杉醇是疏水性紫杉醇和人血白蛋白结合制成的化疗药物,能破坏真核细胞中微管和微管蛋白二聚体间的动态平衡,诱导微管蛋白聚合,抑制微管解聚,通过稳定、无功能的微管阻碍纺锤体和纺锤丝形成,从而抑制肿瘤细胞分裂增殖[12]。吉西他滨属于新型细胞周期特异性抗癌药,主要作用于肿瘤细胞脱氧核糖核酸(deoxyribonucleic acid,DNA)合成期,能在体内代谢为二磷酸,抑制核苷酸还原酶,阻止DNA双链延长,终止DNA连复制,导致肿瘤细胞发生凋亡[13]。本研究结果显示,G组和T组在DCR、ORR、PFS、中位PFS方面差异无统计学意义,表明信迪利单抗联合白蛋白结合型紫杉醇与信迪利单抗联合吉西他滨治疗sqNSCLC的临床效果相似。
SCC是一种由鳞状上皮细胞分泌的糖蛋白,参与鳞状上皮层的分化,对于所有鳞状细胞癌均有特异性,其血清水平与患者病情程度密切相关,临床常用SCC来检测sqNSCLC患者治疗效果及预后评估等[14]。CYFRA21-1主要分布在肺泡上皮中,当细胞癌变时,CYFRA21-1会以溶解片段释放入循环血中,其对非小细胞肺癌特别是sqNSCLC具有较高的灵敏度,高浓度CYFRA21-1通常提示患者疾病进展、预后不良[15]。CEA是临床最广谱的肿瘤标志物,其水平升高常见于多种恶性肿瘤,监测血清CEA水平对于sqNSCLC患者病情好转或病情发展具有一定评估价值。本研究比较两组患者血清肿瘤标志物水平发现,G组和T组患者SCC、CYFRA21-1、CEA均较治疗前降低,但两组组间比较差异无统计学意义,佐证了信迪利单抗联合白蛋白结合型紫杉醇与信迪利单抗联合吉西他滨治疗sqNSCLC的有效性,且两组方案疗效相近。
联合治疗带来的更强毒性不容小觑,本研究比较两组患者治疗过程中不良反应发现,G组和T组患者用药不良反应均较高,临床对于接受化学免疫联合治疗的患者需密切观察,以便及时处理。两组患者消化道反应、骨髓抑制、血钠减少、免疫相关肺炎、甲状腺功能异常发生率比较差异无统计学意义,但T组肝肾功能异常发生率低于G组,因此对于已有肝肾功能损害、高龄、体力状况差等高危sqNSCLC患者,建议考虑采用信迪利单抗联合白蛋白结合型紫杉醇的方案治疗,以提高患者耐受性,完成治疗,改善预后。
4 结论
信迪利单抗联合白蛋白结合型紫杉醇对鳞状非小细胞非癌的疗效不劣于信迪利单抗联合吉西他滨。

