吗啉硝唑临床应用的研究进展
田丹丽 黄龙千 梁春坡
摘要:从结构特点、抗菌机制、抗菌活性、药动学、药物相互作用及临床应用等方面全面介绍吗啉硝唑的研究进展,为深入研究提供参考。吗啉硝唑作为新型硝基咪唑类抗菌药,抗菌活性强,不易产生耐药性,臨床应用日益增多。多项研究证实吗啉硝唑疗效显著,安全性高。吗啉硝唑具有科研和临床应用价值,值得深入研究。
关键词:吗啉硝唑;临床应用;不良反应;抗菌作用机制;抗菌活性
中图分类号:R978.1文献标志码:A
Research progress in the clinical application of morinidazole
Abstract This research progress on morinidazole was reviewed from the perspectives of structure, antibacterial mechanism, antibacterial activity, pharmacokinetics, drug interaction and clinical application to provide references for further study. As a new type of nitrazole antibiotic, morinidazole has strong antibacterial activity and is not easy to produce drug resistance, so its clinical application is increasing day by day. Many studies have confirmed that morinidazole is effective and safe. Morinidazole has the value of scientific research and clinical application, which makes it worthy of further study.
Key words Morinidazole; Clinical application; Adverse reactions; Antibacterial mechanism; Antimicrobial activity
抗菌药物是指能够抑制或者消灭病原菌活性的抗生素或者人工合成药物[1],人工合成的抗菌药包括喹诺酮类,磺胺类和硝基咪唑类等。其中,硝基咪唑类药物因对厌氧菌及原虫有独特的杀灭作用、杀菌能力强、抗厌氧菌谱广和价格低廉等优点,被广泛应用于临床,与其他抗菌药物联合应用于厌氧菌与需氧菌的混合感染及各种原虫感染[2-3]。由于具有多种生物活性,硝基咪唑类化合物在新药研发领域占据着重要位置[4]。吗啉硝唑属于新型硝基咪唑类药物,2014年上市,体内和体外药效学试验均表明[5-7],吗啉硝唑抗厌氧菌活性强于甲硝唑、替硝唑及奥硝唑,且安全性更好。但吗啉硝唑作为最新研制的第三代硝基咪唑类药物,上市时间较短,有关的研究较少。本文就吗啉硝唑的结构特点、抗菌机制、抗菌活性、药动学、药物相互作用及临床应用进行较为全面的综述,以期为临床用药提供参考。
1 吗啉硝唑的结构特点及抗菌机制
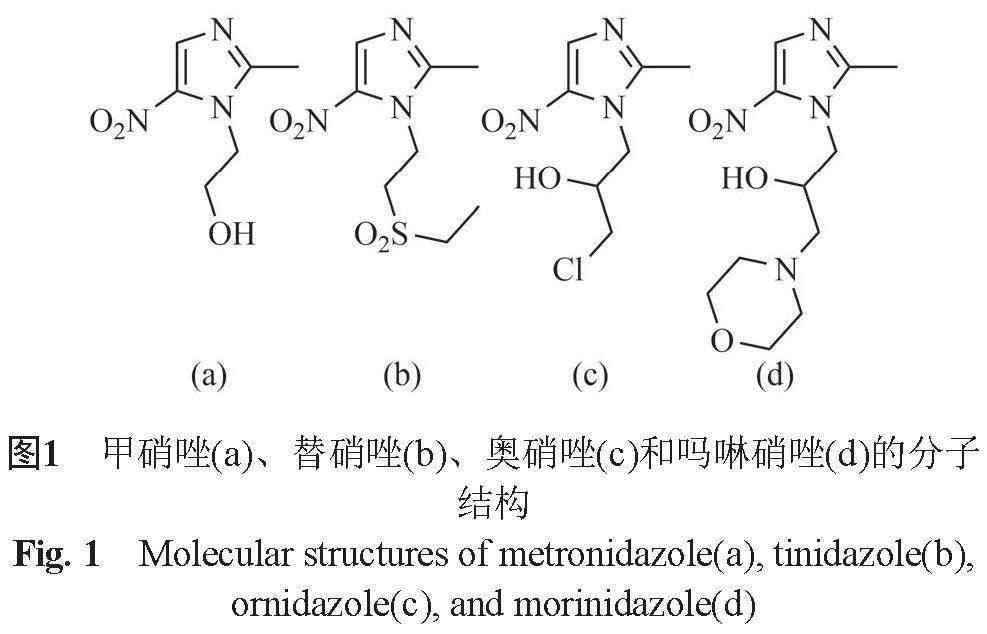
硝基咪唑类药物在结构上的共同特点是咪唑环上有硝基取代,经过对其结构不断地修饰和优化,相继开发出了不同的硝基咪唑类抗菌药物[3]。根据咪唑环上取代基的种类和位置的不同分类,包括甲硝唑、替硝唑、奥硝唑、左奥硝唑和吗啉硝唑等。其中,吗啉硝唑为5-硝基咪唑类抗菌药物,将奥硝唑中不稳定的氯离子改为较为稳定的吗啉环,不仅使其结构更稳定,而且不良反应发生率更低、具体结构见图1。抗菌药物的作用机制可分为破坏病原体细胞的细胞壁,影响其核酸的复制及修复和抑制细胞内的蛋白质的合成[1]。人工合成的抗菌药通常影响核酸的代谢,硝唑类药物在进入易感的微生物细胞后,分子结构中的硝基在无氧或者少氧的环境中,在较低的氧化还原电位下被电子传递蛋白还原为具有细胞毒性的氨基,破坏DNA的双螺旋结构,使得已合成的DNA降解,抑制细胞的DNA合成和转录,导致病原体细胞死亡[1]。
2 吗啉硝唑的抗菌活性
体外药效学结果显示,吗啉硝唑对临床分离厌氧革兰阴性无芽胞杆菌和革兰阳性球菌具有较强抗菌作用。对脆弱拟杆菌、韦荣球菌和产气荚膜梭菌的抗菌活性与奥硝唑相当,比甲硝唑、替硝唑强2到8倍;对吉氏拟杆菌和卵圆形拟杆菌的抗菌活性与奥硝唑相当,比甲硝唑、替硝唑强2~4倍[6]。
3 吗啉硝唑的药动学
3.1 健康受试者
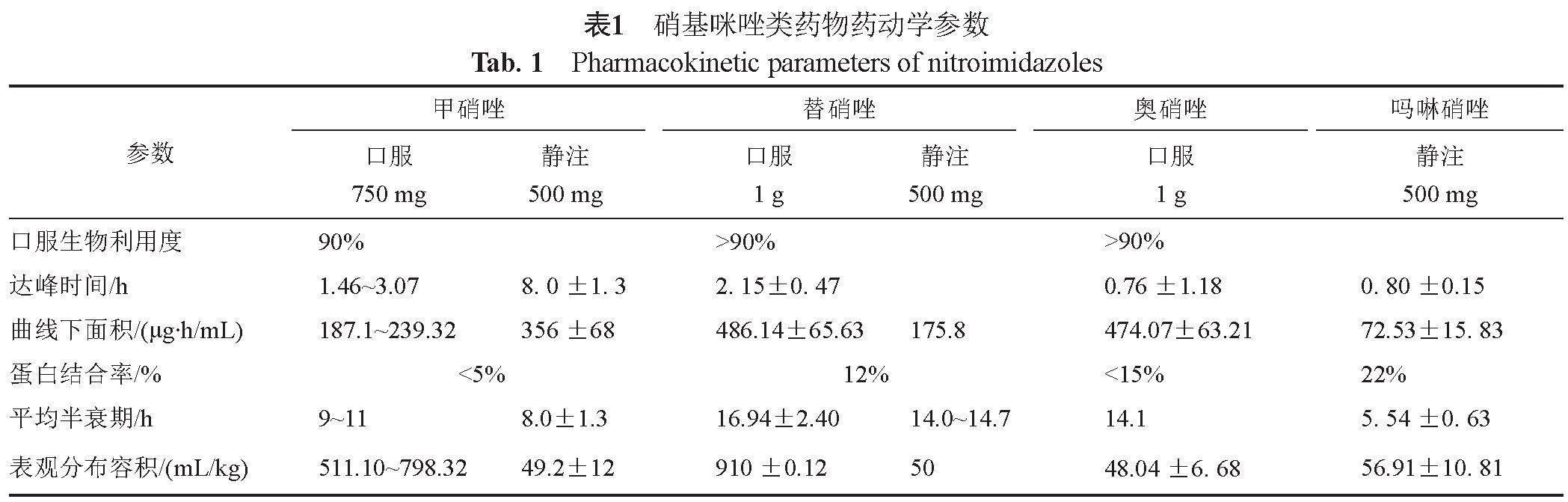
健康受试者的药动学数据显示,吗啉硝唑注射液的血药峰浓度(Cmax)和曲线下面积(AUC0-t)与给药剂量呈正相关,与甲硝唑相同,呈线性药动学。吗啉硝唑在体内分布较为广泛和均匀,其他硝基咪唑类也广泛分布在各组织和体液中,其中替硝唑对血脑屏障的穿透性较强,比甲硝唑高。吗啉硝唑蛋白结合率为22%左右,略高于甲硝唑(小于5%)、替硝唑(12%)和奥硝唑(小于15%)。硝基咪唑类药物主要经过肝脏代谢,大部分有肝脏细胞色素P450酶的参与。但吗啉硝唑主要的代谢途径为原型药物与葡萄糖醛酸和硫酸的结合,不通过细胞色素P450介导。半衰期为5.6~6.4 h,70%以原形和II相代谢物形式经过肾脏排泄。甲硝唑经过肝脏细胞色素P450系统代谢,并为CYP2C9的抑制剂。肝脏代谢形成5种代谢产物,半衰期为8 h,其大部分由尿液排泄 (60%~80%),小部分通过粪便排泄(10%)和皮肤排泄(14%)。替硝唑口服吸收完全,生物利用度比甲硝唑更高,消除半衰期更长,大约为12~14 h,是甲硝唑的2倍。在体内主要由CYP3A4(77%)和CYP2B6(12%)同工酶代谢,且为这两种酶的底物。60%~65%经肾脏排泄,12%经粪便排泄。奥硝唑经胃肠道吸收,口服生物利用度大于90%,高于甲硝唑,消除半衰期14 h。肝脏也是奥硝唑的主要代谢场所,其主要清除途径为与葡萄糖醛酸结合,然后63%经肾脏排泄,22%经粪便排泄。硝基咪唑类的主要药动学参数详见表1[2-3]。
3.2 特殊人群
健康受试者吗啉硝唑药动学和相互作用的研究显示,人尿中原形药物和代谢物总累积排出率为70.4%,原形药物仅占其中21.2%,提示该药主要经肝脏代谢消除为主[7]。陈钊等[7]研究吗啉硝唑注射液在肝功能中度减退受试者中的药动学特征,结果发现,与健康受试者组相比,肝功能减退组药物在体内有一定蓄积,吗啉硝唑在人体内药物暴露量(AUC)增加约68%,t1/2延长近3.7 h。对于轻度和中度肝功能减退者,吗啉硝唑的给药方案可以不变,但对于肝肾功能同时减退者,建议根据减退的程度调整给药方案 [8]。
在肾功能严重损害的患者中,有学者评估肾功能损害对吗啉硝唑药动学的影响。健康受试者和严重肾功能不全患者静脉注射500 mg吗啉硝唑后,收集血浆和尿液样本。严重肾功能不全患者M7、M8-1和M8-2的AUC分别是健康受试者的15.1、20.4和17.4倍,吗啉硝唑的AUC高出1.5倍、0~48 h两组主要代谢物的尿回收率无显著差异,但患者M7、M8-1和M8-2的肾清除率分别降低85.3%、92.5%和92.2%[9]。这些结果表明在严重肾功能不全的患者中肾摄取转运蛋白的功能或活性可能受损,导致吗啉硝唑及其代谢物的肾清除率降低,血浆暴露风险增加。其他研究发现,给予单剂量吗啉硝唑注射液后,重度肾功能不全患者原型药物的清除率只有65%,可能引起体内蓄积,建议严重肾功能不全患者谨慎应用吗啉硝唑[10-11]。
3.3 药物相互作用
吗啉硝唑在体内主要经肾脏清除,主要代谢途径不是CYP450酶介导,提示吗啉硝唑因CYP450抑制造成的药物相互作用风险较小。利福平和酮康唑对吗啉硝唑和N(+)-葡糖苷酸的血浆暴露量的影响小于50%,对吗啉硝唑药动学的临床影响较小。合用时,未发现药物相互作用,无需调整剂量[12]。由于吗啉硝唑的代谢需结合葡萄糖醛酸后通过尿液排泄,人体肾脏内转运结合物的主要转运体为有机阴离子转运体(OAT)和有机阳离子转运体,虽然肾脏摄取和外排转运蛋白在吗啉硝唑及其结合代谢物的主动肾小管分泌中的作用尚不清楚。但能抑制OAT的药物可能会对其PK有影响。富马酸替诺福韦酯 (TDF)是替诺福韦的口服前药和OAT的有效底物,一项单中心、开放性研究替诺福韦对单剂量静脉注射吗啉硝唑时药动学的影响,结果发现并没有引起有临床意义的药物相互作用[13]。汤文玲等[14]测定大鼠血浆中吗啉硝唑与药物之间的相互作用,对吗啉硝唑与丙磺舒、西咪替丁、二甲双胍、替诺福韦联用后R-吗啉硝唑与S-吗啉硝唑的药动学变化进行研究。结果发现吗啉硝唑与二甲双胍联用后,仅R-吗啉硝唑的tmax参数差异具有统计学意义,与其他药物联用后药动学参数无显著变化。化学结构相似的药物可能拥有同样的药物相互作用,吗啉硝唑与甲硝唑化学结构类似,甲硝唑与氟尿嘧啶合用时体内清除率明显降低,导致不良反应[15]。因此吗啉硝唑也可能产生同样的相互作用,合用时需监测氟尿嘧啶相关的毒性反应。
4 临床应用
4.1 妇科感染
盆腔炎主要是由于病原微生物由下生殖道(宫颈和阴道)上行感染至上生殖道所致。因此盆腔炎实际上是由多种致病微生物引起,其中包括淋病奈瑟菌、沙眼衣原体、生殖器支原体、阴道内厌氧及需氧菌群。治疗以广谱、经验性抗生素抗感染治疗为主,覆盖可能的病原体[16]。硝基咪唑类抗菌药作为一种抗厌氧菌作用强的抗菌药常用于盆腔炎的治疗。一项比较吗啉硝唑与奥硝唑治疗盆腔炎的疗效和安全性的多中心、双盲、随机的研究中,338例盆腔炎患者,随机分为两组,观察组予吗啉硝唑500 mg 静滴,每天2次,疗程14 d,对照组给予奥硝唑500 mg静滴,每天2次,疗程14 d。实验结果表明,临床治愈率分别为96.86%和96.73%,微生物学清除率为100%和89.66%,药物相关不良事件发生率吗啉硝唑(32.74%, 55/168)低于奥硝唑(47.06%, 80/170)(P<0.01)。对于患有盆腔炎的女性,每天两次吗啉硝唑与每天2次奥硝唑治疗14 d在临床治愈率和细菌学清除率上疗效相当,且前者与药物相关的不良事件比后者更少[17]。这意味着在临床用药中,使用吗啉硝唑在保证疗效的前提下能减少不良反应的发生,安全性更好。
4.2 腹腔感染
腹腔感染(intra-abdominal infection, IAI)是腹部外科常见病,可继发于消化道的穿孔、坏死与坏疽,也是腹部外科手术的常见并发症,具有较高的发病率和病死率。腹腔感染通常为多种肠道微生物的混合感染,经验性用药应覆盖肠道的需氧菌和厌氧菌[18]。吗啉硝唑抗厌氧菌活性强,在腹腔感染中应用广泛,尤其是阑尾炎的治疗。陈志达等[19]回顾性分析解放军总医院2017—2019年收治的387名急性阑尾炎患者的病例资料,探讨吗啉硝唑治疗急性复杂性阑尾炎的有效性和安全性。研究发现,吗啉硝唑组的术前、术后炎症指标变化程度均高于对照组,而且住院时间和使用抗菌药物的时间均短于对照组,结果都具有统计学差异,体现了吗啉硝唑良好的有效性和安全性。一项评估吗啉硝唑联合阑尾切除术治疗化脓性和坏疽性阑尾炎的随机、双盲、多中心和对照的研究,纳入437例化脓性和坏疽性阑尾炎的受试者,对照组给予奥硝唑治疗,试验组给予吗啉硝唑治疗,连续5~7 d,比较两组患者臨床疗效、厌氧菌清除率及不良反应发生率。结果显示,吗啉硝唑比起奥硝唑的临床治愈率和厌氧菌消除率并未有显著性差异,但是不良反应的发生率有所降低[3]。另外一项评估吗啉硝唑治疗化脓性坏疽性阑尾炎效果的单中心研究也得出类似的结论,吗啉硝唑和奥硝唑治疗化脓性坏疽性阑尾炎疗效相当,但吗啉硝唑的不良反应发生率更低,安全性更好[20]。黄冠[21]研究吗啉硝唑在急性阑尾炎中的疗效,选取134例急性阑尾炎的患者,随机分为对照组和观察组各67例,对照组给予奥硝唑,观察组给予吗啉硝唑,结果发现临床治愈率和厌氧菌清除相当,而不良反应的发生率吗啉硝唑组显然低于奥硝唑组。而在老年化脓性阑尾炎围手术期抗感染治疗研究中,庄鑫等[5]采用随机、双盲和对照研究,前瞻性分析吗啉硝唑在老年化脓性阑尾炎围手术期抗感染治疗中的有效性和安全性。结果显示吗啉硝唑组的腹腔感染的术后并发症发生率低于奥硝唑组,临床治愈率高于奥硝唑组,表明老年化脓性阑尾炎患者使用吗啉硝唑抗感染治疗安全有效。
有研究表明对于胆道感染患者,应用吗啉硝唑抗感染效果良好,安全性高。瞿胜[22]分析了吗啉硝唑氯化钠注射液对胆囊结石合并胆总管结石患者术后细菌感染的杀菌效果,将70例胆囊结石合并胆总管结石的术后细菌感染患者随机均分为两组,两组均已接受相应的手术治疗,手术后对照组采用奥硝唑常规抗感染药物治疗,观察组采用吗啉硝唑治疗,对比两组的杀菌效果、治疗前后感染指标、不良反应发生情况,结果发现观察组与对照组的细菌完全清除率分别为91.43%和71.43%,观察组高于对照组,不良反应总发生率分别为5.72%和22.85%,观察组低于对照组。
以上研究均表明吗啉硝唑对于腹腔感染的治疗安全有效。这些研究中均采用随机对照实验,但是由于樣本量的限制和回顾性研究筛选数据导致的偏向性,最后的实验结果存在一定误差的可能,但是从不同的研究对象以及多次的对照研究来看,吗啉硝唑确实比起奥硝唑在临床实际应用中有着更好的安全性和更低的不良反应发生率。
4.3 预防术后感染
手术部位感染(surgical site infection, SSI)是指没有植入物的患者术后30 d内或有植入物患者术后1年内发生与手术相关感染,包括浅层切口感染、深层切口感染及器官和(或)腔隙感染[23]。手术部位感染是临床上常见的感染类型,常导致住院时间延长和患者死亡,预防性应用抗菌药物是降低手术部位感染的有效措施之一。全子宫切除术作为常见的妇科手术,术中失血和术后创口会导致患者术后感染风险增加。金峰等[24]选取经腹全子宫切除术后患者58例为研究对象,按随机数字表法分为对照组(n=29)和研究组(n=29)。对照组采用奥硝唑治疗,研究组采用吗啉硝唑治疗。2组对比后发现,手术后最高体温和白细胞计数均无显著性差异,但是研究组退热时间明显减少。采用吗啉硝唑在经腹全子宫切除术后抗感染治疗中,可缩短退热时间,缓解炎性反应,降低阴道残端及切口感染率,缩短住院时间,减少药物费用。吗啉硝唑对肛周脓肿患者术后创面感染治疗临床疗效确切。石健等[25]探讨吗啉硝唑治疗肛周脓肿根治术后感染的临床疗效,将30例确诊的肛周脓肿患者作为研究对象,随机分为观察组和对照组各15例,观察组予以吗啉硝唑静脉滴注,对照组予以奥硝唑静脉滴注。2组在术后第7天血白细胞计数、中性粒细胞计数比治疗前降低明显,且观察组显著低于对照组;其中总体细菌清除率差异观察组优于对照组,表明吗啉硝唑的整体治疗效果更优。在头孢菌素联合吗啉硝唑预防肠外瘘患者SSI的临床价值的研究中,107例患者中,43例患者给予头孢菌素预防SSI,设为头孢菌素单药组;64例患者给予头孢菌素联合吗啉硝唑预防SSI,设为联合用药组。采用回顾性队列研究方法观察SSI发生情况,结果为头孢菌素单药组患者发生总体SSI、浅层切口感染、深层切口感染、器官和(或)腔隙感染的例数分别为18、7、5、6例,联合用药组上述指标分别为11、8、2、1例,两组患者总体SSI比较差异有统计学意义[26]。表明在预防肠外瘘患者SSI中,吗啉硝唑具有良好的临床应用价值。胃肠外科SSI发生率为9.4%~23.2%,而污秽-感染手术切口SSI发生率可高达17.8%~39.8%[27]。普通外科手术中的肝胆系统及胰腺手术、结肠、直肠、阑尾手术推荐使用头孢菌素单药或联合甲硝唑预防SSI。然而甲硝唑的不良反应较多,且耐药菌已经出现,使其广泛使用受到限制[28]。吗啉硝唑作为改进后的硝唑类药物,其耐药性更好,比起甲硝唑、奥硝唑等拥有更大的应用范围和临床价值。但有研究表明,虽然与奥硝唑相比,吗啉硝唑治疗厌氧菌疗效高、不良反应发生率低,但奥硝唑注射液更具有经济性[4]。
5 安全性评价
吗啉硝唑的不良反应主要集中于消化系统(包括恶心,消化不良和肠胃不适)、神经系统(包括头晕,嗜睡和乏力)、转氨酶升高和白细胞计数下降等。在两项III期临床实验中,对盆腔炎妇女患者和坏疽性阑尾炎患者中的主要不良反应发生率均小于2%[3]。其临床应用中的不良反应与报道基本一致[29]。吗啉硝唑禁忌症为硝基咪唑类药物过敏患者,脑和脊髓发生病变的患者,癫痫及各种器官硬化患者,造血功能低下、慢性酒精中毒患者[6]。吗啉硝唑能透过血脑屏障,对中枢神经系统具有毒性,因此在使用中发现不良反应时应该密切关注。
6 总结和展望
吗啉硝唑作为第三代硝基咪唑类抗菌药,虽然上市不久,但结构稳定,对厌氧菌作用效果好,不良反应发生率也较低,已经广泛应用于临床,多用于妇科盆腔炎和阑尾炎。目前对于吗啉硝唑临床应用的有关研究仍然较少,样本量不够,还有很大的可发掘空间,需要更多大样本、多中心的研究加以验证。
参 考 文 献
Lamp K C, Freeman C D, Klutman N E, et a1. Pharmacokinetics and pharmacodynamics of the nitroimidazole antimicrobials[J]. Clin Pharmacokinet, 1999, 36(5): 353-373.
汪复, 张婴元. 实用抗感染治疗学[M]. 北京: 人民卫生出版社, 2020: 659-669.
陈迁, 梅和坤, 白楠, 等. 硝基咪唑类药物在人体内代谢的研究进展[J]. 中国药学杂志, 2015, 50(14): 1169-1173.
赵正崇, 卢勇, 徐志. 硝基咪唑类化合物的抗菌与抗结核活性[J]. 国外医药抗生素分册, 2019, 40(6): 544-553.
庄鑫, 潘亚强, 叶欣. 吗啉硝唑在老年化脓性阑尾炎围手术期抗感染治疗中的疗效研究[J]. 中华普通外科杂志, 2020, 35(11): 879-881.
唐云, 童明庆, 于浩, 等. 吗啉硝唑联合阑尾切除术治疗化脓性或坏疽性阑尾炎的有效性和安全性研究[J]. 中华普通外科杂志, 2017, 32(8): 678-682.
陈钊, 武晓捷, 张菁, 等. 吗啉硝唑在中度肝功能减退者中的药动学[J]. 中国感染与化疗杂志, 2013, 13(3): 161-166.
金舒, 张逸凡, 陈笑艳, 等. 对映体选择性LC-MS/MS法测定人血浆中R/S-华法林及其在药物相互作用研究中的应用[J]. 药学学报, 2012, 47(1): 105-109
Zhong K, Li X, Xie C, et al. Effects of renal impairment on the pharmacokinetics of morinidazole: Uptake transporter-mediated renal clearance of the conjugated metabolites[J]. Antimicrob Agents Chemother, 2014, 58(7): 4153-4161.
Kong F, Pang X, Zhong K, et al. Increased plasma exposures of conjugated metabolites of morinidazole in renal failure patients: A critical role of uremic toxins[J]. Drug Metab Dispos, 2017, 45(6): 593-603.
Zhang H, Huang L, Huang Y Y, et al. Pharmacokinetics of single-dose morinidazole in patients with severe renal impairment[J]. Int J Clin Pharmacol Ther, 2014, 52(2): 159-165.
Pang X, Zhang Y, Gao R, et al. Effects of rifampin and ketoconazole on pharmacokinetics of morinidazole in healthy chinese subjects[J]. Antimicrob Agents Chemother. 2014, 58(10): 5987-5993.
Wu G, Tang W, Lv D, et al. Effects of tenofovir on the single-dose pharmacokinetics of intravenous morinidazole in healthy chinese subjects[J]. Antimicrob Agents Chemother, 2020, 64(5): e02067-19.
湯文玲, 沈旭, 王俏, 等. LC-MS/MS法测定大鼠血浆中R/S-吗啉硝唑及其在药物-药物相互作用研究中的应用[J]. 药物分析杂志, 2020, 40(7): 1217-1225.
张艳华, 宁华. 抗肿瘤药的配伍与用药安全评价[J]. 中国医院用药评价与分析, 2008, 8(1): 12-14.
苗娅莉, 王建六. 盆腔炎症性疾病诊治规范[J]. 中国全科医学, 2005, 8(18): 1479-1480.
Cao C, Luo A, Wu P, et al. Efficacy and safety of morinidazole in pelvic inflammatory disease: Results of a multicenter, double-blind, randomized trial[J]. Eur J Clin Microbiol Infect Dis, 2017, 36(7): 1225-1230.
中华医学会外科学分会, 中国研究型医院学会感染性疾病循证与转化专业委员会, 中华外科杂志编辑部. 外科常见腹腔感染多学科诊治专家共识[J]. 中华外科杂志, 2021, 59(3): 161-178.
陈志达, 郗洪庆, 唐云. 吗啉硝唑联合腹腔镜微创手术治疗急性非单纯性阑尾炎有效性及安全性分析[J]. 中华普通外科杂志, 2022, 37(1): 35-38.
曾少华. 阑尾切除术分别联合吗啉硝唑及奥硝唑治疗化脓性坏疽性阑尾炎的效果对比[J]. 海峡药学, 2018, 30(8): 111-113.
黄冠. 吗啉硝唑氯化钠注射液在急性阑尾炎治疗中的疗效[J]. 黑龙江医药, 2021, 34(5): 1069-1071.
瞿胜. 吗啉硝唑氯化钠注射液对胆囊结石合并胆总管结石患者术后细菌感染的杀菌效果[J]. 药品评价, 2021, 18(18): 1124-1127.
Berríos-Torres S I, Umscheid C A, Bratzler D W, et al. Centers for disease control and prevention guideline for the prevention of surgical site infection, 2017[J]. JAMA Surg, 2017, 152(8): 784-791.
金峰, 钟晴. 吗啉硝唑在经腹全子宫切除术后抗感染治疗中的应用效果[J]. 临床合理用药杂志, 2021, 14(30): 149-151.
石健, 孙春元, 鲍炳州, 等. 吗啉硝唑治疗肛周脓肿根治术后感染的临床疗效[J]. 中华普通外科杂志, 2021, 36(1): 50-52.
郑涛, 王革非, 顾国胜, 等. 头孢菌素联合吗啉硝唑预防肠外瘘手术部位感染的临床价值[J]. 中华消化外科杂志, 2021, 20(11): 1206-1211.
Bhangu A, Ademuyiwa A O, Aguilera M L. Surgical site infection after gastrointestinal surgery in high-income, middle-income, and low-income countries: A prospective, international, multicentre cohort study[J]. Lancet Infect Dis, 2018, 18(5): 516-525.
Sobel R, Sobel J D. Metronidazole for the treatment of vaginal infections[J]. Expert Opin Pharmacother, 2015, 16(7): 1109-1115.
田丹丽, 梁春坡, 周梦瑜, 等. 吗啉硝唑注射剂在普通外科的临床应用及安全性调查分析[J]. 中国医院药学杂志, 2021, 41(24): 2569-2572.

