马铃薯块茎蛾取食胁迫对马铃薯根际可培养细菌物种多样性和群体多度的影响*
李俊逸,矣晓翠,刘福翠,姚 遥,祝春月,刘一依,尹丽肖,肖关丽
(云南农业大学 农学与生物技术学院,云南 昆明 650201)
马铃薯块茎蛾[Phthorimaea operculella(Zeller)]隶属于鳞翅目(Lepidoptera)麦蛾科(Gelechiidae),是一种寡食性害虫,也是世界范围内茄科(Solanaceae)作物的主要害虫[1-4],在田间取食马铃薯叶和茎,可使马铃薯减产20%~30%[5];在储藏期,钻蛀取食薯块,引起马铃薯块茎干瘪或腐烂,非低温储藏时马铃薯为害率高达100%[3,6]。近年来,随着气候环境条件及种植结构的变化,该虫已成影响马铃薯生产的重要因素[7-8],使用化学农药仍是防治该虫的主要措施[7,9]。探索利用不同马铃薯品种对马铃薯块茎蛾的抗虫性及胁迫响应调控该虫为害已引起许多学者的关注[4-5,10-12],对于科学制定防控措施具有重要意义。
根际微生物在植物保护及植物生命活动中发挥着重要作用,其组成结构及多度的变化能反映植物健康状况[11-14]。不同植物的根际微生物群落组成结构不同,且随着植物的生长发育,根际微生物群落也随之发生变化。植物根际微生物除促进植物的正常生长发育、协助植物应对包括干旱、盐分、水、温度等非生物胁迫外[15],还诱导植物抵抗植物病原体和植食性昆虫等生物胁迫[13,16-17]。MUKHTAR 等[18]对盐水和非盐水土壤样品进行高通量测序分析,结果表明:土壤盐度会影响根际微生物,且放线菌在盐渍土样品中占主导地位,蛋白杆菌在非盐渍土壤样品中占主导地位;GOODWIN[19]研究指出:多种人参根际微生物具有提高人参产量的潜力;冯丹等[20]研究表明:蜡状芽孢杆菌CLY07 对南方红豆杉有明显促生长作用,能显著改善其幼苗生长状况,提高养分代谢能力。植物—害虫—根际微生物互作是目前国际上研究的重点和热点[11,13],监测健康和受胁迫根际的微生物群落种群和多度的变化过程,通过合理补充微生物种群可以调节重要农作物微生态平衡,实现单个或简单复配菌株无法实现的生态功能,从而提高农作物的产量、质量及抗病虫害能力。植物根际微生物引起植物防御反应功能从而协助植物对抗咀嚼式昆虫或病原微生物危害的报道较多[21-23],一些有益根际微生物可以协助植物抵御病虫害胁迫,如MAO 等[24]通过分析马铃薯黑胫病、疑似马铃薯黑胫病和健康环境马铃薯根际微生物,发现马铃薯黑胫病与根际微生物种群的组成密切相关;IDRISSI 等[25]分离筛选了不同地区的马铃薯块茎和根际微生物,发现有多种菌株对马铃薯黑胫病和块茎软腐病表现出不同程度的抑制作用;马铃薯地上叶片通过调节MDA、H2O2和可溶性糖的含量以及SOD 和POD活性对马铃薯块茎蛾取食胁迫表现出明显的生理响应[5,26]。
根际微生物在马铃薯抵御病虫害胁迫时发挥着重要作用[4,10],但目前鲜有关于蛀食性害虫取食胁迫后马铃薯根际细菌群落组成结构的研究,马铃薯根际细菌对马铃薯块茎蛾取食胁迫的响应尚不清楚。因此,本研究通过室内分离马铃薯块茎蛾取食胁迫后的马铃薯根际土壤,分析其中细菌微生物的组成结构和多样性,探究害虫取食胁迫对马铃薯根际细菌群落组成结构的影响,可为进一步筛选马铃薯根际有益微生物提供依据。
1 材料与方法
1.1 试验材料
供试马铃薯品种为青薯9 号;供试马铃薯块茎蛾为云南农业大学植物保护学院昆虫学实验室长期饲养建立的稳定种群。
供试LB 培养基:参考昌艳萍等[27]的方法配制,配方包括胰蛋白胨10 g,酵母提取物5 g,NaCl 10 g,琼脂15 g,水1 000 mL,调整pH 值为 7.0~7.2。
主要试剂及仪器:细菌通用引物27F (5 ′ -AGAGTTTGATCCTGGCTCAG-3 ′)和1492R (5 ′ -GGTTACCTTGTTACGACTT-3 ′)、TaqPCR Mix(擎科生物科技有限公司);LDZX-0L-I 立式高压蒸汽灭菌器(上海申安医疗器械厂)、2-16R 型离心机(湖南恒诺仪器设备有限公司)、Mastercycler®nexus 型PCR 仪(德国 Eppendorf 公司)和DYY-2C型电泳仪(北京六一生物科技有限公司)。
1.2 试验方法
1.2.1 样品采集和处理
采用云南农业大学后山农田土壤进行室内盆栽(10 cm×20 cm)种植青薯9 号马铃薯,待马铃薯第5 枝侧枝长出时进行马铃薯块茎蛾胁迫试验。接虫前对马铃薯块茎蛾3 龄幼虫进行饥饿处理12 h,之后在马铃薯每一侧枝接种马铃薯块茎蛾1 头,每株马铃薯接种5 头,每组设置3 个重复。取食胁迫3、7 和14 d 时,对接虫处理的马铃薯及空白对照组进行取样。
取样时将马铃薯整株挖出,抖落根际大块土壤,将马铃薯根收集到加有生理盐水25 mL的50 mL 无菌离心管中,剧烈摇动30 s,以12 377 r/min 离心10 min,去除上清液;用无菌镊子去除根组织,沉淀即为根际土壤[28];于-80 °C冰箱中保存备用。
1.2.2 细菌分离培养和纯化
采用传统分离培养法进行分离培养。在超净工作台上称取马铃薯根际土样 1.0 g,加入含有无菌水 9 mL 的离心管中充分振荡稀释,得到10-1土壤稀释液,并依次稀释至10-4、10-5和10-6,每个梯度 3 个处理。用移液枪吸取土壤稀释液50 μL涂布于LB 培养基,再将LB 培养基置于28 ℃恒温培养箱中培养2~3 d 后观察长出的菌落[29],并每天定时观察菌落颜色、形态、表面光滑度等,用无菌接种环将所有菌落挑取在新的LB 平板上进行纯化,反复纯化2~3 次得到单菌落。
1.2.3 细菌菌种鉴定
形态学鉴定:观察并记录菌落的形状和颜色、细胞大小等培养性状,并使用革兰氏染色法对所分离的细菌进行染色观察,记录细胞的形态及革兰氏阴性或阳性。
分子鉴定:采用冻溶法[30]提取所有分离纯化得到的根际土壤细菌菌株的基因组 DNA。分别从纯化的 LB 平板中挑取单菌落加入有无菌水500 μL 的2 mL 无菌离心管中,充分振荡,直至菌体与水混匀,将混匀的菌悬液置于液氮冰冻10 min,再沸水浴5 min,于12 000 r/min 下离心2 min,上清液即可作为PCR 模板备用。反应体系为25.0 μL,包括细菌16S rRNA 基因扩增通用引物27F 和1492R 各1.0 μL,细菌上清液1.0 μL,2×TaqPCR Mastermix 12.5 μL,ddH2O 9.5 μL。PCR 仪设置反应条件:94 ℃预变性5 min;94 ℃变性1 min,53 ℃退火1 min,72 ℃延伸2 min,32个循环;72 ℃延伸10 min。吸取 PCR 产物3 μL进行凝胶电泳检测,将合格的 PCR 产物送至上海生物工程股份有限公司进行双向测序。使用 CExpress 软件对测序结果进行比对和拼接,再将拼接后的序列提交到NCBI (https://blast.ncbi.nlm.nih.gov) 查找相似性最高的典型菌株并下载序列;使用MEGA 7 软件的邻位相连法和 Kimura 双参数矫正模型构建系统发育树,以重复抽样1 000 次进行 Bootstrap 验证,分析评估系统进化树拓扑结构的稳定性。
1.3 数据统计与分析
根据培养基上培养菌株的数量,并依据细菌形态学和分子学鉴定结果去除、整合重复的细菌菌株,按公式计算各菌株的相对多度:相对多度=单个菌株的菌落数/总菌落数×100%。采用Origin 2021 进行相对多度绘图。
2 结果与分析
2.1 马铃薯根际土壤可培养细菌的种类组成
根据菌落形态特征及鉴定结果去除重复菌株,得到马铃薯根际细菌菌株24 株(表1),分属于4 门11 科15 属22 种。胁迫3 d 时,马铃薯根际土壤细菌有8 种,分别为滋养节杆菌(Arthrobacter pascens)、大洋沉积物纤维芽孢杆菌(Cytobacillus oceanisediminis)、硝基愈创木胶类节杆菌(Paenarthrobacter nitroguajacolicus)、菜豆萎蔫病菌 (Curtobacterium flaccumfaciens)、稻壳罗塞略莫拉氏菌(Rossellomorea oryzaecorticis)、海水罗塞略莫拉氏菌(R.aquimaris)、长孢黄色链霉菌(Streptomyces longisporoflavus)和阿尔及利亚微杆菌(Microbacterium algeriense),其中处理组特有菌株为海水罗塞略莫拉氏菌、长孢黄色链霉菌和阿尔及利亚微杆菌;胁迫7 d 时,马铃薯根际土壤细菌有8 种,分别为滋养节杆菌、硝基愈创木胶类节杆菌、菜豆萎蔫病菌、稻壳罗塞略莫拉氏菌、马氏副球菌(Paracoccus marcusii)、加德那氏链霉菌 (Streptomyces gardneri)、叶片微杆菌(M.foliorum)和布鲁氏菌根瘤菌(Brucella rhizospha),其中处理组特有菌株为稻壳罗塞略莫拉氏菌和马氏副球菌;胁迫14 d 时,马铃薯根际土壤细菌有7 种,分别为滋养节杆菌、硝基愈创木胶类节杆菌、菜豆萎蔫病菌、产吲哚金黄杆菌(Chryseobacterium indologenes)、长孢黄色链霉菌、布鲁氏菌根瘤菌和阿氏普里斯特氏菌(Priestia aryabhattai),其中处理组特有菌株为产吲哚金黄杆菌和布鲁氏菌根瘤菌。
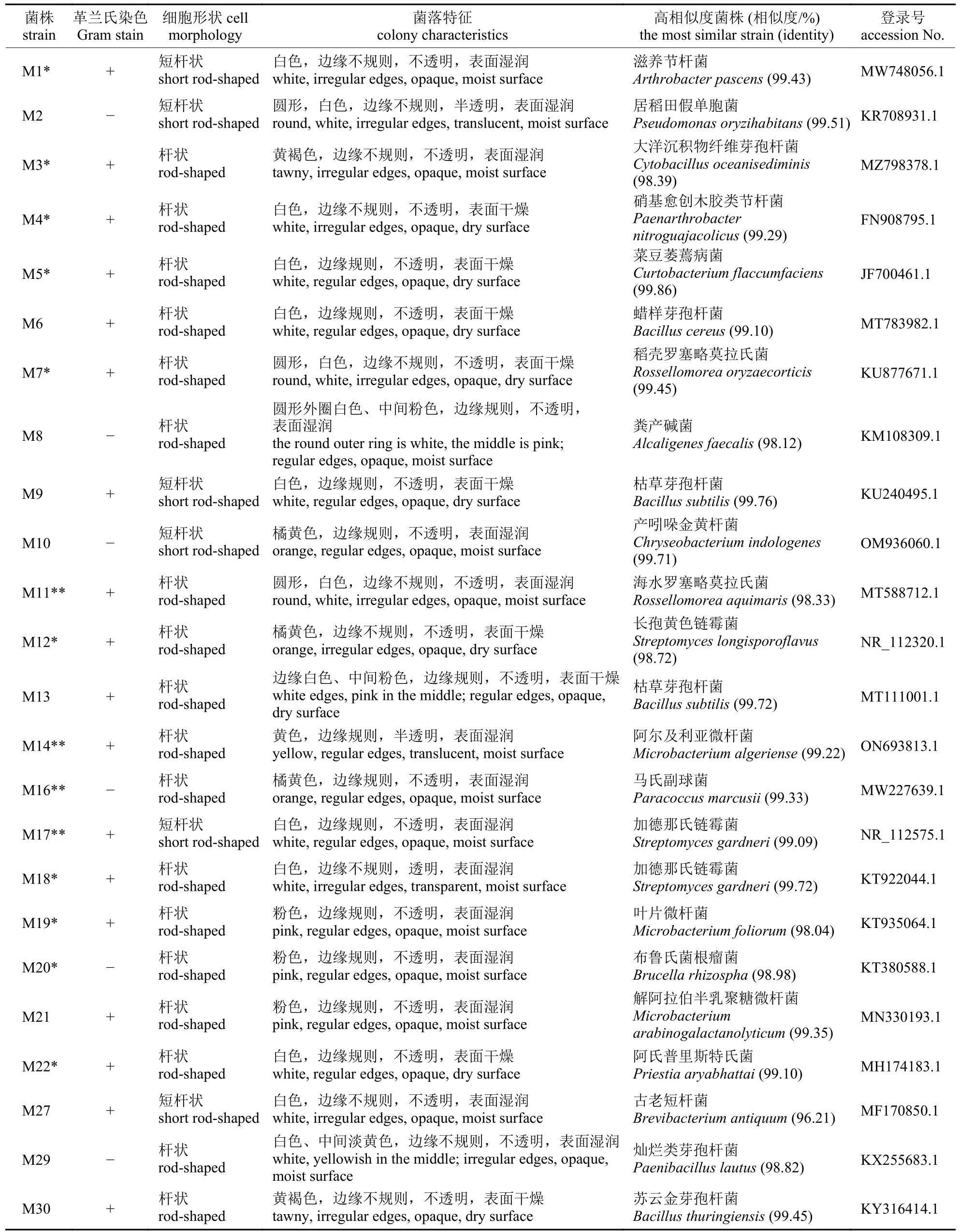
表1 马铃薯根际细菌菌落形态及种类组成Tab.1 Morphology and species composition of potato rhizosphere bacterial colonies
2.2 马铃薯根际可培养细菌的系统发育树
由图1 可知:系统发育树可聚为4 大支,第1 大支由放线菌门(Actinobacteria)短杆菌属(Brevibacterium)、链霉菌属(Streptomyces)、细杆菌属(Microbacterium)、类节杆菌属(Paenarthrobacter)、短小杆菌属(Curtobacterium)和节杆菌属(Arthrobacter)组成,第2 大支由厚壁菌门(Firmicutes)细胞杆菌属(Cytobacillus)、Rossellomorea和芽孢杆菌属(Bacillus)组成,第3 大支由变形菌门(Proteobacteria)产碱杆菌属(Alcaligenes)、生丝菌属(Hyphomicrobiales)、假单胞杆菌属(Pseudomonas)和副球菌属(Paracoccus)组成,拟杆菌门(Bacteroidetes)金黄杆菌属(Chryseobacterium)为第4 大支。其中,M1 和M4 分别与其模式菌株聚为1 小支后再聚为1 大支,M2 和M8 分别与其模式菌株聚为1 小支后再聚为1 大支,说明它们虽然不属于同一属但2 种菌之间亲缘关系较近;M12、M18 和M17 分别与其模式菌株聚为1 小支后再聚为1 大支,说明根际可培养细菌中的这些链霉菌属菌株亲缘关系较近。
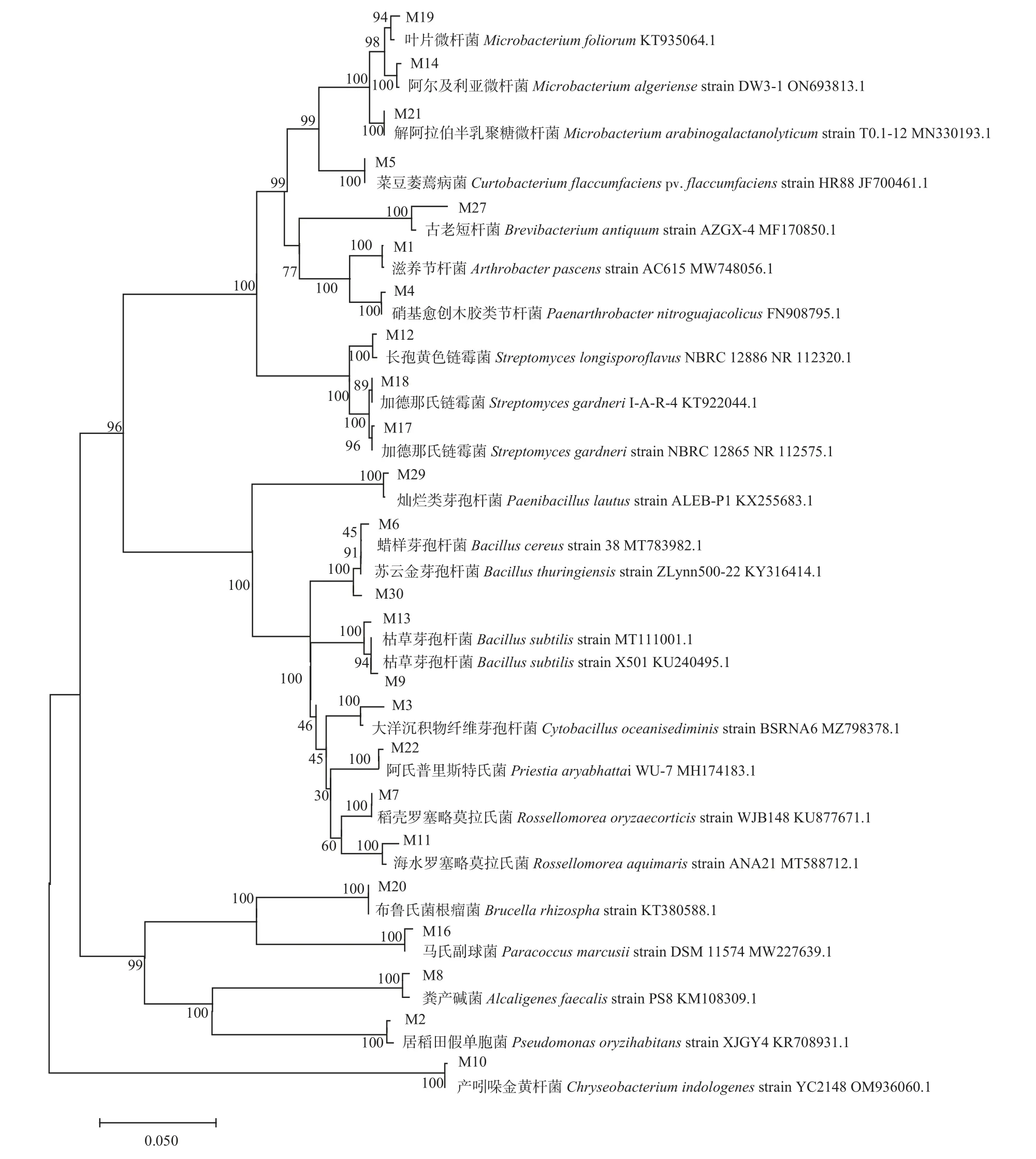
图1 基于16S rRNA 序列构建马铃薯根际可培养细菌系统发育树Fig.1 Phylogenetic tree of culturable rhizosphere bacteria under normal potato growth based on 16S rRNA sequence
2.3 马铃薯块茎蛾取食胁迫下马铃薯根际细菌的相对多度
由图2 可知:在门水平上,随着马铃薯块茎蛾胁迫时间的延长,根际细菌主要优势菌门均为放线菌门、变形菌门、厚壁菌门和拟杆菌门。与对照组相比,取食胁迫3、7 和14 d 时放线菌门细菌相对多度分别增加23.49%、12.56%和28.06%,其中在胁迫第3 天时放线菌门细菌相对多度最高。
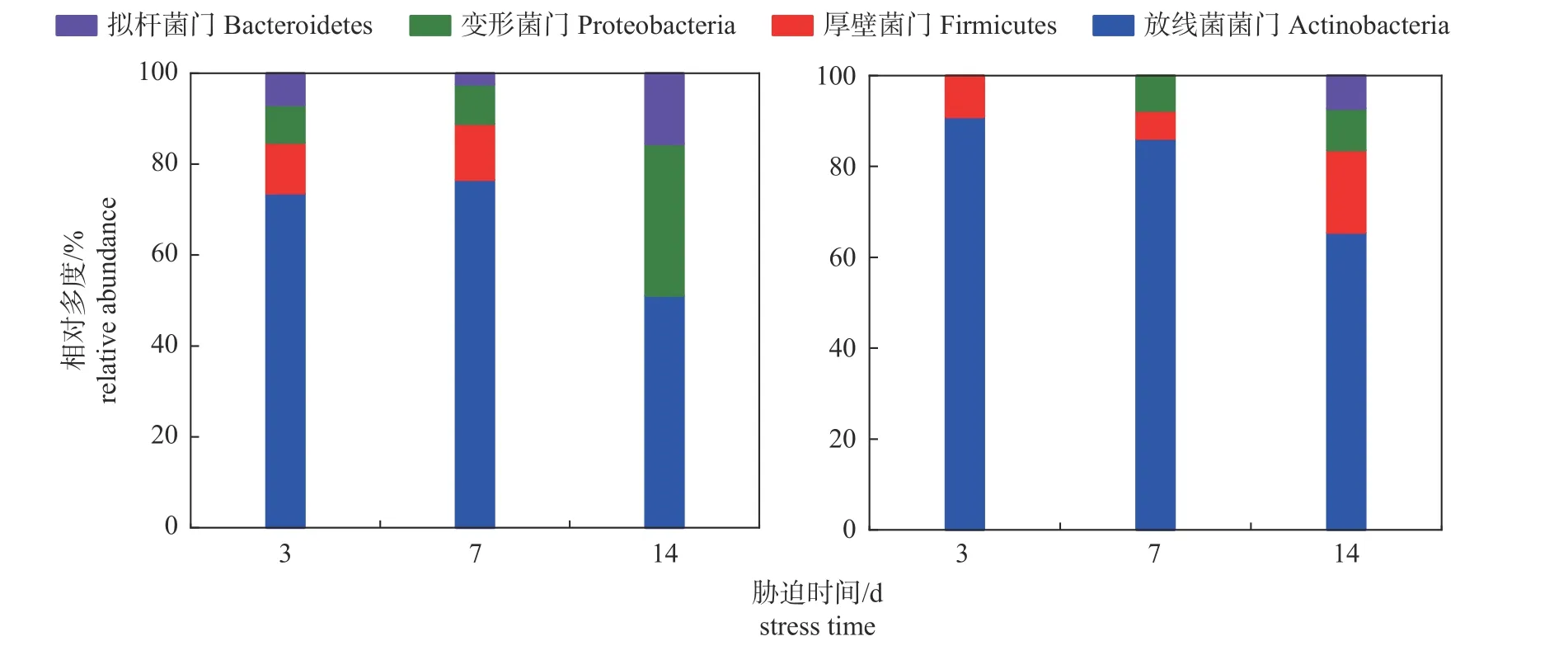
图2 对照组 (左) 和处理组 (右) 马铃薯根际细菌在门水平上的相对多度Fig.2 Relative abundance of potato rhizosphere bacteria at the phylum level in control group (left) and treatment group (right)
在科水平上,马铃薯块茎蛾取食胁迫影响了马铃薯根际可培养细菌的相对多度和多样性(图3)。与对照组相比,马铃薯块茎蛾胁迫后马铃薯根际细菌中微球菌科(Micrococcaceae)的相对多度增加,取食胁迫3、7 和14 d 时分别增加84.31%、70.78%和80.02%;微杆菌科(Microbacteriaceae)的相对多度在胁迫3 和7 d 时分别减少59.20%和35.20%。此外,马铃薯根际可培养细菌在科水平上的菌株多样性受马铃薯块茎蛾取食胁迫的影响有所降低,在处理第3 天时效果最为明显,随着胁迫时间的延长,该影响逐渐趋于平缓。

图3 对照组 (左) 和处理组 (右) 马铃薯根际细菌在科水平上的相对多度Fig.3 Relative abundance of potato rhizosphere bacteria at the family level in control group (left) and treatment group (right)
在属水平上,马铃薯块茎蛾取食胁迫改变了马铃薯根际细菌的优势菌属(图4)。与对照组相比,取食胁迫后马铃薯根际细菌中节杆菌属的相对多度增加,在胁迫3、7 和14 d 时分别增加103.50%、65.37%和28.57%;短小杆菌属的相对多度在胁迫3 和7 d 时分别减少69.49%和32.03%,在胁迫14 d 时增加63.64%。此外,取食胁迫降低了马铃薯根际细菌在属水平上的细菌多样性。
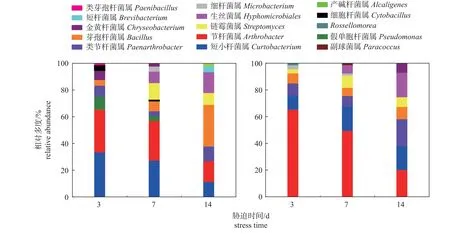
图4 对照组 (左) 和处理组 (右) 马铃薯根际细菌在属水平上的相对多度Fig.4 Relative abundance of potato rhizosphere bacteria at the genus level in control group (left) and treatment group (right)
综上所述,马铃薯块茎蛾取食胁迫第3 天时马铃薯根际细菌相对多度变化最明显,随着处理时间的延长,影响效果逐渐减弱;胁迫14 d时,马铃薯块茎蛾取食胁迫与对照组之间的差异最小。
3 讨论
根际是植物与土壤接触的直接区域,生存着大量的微生物和无脊椎动物,其环境具有高度复杂的特点。植物根系通过分泌物吸引大量特定的土壤微生物,了解根际生态独特的动态变化过程有助于更好地进行马铃薯田间栽培管理[31]。本研究发现:马铃薯块茎蛾胁迫后,马铃薯根际细菌优势菌门均为放线菌门、厚壁菌门、变形菌门和拟杆菌门。高天鹏等[32]以碱蓬和骆驼蓬为试验材料,通过高通量测序技术分析可知:植物根际细菌中变形菌门、厚壁菌门、放线菌门和酸杆菌门为优势菌门;王莉莉等[33]发现:干旱胁迫前后,马铃薯冀张薯8 号和夏波蒂苗期根际细菌优势菌门均为变形菌门、放线菌门、酸杆菌门、绿弯菌门和拟杆菌门;李华伟等[34]对闽薯2 号的研究显示:晚疫病改变了马铃薯根际细菌的相对多度,但对其组成结构影响不大,本研究也得到相似结果。可见,马铃薯块茎蛾取食胁迫后,马铃薯根际微生物主要组成趋于一致,但相对多度存在差异,反映了马铃薯对马铃薯块茎蛾取食危害的胁迫响应与其他植物相近,但相对多度的差异是否也是马铃薯对块茎蛾的抗性机理之一还需要进一步研究。此外,本研究仅测定了马铃薯根际可培养细菌组成结构及多样性的变化,其根际不可培养细菌组成结构及多样性的变化也有待进一步研究。
有研究指出:放线菌门细菌是田间土壤中的典型有益细菌种群,其含有大量的植物促生功能菌和病原拮抗菌,为植物获取生长发育所需的营养物质提高了效率,对植物生长起促进作用,同时还能抑制土传病原微生物侵染,在生物防治方面有大量的应用[35-37]。本研究中,马铃薯块茎蛾取食胁迫增加了根际细菌中放线菌门的相对多度,但随着处理时间的延长,放线菌门相对多度的增加效果逐渐减弱,这可能是马铃薯植株在受到害虫胁迫时,通过某种途径捕获了对植物有促生作用的放线菌门菌株,从而提高了马铃薯对马铃薯块茎蛾取食胁迫的抗性。从马铃薯块茎蛾取食胁迫下马铃薯根际土壤中可培养细菌的属水平看,正常生长和马铃薯害虫胁迫后的马铃薯根际可培养细菌的组成和相对多度均存在明显差异,说明马铃薯块茎蛾胁迫对其产生了影响。有研究指出:根系分泌物是植物调控根际微生物组成结构的主要方式[38-39],而生物胁迫又会使植物向根际土壤中释放多种生物活性化合物来抵御食草动物侵害[40],推测马铃薯块茎蛾的取食胁迫影响了马铃薯根系分泌物,从而进一步改变了其根际微生物的组成结构。
已有研究表明:节杆菌属的多种菌株对植物生长有促生作用。VANISSA 等[41]研究表明:对玉米接种节杆菌属细菌后,限制了植物对钠离子的吸收,增加了对钾离子的吸收,促进了植株生长;KIM 等[42]研究表明:土壤节杆菌属细菌增强了水稻的耐寒性。本研究中,马铃薯块茎蛾取食胁迫使马铃薯根际细菌中节杆菌属相对多度明显增加,随着处理时间的延长,增加的节杆菌属相对多度逐渐降低,这可能是马铃薯植株在受到马铃薯块茎蛾取食胁迫后吸引了具有促生作用的根际节杆菌属来抵御胁迫,增强了对马铃薯块茎蛾取食胁迫的抗性。植物根际中放线菌门和节杆菌属菌株对增强植物抗逆性及促生作用的机制值得深入研究。
4 结论
马铃薯块茎蛾取食胁迫后,马铃薯植株根际可培养细菌的组成结构及物种多样性与正常生长的植株有明显差异,改变了放线菌门和节杆菌属菌株的相对多度。研究结果为系统研究马铃薯—根际细菌—马铃薯块茎蛾的互作关系及马铃薯抗虫机理提供了依据。

