高温烟气活化生物炭制备活性炭及其Cu2+吸附性能
骆美宇,李 音,刘玉鹏,邸 婧,单胜道,盖希坤
(1.浙江科技学院 生物与化学工程学院,浙江 杭州 310023;2.杭州职业技术学院 生态健康学院,浙江 杭州 310018;3.中国林业科学研究院 林产化学工业研究所,江苏 南京 210042)
重金属污染具有生物毒性、生物不可降解性和生物累积等特征,对生态环境和人体健康造成巨大威胁[1]。Cu2+是水体中常见的重金属污染物,及时去除污染水体的Cu2+成为当前研究的热点[2]。活性炭因具有比表面积大、孔隙结构发达、孔径分布广泛和表面官能团丰富等优点,被认为是去除重金属的最佳吸附剂。传统的活性炭制备以煤为主要原料,存在成本高、污染大的缺点。生物质是自然界中唯一含碳的清洁可再生能源,具有资源丰富、硫氮含量低,以及生长利用全生命周期零碳排放的优点,是更具潜力的活性炭原料。开发农林废弃生物质高效清洁制备活性炭技术,对于实现国家双碳战略目标具有重大意义[3]。
生物质热解通常是指在无氧或低氧环境下,生物质被加热引起分子分解产生焦炭、可冷凝液体和气体产物的过程[4]。国内外学者对生物质热解技术已进行了多年研究,包括反应器的设计、工艺条件的优化等。本课题组[5-6]在综合分析了我国农林废弃生物质资源特性、分布状况、投资规模和市场需求的基础上,提出了生物质快速热解分级提质多联产技术。其中,生物质快速热解后生成一部分生物炭,由于热解过程中产生的焦油状物质和无定形碳堵塞了生物炭的孔隙结构,导致其比表面积降低,吸附性能受到限制[7]。目前,生物炭主要被用于燃料、土壤改良[8]等,附加值并不高,对生物炭进行活化制备活性炭可大大提高生物炭的利用价值。活化方法主要包括物理活化和化学活化。其中,化学活化由于化学试剂的掺入不仅增加了制备成本,而且会产生有毒有害物质,可能造成二次污染;物理活化具有成本低、污染小、操作简单等优点,越来越受到人们的关注[9]。物理活化的活化剂一般采用CO2、水蒸气、空气或其两种或者三种的混合物等。ETTⅠSH 等[10]使用CO2活化肉桂棒,发现最佳活化温度为900 °C,活化时间为2 h,CO2流量为150 cm3/min,对氯吡硫磷的最大单层吸附量为12.37 mg/L。MAⅠ等[11]使用不同比例的CO2-水蒸气为活化剂,活化线状二毛蕨(D.linearis)制备活性炭,发现活性炭的比表面积随着水蒸气比例的增多而增大,水蒸气促进了介孔的产生,通过调控CO2与水蒸气的比例,可以制备具有不同空隙结构的活性炭。目前,国内外对生物质活化的研究较多,对生物炭活化的研究较少。结合工艺特点,开发生物炭连续低成本的活化方法成为该领域研究的重点。
在正常工况下,流化床燃烧炉出口的高温烟气主要由N2和CO2组成,将高温烟气作为活化剂活化生物炭能够充分利用高温烟气的热量和CO2,大大降低活性炭的制备成本,提高生物质快速热解分级提质多联产技术的经济性。为了提高高温烟气的活化效率,本研究向高温烟气中通入水蒸气,研究混合气体对马尾松生物炭的活化效果,考察水蒸气流量、活化温度和活化时间对活性炭碘吸附值和产率的影响,对活化条件进行优化,并探索pH、吸附时间、活性炭投加量、Cu2+初始浓度(质量浓度)等对活性炭吸附性能的影响规律,通过拟合动力学和吸附等温线模型探究吸附机理。
1 实验部分
1.1 实验原料与试剂
马尾松生物炭由实验室自制。马尾松生物炭的分析结果见表1,工业分析和元素分析以干燥基为基准,固定碳和氧元素通过差减法求得。

表1 马尾松生物炭的分析结果Table 1 Analysis results of Masson pine biochar
碘、碘酸钾、盐酸、五水硫酸铜、氢氧化钠、硫代硫酸钠、无水碳酸钠,上海凌峰化学试剂有限公司;可溶性淀粉、碘化钾,上海阿拉丁生化科技股份有限公司,以上化学试剂皆为分析纯。
1.2 实验仪器
SKGL-1200C 超值开启式管式炉,上海钜晶精密仪器制造有限公司;干燥箱,上海一恒科学仪器有限公司;HL-2B 数显恒流泵,上海驰唐电子有限公司;THZ-92C 气浴恒温振荡器,上海博迅实业有限公司医疗设备厂;Autosorb-ⅠQ-C全自动物理化学吸附仪,美国康塔仪器公司;SU1510扫描电镜(SEM),日本日立公司;VERTEX70 傅里叶变换红外光谱仪(FTⅠR),德国Bruker 公司;Avio 200 电感耦合等离子体发射光谱仪,美国PerkinElmer仪器有限公司。
1.3 活性炭的制备
称取(6 ± 0.1) g马尾松生物炭放入石英舟,将石英舟放入石英管(石英管内径为28 mm、长为85 cm),然后将石英管放入开启式管式炉。开启N2瓶阀门,通气20 min以排除管内空气。20 min后,继续通入N2,设置管式炉以10 °C/min的升温速率升至活化温度,然后,打开CO2气瓶阀门和数显恒流泵以通入CO2与水蒸气。其中,N2和CO2的体积流量比为78:21,模拟高温烟气组成;固定高温烟气流量为100 mL/min,水蒸气流量为0.00~1.85 mL/min,保持1.0~2.5 h活化时间进行恒温处理,具体的制备条件如表2 所示。活化结束后,关闭CO2气瓶阀门与恒流泵,活性炭在N2氛围下自然冷却至室温,关闭管式炉,取出活性炭放入干燥箱,105 °C下干燥4 h,冷却后称重,计算产率。活性炭产率计算方法见式(1):

表2 制备条件Table 2 Preparation conditions
式中,Y为活性炭产率,%;m和m0分别为活性炭和马尾松生物炭的质量,g。
1.4 活性炭的表征
按照GB/T 12496.8—2015《木质活性炭试验方法碘吸附值的测定》测定活性炭碘吸附值。称取一定量试样放入锥形瓶,加入10 mL盐酸加热至微沸,冷却后加入50 mL已标定的碘标准溶液,振荡15 min后过滤。吸取10 mL滤液加入装有10 mL去离子水的锥形瓶,用已标定的硫代硫酸钠标准溶液滴定,滴定完成后记录使用的硫代硫酸钠体积数,通过公式计算碘吸附值。
采用全自动物理化学吸附仪测定活性炭的比表面积和孔径分布,以氮气为吸附介质,在77.35 K下进行N2吸/脱附测定,测试前样品在180 °C 脱气6 h 以除去水等杂质,根据Brunauer Emmett Teller(BET)方程计算活性炭的比表面积,采用Density functional theory(DFT)模型分析活性炭的孔径分布;采用扫描电镜观测马尾松生物炭和活性炭的表面形貌,样品在分析前先进行喷金处理,检测电压为15 kV;采用傅里叶变换红外光谱仪测定马尾松生物炭和活性炭的表面官能团,使用KBr 压片法,波数4000~400 cm-1,分辨率为4 cm-1,扫描速率为32 min-1。
1.5 活性炭对Cu2+的吸附实验
用CuSO4•5H2O配制Cu2+浓度为1 g/L的标准母液,进而用于配制不同浓度的Cu2+溶液。准确量取100 mL不同浓度的Cu2+溶液移入锥形烧瓶,加入浓度均为0.1 mol/L的NaOH和HCl用于调节溶液pH,加入不同质量的活性炭,在恒温振荡器内25 °C、120 r/min 的条件下振荡一定时间,然后取溶液经0.22 µm滤膜过滤,用Avio 200电感耦合等离子体发射光谱仪测定溶液中剩余Cu2+浓度。活性炭对Cu2+的吸附量和去除率计算方法分别见式(2)和式(3):
式中,qt为t时刻的吸附量,mg/g;C0和Ct分别为初始和t时刻的Cu2+浓度,mg/L;V为Cu2+溶液体积,L;me为活性炭投加量,g;η为Cu2+去除率,%。
2 结果与讨论
2.1 工艺参数对活性炭碘吸附值和产率的影响
2.1.1 水蒸气流量的影响
当活化温度为850 °C,活化时间为2.0 h 时,考察了水蒸气流量对活性炭碘吸附值和产率的影响,影响结果如图1 所示。由图1 可知,水蒸气的加入明显降低了活性炭的产率,但提高了活性炭的吸附性能。随着水蒸气流量的增加,活性炭产率不断降低,碘吸附值先增大后减小,在水蒸气流量为0.9 mL/min 时,碘吸附值达到最大值为1861 mg/g,此时活性炭产率为14.58%。CO2与碳原子的反应速率慢、活性低,温度在1000 °C以上时才能达到较好反应状态,而水蒸气与碳原子在较低温度下就能充分反应[12]。本实验中,通入适量的水蒸气可以促进与碳原子的反应,生成CO和H2并从表面溢出,引起闭孔打开和扩宽。水蒸气与碳原子发生的主要反应见式(4)~式(6)[13]。随着通入水蒸气流量的继续增大,扩孔反应成为了主导反应,导致微孔结构遭到破环,微孔发生膨胀甚至坍塌,微孔率降低[14],因此碘吸附值逐渐下降。
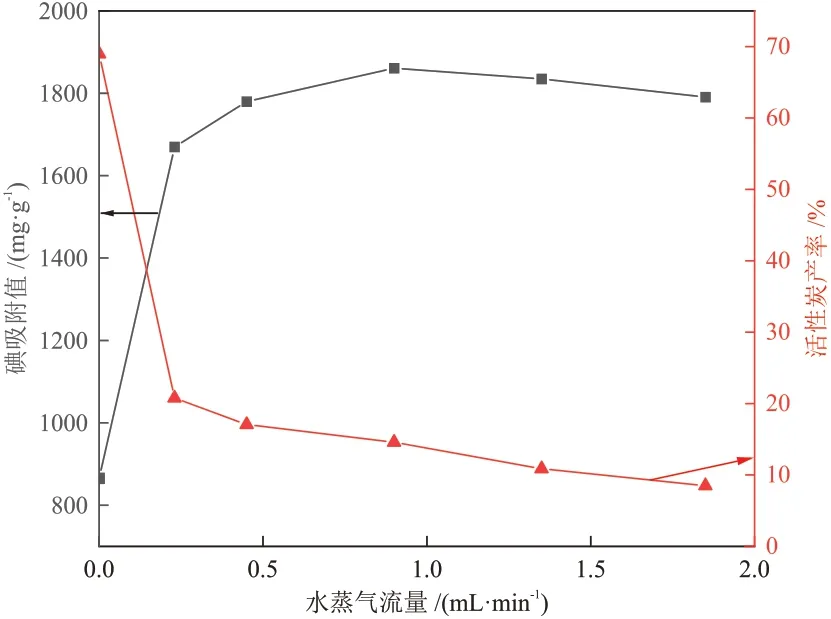
图1 水蒸气流量对碘吸附值和活性炭产率的影响Fig.1 Effect of water vapor flow rate on iodine adsorption value and activated carbon yield
2.1.2 活化温度的影响
由于流化床燃烧炉的出口温度通常最高为850 °C,本实验选择实验温度范围为700~850 °C。当水蒸气流量为0.9 mL/min、活化时间为2.0 h,考察了活化温度对活性炭碘吸附值和产率的影响,如图2所示。
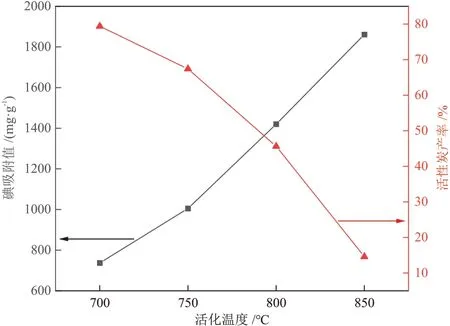
图2 活化温度对碘吸附值和活性炭产率的影响Fig.2 Effect of activation temperature on iodine adsorption value and activated carbon yield
随着活化温度的升高,碘吸附值逐渐增大,而活性炭产率单调降低。碳原子与活化气体反应需要较高的活化能,低温时,活性碳原子没有足够的能量,因此反应不够充分[15]。随着活化温度升高,碳原子活性增强,反应速率加快,碳原子以及孔隙中堵塞的物质与CO2、水蒸气反应,转化为挥发性物质不断逸出,碳原子不断消耗,促进了微孔和中孔的产生[16],因此碘吸附值增大,产率减少。
2.1.3 活化时间的影响
活化时间直接影响到活化反应器的体积和成本,活化时间越长,则活化反应器的体积越大、成本越高,因此,反应时间不宜太长。本实验考察的最大活化时间为2.5 h。当水蒸气流量为0.9 mL/min,活化温度为850 °C时,活化时间对活性炭碘吸附值和产率的影响如图3 所示。随着活化时间的增加,碘吸附值不断升高,活性炭产率不断降低。这是因为活化时间短时,活化气体与生物炭的反应不充分;活化时间越长,越多的水分子扩散到颗粒表面参与反应,碳原子不断被消耗,堵塞的孔不断被打开[15]。因此活性炭的碘吸附值逐渐提高,活性炭产率逐渐降低。
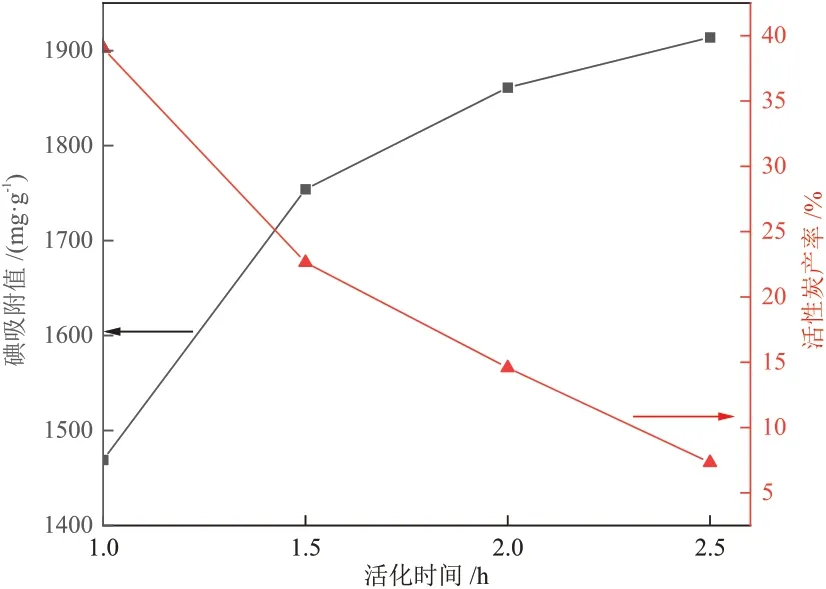
图3 活化时间对碘吸附值和活性炭产率的影响Fig.3 Effect of activation time on iodine adsorption value and activated carbon yield
综合以上分析,马尾松生物炭制备活性炭的最佳工艺条件为:高温烟气100 mL/min、水蒸气流量0.9 mL/min、活化温度850 °C、活化时间2.5 h。该条件下制备的活性炭碘吸附值为1914 mg/g,活性炭产率为7.32%。因此,后续的表征和吸附Cu2+实验均采用此活化条件下制备的活性炭。
2.2 活性炭表征结果分析
2.2.1 孔结构分析
活性炭的比表面积和孔隙结构关系着活性炭表面的活性位点,通常较大的比表面积以及丰富的孔隙结构有利于加快离子扩散速率,提高吸附性能[17]。图4(a)和(b)分别为未加水蒸气制备的活性炭以及0.9 mL/min水蒸气下制备的活性炭的N2物理吸附等温线和孔径分布。由图4(a)可知,无水蒸气时的符合Ⅰ型等温线,表明活性炭以微孔为主;0.9 mL/min水蒸气时的符合Ⅳ型等温线,p/p0在0.05~0.1时出现明显的H4 型回滞环,这是因为存在毛细冷凝现象,说明水蒸气促进了介孔的产生,活性炭中存在一定数量的介孔[18]。由图4(b)可知,两者均有明显的微孔峰(<2 nm),无水蒸气时的微孔含量更小,且孔径主要集中在0~4 nm,而0.9 mL/min 水蒸气时的活性炭在4~30 nm 显示出中孔特征,具有更宽的孔径分布。2 种活性炭的孔结构参数如表3 所示。由表3 可知,活性炭比表面积增加了874 m2/g,总孔容与微孔孔容均有所提高,但微孔率明显降低。总的来说,水蒸气的加入具有增孔和扩孔的作用,更大的比表面积和更广泛的孔径分布更有利于活性炭在吸附中的应用。
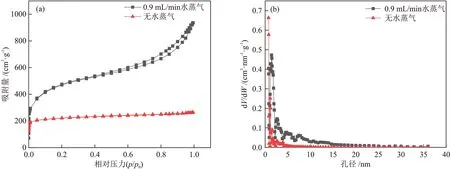
图4 活性炭的N2吸/脱附等温线(a)和孔径分布(b)Fig.4 N2 adsorption/desorption isotherms (a) and pore size distribution (b) of activated carbon

表3 活性炭的孔结构参数Table 3 Pore structure parameters of activated carbon
2.2.2 SEM结果分析
通过SEM得到样品的表面形貌,马尾松生物炭与最佳制备条件下的活性炭在不同放大倍数下的SEM照片如图5所示。
由图5(a)、(b)可知,马尾松生物炭结构紧密,呈长条状,表面粗糙且凹凸不平,存在孔道结构,但裂缝和孔隙较少,孔隙结构并不发达。由图5(c)、(d)可知,经混合气体活化后的活性炭保留了生物炭的基本形状,但经活化气体烧蚀后,结构变得疏松,为吸附质提供了大量有效吸附位点。
2.2.3 FTⅠR结果分析
活性炭的表面官能团是影响其吸附性能的关键因素。马尾松生物炭与活性炭表面含有多种官能团,如图6 所示。马尾松生物炭在3423 cm-1处的吸收峰是由O—H键的伸缩振动引起的,在2918 cm-1附近的吸收峰为甲基或亚甲基C—H键的伸缩振动峰[19],位于2345 cm-1附近的吸收峰为C==C键的伸缩振动峰,1596 cm-1处的吸收峰为酮和醛的羰基C==O键的伸缩振动峰[20],1436~1383 cm-1处的吸收峰与酯基—COOC—有关,1187 cm-1处的吸收峰与醇、酚、酯的C—O键伸缩振动有关[21],856~693 cm-1附近的吸收峰则是由芳烃C—H键的平面外弯曲振动引起的[22]。
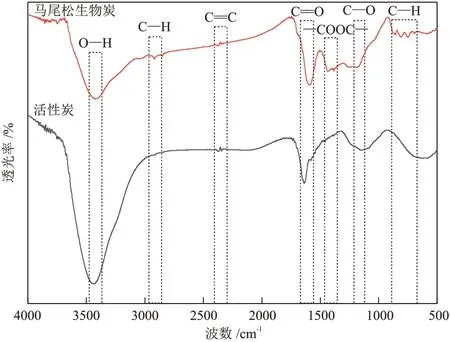
图6 马尾松生物炭与活性炭的FTIR谱图Fig.6 FTIR spectra of Masson pine biochar and activated carbon
与马尾松生物炭的红外光谱图相比,活性炭在2918 cm-1、1436~1383 cm-1以及856~693 cm-1处几乎不存在吸收峰,C—H 键的消失说明原料已经完全被碳化;而—COOC—的消失是因为热解炭中残留的挥发性化合物在活化过程中不断挥发逸出[11]。位于3434 cm-1处的O—H键吸收峰以及1145 cm-1处的C—O键吸收峰强度增加明显,说明马尾松活性炭含有更多的含氧官能团。含有O—H、C—O、C==C 和C==O键等化学键的官能团提供了充足的吸附位点,可能导致Cu2+以与官能团形成表面络合物的形式除去[19]。
2.3 吸附Cu2+实验结果分析
2.3.1 溶液pH对Cu2+吸附性能的影响
在实验中发现,当溶液pH 接近6 时,溶液出现浑浊,说明此时已发生Cu(OH)2沉淀,再进行吸附研究已无意义,因此本实验选择pH 范围为2.5~5.5。固定Cu2+溶液为20 mg/L,活性炭投加量为1 g/L,吸附时间为30 min,考察溶液pH对Cu2+去除率和吸附量的影响,如图7所示。
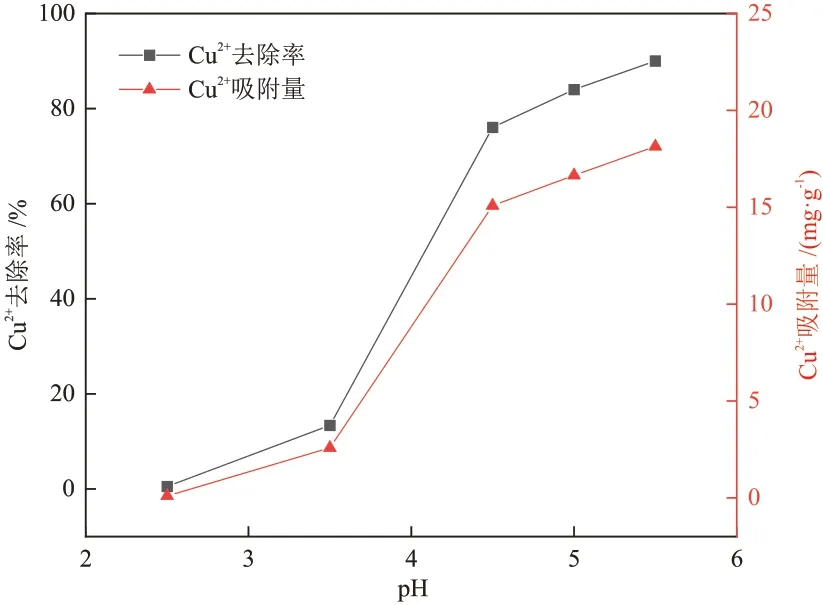
图7 pH对Cu2+去除率和吸附量的影响Fig.7 Effect of pH on Cu2+ removal rate and adsorption capacity
当溶液pH为2.5时,Cu2+去除率和吸附量极低,几乎接近于0;pH 为2.5~5.5 时,Cu2+去除率和吸附量随着pH的增加不断增大;Cu2+去除率和吸附量在pH 为5.5 时达到最大值,去除率为90.02%,吸附量为18.14 mg/g。这是因为pH 会影响溶液中的离子分布以及活性炭的表面官能团和电荷。pH 影响静电作用,pH低时,溶液中存在大量H+,H+与Cu2+存在竞争关系,占据了部分吸附活性位点[21];pH增大,溶液中H+浓度降低且活性炭表面官能团发生解离,使更多的活性位点裸露出来,增加了Cu2+与活性位点结合的机会[23]。综上,选取5.5为后续实验的pH值。
2.3.2 吸附时间对Cu2+吸附性能的影响
固定Cu2+溶液为20 mg/L,活性炭投加量为1 g/L,溶液pH 为5.5,考察吸附时间对Cu2+去除率和吸附量的影响,如图8 所示。吸附时间在0~5 min,活性炭对Cu2+的去除率和吸附量迅速升高;5~30 min,去除率和吸附量上升缓慢;30 min后,吸附达到平衡。30 min时,去除率最高为90.02 %,吸附量为18.14 mg/g;吸附刚开始时,活性炭表面还存在大量活性吸附位点,且Cu2+溶液与活性炭表面Cu2+浓度差较大,意味着具有较强的吸附推动力,因此去除率和吸附量增大且速率很快[24]。随着吸附时间的增加,活性炭Cu2+去除率和吸附量增加缓慢,一是因为活性炭上可利用的吸附位点减少,活性炭表面与溶液中Cu2+的静电斥力越来越强[23];二是因为Cu2+溶液与活性炭表面浓度差越来越小,导致吸附推动力减少,Cu2+在微孔内的扩散速率缓慢[25]。
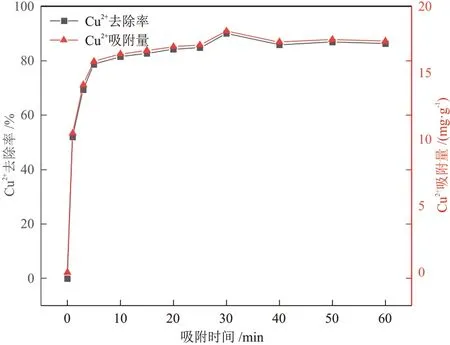
图8 吸附时间对Cu2+去除率和吸附量的影响Fig.8 Effect of adsorption time on Cu2+ removal rate and adsorption capacity
2.3.3 活性炭投加量对Cu2+吸附性能的影响
固定Cu2+溶液为20 mg/L,溶液pH 为5.5,吸附时间为30 min,考察活性炭投加量对Cu2+去除率和吸附量的影响,如图9 所示。Cu2+去除率随着活性炭投加量的增加而增大,当活性炭投加量增加到1.5 g/L 时,去除率达到99.24 %,之后基本保持稳定。Cu2+吸附量随着活性炭投加量的增加先上升后降低,投加量为1 g/L时,吸附量最大,为18.14 mg/g。从去除率看,投加量增加,可供吸附的活性吸附位点增多,吸附平衡后剩余的Cu2+浓度降低,又因Cu2+初始浓度一定,因此去除率增大。投加量为1.5 g/L时,吸附达到饱和,去除率基本保持稳定,接近100%。从吸附量看,投加量较少时,Cu2+能够充分被吸附,因此吸附量上升。投加量大于1 g/L 后,吸附平衡在较低浓度下建立,再增加投加量,单位质量的活性炭吸附的Cu2+数量减少,因此吸附量降低。最终确定去除率最大时的活性炭投加量为1.5 g/L。
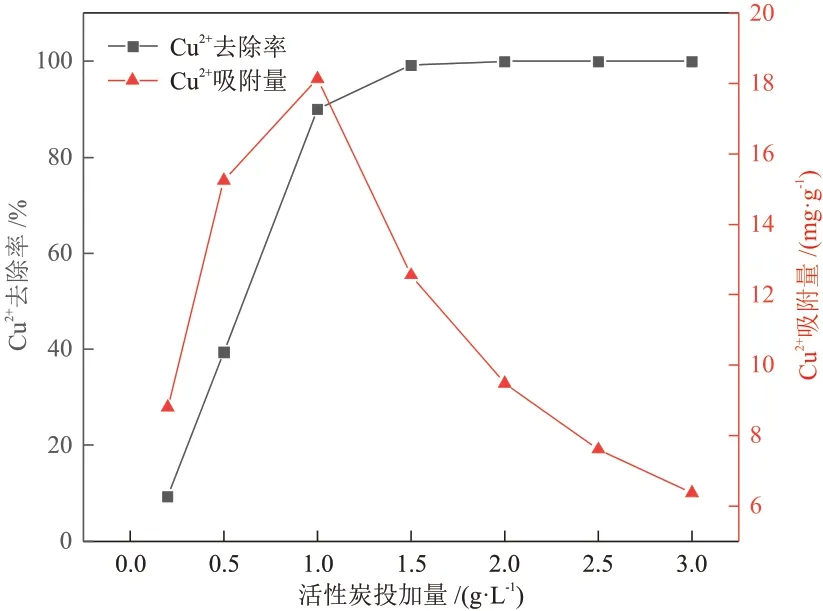
图9 活性炭投加量对Cu2+去除率和吸附量的影响Fig.9 Effect of activated carbon dosage on Cu2+ removal rate and adsorption capacity
2.3.4 Cu2+初始浓度对Cu2+吸附性能的影响
固定溶液pH为5.5,吸附时间为30 min,活性炭投加量为1.5 g/L,Cu2+初始浓度对Cu2+去除率和吸附量的影响如图10 所示。随着Cu2+初始浓度的增加,Cu2+吸附量不断增大,去除率不断减少。Cu2+初始浓度较低时,活性炭表面有充足的吸附位点吸附少量的Cu2+,Cu2+去除率较大,Cu2+吸附量快速增大。随着初始浓度的增加,活性炭上的活性位点趋于不足,导致剩余Cu2+增多,影响溶液中Cu2+与活性炭表面的相互作用[26],从而Cu2+去除率降低,Cu2+吸附量上升缓慢。
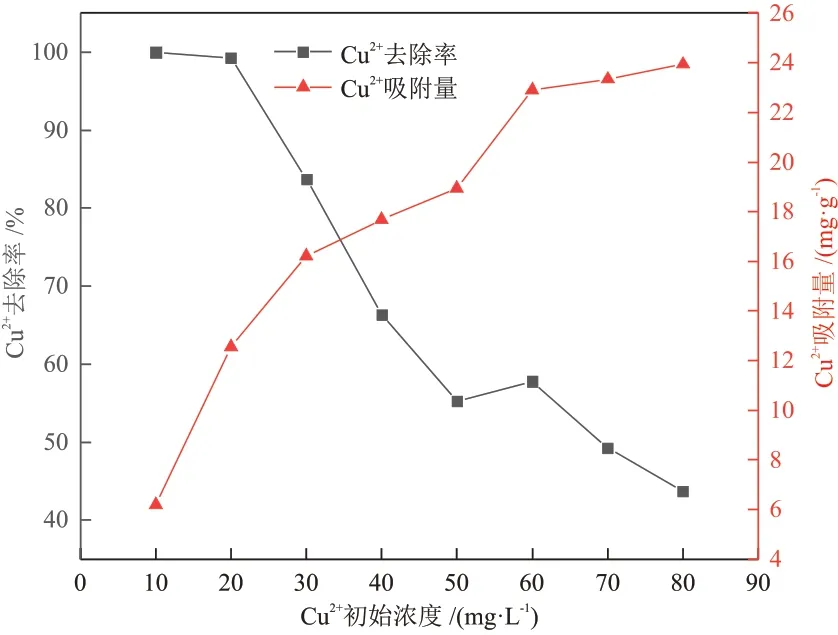
图10 Cu2+初始浓度对Cu2+去除率和吸附量的影响Fig.10 Effect of initial Cu2+ concentration on Cu2+ removal rate and adsorption capacity
2.4 吸附动力学模型
吸附动力学是了解吸附机制和活性炭对Cu2+的吸附速率的重要途径。在吸附温度为25 °C、Cu2+初始浓度为20 mg/L、溶液pH 为5.5、活性炭投加量为1 g/L 的条件下,得到不同吸附时间的吸附量(qt,mg/g)。对实验数据进行拟合,分别采用准一级动力学模型(式(7))、准二级动力学模型(式(8))以及颗粒内扩散模型(式(9))对Cu2+的吸附过程进行拟合。
式中,qe为吸附平衡时的吸附量,mg/g;t为吸附时间,min;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g/(mg·min);kid为颗粒内扩散速率常数,mg/(g·min)0.5;C1为边界层有关的常数,mg/g。
准一级、准二级动力学模型拟合结果如图11(a)和表4所示。
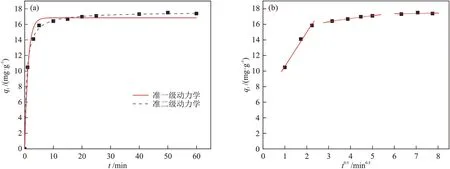
图11 活性炭对Cu2+的吸附动力学模型(a)和颗粒内扩散拟合曲线(b)Fig.11 Adsorption kinetics models (a) and intraparticle diffusion fitting curve (b) of Cu2+ on activated carbon

表4 吸附动力学模型参数Table 4 Adsorption kinetics model parameters
通过回归系数R2以及比较qe值来评估拟合的准确性。准二级动力学模型R2的值为0.9990,高于准一级动力学,且计算出的平衡吸附量qe(17.61 mg/g)与实验结果(18.14 mg/g)更加接近,说明活性炭对Cu2+的吸附遵循准二级动力学模型,以化学吸附为主,吸附速率取决于吸附容量[27]。
采用颗粒内扩散模型进一步分析吸附过程,如图11(b)所示。吸附分为3个阶段,第一阶段为液膜扩散,Cu2+通过液膜迅速吸附到活性炭外表面,扩散速率较快;第二阶段为颗粒内扩散,Cu2+扩散进入活性炭孔隙中;第三阶段为吸附平衡阶段。3 段的拟合曲线均未通过原点,说明颗粒内扩散不是唯一的速率控制步骤[28]。
2.5 吸附等温线模型
为进一步探究活性炭对Cu2+的吸附过程及机理,在25 °C,得到不同Cu2+初始浓度下的平衡Cu2+剩余浓度Ce和平衡吸附量qe,采用Langmuir 模型(式(10))和Freundlich模型(式(11))对数据进行拟合。
式中,Ce为吸附平衡时的Cu2+浓度,mg/L;qm为最大吸附量,mg/g;KL为Langmuir 吸附平衡常数,L/mg;KF为Freundlich吸附平衡常数,(mg/g)/(mg/L)1/n;n为Freundlich模型常数,和吸附强度有关,n值越大,代表吸附越容易发生。
式(12)用于表达Langmuir 等温模型的可行性,RL为分离因子。当RL=0 时,吸附是不可逆的;当0
活性炭对Cu2+的温吸附模型如图12所示,模型参数如表5 所示。Langmuir 模型的拟合系数R2(0.9894)优于Freundlich模型的拟合系数R2(0.9612),说明活性炭对Cu2+的吸附更符合Langmuir模型,反映了Cu2+在活性炭的表面是单分子层吸附,且吸附过程由表面上的均匀吸附位点控制[29]。常以分离系数RL判断吸附过程的难易程度,Langmuir模型的分离系数RL为0.15,介于0和1之间,说明该吸附过程是易于发生的。
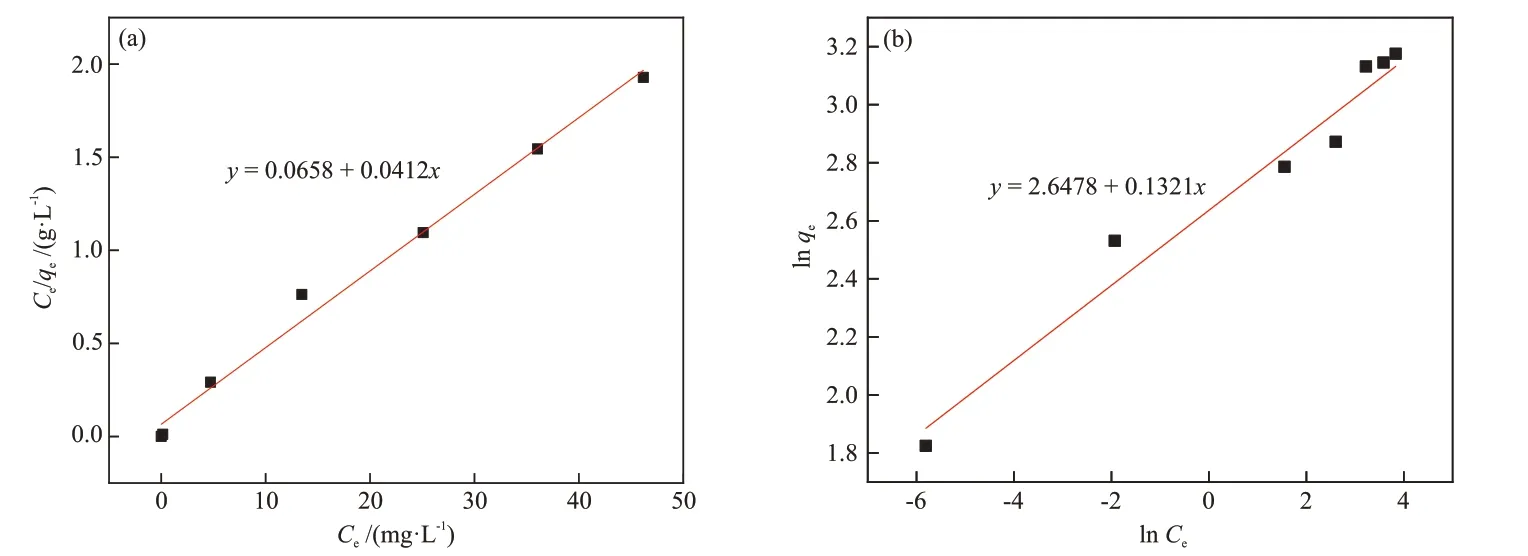
图12 活性炭对Cu2+的Langmuir(a)和Freundlich(b)吸附等温模型Fig.12 Langmuir (a) and Freundlich (b) adsorption isotherm models for Cu2+ on activated carbon

表5 吸附等温模型参数Table 5 Adsorption isotherm model parameters
3 结论
以马尾松生物炭为原料,模拟填加水蒸气的高温烟气为活化剂,通过改变水蒸气含量、活化温度、活化时间制备了活性炭,表征了活性炭的物化性质和结构特征;同时考察了pH、吸附时间、活性炭投加量以及Cu2+初始浓度对活性炭吸附Cu2+性能的影响,得到以下主要结论。
(1)活性炭碘吸附值随着水蒸气流量(0.00~1.85 mL/min)的增大先增加后减少,随着活化温度(700~850 °C)的升高以及活化时间(1.0~2.5 h)的延长不断增加。本文研究范围内,确定了最佳的制备条件,即当生物炭质量为6 g时,高温烟气100 mL/min、水蒸气流量为0.9 mL/min、活化温度为850 °C、活化时间为2.5 h,制备的活性炭的碘吸附值为1914 mg/g,产率为7.32%。
(2)马尾松基活性炭纤维外壁破裂,表面相对光滑,比表面积为1556 m2/g,孔结构以微孔为主,表面官能团含有丰富的O—H、C==C、C==O和C—O键等化学键。
(3)马尾松基活性炭可有效去除水中Cu2+,最佳吸附工艺为:pH 5.5,吸附时间30 min,活性炭投加量1.5 g/L,Cu2+初始浓度10 mg/L,此时活性炭对Cu2+的去除率达到99.97%,剩余Cu2+浓度为0.003 mg/L,符合我国生活饮用水标准(<1 mg/L)。
(4)马尾松基活性炭对Cu2+吸附符合准二级动力学模型;Langmuir 模型能更好地描述吸附过程,Cu2+在活性炭的表面是单分子层吸附,颗粒内扩散并不是唯一的速率控制步骤,活性炭对Cu2+的吸附机理可能包括静电相互作用和络合反应。

